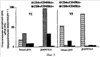Патент на изобретение №2356577
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБЫ ВАКЦИНАЦИИ ПРОТИВ МАЛЯРИИ
(57) Реферат:
Изобретение относится к биотехнологии и медицине. Способ по изобретению включает примирование антималярийного иммунного отклика с помощью вакцины, основанной на ДНК, и стимулирование этого отклика с помощью вакцины на белковой основе. Описана вакцина, включающая, в качестве отдельных компонентов, примирующий состав, включающий, по крайней мере, один полинуклеотид, кодирующий, по крайней мере, один первый малярийный антиген, и стимулирующий состав, состоящий из, по крайней мере, одного полипептида, дополнительно включающего, по крайней мере, один второй малярийный антиген. Раскрыт набор для иммунизации человека против вызывающего малярию патогена. Изобретение позволяет расширить получаемый иммунный отклик с помощью повторной иммунизации (стимулирования) вакциной на белковой основе. 4 н. и 40 з.п. ф-лы, 12 ил., 5 табл.
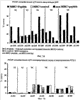
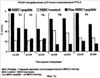
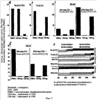
Ссылки на относящиеся к данному вопросу заявки Данная заявка основывается на и использует преимущества первоначальной заявки США Введение Малярия является одной из самых больших проблем общественного здравоохранения в тропиках и субтропиках. Каждый год от 300 до 500 миллионов людей заражаются инфекциями с плазмодиями, и до 2,7 миллионов умирают от малярии в развивающемся мире (110). Plasmodium falciparum являются видами плазмодий, ответственными за большинство смертей, вызванных малярией. Цикл жизни Р.falciparum протекает в четырех отдельных стадиях, три из которых происходят в теле человека. См. общую информацию в 115. На первой стадии комар, переносящий инфекционные спорозоиты в своих слюнных железах, получает питание кровью от человека и, осуществляя это, переносит эти спорозоиты в кровяной поток человека. Очутившись в паренхимальных клетках печени, спорозоиты размножаются и образуют мерозоиты. На второй стадии мерозоиты передвигаются по кровяному потоку, инфицируя красные кровяные клетки (ККК). Как только ККК заполняется мерозоитами, она разрывается, высвобождая потомство, которое инфицирует новые ККК. Анемия является обычным симптомом на данной стадии инфекции. Постепенно некоторые из этих ККК создадут мужские и женские гаметоциты (третья стадия). На заключительной стадии неинфицированный комар кусает инфицированного человека, впитывая гаметоциты. В комаре оплодотворение женского гаметоцита постепенно приводит к производству инфицированных спорозоитов, тем самым завершая цикл. Когда такой патоген как Р.falciparum проникает в тело человека, тело откликается активацией иммунной системы. Сначала происходит обобщенный отклик, за которым следует патогенно-специфический отклик. Патогенно-специфический отклик нацелен на антигены, уникальные для проникающего патогена. Два основных вида патогенно-специфического отклика являются клеточным и гуморальным. Т клетки CD8+ и CD4+ участвуют в клеточном иммунном отклике. В частности, Т клетки CD8+ производят такие цитокины как гамма-интерферон (IFN- В контексте малярийной инфекции различные виды патогенно-специфического отклика являются наиболее эффективными на определенных стадиях цикла жизни Р.falciparum. Когда инфицированные спорозоиты перемещаются в печень и поступают в клетки печени, спорозоиты становятся внутриклеточными патогенами, проводя мало времени за пределами инфицированных клеток. На данной стадии Т клетки CD8+ и Т клетки CD4+ являются наиболее важными, так как эти Т клетки и их цитокиновые продукты, такие как IFN- Вакцины ДНК вызывают опосредованные клетками иммунные отклики, включая отклики антиген-специфических цитотоксических Т лимфоцитов (ЦТЛ) CD8+ и отклики Т клеток CD4+ со смещением Тh1, которые являются основными механизмами защиты от внутриклеточных патогенов и опухолей (6, 11, 45, 63, 104, 106). Однако до сих пор вакцины ДНК показывали себя недостаточно оптимально для индуцирования защитного иммунного отклика в человеке. В отличие от этого, когда малярийная инфекция достигает второй стадии и заражает ККК, инфицированные мерозоиты не только воспроизводятся внутри ККК, они свободно циркулируют в кровяном потоке. Антитела являются наиболее эффективными при лечении этой стадии инфекции по двум причинам. Во-первых, ЦТЛ нужны инфицированные клетки-хозяева для создания антигенов на специальном белке, называемом главный комплекс гистосовместимости – I (MHC-I). ККК не осуществляют экспрессию MHC-I, тем самым снижая эффективность ЦТЛ. Во-вторых, как обсуждалось ранее, антитела являются посредниками в фагоцитозе патогенов, не связанном с клетками-хозяевами. Таким образом, на второй стадии инфекции, как В клетки, так и Т клетки CD4+, которые стимулируют В клетки, являются важными для победы над инфекцией. Сложность иммунного отклика человека на Р.falciparum, а также многоэтапный цикл жизни паразитов с зависящей от каждого этапа экспрессией белков, вносят вклад в трудность разработки вакцины против Р.falciparum. Тем не менее, необходимость в вакцине от малярии сохраняется. Стадия спорозоитов Р.falciparum была идентифицирована как потенциальная мишень для вакцины от малярии. Основной поверхностный белок спорозоита известен как белок циркумспорозоит (белок CS). Был клонирован белок из штамма 7G8, он был выделен и секвентирован (21). Он характеризуется тем, что имеет центральную иммунодоминантную зону повтора, включающую тетрапептид Asn-Ala-Asn-Pro, повторяющийся 37 раз, но перемежающийся с четырьмя более мелкими повторами Asn-Val-Asp-Рrо. В других штаммах число больших и малых повторов колеблется. Так же, как и их относительная позиция. Эта центральная часть примыкает к N и С-терминальной части, состоящей из неповторяющихся последовательностей аминокислот, обозначаемых как бесповторная часть белка CS. Основанная на ДНК вакцина, содержащая плазмид, который производит экспрессию гена циркуспорозоита Р.falciparum (P Плазмид ДНК P Предклинические иммуногенетические исследования вакцины ДНК P Перед использованием в клинических испытаниях были проведены обширные предклинические исследования безопасности. Эти исследования включали: 1) изучение распределения в ткани мыши плазмида ДНК, введенного либо внутривенно (IV), либо внутримышечно (IM); 2) исследования безопасности дозы повторения на мышах и кроликах; и 3) исследование интеграции плазмида ДНК на мышах (67, 75). Эти исследование обобщены ниже. Исследования распределения плазмида: Паркер и др. оценили распределение плазмида в различных тканях мыши (57). Мыши внутривенно или внутримышечно вводилась единственная доза плазмида P Изучение безопасности дозы повтора: Паркер и др. также рассмотрели безопасность введения повторных доз вакцины на мышах и кроликах (75). В исследовании безопасности дозы повтора на мышах животные получали 8 повторных внутримышечных вливания плазмида ДНК P Интеграционные исследования: Мартин и др. произвели оценку, интегрирует ли плазмид P Как только исследователи уточнили безопасность вакцины P Ни у одного из 20 субъектов не было индуцирования антител анти-двухцепочечного ДНК или увеличения титров AHA (антинуклеарного антитела) по сравнению с базовым уровнем. Ванг и др. показали, что ни у одного из добровольцев не развились антитела к P Во втором клиническом испытании, начатом в апреле 1999 года, 14 здоровых взрослых добровольцев были иммунизированы через 0, 4 и 8 недель вакциной ДНК P В целом, вакцина была безопасной и хорошо переносимой. Добровольцы не испытывали каких-либо тяжелых или серьезных побочных эффектов (АЕ), связанных с вакциной. Никто из добровольцев не испытывал серьезных лабораторных аномалий, связанных с приемом вакцины P Что касается иммунного отклика на вакцину, то ни один из добровольцев не выработал антител к P Все четыре добровольца в игловой внутримышечной группе реагировали на 7/9 пептидов в 17,6% (26/148) анализов. Все пять добровольцев в внутримышечной группе Biojector реагировали на 9/9 пептидов в 26,5% (49/185) анализов. Четыре из пяти добровольцев в внутримышечной/подкожной группе Biojector реагировали на 7/9 пептидов в 17,3% (32/185) анализов. Восемь из 14 добровольцев имели детектируемый отклик ЦТЛ. Из этих восьми два были в игловой внутримышечной группе (реагировавшей на 4/7 пептидов в целом из 5/126 анализов), три были в внутримышечной группе Biojector (реагировавшей на 6/8 пептидов в целом из 11/168 анализов) и три были в внутримышечной/подкожной группе Biojector (реагировавшей на 6/6 пептидов в целом из 14/162 анализов) (107). В общем, в этом испытании было установлено, что внутримышечный путь прививки Biojector был наиболее эффективным для индуцирования специфического для антигена отклика IFN- В сумме, эти два клинических испытания показали, что полинуклеотидная вакцина P Как обсуждалось выше, в дополнение к откликам Т клеток CD8+ антитела против любого пептида белка P Прием 2 или 3 доз RTS,S в среднем защищал в среднем 44% из более 60 добровольцев, имеющих провокационную пробу Р.falciparum через 2-3 недели после последней иммунизации (8, 54, 99) и защищал 70% полуиммунных гамбийцев два месяца после последней иммунизации (8). Однако эта защита имеет короткий срок (8, 100). Иммунизация с помощью RTS,S индуцирует антитела против P Изобретение Настоящее изобретение обеспечивает новый метод вакцинации, который первоначально вызывает иммунный отклик с помощью примирующей вакцины (здесь и далее «примирование» – первичное введение вакцины), включающей полинуклеотид, кодирующий, по крайней мере, один первый малярийный антиген, и затем стимулирует первичный отклик с помощью стимулирующей вакцины, включающей, по крайней мере, один полипептид, по крайней мере, один второй малярийный антиген, имеющий, по крайней мере, один эпитоп общий с, по крайней мере, одним первым малярийным антигеном примирующей вакцины. Эта комбинация обеспечивает три важных улучшения по сравнению с существующей антималярийной стратегией вакцинации. Во-первых, комбинация двух ксеногенных вакцин активирует оба ответвления иммунной системы, Т клетки CD8+ CD4+ и антитела. Конкретно, основываясь на результатах клинических испытаний с использованием вакцины P Второе значительное усовершенствование изобретения по сравнению с текущими стратегиями вакцинации заложено в том факте, что в нем используется белковая вакцина для стимуляции отклика Т клеток CD8+ у человека. Способ по данному изобретению стимулирует отклики Т клеток путем использования основанной на белке вакцины, которая до того времени считалась неэффективной для стимуляции отклика Т клеток CD8+ (61). В заключение, третьим значительным усовершенствованием по сравнению с настоящими антималярийными стратегиями вакцинации, обеспечиваемым настоящим изобретением, является то, что оно расширяет иммунный отклик двумя путями. Во-первых, более широкий репертуар Т клеток, производящих IFN- Краткое описание изобретения Настоящее изобретение относится к способам иммунизации человека от малярии, включающим этапы: а) примирования иммунного отклика в человеке путем приема примирующей вакцины, включающей полинуклеотид, кодирующий, по крайней мере, один антиген малярии; и б) стимуляции примированного иммунного отклика путем последующего приема стимулирующей вакцины, включающей, по крайней мере, один полипептид, который включает, по крайней мере, один антиген малярии, имеющий, по крайней мере, один общий эпитоп с антигеном малярии или антигенами примирующей вакцины, что вызывает как клеточный иммунный отклик, так и гуморальный иммунный отклик на малярию. В одном примере осуществления данного изобретения примирующая вакцина кодирует тот же полипептид, который присутствует в стимулирующей вакцине. В других примерах осуществления изобретения либо примирующая вакцина кодирует часть малярийного антигена, присутствующего в стимулирующей вакцине, либо полипептид, присутствующий в стимулирующей вакцине, является частью малярийного антигена, кодируемого примирующей вакциной. В другом примере осуществления изобретения вакцины совместно используют, по крайней мере, один эпитоп малярийной Т клетки. В еще одном примере осуществления изобретения вакцины совместно используют, по крайней мере, один малярийный эпитоп Т клетки CD8+. В альтернативном примере осуществления изобретения две вакцины совместно используют несколько малярийных эпитопов. Любой патоген, который вызывает малярию, может быть использован в способе изобретения. В одном примере изобретения патогеном является Р.falciparum. В других примерах осуществления данного изобретения, например, патогеном может быть P.vivax, Р.ovale или P.malariae. Подобным же образом, способ по данному изобретению может использоваться с любым антигеном малярии, выраженным на любой стадии цикла жизни патогена. В одном примере осуществления изобретения примирующая вакцина кодирует, а стимулирующая вакцина включает один или более антигенов, выраженных во время стадии пред ККК патогена, включая печеночную стадию. В еще одном примере осуществления изобретения полинуклеотид примирующей вакцины кодирует, по крайней мере, одну часть циркумспорозоитного белка, а стимулирующая вакцина включает, по крайней мере, одну часть циркумспорозоитного белка, который выражен во время печеночной стадии инфекции. В еще одном примере осуществления изобретения полинуклеотид примирующей вакцины кодирует практически весь циркумспорозоитный белок, а стимулирующая вакцина включает часть циркумспорозоитного (CS) протеина. Минимальная часть белка CS включает, по крайней мере, один эпитоп или несколько эпитопов. В одном специфическом примере осуществления изобретения примирующая вакцина включает P Изобретение далее обеспечивает фармацевтический набор, включающий описанные здесь примирующую и стимулирующую вакцину. Изобретение далее обеспечивает использование описанных здесь примирующей вакцины и стимулирующей вакцины в подготовке вакцины для профилактики или снижения тяжести малярии. Таким образом, изобретение обеспечивает использование полинуклеотида, кодирующего, по крайней мере, один антиген малярии, в частности белок CS или его фрагмент в качестве примирующей вакцины и полипетида, включающего, по крайней мере, один малярийный антиген, в частности белок CS или его фрагмент, в качестве стимулирующей вакцины при приготовлении примирующей и стимулирующей вакцины против малярии. В одном конкретном примере осуществления изобретения один полинуклеотид имеет форму плазмида ДНК, предпочтительно осуществляющего экспрессию белка CS полной длины или его фрагмента. Полинуклеотид, кодирующий белок CS или фрагмент, может находиться под контролем ксеногенного промотера, известного в данной области техники. В одном примере осуществления изобретения промотер является промотером HCMV, дополнительно включающим Эксон 1. В одном конкретном примере осуществления изобретения полипептид стимулирующей вакцины является гибридным белком, включающим карбокси-терминальную часть белка CS, например, по крайней мере, 160 аминокислот из карбокси-терминальной части, дополнительно исключая 12 аминокислот из карбокси-терминала. Любой или оба из примирующего и стимулирующего состава могут включать дополнительные малярийные антигены или другие антигены. В примере осуществления изобретения в соответствии с данным аспектом изобретения примирующая вакцина включает полинуклеотид, кодирующий белок CS полной длины, присутствующий в плазмиде ДНК под контролем ксеногенного промотера, а стимулирующая вакцина включает RTS,S в комбинации с индуцирующим Тh1 адъювантом, в частности адъювантом, который включает QS21, 3D-MPL и масло в водяной эмульсии. Примирующая и стимулирующая вакцины могут быть обеспечены в форме фармацевтического набора. Изобретение обеспечивает частичную, усиленную или полную защиту человека, который ранее не подвергался воздействию вызывающего малярию патогена или подвергался ему, но не является полностью защищенным. Изобретение может также использоваться для снижения шанса выработки малярийной инфекции, снижения шанса заболевания при инфицировании, снижения тяжести симптомов болезни, таких как лихорадка, когда человек инфицируется, снижения концентрации паразитов в инфицированном человеке или снижения смертности от малярии, когда человек подвержен воздействию малярийных паразитов. В регионах, в которых малярия является эндемичной, даже частичная защита приносит пользу. Например, стратегия лечения вакциной, которая приводит к защите около 30% населения, может иметь значительное воздействие на сообщество. Краткое описание графических материалов На фиг.1 показан отклик ЦТЛ для каждого положительного субъекта и каждого положительного пептида сразу же после примирования ДНК (фиг.1а), непосредственно перед стимулированием RTS,S (фиг.1b) и затем после стимулирования RTS,S (фиг.1с). Черные полосы представляют образцы, содержащие тестовый пептид и соответствующее представление главного комплекса гистосовместимости. Заштрихованные полоски представляют собой образцы, содержащие контрольный пептид и соответствующее представление главного комплекса гистосовместимости. Полосатые полоски представляют собой образцы, содержащие тестовый пептид без соответствующего представления главного комплекса гистосовместимости (МНС). Свежие мононуклеары периферической крови, взятые после примирования ДНК (а), перед стимулированием (б) или спустя 2 недели после первой (число добровольцев 6=V6) или второй (V2, 3, 8 и 9) дозы RTS,S (с), стимулировались in vitro с помощью ALVAC, производящего экспрессию P для, по крайней мере, 2 эффекторных клеток в отношении соотношения клеток мишеней (Е:Т). Представлен процент лизиса для каждого пептида с его одновременно оцениваемыми контрольными образцами при едином соотношении Е:Т (20:1 или 40:1). На фиг.2 характеризуются Т клетки, участвующие в откликах IFN- На фиг.3 показаны уровни экспрессии IFN- На фиг.4 показан сдвиг от индуцированной ДНК схемы отклика IFN- На фиг.5 показаны титры антитела IFAT добровольцев, примированных ДНК/стимулированных RTS,S. Титры антител представляли среднегеометрическое значение +/- SE (95% уверенных интервалов) в примированных ДНК (+) и непримированных (-) добровольцах с (+) и без (-) антител к HBsAg перед первой дозой RTS,S. Анализы антител выполнялись после 1-ой и 2-ой иммунизации RTS,S. He было значительных отличий в титрах между любыми из групп, за исключением 2 недель после первой дозы, когда добровольцы ДHK-/HBsAg+ имели значительно большие титры, чем при ДНК+/ HBsAg+(P<0,02). Детальное описание изобретения Как было продемонстрировано, многовидовой иммунный отклик на малярийную инфекцию примируется иммунизацией человеческих субъектов примирующей вакциной, включающей полинуклеотид, кодирующий, по крайней мере, один антиген малярии, и затем стимулируется иммунизацией стимулирующей вакциной, включающей, по крайней мере, один полипептид, который включает, по крайней мере, один малярийный антиген, имеющий, по крайней мере, один общий эпитоп с антигеном или антигенами малярии примирующей вакцины. Удивительно, настоящий способ иммунизации стимулирует и расширяет примированный отклик, используя полипептидную вакцину. «Вакцина» – это состав из материи, включающий молекулу таким образом, что при введении субъекту она индуцирует иммунный отклик. Вакцины могут содержать молекулы полинуклеотида, молекулы полипептида и молекулы карбогидрата, а также их производные и комбинации, такие как гликопротеины, липопротеины, карбогидрат-протеиновые конъюгаты, слияния между двумя или более полипептидами или полинуклеотидами, и тому подобное. Вакцина далее может включать растворитель, адъювант, носитель или их комбинации, как это легко могут понять специалисты в данной области. Может использоваться любой способ или путь прививки либо отдельно, либо в комбинации для доставки полинуклеотидной вакцины или протеиновой вакцины человеческому субъекту. Пути приема включают внутривенный, внутримышечный, подкожный, внутрикожный или относящийся к слизистой оболочке. Средства доставки могут быть разными. Можно, например, делать инъекцию человеку внутривенно, внутримышечно, подкожно или внутрикожным путем. Можно также делать прививку человеку по слизистому пути. Альтернативно, доставка может быть по безыгловому средству, такому как использование безыгловой «генной пушки», например, Biojector® или другого средства введения или биолостическую доставку. Полинуклеотид может быть доставлен в бактерии, содержащей ДНК вакцины P Примеры приемлемых вирусных векторов включают вирусные векторы герпес симплекс, вакциновые или альфа-вирусные векторы и ретровирусы, включая лентивирусы, аденовирусы и адено-ассоциированные вирусы. В оном примере осуществления изобретения эти вирусы представляют собой векторы репликационно дефективного вируса. Методы переноса генов с использованием этих вирусов известны специалистам в данной области. Например, ретровирусные векторы могут быть использованы для стабильной интеграции полинуклеотида по изобретению в геном хозяина, хотя подобная рекомбинация и не может быть рекомендована. Репликационно дефективные аденовирусные векторы в отличие от этого остаются эписомными и, следовательно, допускают переходную экспрессию. В специфическом примере осуществления изобретения аденовирус, использованный в живом векторе, является репликационно дефективным аденовирусом человека или обезьяны. Обычно эти вирусы включают делецию Е1 и могут быть выращены на клеточных линиях, которые трансформируются с геном Е1. Приемлемыми обезьяньими аденовирусами являются, например, вирусы, выделенные из шимпанзе. Примеры вирусов, пригодных для использования в настоящем изобретении, включают С68 (также известные как Pan 9) (патент США Вакцина может состоять из отдельных компонентов. При использовании здесь «отдельные компоненты» относятся к ситуации, в которой термин «вакцина» фактически включает две дискретные вакцины, которые отдельно вводятся субъекту. В этом смысле вакцина, включающая отдельные компоненты, может рассматриваться как набор или пакет, включающий отдельные компоненты вакцины. Например, в контексте данного изобретения пакет может включать компонент полинуклеотидной вакцины и компонент полипептидной вакцины. Вакцина «индуцирует» иммунный отклик, когда антиген или антигены, присутствующие в вакцине, вызывает рост иммунного отклика у иммунизированного субъекта на данный антиген или антигены. Вакцинированный субъект будет генерировать иммунный отклик, о чем свидетельствует активизация иммунной системы, что включает производство вакцинных антиген-специфических Т клеток, вакцинных антиген-специфических В клеток, вакцинных антиген-специфических антител и цитокинов. Получаемый в результате иммунный отклик может быть измерен несколькими способами, включая анализы ELISPOT, ELISA, анализы выхода хрома, межклеточным цитокинным окрашиванием, анализом с помощью клеточного сортера с возбуждением флуоресценции (FACS) и окрашиванием тетрамера главным комплексом гистосовместимости (МНС) (для идентификации пептидно-специфических клеток). Опытный исследователь может также использовать эти способы для измерения первичного иммунного отклика или вторичного иммунного отклика. «Антиген» является веществом, способным генерировать иммунный отклик в субъекте, подвергнутом воздействию антигена. Антигены обычно являются полипептидами и являются центром иммунного отклика хозяина. «Эпитоп» или «антигенный детерминант» является той частью антигена, к которой конкретно привязываются Т клетки и антитела. Антиген может включать множественные эпитопы. Примирующая вакцина, используемая в способе по данному изобретению, включает полинуклеотид, кодирующий малярийный антиген, как это рассматривается ниже. Примирующая вакцина может быть только ДНК или ДНК, которая находится под контролем постороннего промотора внутри бактерии или вируса. Полинуклеотид примирующей вакцины присутствует в приемлемом доставочном векторе, подобном плазмиду, или другом векторе, таком как бактериальный или вирусный вектор. Полинуклеотид может быть под контролем приемлемого промотора, подобного промотору, полученному из гена HCMV IE. Примирующая вакцина вводится в количестве, эффективном для примирования иммунного отклика на малярийный антиген. При использовании здесь «примирование» иммунного отклика происходит, когда антиген представляется Т клеткам или В клеткам. В результате, примированные клетки откликаются на тот же антиген вновь как клетки памяти во втором, последующем иммунном отклике. Таким образом, примирование генерирует как первичный иммунный отклик, так и устанавливает иммунологическую память. Специалист в данной области оценит, что первичный иммунный отклик представляет собой адаптивный иммунный отклик после первоначального воздействия антигена в определенном контексте, таком как патоген, или в вакцине. Однако будет также оценено, что изобретение не ограничивается использованием примирующей вакцины в контексте иммунологически не подвергнутых иммунологическому воздействию индивидуумов. Скорее примирование может также происходить в индивидуумах, которые были подвергнуты воздействию антигена, но не получали примирующей вакцины. «Эффективная» примирующая доза может колебаться между 0,01 мкг и 50 мг ДНК. Альтернативно, доза может быть между 1 мкг и 10 мг ДНК или 2,5 и 5 мг ДНК. Полинуклеотидная вакцина может вводиться один раз перед приемом стимулирующей полипептидной вакцины. В другом примере осуществления изобретения примирующая вакцина может приниматься несколько раз. «Эффективное» количество прививок может колебаться между 1 и 5 дозами. Альтернативно, число доз может быть между 1 и 3 дозами или 1 и 2 дозами перед приемом стимулирующей вакцины. «Полинуклеотид» обычно относится к любому полирибонуклеотиду (рибонуклеиновая кислота, РНК) или дезоксирибонуклеиновая кислота (ДНК), которые могут быть немодифицированными или модифицированными РНК или ДНК. Полинуклеотиды включают, без ограничения, однонитевые или двухнитевые ДНК, ДНК, которая является смесью однонитевых и двухнитевых зон, однонитевых и двухнитевых РНК, РНК, которая является смесью однонитевых и двухнитевых зон. Полинуклеотиды также включают гибридные молекулы, включающие ДНК и РНК, которые могут быть однонитевыми, или более типично, двухнитевыми, или смесью однонитевых и двухнитевых зон. В дополнение, «полинуклеотид» относится к трехнитевым зонам, включающим РНК или ДНК, или как РНК, так и ДНК. Полинуклеотиды также включают ДНК или РНК, содержащие одну или более модифицированных баз, и ДНК или РНК с основами, модифицированными для стабильности или по другим причинам. «Модифицированные» базы включают, например, тритилированные базы и необычные базы, такие как инозин. В ДНК и РНК можно сделать разнообразные модификации; таким образом, «полинуклеотид» включает химически, ферментно или метаболически модифицированные формы полинуклеотидов, которые обычно находятся в природе, а также химические формы ДНК и РНК, характерные для вирусов и клеток. Олигонуклеотиды являются относительно короткими полинуклеотидами. «Фрагмент» последовательности полинуклеотидов относится к полинуклеотидной последовательности, которая короче, чем эталонная последовательность, но которая сохраняет биологическую функцию или активность, которые признаются такими же, как и у эталонного полинуклеотида. Фрагмент кодирует, по крайней мере, один эпитоп эталонного полипептида, кодируемого эталонной последовательностью полинуклеотида. При использовании здесь термин «практически вся» при использовании для описания полинуклеотида или полипептида, относится к молекуле, которая, за исключением незначительных делеций баз нуклеотида или остатков аминокислот, кодирует или представляет целый полинуклеотид или полипептид полной длины. Стимулирующая вакцина, используемая в способе по данному изобретению, может включать слитый белок, включающий, по крайней мере, один полипептид малярийного антигена, рассматриваемый ниже. Используемые в данной вакцине полипептиды могут быть изолированы из природного источника, произведенного в качестве рекомбинантного белка в постороннем организме, подобном бактерии, или синтезированы химическими средствами. Стимулирующая вакцина может далее включать дополнительные немалярийные полипептиды для усиления иммуногенетичности малярийного полипептида. Например, можно использовать часть или весь поверхностный антиген вируса гепатита В. Примирующая вакцина и стимулирующая вакцина совместно имеют, по крайней мере, один общий малярийный эпитоп. Приемлемый слитый белок для использования в стимулирующей вакцине по данному изобретению может включать гибридный белок, включающий практически всю С-терминальную часть белка CS, четыре или более тандемных повторов иммунодоминантной области, и поверхностный антиген из вируса гепатита В (HbsAg). Гибридный белок включает последовательность, которая содержит, по крайней мере, 160 аминокислот, которые практически гомологична к С-терминальной части белка CS. В одном примере осуществления изобретения белок CS может быть лишен последних 12 аминокислот от С-терминала. Приемлемый гибридный белок включает, например, часть белка CS P.falciparum практически соответствующего аминокислотам 210-398 Р.falciparum 7G8, слитого в рамку через линейный линкер (связывающий агент) к N-терминалу HbsAg. Линкер может включать часть preS2 от HbsAg. Другой пример осуществления данного изобретения является гибридной частицей, обозначенной как RTS,S, которая описана в патенте США 5,928,902 и в международной заявке на патент WO 93/10152, которые включены здесь в качестве ссылки. Данный гибрид состоит из: 1) остатка метионина, кодируемого нуклеотидами 1059 по 1061, полученными из Saccharomyces cerevisiae TDH3 генной последовательности (71); трех аминокислот Met Ala Pro, полученных из нуклеотидной последовательности (1062 по 1070), созданной процедурой клонирования, используемой для конструирования гибридного гена; 3) фрагмента 189 аминокислот, кодируемых нуклеотидами 1071 по 1637, представляющих аминокислоты с 210 по 398 белка циркумспорозоита (CSP) штамма Plasmodium falciparum 7G8 (21); 4) аминокислоты (Arg), кодируемой нуклеотидами 1638 по 1640, созданных процедурой клонирования, используемой для конструирования гибридного гена; 5) четыре аминокислоты Pro Val Thr Asn, кодируемых нуклеотидами 1641 по 1652, и представляющими четыре карбокси-терминальных остатка вируса гепатита В (серотип adw) белка preS2 (103) и 6) фрагмента 226 аминокислот, кодируемых нуклеотидами 1653 по 2330, и определяющими S белок вируса гепатита В (серотип adw). Стимулирующая вакцина вводится в количестве, эффективном для «стимулирования» примированного иммунного отклика на малярийный антиген. При использовании здесь «стимулирование» иммунного отклика означает индуцирование вторичного иммунного отклика в субъекте, который был примирован (т.е. уже подвергнут влиянию) под первоначальным воздействием антигена. Вторичный иммунный отклик характеризуется активизацией и расширением специфических Т клеток памяти и В клеток. Таким образом, стимулирование специфического иммунного отклика усиливает примированный иммунный отклик путем индуцирования иммунных клеток к пролиферации и дифференциации после последующего воздействия данного антигена. Как обсуждалось ранее, белок CS полной длины вакцины P «Эффективная» доза стимулирования может колебаться между 1 мкг и 100 мкг или между 10 мкг и 75 мкг или между 40 мкг и 60 мкг. В другом примере осуществления изобретения стимулирующая доза может быть 50 мкг. В еще одном примере осуществления изобретения стимулирующая доза может быть 25 мкг. Стимулирующая вакцина может вводиться один раз или многократно. «Эффективное» количество стимулирующих доз может колебаться между 1 и 5 дозами стимулирующей вакцины. Альтернативно, число доз может быть между 1 и 3 дозами или между 1 и 2 дозами для субъекта человека. В другом примере осуществления изобретения как вакцина ДНК, так и белковая вакцина, могут использоваться для стимуляции первичного иммунного отклика. «Полипептид» относится к любому полипептиду, включающему две или более аминокислот, соединенных друг с другом пептидными связями или модифицированными пептидными связями, т.е. пептидными изостерами. «Полипептид» относится как к коротким цепочкам, обычно называемыми пептидами, олигопептидами или олигомерами, так и к более длинным цепочкам, обычно называемым белками. Полипептиды могут содержать аминокислоты, отличающиеся от обычно кодируемых кодоном. Полипептиды включают последовательности аминокислот, модифицированные либо природными процессами, такими как пост-трансляционная обработка, или методами химической модификации, которые хорошо известны в данной области. Подобные модификации хорошо описаны в базовых текстах и в более детальных монографиях, а также в объемной исследовательской литературе. Модификации могут возникнуть в любом месте в полипептиде, включая основу полипептида, боковые цепочки аминокислот и амино или карбоксильные терминалы. Подобные модификации могут присутствовать в той же или отличающейся степени в нескольких сайтах в данном полипептиде. Также данный полипептид может содержать много типов модификаций. Полипептиды могут быть разветвленными в результате убиквитинирования, и они могут быть циклическими, с разветвлением и без. Циклические, разветвленные и разветвленные циклические полипептиды могут возникнуть из пост-трансляционных природных процессов или могут быть выполнены синтетическими методами. Модификации включают ацетиляцию, ациляцию, ADP-рибосиляцию, амидирование, биотинилирование, ковалентное присоединение флавина, ковалентное присоединение доли протогема, ковалентное присоединение нуклеотида или производного нуклеотида, ковалентное присоединение липида или производного липида, ковалентное присоединение фосфотидилинозитола, перекрестное сшивание, циклизацию, формирование дисульфидной связи, деметилирование, формирование ковалентных перекрестных связей, формирование цистина, формирование пироглютамина, формилирование (введение радикала), гамма-карбоксилирование, гликозилирование, формирование GPI домена, гидроксилирование, иодирование, метилирование, миристоилирование, оксидирование, протеолитическую обработку, фосфорилирование, пренилирование, рацемизацию, селеноилирование, сульфацию, добавление аминокислот, усредненное пересылкой ДНК в белки, такие как аргинилирование и убиквитинирование (79, 82, 94, 113). «Фрагмент» последовательности полипептида относится к последовательности полипептида, которая короче эталонной последовательности, но которая сохраняет биологическую функцию или активность, которая признается такой же, как и у эталонного полипептида. Подобная активность может включать, например, способность стимулировать иммунный отклик. Фрагмент сохраняет, по крайней мере, один эпитоп эталонного полипептида. «Часть» полипетида относится к поднабору последовательности аминокислот эталонного полипептида. Часть может быть описана ее относительным местоположением в полипептиде, например, С-терминальной части или N-терминальной части. Изобретение может использоваться с любым малярийным антигеном, подобным показанным в таблице А и Таблице В.
Белок циркумспорозоит или «CSP» является главным поверхностным полипептидом на поверхности малярийных спорозоитов. CSP от штамма 7G8 Plasmodium falciparum (P “RTS,S”, при использовании здесь, относится к определенному малярийному антигену и представляет один пример осуществления настоящего изобретения. RTS,S и его производство более полно описаны в патенте США «Расширение» относится к увеличению репертуара откликов Т клеток. В данном случае более широкий репертуар Т клеток, производящих IFN- «Расширение» также относится к увеличению диапазона эпитопов, на которые будет реагировать иммунный отклик. В дополнение к первоначально примированным иммунным клеткам также индуцируется расширение и активация иммунных клеток, которые либо не были примированы или имеются в таком небольшом количестве, что они не могут быть детектированы. Таким образом, расширенный иммунный отклик не только расширяет первоначально примированный отклик, он также содержит отклики на новые эпитопы, которые не были частью первичного отклика. Опытный специалист может детектировать расширенный иммунный отклик путем использования антиген-специфических анализов детектирования. Например, опытный специалист может использовать анализ ELISPOT (иммуноферментный спот-анализ) или тетрамерное окрашивание главного комплекса гистосовместимости (МНС) для определения репертуара эпитопов, на которые реагирует первоначальный иммунный отклик, и сравнить этот диапазон с репертуаром эпитопов, на которые реагирует вторичный иммунный отклик. Если вторичный иммунный отклик реагирует на большее количество эпитопов, чем первичный иммунный отклик, вторичный иммунный отклик был расширен. «Т клетки CD8+ представляют собой класс Т лимфоцитов, характеризуемых обладанием поверхностным маркером клетки CD8. Т клетки CD8+ являются МНС класса I ограниченными «ЦТЛ» или подавляющими Т клетками. «Т клетки CD4+» представляют собой класс Т лимфоцитов, характеризуемых обладанием поверхностным маркером клетки CD4. Т клетки CD4+ являются МНС класса II ограниченными Т лимфоцитами. Имеется два типа Т клеток CD4+, называемых «Т клетки помощники» типа 1 или типа 2. Как обсуждалось выше, иммунный отклик генерируется на антиген через взаимодействие антигена с клетками иммунной системы. Получаемый в результате иммунный отклик может быть широко определен в две крайние категории, являясь гуморальными или вызванными клетками иммунными откликами (традиционно характеризуемыми механизмами защиты антител и клеточных эффекторных механизмов, соответственно). Эти категории откликов назывались откликами типа Тh1 (вызванные клетками отклики) и иммунный отклик типа Th2 (гуморальный отклик). Экстремальный иммунный отклик типа Тh1 может быть охарактеризован генерацией антиген-специфических, ограниченных гаплотипом ЦТЛ, естественным откликом клеток убийц. У мышей отклики типа Тh1 часто характеризуются генерацией антител подтипа IgG2a, в то время как у человека они соответствуют антителам типа IgG1. Иммунные отклики типа Th2 характеризуются генерацией широкого диапазона изотипов иммуноглобулина, включая у мышей IgG1, IgA и IgM. Движущей силой, лежащей за развитием этих двух типов иммунных откликов, являются цитокины, ряд идентифицированных белковых посредников, которые служат для помощи клеткам иммунной системы и делают последующий иммунный отклик либо откликом Тh1, либо Th2. Таким образом, высокие уровни цитокинов типа Тh1 имеют тенденцию индуцировать управляемый клетками иммунный отклик на данный антиген, в то время как высокие уровни цитокинов типа Th2 имеют тенденцию благоприятствовать индуцированию гуморальных иммунных откликов на антиген. Важно помнить, что различие иммунных откликов Тh1 и Th2 не является абсолютным. В реальности индивидуум будет поддерживать иммунный отклик, который описан как преобладающе Th1 или преобладающе Th2. Однако часто удобно рассматривать семьи цитокинов с точки зрения описанного в клонах мышиных клеток CD4+ Мосманном и Коффманом (70). Традиционно отклики типа Th-1 связаны с производством INF- Приемлемые адъюванты для использования в изобретении включают алюминиевую соль, подобную гелю гидроокиси алюминия (квасцы) или фосфату алюминия, но могут также быть солью кальция, железа или цинка, или могут быть нерастворимой суспензией ацилированного тирозина или ацилиновых сахаров, катионно или анионно произведенных полисахаридов, полифосфазенов или липосом монтанида. При приготовлении вакцин для использования в данном изобретении, в контексте плазмида P Некоторые адъюванты вакцины особенно пригодны для стимулирования либо отклика Th1, либо цитокинного отклика типа Th2. Традиционно наилучшие показатели баланса Th1:Th2 иммунного отклика после вакцинации или инфекции включают прямое измерение производства цитокинов Th1 или Th2 Т лимфоцитами in vitro после повторной стимуляции антигеном и/или измерения соотношения IgG1:IgG2a специфических для антигена иммунных откликов. Таким образом, адъювант типа Th1 является адъювантом, который стимулирует изолированные популяции Т клеток для производства высоких уровней цитокинов типа Th1 при повторной стимуляции антигеном in vitro и индуцирует специфические для антигена иммунные отклики, связанные с изотипом типа Th1. Например, иммуностимулянты типа Th1, которые могут быть составлены для производства адъювантов, приемлемых для использования в настоящем изобретении, могут включать липид А монофосфорила, в частности 3-dе-O-ацилированный липид А монофосфорила (3D-MPL). 3D-MPL является хорошо известным адъювантом, производимым компанией Риби Иммунохим (Ribi Immunochem), Монтана. Химически он часто поставляется как смесь 3-dе-O-ацилированный липида А монофосфорила с либо 4, 5 или 6 ацилированными цепочками. Он может быть очищен и подготовлен способами, указанными в патенте Великобритании GB 2122204 В, ссылка которого также раскрывает приготовление липида А дифосфорила и его 3-O-деацилированный вариантов. Были описаны и другие очищенные и синтетические липополисахариды (патент США 6,005,099, 42, 43, ЕР 0729473 B1, EP 0729473 B1, EP 0549074 B1). В одном примере осуществления изобретения 3D-MPL имеет форму состава из макрочастиц, имеющих небольшой размер частиц, менее 0,2 мкм в диаметре, и способ его производства описан в ЕР 0689454. Сапонины являются другим примером иммуностимулянтов Th1, которые могут быть использованы с изобретением. Сапонины являются хорошо известными адъювантами (60). Например, Quil А (полученный из коры Южно Американского дерева Quillaja Saponaria Molina) и его доли описаны в патенте США 5,057,540, ЕР 0362279 B1 и у Кензила (52). Гемолитические сапонины QS21 и QS17 (очищенные жидкостной хроматографией высокого разрешения доли Quil А) были описаны как потентные системные адъюванты, и способ их производства раскрыт в патенте США 5,057,540 и ЕР 0362279 B1. В этих ссылках также описывается использование QS7 (не-гемолитической фракции Quil-А), которая действует как потентный адъювант для системных вакцин. Использование QS21 далее описано в Кензил и др. (51). Комбинации QS21 и полисорбата или циклоэкстрина хорошо известны (WO 99/10008). Адъювантные системы из макрочастиц, включающие фракции QuilA, такие как QS21 и QS7 описаны в WO 96/33739 и WO 96/11711. Еще одним примером иммуностимулянта является иммуностимулирующий олигонуклеотид, содержащий неметилированные динуклеотиды CpG (“CpG”). CpG является сокращением для цитозин-гуанозин динуклеотидных мотивов, присутствующих в ДНК. CpG известен в данной области как адъювант при приеме как систематическим, так и слизистым путями (WO 96/02555, ЕР 468520, 23, 68). Исторически наблюдалось, что фракция ДНК бацилл Калмет-герин (BCG) могли оказывать противоопухолевый эффект. В дальнейших исследованиях синтетические олигонуклеотиды, полученные из генной последовательности BCG, были способны индуцировать иммуностимулирующие эффекты (как in vitro, так и in vivo). Авторы этих исследований пришли к заключению, что некоторые палиндромные последовательности, включая центральный мотив CG, осуществляли эту активность. Центральная роль мотива CG в иммуностимуляции была позже раскрыта Криегом (57). Детальный анализ показал, что мотив CG должен быть в контексте определенной последовательности, и что такие последовательности являются обычными в бактериальной ДНК, но редки в ДНК позвоночных. Иммуностимулирующая последовательность часто представляет собой: Пурин, Пурин, С, G, пиримидин, пиримидин; в которой мотив CG не метилированный, но другие неметилированные последовательности CpG известны как иммуностимулирующие и могут быть использованы в настоящем изобретении. В определенных комбинациях шести нуклеотидов может присутствовать палиндромная последовательность. Некоторые из этих мотивов, либо в качестве повторов одного мотива, либо комбинации различных мотивов, могут присутствовать в одном и том же олигонуклеотиде. Присутствие одного или более из этих иммуностимулирующих последовательностей, содержащих олигонуклеотиды, может активировать различные иммунные поднаборы, включая природные клетки убийцы (которые могут производить интерферон Иммуностимулянты, подобные описанным выше, могут быть сформулированы вместе с носителями, такими как, например, липосомы, масло в водной эмульсии, или соли металлов, включая алюминиевые соли (такие как гидроокись алюминия). Например, ED-MPL может быть приготовлен с гидроокисью алюминия (ЕР 0689454) или в водяных эмульсиях масла (WO 95/17210); QS21 может преимущественно быть сформулирован с холестеролом, содержащим липосомы (WO 96/33739), масло в водяных эмульсиях (WO 95/17210) или квасцы (WO 98/15287); CpG может быть приготовлен с квасцами (9, 23) или с другими катионными носителями. Могут также использоваться комбинации иммуностимулянтов, такие как комбинация липида А монофосфорила и производного сапонина (WO 94/00153; WO 95/17210; WO 96/33739; WO 98/56414; WO 98/05355, WO 99/12565; WO 99/11241) или как комбинация QS21 и 3D-MPL, раскрытые в WO 94/00153. Альтернативно, в настоящем изобретении может также использоваться комбинация CpG плюс сапонин, такая как QS21. Таким образом, приемлемые системы адъювантов включают, например, комбинацию липида А монофосфорила, такую как 3D-MPL, вместе с солью алюминия. В другом примере осуществления изобретения объединяется липид А монофосфорила и производная сапонина, подобная комбинации QS21 и 3D-MPL, раскрытой в WO/00153, или менее реактогенная композиция, где QS21 закаливается в холестероле, содержащем липосомы (DQ), как раскрыто в WO 96/33739. Еще один адъювантный состав, включающий QS21, 3D-MPL и токоферол в водяной эмульсии описан в WO 95/17210. В другом примере осуществления изобретения олигонуклеотиды CpG используются отдельно или вместе с солью алюминия. Примеры дополнительных комбинаций адъюванта и/или носителя включают: 3D-MPL + QS21 в DQ; квасцы + 3D-MPL; квасцы + QS21 в DQ + 3D-MPL; квасцы + CpG; 3D-MPL + QS21 в DQ + масло в водяной эмульсии; и CpG. В другом примере осуществления изобретения 3D-MPL и QS21 объединяются с или без CpG. Соотношение QS21:3D-MPL может быть порядка 1:10 до 10:1; 1:5 до 5:1; или 1:1. В другом примере осуществления изобретения соотношение равно 2,5:1 до 1:1 MPL:QS21. Обычно для приема человеком QS21 и 3D-MPL будут присутствовать в вакцине в диапазоне 1 pig – 2004 г, подобно 1-1004 г или 10~Lg-50~tg на дозу. Обычно масло в воде будет включать от 2 до 10% сквалена, от 2 до 10% альфа токоферола и от 0,33 до 3% эмульгатора 80. Соотношение сквален:альфа токоферол равно или меньше чем 1, так как это обеспечивает более стабильную эмульсию. Спан 85 может также присутствовать на уровне 1%. В некоторых случаях может быть связано с преимуществами, что вакцины по настоящему изобретению будут содержать стабилизатор. Адъюванты для использования с полипептидной стимулирующей вакциной по настоящему изобретению, включающие белок CS или иммуногенную его часть, дополнительно в таком гибридном белке как RTS,S могут включать комбинацию 3D-MPL и QS21 с или без CpG. Как предшествующее общее описание, так и последующее детальное описание являются примерами и объясняют, а не ограничивают заявленное изобретение. Более того, изобретение не ограничивается определенными описанными примерами осуществления изобретения, так как они, конечно, могут варьироваться. Далее, терминология, используемая для описания определенных примеров осуществления изобретения, не является ограничивающей, так как объем настоящего изобретения не будет ограничен только его формулой. Что касается диапазонов значений, то изобретение включает каждое из промежуточных значений между верхним и нижним пределами диапазона до, по крайней мере, одной десятой единицы нижнего предела, за исключением случаев, когда в контексте четко указано противоположное. Далее, изобретение включает любые другие указанные промежуточные значения. Более того, изобретение также включает диапазоны, исключающие либо один из либо оба из верхнего и нижнего диапазонов, за исключением конкретно исключенных из указанного диапазона. За исключением по иному определенных случаев, значение всех используемых здесь технических и научных терминов являются общепринятыми для обычного специалиста в области, к которой относится изобретение. Обычный специалист в данной области также поймет, что любые способы и вещества, подобные или эквивалентные описанным здесь, могут также использоваться для применения или тестирования изобретения. Далее, все упомянутые здесь публикации включены в виде ссылки. Следует отметить, что при использовании здесь и в прилагаемой формуле формы единственного числа включают формы множественного числа за исключением случаев, когда из контекста очевидно иное. Таким образом, например, ссылка на «субъект полипептид» включает множество подобных полипептидов, а ссылка на «агент» включает ссылку на один или более агентов и их эквивалентов, известных специалистам в данной области, и так далее. Далее, все числа, выражающие количества ингредиентов, условия реакции, % чистоты, длины полпептида и полинуклеотида, и так далее, используемые в спецификации и формуле, модифицируются термином «около», за исключением по иному указанных случаев. Соответственно, числовые параметры, изложенные в спецификации и формуле, являются аппроксимациями, которые могут меняться в зависимости от желаемых свойств настоящего изобретения. В любом случае, не в качестве попытки ограничить применение доктрины эквивалентов объемом формулы, каждый числовой параметр должен, по крайней мере, толковаться в свете числа отмеченных значимых цифр, применяя обычные методы округления. Тем не менее, числовые значения, изложенные в конкретных примерах, приводятся как можно точнее. Любое числовое значение, однако, внутренне содержит некоторые погрешности из-за стандартного отклонения его экспериментального измерения. Приведенные далее примеры иллюстрируют изобретение. Они только иллюстративные и раскрывают различные полезные свойства определенных примеров осуществления изобретения. Следующие примеры не должны толковаться как ограничивающие изобретение. Примеры Пример 1 Стимулирование примированного отклика анти-P Для данного исследования было набрано двадцать четыре HLA-A* 0201-позитивных добровольца. Разнообразие главного комплекса гистосовместимости человека (HLA) добровольцев было ограничено наиболее обычным подтипом HLA класса I в данной популяции для того, чтобы допустить межгрупповые сравнения генетически ограниченных откликов Т клеток. Ни один из этих добровольцев не подвергался ранее воздействию малярии. Из этих 24 индивидуумов 10 участвовали в описанном выше втором клиническом испытании вакцины P Все 24 добровольца получали две инъекции вакцины RTS,S через 0 и 8 недель с помощью внутримышечной инъекции в левую дельтавидную мышцу. Вакцина RTS,S содержала аминокислоты 207 по 395 белка CSP Plasmodium falciparum (NF54/3D7), слитого с поверхностным антигеном гепатита В (HBsAg). Вкратце, белок RTS,S является гибридным белком, включающим практически всю С-терминальную часть белка CS, четыре или более тандемных повтора иммунодоминантной зоны и HBsAg. Общее описание подготовки RTS,S приводится в WO 93/10152 и патенте США 5,928,902, которые включены здесь в виде ссылки. Экспрессия получаемого рекомбинантного белка RTS,S осуществлялась в дрожжах (99), и он объединялся с иммуностимулирующим липидом А монофосфорила и QS21 в масловодяной эмульсии (Глаксо СмитКлайн Инк., Риксенсарт, Бельгия) для производства вакцины RTS,S. Конкретно, лиофилизированный (высушенный в вакууме) состав содержал гранулу RTS,S и адъювантный разбавитель. Гранула содержала RTS,S (50 мкг) и лактозу (3,15%) в качестве криозащиты. Адъювантный разбавитель содержал MPL (50 мкг), QS-21(50 мкг) и масловодяную эмульсию. Получаемые составы вакцины включали 50 мкг RTS,S в 1 мл объема эмульсии и готовились за 30 минут до введения. Три добровольца с несогласованным главным комплексом гистосовместимости человека (HLA) не получали ни вакцину ДНК P Был ряд эпитопов Т клеток, содержащихся в восходящей области последовательности P Примеры 2-7 детально описывают анализы, которые впоследствии были произведены на образцах крови, взятых у каждого из добровольцев. Вкратце, отклики Т клеток исследовались через 12-14 месяцев после последней дозы вакцины ДНК P Пример 2 Отклики ЦТЛ (цитотоксического Т лимфоцита) Как обсуждалось ранее, иммунизация только вакциной RTS,S индуцирует отклики антител и зависящие от гамма-интерферона (IFN- Анализ выхода хрома in vitro выполнялся, как было написано ранее (105). Конкретно, для генерации эффекторных клеток, 20% всех РВМС инфицировалось ALVAC, производящим экспрессию P Синтетические пептиды при 80-95% чистоте использовались для сенсибилизации мишеней ЦТЛ и были получены от Хирон Технолоджиз (Клейтон, Виктория, Австралия). Было использовано восемь пептидов, произведенных из P Создание вторичного иммунного отклика индуцированных ДНК ЦТЛ памяти путем стимулирования RTS,S Никаких ЦТЛ не детектировалось в примированных ДНК или непримированных добровольцах непосредственно перед приемом вакцины RTS,S. Никаких откликов ЦТЛ не было детектировано в любых из 14 непримированных добровольцах, которые получали только вакцину RTS,S. Антиген-специфические и генно-ограниченные отклики ЦТЛ были детектированы в 5/10 примированных ДНК добровольцах (фиг.1с). Один из 5 отвечающих организмов (респондеров) имел ЦТЛ (V6) через одну неделю после первой дозы, и другие имели ЦТЛ после второй дозы RTS,S. Частота откликов ЦТЛ (7/113 анализов, 6,2%) была значительно больше в примированных ДНК добровольцах (Р=0,0047) по сравнению с непримированными добровольцами (0/125 анализов, 0%). Частота откликов ЦТЛ была сопоставима с частотой, которая наблюдалась после иммунизации только ДНК среди 15 добровольцев, которые получили 3 дозы вакцины ДНК РfCSP за 12-14 месяцев (30/458 анализов, 6,6%) (107). Величина ЦТЛ в добровольцах, которые были примированы ДНК и стимулированы RTS,S (диапазон процентно-специфического лизиса [среднегеометрическое значение]: 11,4-28,1 [15,4] был также в том же диапазоне, что и индуцированный только иммунизацией ДНК (10,5-90,0 [15,6]). Вакцина RTS,S не содержала эпитопы Т клетки CD8+, связанные с наивысшим преобладанием отклика в двух предшествующих исследованиях (105, 107). Были детектированы отклики ЦТЛ на все 4 определенных P Среди 5 примированных ДНК добровольцев, которые имели положительные отклики ЦТЛ после стимулирования вакциной RTS,S, 3 добровольца не имели предшествующее детектируемой активности ЦТЛ против тех же эпитопов, когда они тестировались через 2 и 6 недель после второй и третьей дозы иммунизации ДНК P Стимулированный RTS,S отклик ЦТЛ шире, чем примированный ДНК отклик ЦТЛ Из 5 добровольцев, примированных ДНК, которые имели положительные отклики ЦТЛ после стимулирования вакциной RTS,S, три из них (V3, V6 и V8) откликались на эпитопы после стимулирования RTS,S, на которые не откликались после примирования ДНК. Конкретно, отклики ЦТЛ считались положительными только если процентно-специфический лизис после иммунизации был Как обсуждалось ранее, специалисты в данной области не рассматривали основанные на белках вакцины как эффективные для стимуляции откликов ЦТЛ. Подобным же образом, основанные на белке вакцины, ранее считались неэффективными для стимуляции отклика Т клетки CD8+. В отличие от того, что было известно, вышеприведенные данные четко демонстрируют, что после примирования ДНК RTS,S может стимулировать отклики ЦТЛ на новые эпитопы ЦТЛ. Частота и величина пептидно-специфических откликов IFN- Пример 3 Отклики IFN- Отклики IFN- При использовании здесь, термин «частота положительных отвечающих организмов (респондеров)» в анализе ELISPOT на IFN- РВМС (мононуклеары периферической крови), изолированные за 1-2 недели до, и 1, 2 и 6 недель после, первой и второй доз вакцины RTS,S использовались в анализе ELISPOT (иммуноферментном спот-анализе). В этих анализах РВМС инкубировались с 8 определенными пептидами P Примированные ДНК или непримированные добровольцы не имели детектированных P
После второй дозы вакцины RTS,S отклики IFN- На уровне эпитопа отклики IFN- Как видно из Таблицы 2, отклики IFN-
Также, как показано в Таблице 2, отклики IFN- Отклики IFN- Подобным же образом, после двух доз вакцины RTS,S, не было разницы в частоте положительно откликающихся индивидуумах между примированной ДНК группой и группой только с RTS,S (8/10 против 11/13). См. Таблицу 1. Индивидуумы в примированной ДНК группе откликались на значительно большее число испытываемых пептидов, чем добровольцы, которые получали только вакцину RTS,S. Из 8 респондеров в 10 примированных ДНК добровольцах, один имел отклики против всех четырех испытываемых пептидов 15-20 аминокислот, один откликался на три пептида, 5 на два пептида и только один откликался на один пептид. Из 11 респондеров в 13 непримированных добровольцах, один откликался на 3 пептида, два откликались на 2 пептида и восемь откликались только на один пептид (2/8 откликались на DR.316 и 6/8 откликались на DR.363). В целом 7 из 8 примированных ДНК добровольцев по сравнению с 3 из 11 непримированных добровольцев откликались на, по крайней мере, два испытываемых пептида (р=0,0094). Пример 4 Отклики IFN- RTS,S является слитым белком части P
В непримированных добровольцах отклики IFN- Как это видно из Таблицы 3, отклики IFN- В примированных ДНК добровольцах, которые также имели положительную реакцию на HBsAg, число положительных анализов после первой дозы RTS,S было больше на HBsAg, чем на P Пример 5 Вакцина ДНК индуцирует отклики как типа Тс1 (СD8+), так и отклики типа Тh1 (CD4+), в то время как RTS,S индуцирует только отклики Тh1 у человека Как одна вакцина ДНК P Т клеточные профили откликов IFN- Анализы ELISPOT выполнялись с РВМС обедненных Т клеток CD4+ или CD8+ до культивирования с пептидами, используя покрытые анти-CD4+ или анти-CDS4+ Dynabeads М-450 (Динал Инк., Грейт Нек, Нью-Йорк). Уровни экспрессии IFN- Для количественного определения IFN- (hIFN-g-F, TTGGTGATGATTTGAACATTGGA, последовательность hIFN-g-R, CCCAGTTCCTGCAGAGTAGAAAA, последовательность hGAPDH,5’GAAGGTGAAGGTCGGAGTC, последовательность hGAPDH-R,GAAGATGGTGATGGGATTTC последовательность пробы: (проба hIFN-g:TGTCACTTGCAAACACACAGCTTGTCGAA, последовательность проба hGAPDH:CAAGCTTCCCGTTCTCAGCC, последовательность Обедненные популяции Т клетки инкубировались с определенными пептидами P Индуцирование in vitro откликов IFN- Уровни экспрессии IFN- Проведя параллельные анализы с двумя стандартами, как описано выше, мы выяснили профили Т клетки для откликов IFN- Уровни экспрессии IFN- Отклики IFN- Уровни экспрессии IFN- Пример 6 Примирование ДНК/стимулирование RTS,S расширяет репертуар Т клеток, производящих IFN- Репертуар Т клеток, производящих гамма-интерферон (IFN- CD8+)зависел только от Т клетки CD4+ в добровольцах, иммунизированных либо только вакциной P Отклики IFN- В индукционной фазе in vitro детектировались как зависящие от Т клетки CD4+, так и от Т клетки CD8+ отклики IFN- В целом, позитивное регулирование IFN- Приведенные выше данные демонстрируют зависящие от Т клетки CD8+ отклики IFN-
Критерии подсчета отклика основаны на статистически значимом увеличении (р<0,05) с точки зрения (1) частоты положительных респондеров, (2) частоты положительных анализов, и (3) величины положительных откликов по сравнению с базовой линией, а также (4) значительного увеличения откликов IFN- Пример 7 Отклики антитела в примированных ДНК/стимулированных RTS,S добровольцах Отклики антитела на высушенные на воздухе спорозоиты Р.falciparum оценивались перед иммунизацией RTS,S и через 2, 4, 6 и 8 недель после первой и 1, 2, 4 и 6 недель после второй дозы RTS,S. Титры антител определялись непрямым флуоресцентным тестом антител (IFAT), как это было описано ранее (33). Как и ожидалось, титры антител были превосходные, хотя имела место некоторая переменчивость в откликах антител среди групп (фиг.5). Титры имели пик через 44 недели после второй дозы вакцины RTS,S при геометрическом среднем титров в диапазоне от 5120 до 20480. Однако не было статистически значимой разницы в титрах антител против всех спорозоитов в любой момент времени с одним исключением. Через 2 недели после первой дозы геометрический средний титр антител, определенный IFAT, 3225, в группе добровольцев, которые никогда не принимали P Заключение Процесс разработки эффективной, устойчивой вакцины против такой инфекции как Р.falciparum, Mycobacterium tuberculosis и ВИЧ, оказался более медленным, более трудным и сложным, чем ожидалось. Вышеупомянутый анализ изобретения демонстрирует, что примирование P Этот анализ показывает, что примированные ДНК специфические к P Результаты также дают основания полагать, что примирование ДНК/стимулирование RTS,S расширяет репертуар производящих IFN- CD4+ отклики CD8+ типа 1, а только RTS,S индуцировала отклики CD4+ типа 1. Однако примирование ДНК и стимулирование RTS,S индуцировало обе схемы откликов IFN- Т клетки CD4+ могут функционировать в качестве фоновой (отвечающей на данный антиген) клетки помощника для производства IFN- Представленные здесь результаты дают основания полагать, что примирование может направлять послестимуляционные отклики на примированный антиген. Что касается иммунизации RTS,S, это кажется особенно важным. RTS,S была сконструирована с HBsAg в качестве носителя, который бы усиливал отклики Т клеток на антиген малярии P Сравнение откликов IFN- Теперь значительные усилия направлены на создание рекомбинантных слитых белков и рекомбинантных вирусов и бактерий, которые осуществляют экспрессию намеченных белков. Во многих случаях для HBsAg, вакцинальной болезни, полиовируса и Salmonella typhi, иммунизированные индивидуумы имели ранее существовавшие антитела против этих основных компонентов вакцины. Тот факт, что в индивидуумах с антителами на основной компонент вакцины (например, HBsAg,), примирование ДНК, кодирующее намеченные белки, значительно усиливало иммунные отклики Т клетки на эти белки по сравнению с примированием только рекомбинантным белком, может быть преимуществом данной стратегии иммунизации примирования и стимулирования.
Примирование иммунных откликов с использованием ДНК в качестве вакцины позволяет фокусировать первоначальные отклики Т клетки на рекомбинантном иммуногене просто потому, что это единственный посторонний белок, экспрессия которого была осуществлена в вакцине ДНК. Хотя рекомбинантный RTS,S или вирусы оспы могут быть внутренне более иммуногенными, чем векторы ДНК в качестве средства переноса вакцины, инфицированные вирусом клетки производят большое количество полученных от вирусов эпитопов, которые конкурируют с рекомбинантным иммуногеном за доминирование антигенной специфичности на поверхности Т клетки. Многие индивидуумы, принимающие вакцину, наиболее вероятно подвергались воздействию антигенам носителям, или получали другие вакцинации, содержащие антиген в рекомбинантном вирусе или белке, так что эффекторный отклик на антигены носители будет препятствовать индуцированию откликов на специфические антигены. В данном исследовании антиген-специфичная клетка помощник CD4+, зависимые от Т клетки CD8+ отклики ЦТЛ и IFN- Следующие публикации, а также упомянутые в любом другом месте данной заявки, конкретно включаются в данный материал в виде ссылки. 1. Агуяр Дж.С, Хедстром Р.С., Роджерс В.О., Чароенвит Й., Саци Дж.Б. младший, Ланар Д.Е., Маджам В.Ф., Стоут P.P. и Хоффман С.Л. Усиление иммунного отклика в кроликах на вакцину ДНК малярии путем иммунизации безыгловым устройством. Вакцина 20: 275-80 (2001). 2. Айду М., Лалвани А., Олсопп С.Е, Плебански М., Мейснер С.Дж., Крауса П., Броунинг М., Морис Джонс С., Готч Д.А., Фидок Д.А. и др., Идентификация консервированного антигенного компонента для цитотоксической индуцирующей Т лимфоциты вакцины от малярии. Лансет 345: 1003 (1995). 3. Яман Ф., Гентон Б., Андерс Р., Фальк М., Триглия Т., Льюис Д. и др. Отношение между гуморальным откликом на мерозоитный поверхностный антиген Plasmodium falciparum и заболеваниями малярии в высокоэндемичной области Папуа Новой Гвинеи. Американский журнал тропической медицины, 51: 593 (1994). 4. Эл Яман Ф., Гентон Б., Андерс Р., Тарайка Дж., Гинни М., Меллор С. и др. Оценка роли гуморального отклика на Plasmodium falciparum MSP2 по сравнению с RESA и SPf66 в защите детей района Папуа Новой Гвинеи от клинической малярии. Парсит Иммунол 17: 493 (1995). 5. Андерс Р.Ф. Грюзер П.Е., Эдвардс С., Маргеттс М., Мэтью М.Л., Полок Б., Пай Д. Иммунизация рекомбинантным АМА-1 защищает мышей от инфекции Plasmodium Chabaudi. Вакцина 16 (2-3): 240-7 (1998). 6. Бароуч Д.Х., и др. Контроль виремии (наличия вируса в крови) и профилактика клинического ВИЧ в макаках-резус цитокиновой, усиленной ДНК, вакцинацией. Наука. 290, 486-92 (2000). 7. Блекман М.Дж., Хейдерик Х.Г., Доначи С., МакБрайд Дж.С. и Холдер А.А. Отдельный фрагмент поверхностного белка мерозоита малярии остается на паразите во время захвата красной кровяной клетки и является целью антител, ингибирующих захват. Журнал экспериментальной медицины. 172Ж379 (1990). 8. Боджанг К.А., Миллиган П.Дж., Пиндер М., Вигнерон Л., Аллоуче А., Кестер К.Е., Баллоу В.Р., Конвей Д.Дж., Риис В.Х., Готар П., Яаммуах Л., Делчасмбер М., Восс Г., Гринвуд В.М., Хилл А., Мак Адам К.Р., Торниепорт Н., Кохен Дж.Д., Дохерти Т. Команда испытания вакцины RTS,S против малярии. Эффективность RTS,S/AS03 вакцины против малярии против инфекции Plasmodium falciparum в полуиммунных взрослых мужчинах в Гамбии: рандомизированное испытание. Ланцет 358: 1927-34 (2001). 9. Бразолот Милан КЛ., Виратна Р., Крег А.М., Сигрист С.А., Дейвис Х.Л. ДНК CpG может индуцировать сильные гуморальные и клеточные иммунные отклики Th1 против поверхностного антигена гепатита В в молодых мышах. Proc Natl Acad Sci USA 95: 15553-8 (1998). 10. Бернс Дж.М., Делай Т.М., Вайдия А.В. и Лонг СА. 3’порция гена поверхностного антигена мерозоита Plasmodium yoelii кодирует эпитоп, распознаваемый защитным моноклинальным антителом. Proc Natl AcadSci USA 5:602 (1988). 11. Каларота С. и др. Клеточный цитотоксический отклик, индуцируемый вакцинацией ДНК в зараженных ВИЧ-1 пациентах. Ланцет 351:1320-25 (1998). 12. Чанг С.П., Кейс С.Е., Госнелл В.Л., Хашимото А., Крамер К.Дж., Тем Л.К., Хаширо К.К., Никайдо С.М., Гибсон Х.Л., Ли НГ С.Т, Барр П.Дж., Йокота В.Т., и Хат Г.С. Рекомбинантный бациловирус в 42-килодалтон С-терминального фрагмента поверхностного белка 1 мерозоита Plasmodium falciparum защищает обезьян Aotus против малярии. Infect. Immun. 64:253 (1996). 13. Чароенвит Й., Лиф М.Л., Яан Л.Ф., Седегах М. и Бодуа Р.Л. Характеристика моноклинальных антител Plasmodium yoelii, направленная против специфичных к стадии антигена спорозоитов. Infect. Immun. 55: 604 (1987). 14. Чароенвит Й., Коллинз В.Е., Джонс Т.Р., Миллет П., Яан Л., Кемпбелл Г.Х, Бодуа РЛ., Бродерсон Дж.Р. и Хоффман. Неспособность малярийной вакцины индуцировать антитела на защитный эпитоп в рамках его последовательности. Наука. 251: 668 (1991). 15. Чароенвит Й., Меллоук С., Коул С., Бечара Р. и др. Plasmodium yoelii: 17-kD белок гепатитной и эритроцитовой стадии является мишенью ингибирующего моноклинального антитела. Exp Parasitol. 80: 419-429 (1995). 16. Чароенвит Й., Фалларм Маджам В., Коррадин Г.П. и др. Зависимая от Т клетки CD4+ и гамма-интерферона защита против малярии у мышей путем иммунизации линейным синтетическим пептидом из Plasmodium yoelii 17 килодалдон гепатоцитного эритроцитного белка. Infect. Immune. 67: 5604-5614 (1999). 17. Кларк Дж. Т., Доначи С., Ананд Р. и др. Гликопротеин 46063 kD от поверхностных мерозоитов Plasmodium falciparum. Молекулярная биохимия 32: 15-24 (1988). 18. Коллинз В.Е., Галланд Г.Г., Салливан Дж.С. и Моррис С.Л. Выбор различных штаммов Plasmodium falciparum для тестирования вакцин кровяной стадии в обезьянах Aotus Nancymai. Американский журнал тропической медицины 51: 224-232 (1994). 19. Коллинз В.Е., Пай Д, Крютер П.Е., Ванденберг К.Л. Галланд Г.Г., Шулзер А.Дж., Кемп Д.Дж., Эдвардз С.Дж, Коппель Р.Л., Салливан Дж.С., Моррис С.Л. и Андерс Р.Ф. Защитный иммунитет, индуцированный у обезьян с рекомбинантным обезьяньим мембранным антигеном 1 Plasmodium fragile. Американский журнал тропической медицины 51: 711-719 (1994). 20. Дали Т.М. и Лонг С.А. Рекомбинантный 15 килодалтон карбоксильно-терминальный фрагмент поверхностного белка 1 мерозоита Plasmodium yoelii 17 XL индуцирует защитный иммунный отклик у мышей. Infect. Immune. 61: 2462-2467 (1993). 21. Дейм Дж.Б., Вильямс Дж.Л., МакКатчер Т.Ф., Вебер Дж.Л., Виртц Р.А., Хокмейер В.Т., Маллой В.Л., Эейнс Дж.Д., Шнайдер И., Робертс Д. Структура гена, кодирующего иммунодоминантный поверхностный антиген на спорозоите паразита малярии человека Plasmodium falciparum. Наука. 225 (4662): 593-9 (1984). 22. Дауберсис П., Томас А.В., Миллет П, Брахими К., Лангерманс Дж.А., Олломо Б., БенМохамед Л., Слиерендрегт Б., Эллинг В., Ван Белкам А., Дубрейл Дж.Ф., Мейз Дж.Ф., Герин-Мэрчанд С., Кайфас С., Кохен Дж., Грас-Массе X., Друилхе П. и Мохаммед Л.Б. Защита от малярии Plasmodium falciparum в шимпанзе путем иммунизации консервированным предэритроцитным антигеном 3 печеночной стадии. Nat Med. 6: 1258-63 (2000). 23. Дейвис Х.Л., Веератна Р., Вальдшмит Т.Дж., Тигретт Л., Шорр Дж., Крейг AM., Вееранта Р. ДНК CpG является сильным усилителем специфического иммунитета в мышах, иммунизированных рекомбинантным поверхностным антигеном гепатита В. Журнал иммунологии. 160: 870-6 (1998). 24. Динз Дж.А. Защитные антигены кровяной фазы паразитов Plasmodium knowlesi. Philos.Trans.R.Soc.Lond.Biol. 307: 159-169 (1984). 25. Динз Дж.А., Найт А.М., Джин B.C., Вотерз А.П., Кохен С. и Митчелл Г.Х. Испытание вакцинации в резус-макаках с помощью малого, инвариантного, антигена мерозоита Plasmodium knowlesi 66 kD. Parasite Immunol. 10: 535-552 (1988). 26. Делплейс П., Бхатия А., Кагнарт М. и др. Белок р126: антиген паразитофорной вакуоли, связанный с выходом мерозоитов Plasmodium falciparum. Биология клетки 64: 215 (1987). 27. Дулан Д.Л., Седеган М., Хедстром Р.С., Хобарт Р., Чароенвит Й. и Хоффман С.Л. Вводящие в заблуждение генетические ограничения защиты против малярии с помощью иммунизации мильтигенной ДНК: иммунитет, зависимый от Т клетка CD8+, гамма-интерферона и оксида азота. Журнал экспериментальной медицины. 183: 1739-1746 (1996). 28. Дулан Д.Л., Хедстром Р.С., Роджерз В.О., Чароенвит Й., Роджерз М., де ла Вега П. и Хоффман С.Л. Идентификация и характеристика защитного гепатоцитоэритроцита гена белка 17 kD Plasmodium yoelii гомолога экспортированного белка 1 Plasmodium falciparum. Журнал биохимии. 271617861-17868 (1996). 29. Дулан Д.Л., Хоффман С.Л., Саузвуд С., Вентворз П.А., Сидней Дж., Чеснат Р.В., Кеогх Е., Апелла Е., Натман Т.Б., Лал А.А., Гордон Д.М., Олоо А. и Сете. Дегенеративные цитотоксические эпитопы Т клетки от Р.falciparum, ограниченные супертипами аллелей HLA-A и HLA-B. Иммунитет 7: 97-112 (1997). 30. Дулан Д.Л., Хедстром Р.С., Гарднер М.Дж., Седегах М., Ванг X., Грамзински Р.А., Маргалит М., Хобарт П. и Хофманн С.Л. Вакцинация ДНК как подход к контролю малярии: текущее состояние и стратегии. Curr Topic Microbiol Immunol 226: 37-56 (1998). 31. Дулан Д.Л., Хоффман С.Л. Клетки Il-12 и NK требуются антиген- специфического адаптивного иммунитета против малярии, инициированного Т клетками CD8+ в модели Plasmodium yoelii. Журнал иммунологии 164(2): 884-92 (1999). 32. Эган Дж.Е., Вебер Дж.Л., Баллой В.Р., Холлингдейл М.Р., Маджариан В.Р., Гордон Д.М., Маллой В.Л., Хоффман С.Л., Вирц Р.А., Шнейдер И., Вуллетт Г.Р., Янг Дж.Ф. и Хокмейер В.Т. Эффективность спорозоитных вакцин от мышиной малярии: подтекст для разработки вакцин для человека. Наука. 236: 453-456 (1987). 33. Эпштейн Дж., Горак Е., Чароенвит Й., Ванг Р., Фрейдберг Н., Осиново О., Ричи Т.Л., Штольц Е., Треспаласиос Ф., Нергес Дж., Нг Дж., Фалларме-Маджам В., Абот Э., Гох Л., Паркер С., Кумар С., Хедстром Р., Норманн Дж., Стаут Р., Хоффман С.Л. Безопасность, переносимость и отсутствие откликов антител после приема противомалярийной вакцины P 34. Этлингер Х.М., Касперс П., Матиль X., Шонкльд Х.Дж., Стубер Д. и Такас Б. Способность рекомбинантных или природных белков защищать обезьян от гетерологового вызова с помощью Plasmodium falciparum. Infect. Immun. 59: 3498-3503 (1991). 35. Фриман P.P. и Холдер А.А. Характеристика защитного отклика мышей BALB/c, иммунизированных очищенным антигеном Plasmodium yoelii schizont. Clin. Exp. Immunol. 54: 609-616 (1983). 36. Гордон Д.М., МакГоверн Т.В., Кржич У., Кохен Дж.С., Шнайдер И., ЛаШанс Р., Хеппнер Д.Г., Йан Г., Холлингдейл М., Слаою М. и др. Безопасность, иммуногенетичность и эффективность рекомбинантно произведенной вакцины циркумспорозоита Plasmodium falciparum поверхностного антигена гепатита В. Журнал инфекционных заболеваний 171: 1576-85 (1995). 37. Грамзински Р.А., Марис Д.С., Дулан Д., Чароенвит Й., Обалдия Н., Россан Р., Седегах М. Ванг Р. Хобарт П., Маргалит М. и Хоффман С. Малярийные вакцины ДНК в обезьянах Aotus. Vaccine. 15: 913-915 (1997). 38. Гурунатан С., Bу С.И., Фрейдаг Б.Л. & Седер Р.А. Вакцины ДНК: ключ к индуцированию долговременного целлюлярного иммунитета. CurrOpin Immunol. 12, 442-7 (2000). 39. Харниутанакорн П., МакБрайд Дж.С., Доначи С., Хейдрич Х.Г., Ридли Р.Г. Ингибиторные моноклональные антитела распознают эпитопы, примыкающие к протеолитовым местам дробления клеток на белке RAP-1 Plasmodium falciparum. Mol Biochem Parasitol. 55: 177-86 (1992). 40. Хедстром Р., Дулан Д., Ванг Р. и др. Экспрессия in vitro и in vivo иммуногенетичности вакцин ДНК предэритроцитной стадии Plasmodium falciparum. Int J Molec med. 2: 29-38 (1998). 41. Херрингтон Д., Дейвис Дж., Нардин Е., Бейер М., Кортез Дж. Едди X., Лосонски Г., Холлингдейл М., Штейн М., Левин М., Нуссензвейг Р.С., Клайд Д. и Эделман Р. Успешная иммунизация людей облученными спорозоитами: гуморальные и клеточные отклики защищенных индивидуумов. Американский журнал гигиены тропической медицины. 45: 539-547 (1991). 42. Хилгерз Л.А., Сниппе X., Джансзе М., Виллерз Дж.М. Синергетический эффект синтетических адъювантов на гуморальный иммунный отклик. Int Arch Allergy Appl Immunol. 79: 392-6 (1986). 43. Хилгерз Л.А., Сниппе X., Джансзе М., Виллерз Дж.М. Синтетические сульфолипополисахариды: новые адъюванты для гуморальных иммунооткликов. Иммунология. 60: 141-6 (1987). 44. Хилл А.В.С., Элвин Дж., Виллис А.С. и др. Молекулярный анализ ассоциации HLA-В53 и сопротивляемости тяжелой малярии. Природа 360: 434 (1992). 45. Хоффман С.Л. и Дулан Д.Л. Малярийные вакцины – нацеленность на инфицированные гепатоциты. Nature med. 6: 1218-19 (2000). 46. Холдер А.А. и Фриман P.P. Иммунизация против родентной малярии кровяной стадии с использованием очищенных антигенов паразитов. Природа 294: 361-364 (1981). 47. Хорн Н.А., Мик Дж.А., Будахазие Г., Маркет М. Генная терапия рака с использованием плазмида ДНК для клинических испытаний на человеке. Генная терапия человека 6(5): 565-73 (1995). 48. Инселбург Дж., Бзик Д.Дж., Ли В.Г., Грин К.М., Кансопон Дж., Хахм В.К., Батурст И.С., Барр П.Дж. и Россан Р.Н. Защитный иммунитет, индуцированный в обезьянах Aotus рекомбинантными белками SERA Plasmodium falciparum. Infect. Immun. 59: 1247-150 (1991). 49. Инселбург Дж., Батурст И.С., Кансопон Дж., Барчфельд П.Дж. и Россан Р.Н. Защитный иммунитет, индуцированный в обезьянах Aotus рекомбинантным белком SERA Plasmodium falciparum: адъювантные эффекты на индуцирование защитного иммунитета. Infect. Immun. 61: 2041-2047 (1993). 50. Кедизрски Л., Блек С.Г. и Коппель Р.Л. Иммунизация рекомбинантным поверхностным протеином мерозоита Plasmodium yoelii 4/5 защищает мышей от опасности летального исхода. Infect. Immun. 68: 6034-7. 51. Кензил С.Р., Пател У. Ленник М., Марциани Д. Выделение и характеризация сапонинов с помощью адъювантной активности от кортекса Quillajasaponaria Molina. Журнал иммунологии. 146: 431-7 (1991). 52. Кензил С.Р. Сапонины как адъюванты вакцин. Crit Rev Ther Drug Carrier Syst., 12: 1-55 (1996). 53. Кестер К.Е., МакКини Д.А., Торнипорт Н., Окенхауз С.Ф., Хеппнер Д.Г., Холл Т., Крзич У., Делчамбр М., Восс Г., Доулер М.Г., Паленски Дж., Виттес Дж., Кохен Дж., Баллоу В.Р. Группа оценки малярийной вакцины RTS,S. Эффективность режимов вакцины рекомбинантного белка циркумспорозоита от экспериментальной малярии Plasmodium falciparum.J Infect Dis 183 (4): 640-7 (2001). 54. Кестер К.Е. и др. Эффективность режимов вакцины рекомбинантного белка циркумспорозоита против экспериментальной малярии Plasmodium falciparum. J Infect Dis 183 (4): 640-47 (2001). 55. Хусмит С., Чароенвит Й., Кумар С., Седегах М., Бодуа Р.Л. и Хоффман С.Л. Защита от малярии путем вакцинации поверхностным белком 2 спорозоита плюс белком CS. Science 252: 715-718 (1991). 56. Хусмит С., Седегах М. и Хоффман С.Л. Полная защита от Plasmodium yoelii путем адоптивного трансфера клона цитотоксической Т клетки CD8+ распознающего поверхностный белок 2 спорозоита. Infect. Immun. 62: 2979-2983 91994). 57. Крайг А.М., Йи А.К., Матсон С., Валдшмит Т.Дж., Бишоп Г.А., Тисдейл Р., Корецки Г.А., Клинман Д.М. Мотивы CpG в бактериальной ДНК запускают прямую активацию В-клетки. Природа. 374-546-9 (1995). 58. Кумар С., Яадава А., Кейстер Д.В., Тиан Дж.Х., Охл М., Пердю Гринфилд К.А., Миллер Л.Х. и Каслов Д.С. Иммуногенетичность и эффективность in vivo рекомбинантного поверхностного белка-1 мерозоита Plasmodium falciparum в обезьянах Aotus. Mol. Med. 1: 325–332 (1995). 59. Кумар С., Коллинз В., Эган А., Яадава А., Гаррауд О., Блекман М.Дж., Патино Дж.А., Диггз С., Каслов Д.С. Иммуногенетичность и эффективность в обезьянах Aotus четырех рекомбинантных вакцин Plasmodium falciparum в многоадъювантных составах, основанных на 19-килодалтон С терминале поверхностного белка 1 мерозоита. Infect. Immun. 68-2215-2223 (2000). 60. Локейл-Дюбуа М. и Вагнер X. Обзор биологической и фармакологической активности сапонинов. Фитомедицина 2:363-386 (1996). 61. Лалвани А., Морис П., Восс Г., Патан А. и др. Потентная индукция фокусированных клеточных и гуморальных откликов типа Тh1 с помощью RTS,S/SBAS2, рекомбинантной малярийной вакцины Plasmodium falciparum. Журнал инфекционных заболеваний 180: 1656-64 (1999). 62. Ле Т., Кунан К., Хедстром Р. и др. Безопасность, переносимость и гуморальные иммунные отклики после внутримышечного введения малярийной вакцины ДНК здоровым взрослым добровольцам. Вакцина 18: 1893-1901 (2000). 63. Ли А.И. и др. Количественное определение числа цитотоксических Т клеток, специфических для иммунодоминантного специфического к HCV эпитопа ЦТЛ, примированного иммунизацией ДНК. Вакцина 18: 1962-68 (2000). 64. Люк С Дж., Карнер К., Лианг X., Барбур А.Г. Основанная на ospA вакцина ДНК защищает мышей от инфекции Borrelia burgdorferi. J Inf Dis 175: 191-7 (1997). 65. Маджарян В.Р., Дали Т.М. и др. Пассивная иммунизация против малярии у мышей с помощью моноклонального антитела IgG3. J Immunol 132: 3131 (1984). 66. Малик А., Эган Дж.Е., Хоугтен Р.А., Садофф Дж.С. и Хоффман С.Л. Цитотоксические Т лимфоциты человека против белка циркумспорозоита Plasmodium falciparum. Proc. Natl. Acad. Sci. USA 88: 3300-3304 (1991). 67. Мартин Т., Паркер С.Е., Хедстром Р. и др. Малярийная вакцина плазмида ДНК: потенциал для геномной интеграции после внутримышечной инъекции. Human Gen Ther 10: 759-68 (1999). 68. МакКлукси М.Дж., Дейвис Х.Л. CPG ДНК является потентным усилителем системных и слизистых иммунных откликов на поверхностный антиген гепатита В при внутриносовом введении мышам. Журналиммунологии. 161: 4463-6 (1998). 69. Морено А., Клавиджо П., Эделман Р., Дейвис Дж., Сзтейн М., Херрингтон Д. и Нардин. Цитотоксические Т клетки CD4+ от иммунизированного спорозоитами добровольца распознают белок CS Plasmodium falciparum. Int. Immunol. 3: 997-1003 (1991). 70. Мосманн Т.Р. и Коффман Р.Л. Клетки ТН1 и ТН2: различные картины секреции лимфокина приводят к различным функциональным свойствам. Годовой обзор иммунологии. 7: 145-173 (1989). 71. Мусти А.М., Зехнер 3., Бостиан К.А., Патресон Б.М. и Крамер Р.А. Транскрипционное картирование двух генов дрожжей, кодирующих глицералдегид 3-фосфат дигидрогеназу, изолированную гомологической последовательностью с геном цыпленка. Ген 25: 133-143 (1983). 72. Уврей С., Боухарун Таюн X., Грас Массе X. и др. Поверхностный белок 3-мерозоита: белок малярии, индуцирующий антитела, которые способствуют убиванию Plasmodium falciparum путем кооперации с моноцитами крови. Кровь 84: 1594 (1994). 73. Уврей С., Боухарун Таюн X., Грас Массе X. и др. Новый поверхностный антиген мерозоита Plasmodium falciparum, идентифицированный антигенностью кооперативного механизма клеточного антитела и биологической активностью антител. Mem Inst Oswaldo Cruz. Дополнение 2: 77 (1994). 74. Панина-Бордигнон П., Тан А., Термиджтелен А., Демоц С., Коррадин Г., Ланзавечия А. Универсально иммуногенетичные эпитопы Т клетки: смешанное связывание с главным комплексом гистосовместимости (МНС) класса II и смешанное распознавание Т клетками. Eur J Immunol 12: 2237-42 (1989). 75. Паркер С.Е., Бореллини Ф., Венк М.Л., и др. Плазмид малярийной вакцины ДНК: распределение тканей и исследование безопасности на мышах и кроликах. Human Gen Ther 10 (5): 741-58 (1999). 76. Перин Л.Х., Дайал Р. и Райдер X. Характеристика антигенов от эритроцитных стадий Plasmodium falciparum, вступающих в реакцию с иммунными сыворотками человека. Trans. R.Soc. Trop. Med. Hyg. 75: 163-165 (1981). 77. Перин Л.Х., Рамирез Е., Ламберт П.Х. и Миесчер П.А. Ингибирование роста Plasmodium falciparum в эритроцитах человека с помощью моноклональных антител. Природа. 289: 301-303 (1981). 78. Поточнияк П., Йошида Н., Нуссензвейг Р.С. и Нуссензвейг В. Моновалентные фрагменты (Fab) моноклональных антител на поверхностный антиген спорозоита (Рb44) защищают мышей от малярийной инфекции. Журнал экспериментальной медицины 151: 1504-1513 (1980). 79. Белки – структура и молекулярные свойства, 2-ое издание, Т.Е.Крейгтон, В.X. Фриман и компания, Нью-Йорк, 1993. 80. Рамазами Р. Исследования гликопротеинов в паразите малярии человека Plasmodium falciparum – свойства связывания лектина и возможные карбогидратно-протеиновые связи. Immunol Cell Biol 65: 147 (1987). 81. Рамазами Р.Дж., Джонз Г., Лорд Р. Характеристика эпитопа, определенного ингибиторным моноклональным антителом на антиген кандидат на малярийную вакцину. Immunol Lett 23: 305 (1990). 82. Раттан и др. Синтез белков: пост-трансляционные модификации и старение. Ann NY Acad Sci 663: 48-62 (1992). 83. Фармацевтические науки Ремингтона, 18 издание (А.Геннаро, редактор; Мак Паб, Истон, Пенсильвания, 1990). 84. Ридли Р.Г., Такас Б., Етлинегр X., Скайф Дж.Г. Рофтри антиген Plasmodium falciparum имеет защитную реакцию в беличьих обезьянах (саймири). Паразитология 101: 187-92 (1990). 85. Родригес М.М., Кордей А.-С., Арреаза Г., Коррадин Г., Ромеро П., Мариянски Дж.Л., Нуссензвейг Р.С. и Завала Ф. Цитолитические клоны Т клетки CD8+,полученные от белка циркумспорозоита Plasmodium yoelii, защищают против малярии. Int. Immunol 3: 579-585 (1991). 86. Роджерз В.О. и др. Многоэтапная мультиантигенная гетерогенная примирующая и стимулирующая вакцина от малярии Plasmodium knowlesi обеспечивает частичную защиту в макаках-резус. Infect Immun 69: 5565-72 (2001). 87. Ромеро П., Мариянски Дж. Л., Коррадин Г., Нуссензвейг В. и Завала Ф. Клонированные цитотоксические Т клетки распознают эпитоп в белке циркумспорозоита и защищают против малярии. Природа 341: 323-325 (1989). 88. Саул А., Лорд Р., Джоунз Г.Л. и др. Защитная иммунизация инвариантными пептидами антигена MSA2 Plasmodium falciparum. J Immunol 148: 208 (1992). 89. Шофилд Л., Бушелл Г.Р., Купер Дж.А. и др. Рофтри антиген Plasmodium falciparum содержит сохраненные и разнообразные эпитопы, распознаваемые ингибиторными моноклинальными антителами. Mol Biochem Parasitol. 18: 183-95 (1986). 90. Шофилд Л., Виллакиран Дж., Ферейра А. и др. Гамма-интерферон, Т клетки CD8+ и антитела, необходимые для иммунитета к спорозоитам малярии. Природа 330: 664-666 (1987). 91. Седегах М. и др. Улучшение защитного иммунитета, индуцированного иммунизацией с основой на ДНК: примирование антигеном и кодирующим GM-CSF плазмидом ДНК и стимулирование производящим экспрессию антигена рекомбинантным вирусом оспы. J Immunol 164: 5905-12 (2000). 92. Седер Р.А. и Хилл А.В. Вакцины против внутриклеточных инфекций, требующие клеточного иммунитета. Природа 406, 793-8 (2000). 93. Сегуин М.С., Клотз Ф.В., Шнайдер И., Вейр Дж.П., Гудбари М., Слейтер М. и др. Индуцирование синтазы окиси азота защищает от малярии мышей, подвергнутых воздействию облученных инфицированных Plasmodium berghei комаров: участие гамма-интерферона и Т клеток CD8+. J Exp Med 180: 353-358 (1994). 94. Сейфтер и др. Анализ модификаций белка и небелковых кофакторов. Meth Enzymol 182: 626-646 (1990). 95. Ши Й.П., Сайд У., Квари С.Х., Робертс Дж.М., Удхаякумар В., Олоо А.Дж., Хаулей В.А., Каслов Д.С., Нахлен Б.Л. и Лал А.А. Природный иммунный отклик на С-терминальную 19-килодалтоновую область поверхностного белка 1 мерозоита Plasmodium falciparum. Infect. Immun. 64: 2716-2723 (1996). 96. Сиддикви В.А., Там Л.К., Крамер К.Дж., Хуи Г.С., Кейс С.Е., Ямага К.М., Чанг С.П., Чан Е.Б. и Канн С.К. Поверхностный пленочный белок предшественник мерозоита полностью защищает обезьян Aotus от малярии Plasmodium falciparum. Proc. Natl. Acad.Sci USA 84: 3014-3018 (1987). 97. Сим БКЛ., Орланди П.А., Хейнз Дж.Д. и др. Первичная структура антигена, связывающего эритроцит 175К Plasmodium falciparum и идентификация пептида, который выявляет антитела, которые ингибируют инвазию мерозоитов малярии. J Cell Biol III: 1877 (1990). 98. Сим БКЛ., Читнис С.Е., Дил С.Д. и др. Plasmodium falciparum: дальнейшая характеристика функционально активной зоны лиганда мерозоита. ЕВА-175 78: 259 (1994). 99. Стаут Дж.А., Слауи Д.Г., Хеппнер Д.Г. и др. Предварительная оценка рекомбинантной вакцины белка циркумспорозоита против малярии Plasmodium falciparum. N Eng J Med 336: 86-91 (1997). 100. Стаут Дж.А., Кестер К.Е., Крзич У. и др. Долговременная эффективность и иммунные отклики после иммунизации малярийной вакциной RTS,S. J Infect Dis 178: 1139-44 (1998). 101. Томас А.В., Трейп Дж.Ф., Роджер С., Гонкалвес А., Росарио В.Е., Нарум Д.Л. Высокое преобладание природных антител против мембранного обезьяньего антигена 83 килодальтон Plasmodium falciparum, (РF83/АМА-1)детектированного захватным, связанным с ферментами, иммуносорбентным анализом с использованием полный рекомбинантный бациловирус PF83/AMA-1. Am J Trap Med Hyg 51: 730-40 (1994). 102. Томас А.В., Нарум Д., Вотерз А.П., Трейп Дж.Ф., Роджер С., Гонкалвес А., Розарио В., Друилхи П., Митчелл Г.Х. Денис Д. Аспекты иммунитета для семейства АМА-1 молекул у человека и приматов, заряженных малярией. Mem Inst Oswaldo Crus 89 дополнение 2: 67-70 (1994). 103. Валензуэла П., Грей П., Куирога М. и др. Нуклеотидные последовательности кодирования генов для мажорного белка поверхностного антигена вируса гепатита В. Природа. 280: 815-819 (1979). 104. Ванг Р., Чароенвит Й., Коррадин Г., де ла Вега П., Франке Е.Д. и Хоффман С.Л. Защита от малярии индуцированием Т клетки CD4+ линейным пептидом 2 поверхностного белка спорозоита Plasmodium yoelii и зависимым от IFN-гамма удалением инфицированных гепатоцитов. Журнал иммунологии. 157: 4061-4067 (1996). 105. Ванг Р., Дулан Д.Л., Ле Т.П., Хедстром Р.С., Кунан К.М., Чароенвит Й., Джонс Т.Р., Хобарт П., Маргалит М., Нг Дж., Вейсс В.Р., Седегах М., де Трайсне С., Норманн Дж.А. и Хоффман С.Л. Индуцирование антиген-специфичных цитотоксических Т лимфоцитов в человеке с помощью малярийной вакцины ДНК. Наука. 282: 476-480 (1998). 106. Ванг Р., Дулан Д.Л., Чароенвит Й., Хедстром Р.С., Гарднер М Дж., Хобарт П., Тайн Дж., Седегах М., Фалларм В., Саци Дж.В. младший. Каур М., Клинман Д.М., Хоффман С.Л., Вейсс В.Р. Одновременное индуцирование множественных антиген-специфичных цитотоксических лимфоцитов у приматов путем иммунизации смесью четырех плазмидов ДНК Plasmodium falciparum 66: 4193-202 (1998). 107. Ванг Р., Эпштейн Дж., Барацерос Ф.М., Горак Е.Дж., Чароенвит Й., Каруччи Д.Дж., Хедстром Р.С., Рахарджо Н., Гей Т., Хобарт П., Стаут Р., Джонс Т.Р., Ричи Т.Л., Паркер С.Е., Дулан Д.Л., Норманн Дж., Хоффман С.Л. Индуцирование зависимых от Т клетки CD4+ откликов CD8+ типа 1 у человека с помощью малярийной вакцины ДНК. PNAS-USA 98(19): 10817-22 (2001). 108. Вейсс В.Р., Седегах М., Бодуан Р.Л., Миллер Л.Х., Гуд М.Ф. Т клетки CD8+ (цитотоксические/супрессоры) необходимы для защиты мышей, иммунизированных спорозоитами малярии. PNAS-USA 85(2): 573-6 (1988). 109. Вейсс В.Р., Берзофски Дж.А., Хаугтен Р.А., Седегах М., Холлиндейл М., Хоффман С.Л. Клон Т клетки, направленный на белок циркумспорозоита, который защищает мышей как от Plasmodium yoelii, так и Plasmodium berghei. J Immunol 15; 149(6): 2103-9 (1992). 110. Отчет ВОЗ. Состояние мировых вакцин и иммунизации. Женева: Всемирная организация здравоохранения (1996). 111. Визел Б., Роджерз В.О., Хайгтен Р.А., Ланар Д.Е., Тайн Дж.А. и Хоффман С.Л. Индуцирование мышиных цитотоксических Т лимфоцитов против поверхностного белка 2 спорозоита Plasmodium falciparum. Европейский журнал иммунологии. 2461487-1495 (1994). 112. Визел Б., Хаугхтен Р., Черч П., Тайн Дж.А., Ланар Д.Е., Гордон Д.М., Баллоу В.Р., Сетт А. и Хоффман С.Л. Ограниченные HLA-A2 цитотоксические отклики Т лимфоцита на множественные эпитопы поверхностного белка 2 спорозоита Plasmodium falciparum в иммунизированных спорозоитами добровольцах. Журнал Иммунологии. 155: 766-775 (1995). 113. Волд Ф. Пост-трансляционные модификации белка: перспективы и прогнозы, 1-12, в пост-трансляционных ковалентных модификациях белков. Б.С. Джонсон; издание Академик Пресс, Нью-Йорк. 1983. 114. Янг С., Коллинз В.Е., Салливан Дж.С. и др. Частичная защита от инфекции Plasmodium vivax на кровяной стадии в обезьянах саймири путем иммунизации рекомбинантным С-терминальным фрагментом поверхностного белка 1 мерозоита в блок кополимерном адъюванте. Infect Imm 67: 342 (1999). 115. Микробиология Зинссер 1180-83 (Волфганг К. Джоклик, Хилда П., Виллетт Д., Бернард Амос и Катрин М. Вилферт, 20 издание, Эплтон и Ландж 1992). Другие примеры осуществления изобретения будут очевидны специалистам в данной области из рассмотрения спецификации и практики использования раскрытого в ней изобретения. Предполагается, что спецификация и примеры будут рассматриваться только в качестве примеров, при том, что подлинный объем и дух изобретения указывается в следующей формуле.
Формула изобретения
1. Способ иммунизации человека против вызывающего малярию патогена, включающий: 2. Способ по п.1, отличающийся тем, что второй малярийный антиген включает весь или часть первого малярийного антигена. 3. Способ по п.1, отличающийся тем, что примирующая доза составляет между 0,01 мкг и 50 мг. 4. Способ по п.3, отличающийся тем, что примирующая доза составляет 2500 мкг. 5. Способ по п.3, отличающийся тем, что примирующая доза вводится между одним и 5 разами перед введением второй вакцины. 6. Способ по п.1, отличающийся тем, что стимулирующая доза составляет между 1 мкг и 100 мкг. 7. Способ по п.6, отличающийся тем, что стимулирующая доза составляет 50 мкг. 8. Способ по п.6, отличающийся тем, что стимулирующая доза составляет 25 мкг. 9. Способ по п.1, отличающийся тем, что примирующая вакцина вводится способом, выбранным из внутримышечного введения, внутривенного, внутрикожного, подкожного, слизистого, с помощью рекомбинантной бактерии, рекомбинантного вируса или генной пушки, или их комбинации. 10. Способ по п.1, отличающийся тем, что стимулирующая вакцина вводится способом, выбранным из внутримышечного введения, внутривенного, внутрикожного, подкожного, слизистого, с помощью рекомбинантной бактерии, рекомбинантного вируса или генной пушки, или их комбинации. 11. Способ по п.1, отличающийся тем, что Т клетки CD8+ включают цитотоксические Т лимфоциты. 12. Способ по п.1, отличающийся тем, что первый малярийный антиген включает, по крайней мере, фрагмент полипептида циркумспорозоита. 13. Способ по п.1, отличающийся тем, что второй малярийный антиген включает, по крайней мере, фрагмент полипептида циркумспорозоита. 14. Способ по п.1, отличающийся тем, что примирующая вакцина включает P 15. Способ по п.1, отличающийся тем, что стимулирующая вакцина включает RTS,S. 16. Способ по п.1, отличающийся тем, что первый малярийный антиген включает практически весь белок циркумспорозоита, и второй малярийный антиген включает RTS,S. 17. Способ по п.1, отличающийся тем, что вызывающим малярию патогеном является P.falciparum. 18. Способ по п.1, отличающийся тем, что примирующая вакцина включает, по крайней мере, один полинуклеотид, кодирующий практически весь белок CS или его фрагмент в примирующей дозе, эффективной для установления иммунного отклика; и стимулирующая вакцина включает, по крайней мере, один полипептид, включающий практически весь белок CS или его фрагмент в стимулирующей дозе, эффективной для стимулирования примированного иммунного отклика. 19. Способ по п.18, отличающийся тем, что примирующая вакцина включает P 20. Способ по п.18, отличающийся тем, что стимулирующая вакцина включает гибридный белок, включающий практически всю С-терминальную часть белка CS, четыре или более тандемных повтора иммунодоминантной зоны и поверхностный антиген от вируса гепатита В (HBsAg). 21. Способ по п.20, отличающийся тем, что стимулирующая вакцина включает RTS,S и индуцирующий Th1 адъювант. 22. Способ по п.18, отличающийся тем, примирующая доза составляет между 0,01 мкг и 50 мг. 23. Способ по п.22, отличающийся тем, что примирующая доза составляет 2500 мкг. 24. Способ по п.22, отличающийся тем, что примирующая доза вводится между одним и 5 разами перед введением второй вакцины. 25. Способ по п.18, отличающийся тем, что стимулирующая доза составляет между 1 мкг и 100 мкг. 26. Способ по п.25, отличающийся тем, что стимулирующая доза составляет 50 мкг. 27. Способ по п.25, отличающийся тем, что стимулирующая доза составляет 25 мкг. 28. Способ по п.18, отличающийся тем, что примирующая вакцина вводится способом, выбранным из внутримышечного введения, внутривенного, внутрикожного, подкожного, слизистого, с помощью рекомбинантной бактерии, рекомбинантного вируса или генной пушки, или их комбинации. 29. Способ по п.18, отличающийся тем, что стимулирующая вакцина вводится способом, выбранным из внутримышечного введения, внутривенного, внутрикожного, подкожного, слизистого, с помощью рекомбинантной бактерии, рекомбинантного вируса или генной пушки, или их комбинации. 30. Вакцина для использования в способе по п.1 для иммунизации человека против вызывающего малярию патогена, включающая, в качестве отдельных компонентов, примирующий состав, включающий, по крайней мере, один полинуклеотид, кодирующий, по крайней мере, один первый малярийный антиген, и стимулирующий состав, состоящий из, по крайней мере, одного полипептида, дополнительно включающего, по крайней мере, один второй малярийный антиген, отличающаяся тем, что введение примирующего состава примирует Т клетки CD8+, и последующее введение стимулирующего состава вызывает вторичный отклик примированных Т клеток CD8+, расширяет отклик примированных Т клеток CD8+ и приводит к генерации антималярийных Т клеток CD8+, антималярийных Т клеток CD4+ и антималярийных антител. 31. Вакцина по п.30, отличающаяся тем, что полинуклеотид кодирует практически весь белок циркумспорозоита. 32. Вакцина по п.30, отличающаяся тем, что примирующий состав включает P 33. Вакцина по п.30, отличающаяся тем, что состав, включающий RTS,S, дополнительно включает адъювант. 34. Набор для иммунизации человека против вызывающего малярию патогена, включающий: 35. Набор по п.34, отличающийся тем, что примирующая вакцина включает P 36. Набор по п.34, отличающийся тем, что стимулирующая вакцина включает вакцину RTS,S. 37. Набор по п.34, отличающийся тем, что примирующая вакцина включает, по крайней мере, один полинуклеотид, кодирующий практически весь белок CS или его фрагмент; а стимулирующая вакцина включает, по крайней мере, один полипептид, включающий практически весь белок CS или его фрагмент. 38. Набор по п.37, отличающийся тем, что примирующая вакцина включает P 39. Набор по п.37, отличающийся тем, что стимулирующая вакцина включает гибридный белок, включающий практически всю С-терминальную часть белка CS, четыре или более тандемных повтора иммунодоминантной зоны и поверхностный антиген от вируса гепатита В (HBsAg). 40. Набор по п.39, отличающийся тем, что стимулирующая вакцина включает RTS,S и индуцирующий Th1 адъювант. 41. Вакцина для иммунизации человека против вызывающего малярию патогена, включающая в качестве отдельных компонентов примирующий состав, включающий, по крайней мере, один полинуклеотид, кодирующий практически весь белок CS или его фрагмент, и стимулирующий состав, включающий, по крайней мере, один полипептид, включающий практически весь белок CS или его фрагмент, отличающаяся тем, что введение примирующего состава примирует Т клетки CD8+, и последующее введение стимулирующего состава вызывает вторичный отклик примированных Т клеток CD8+, расширяет отклик примированных Т клеток CD8+ и приводит к генерации антималярийных Т клеток CD8+, антималярийных Т клеток CD4+ и антималярийных антител. 42. Вакцина по п.41, отличающаяся тем, что примирующий состав включает P 43. Вакцина по п.41, отличающаяся тем, что стимулирующий состав включает гибридный белок, включающий практически всю С-терминальную часть белка CS, четыре или более тандемных повтора иммунодоминантной зоны и поверхностный антиген от вируса гепатита В (HBsAg). 44. Вакцина по п.43, отличающаяся тем, что стимулирующий состав включает RTS,S и индуцирующий Th1 адъювант.
РИСУНКИ
TH4A – Переиздание описания изобретения к патенту Российской Федерации
Причина переиздания: Коррекция в текстах описания, формулы изобретения, графических материалах
Извещение опубликовано: 10.08.2009 БИ: 22/2009
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 60/420,265, поданной 23 октября 2002 г., (досье поверенного
60/420,265, поданной 23 октября 2002 г., (досье поверенного  ), который имеет разнообразные стимулирующие воздействия на другие компоненты иммунной системы, такие как макрофаги. Особый класс Т клеток CD8+ цитотоксические Т лимфоциты (ЦТЛ), специально убивают инфицированные клетки, которые осуществляют экспрессию патогенных антигенов на их поверхности. В отличие от этого Т клетки CD4+ или Т клетки-помощники способствуют развитию ЦТЛ и вызывают деление В клеток и, в конечном итоге, производят антитела. Т клетки-помощники могут быть подразделены на два подвида Т клетки: Тн1 и Тн2 CD4+, которые идентифицируются в соответствии с профилем цитокинов, которые они производят. Вторая группа патогенно-специфического иммунного отклика состоит из гуморального отклика, в котором В клетки воспроизводятся, дифференцируются и постепенно производят антитела, которые связываются непосредственно с патогенами. Антитела особенно полезны для нанесения покрытия на патоген, не связанный с какой-либо клеткой-хозяином. Фагоциты, такие как макрофаги, затем поглощают покрытые антителом патогены.
), который имеет разнообразные стимулирующие воздействия на другие компоненты иммунной системы, такие как макрофаги. Особый класс Т клеток CD8+ цитотоксические Т лимфоциты (ЦТЛ), специально убивают инфицированные клетки, которые осуществляют экспрессию патогенных антигенов на их поверхности. В отличие от этого Т клетки CD4+ или Т клетки-помощники способствуют развитию ЦТЛ и вызывают деление В клеток и, в конечном итоге, производят антитела. Т клетки-помощники могут быть подразделены на два подвида Т клетки: Тн1 и Тн2 CD4+, которые идентифицируются в соответствии с профилем цитокинов, которые они производят. Вторая группа патогенно-специфического иммунного отклика состоит из гуморального отклика, в котором В клетки воспроизводятся, дифференцируются и постепенно производят антитела, которые связываются непосредственно с патогенами. Антитела особенно полезны для нанесения покрытия на патоген, не связанный с какой-либо клеткой-хозяином. Фагоциты, такие как макрофаги, затем поглощают покрытые антителом патогены. CSP) была разработана компанией Викал Инк., Сан Дьего, Калифорния, и Военно-морским медицинским исследовательским центром (47). Вакцина состояла из «оголенной» (депротеинизированной) ДНК в забуференном фосфатом физиологическом растворе (PBS) при концентрации 2500 мкг на 1 мл. Плазмид содержал ген нормальной длины, кодирующий весь ген P
CSP) была разработана компанией Викал Инк., Сан Дьего, Калифорния, и Военно-морским медицинским исследовательским центром (47). Вакцина состояла из «оголенной» (депротеинизированной) ДНК в забуференном фосфатом физиологическом растворе (PBS) при концентрации 2500 мкг на 1 мл. Плазмид содержал ген нормальной длины, кодирующий весь ген P 10%
10%  некроза опухоли (TNF-
некроза опухоли (TNF- +, но не отмечалось, что они вызывают специфические к антигену цитотоксические Т лимфоциты (ЦТЛ) в человеке. Для определения того, могут ли индуцированные ДНК ЦТЛ памяти быть вызваны стимулированием вакциной RTS,S и будет ли стимулированный отклик шире, чем первоначальный примированный ДНК отклик, оценивалась цитотоксическая активность антиген-специфических ЦТЛ у разных добровольцев. Периферийные мононуклеарные кровяные клетки (PBMCs) собирались из крови примированных ДНК или непримированных добровольцев за 1-2 недели перед иммунизацией RTS,S, и 1 или 2 недели спустя первой и/или второй доз RTS,S. Эти РВМС затем использовались в анализе выхода хрома, который детектирует лизис представляющих антиген клеток мишеней (105).
+, но не отмечалось, что они вызывают специфические к антигену цитотоксические Т лимфоциты (ЦТЛ) в человеке. Для определения того, могут ли индуцированные ДНК ЦТЛ памяти быть вызваны стимулированием вакциной RTS,S и будет ли стимулированный отклик шире, чем первоначальный примированный ДНК отклик, оценивалась цитотоксическая активность антиген-специфических ЦТЛ у разных добровольцев. Периферийные мононуклеарные кровяные клетки (PBMCs) собирались из крови примированных ДНК или непримированных добровольцев за 1-2 недели перед иммунизацией RTS,S, и 1 или 2 недели спустя первой и/или второй доз RTS,S. Эти РВМС затем использовались в анализе выхода хрома, который детектирует лизис представляющих антиген клеток мишеней (105).