|
|
(21), (22) Заявка: 2008110652/12, 19.03.2008
(24) Дата начала отсчета срока действия патента:
19.03.2008
(46) Опубликовано: 10.05.2009
(56) Список документов, цитированных в отчете о
поиске:
RU 2318617 C1, 10.03.2008. RU 2083709 C1, 10.07.1997. JP 10223588 A, 21.08.1998. JP 61044716 A, 04.03.1986.
Адрес для переписки:
196604, Санкт-Петербург, г. Пушкин-4, Кадетский б-р, 1, ВМИИ, С.В. Колесникову
|
(72) Автор(ы):
Колесников Сергей Васильевич (RU),
Гаврищук Сергей Михайлович (RU),
Беляев Владимир Павлович (RU)
(73) Патентообладатель(и):
Государственное образовательное учреждение высшего профессионального образования Военно-морской инженерный институт (RU)
|
(54) СПОСОБ ДЕМЕРКУРИЗАЦИИ ПОВЕРХНОСТЕЙ, ЗАГРЯЗНЕННЫХ МЕТАЛЛИЧЕСКОЙ РТУТЬЮ
(57) Реферат:
Изобретение относится к области технической химии, в частности к способам демеркуризации поверхностей, загрязненных металлической ртутью при ее проливе. Способ заключается в удалении капель ртути механическим путем, нанесении водного раствора демеркуризатора с выдержкой демеркуризатора на поверхности. В качестве демеркуризатора используют 10-15% водный раствор перхлората аммония, в 100 граммах которого содержится 10% хлорида аммония. Время демеркуризации составляет не менее 2 часов в интервале температур от +4 до -10°С. Способ позволяет сократить время демеркуризации и повысить эффективность процесса, а также обеспечивает меньшее повреждение обрабатываемой поверхности. 18 ил., 5 табл.
Изобретение относится к области технической химии, в частности к способам демеркуризации поверхностей, загрязненных металлической ртутью при ее проливе при температурах от +4 до -10°С.
Наиболее распространенными способами демеркуризации поверхностей – аналогами настоящего изобретения являются способы нанесения на поверхности растворов различных демеркуризаторов [1]:
мыльно-содовый раствор (4% раствор мыла в 5% водном растворе соды);
20% раствор хлорного железа (FeCl3);
5-10% водный раствор сульфита натрия;
4-5% водный раствор полисульфида натрия;
20% раствор хлорной извести;
5-10% соляная кислота;
2-3% раствор йода в водном растворе йодида калия;
0,2% водный раствор марганцовокислого калия, подкисленного соляной кислотой;
пиролюзит (паста двуокиси марганца);
4-5% растворы моно-, дихлорамина.
Из приведенного перечня демеркуризаторов наилучшими демеркуризирующими свойствами обладают 20% водный раствор хлорного железа и 0,2% водный раствор марганцовокислого калия, подкисленного соляной кислотой. Поэтому дальнейшее сравнение эффективности демеркуризации предлагаемого демеркуризатора проводили с указанными растворами. Сведений о применимости указанных демеркуризаторов при отрицательных температурах не обнаружено.
При взаимодействии с перечисленными растворами ртуть превращается в нерастворимую в воде форму (Hg2Cl2; HgO; HgS и др.) и удаляется с поверхности механическим способом. При этом время взаимодействия ртути в молекулярной форме и демеркуризатора составляет 1,5-2 суток с расходом 0,4-1 л на 1 м2 при положительных температурах. При понижении температуры на 10°С скорость взаимодействия ртути и демеркуризатора падает в среднем в 2-3 раза. При замерзании демеркуризатора взаимодействие с ртутью практически прекращается.
Известны способы термической демеркуризации поверхностей, заключающиеся в нагреве поверхностей до 200-250°C с одновременным отсосом воздуха через фильтр, поглощающий пары ртути. Поглощение паров ртути осуществляется на йодированном активированном угле [2, 3]. Для демеркуризации поверхностей при отрицательных температурах способ не применим.
Известен способ обработки поверхностей 4-5% раствором моно- или дихлорамина в четыреххлористом углероде [4]. При этом время контакта поверхности с раствором должно составлять 8-10 часов. После этого поверхность дополнительно обрабатывается 4-5% раствором полисульфида натрия с временем контакта в течение 8-10 часов. Обработка поверхности получается двухступенчатой: в процессе первой обработки образуются сульфамид ртути и каломель, а в процессе второй обработки – сульфид ртути. Способ сложен в осуществлении и опасен, т.к. испаряющийся четыреххлористый углерод является токсичным и горючим соединением.
Известен способ демеркуризации поверхностей с помощью перекиси водорода [5]. Способ не обеспечивает надежной демеркуризации из-за низкой стойкости перекиси водорода в сравнении со временем, необходимым для проведения демеркуризации. После выделения кислорода, которое произойдет в течение 20-30 мин, раствор замерзнет.
Известен способ демеркуризации изделий, содержащих ртуть [6], в котором лампы, содержащие пары ртути, разбивают в растворе полисульфидов кальция. При отрицательных температурах способ не осуществим.
Прототипом изобретения является патент  2318617 «Способ демеркуризации поверхностей, загрязненных металлической ртутью», основанный на окислении ртути до ее окиси водным раствором перхлората аммония [7]. Недостатками способа прототипа являются 2318617 «Способ демеркуризации поверхностей, загрязненных металлической ртутью», основанный на окислении ртути до ее окиси водным раствором перхлората аммония [7]. Недостатками способа прототипа являются
замерзание демеркуризатора при отрицательных температурах;
снижение эффективности демеркуризации при отрицательных температурах водными растворами при концентрациях 1-5%.
Сущность изобретения заключается в совокупности существенных признаков, которые находятся в причинно-следственной связи и обеспечивают достижение заявляемого результата: удаления ртути с поверхностей в течение не менее 2 часов при температурах от +4 до -10°С. Для достижения этого результата в качестве демеркуризатора были исследованы и применены свойства водных растворов перхлората аммония (ПХА) и хлористого аммония (ХА), нанесенных на поверхность. Способ демеркуризации поверхностей, загрязненных металлической ртутью, включает удаление капель механическим путем, нанесение водного раствора демеркуризатора, выдержку демеркуризатора на поверхности.
Существенными признаками изобретения являются
использование в качестве демеркуризаторов водных растворов перхлората аммония и хлорида аммония;
использование демеркуризирующей рецептуры, наносимой на поверхность, состоящей из водного раствора ПХА с концентрацией от 10% до 15% и 10% водного раствора ХА на 100 г водного раствора. Указанные значения концентраций обеспечивают демеркуризацию ртути в интервале концентраций, величины которых приведены в примерах. Снижение концентрации ПХА приводит к снижению эффективности демеркуризации. Так, 5%, 7% растворы оказались малоэффективными и не обеспечили полное удаление ртути за один цикл обработки;
меньшее время демеркуризации, чем у всех основных демеркуризаторов (около 2 часов при использовании 10-15% раствора при температуре +4÷-10°С);
высокая эффективность демеркуризации, достигающая 100% при однократной обработке.
значительно меньшая повреждающая способность различных поверхностей по сравнению с основными демеркуризаторами.
Хлорид аммония в составе водного раствора ПХА выполняет две функции.
Во-первых, понижает температуру замерзания демеркуризатора. Водный раствор хлорида аммония не замерзает при 10% концентрации до температуры -15°С [8]. Растворы ПХА, напротив, обладают меньшей антифризной способностью. Так, 1% водный раствор ПХА замерзает при -3°С, 5% водный раствор – при -4°С; 10% водный раствор – при -6°С, а 15% водный раствор замерзает при -7°С. Замерзание растворов в небольшой степени зависит от компактности объема. Разлитые по поверхности демеркуризаторы замерзают при меньших температурах по сравнению с демеркуризаторами, находящимися в емкостях. Добавление в эти растворы ХА до концентрации 10% понижает температуру замерзания предлагаемой демеркуризирующей рецептуры. Опытным путем установлено, что 5-15% растворы ПХА+10%ХА не замерзают до температуры -10°С. При дальнейшем понижении температуры, до -12°С, 5-15% растворы ПХА+10%ХА начинают замерзать. Образующиеся кристаллы солей образуют «корку», под которой находятся жидкая фаза демеркуризатора и выпавшие в осадок кристаллы ПХА.
Во-вторых, хлорид аммония повышает эффективность демеркуризации за счет вероятного образования малорастворимого двухъядерного комплекса [Hg(NH3)2]Cl2, который снижает окислительно-восстановительный потенциал реакции (I).
Известно, что окисление ртути происходит по двум реакциям [9]:

и

Стандартные окислительно-восстановительные потенциалы Ео реакций (I) и (II) равны соответственно Ео=0,926 В и Ео=0,854 В [9].
Введение в демеркуризирующий раствор ионов хлора Cl–, входящих в состав хлорида аммония, приводит к снижению стандартного потенциала окисления ртути и увеличению разности окислительно-восстановительных потенциалов за счет протекания реакций:
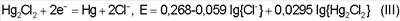
и
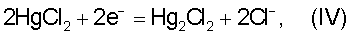
E=0,63-0,054 lg{Cl–}+0,059 lg{HgCl2}-0,0295 lg{Hg2Cl2}
Для реакций (I) и (II) разность стандартного окислительно-восстановительного потенциала Eo составляет
Eо(I)=1,36-0,926=0,434 В;
Ео(II)=1,36-0,854=0,506 В,
а для реакций (III) и (IV):
Ео(III)=1,36-0,268=1,092 В;
Ео(IV)=1,36-0,63=0,73 В.
Следует отметить, что кроме хлорид-ионов Cl–, введение в водный раствор ионов аммония NH4 + приведет к дальнейшему снижению окислительного потенциала ртути за счет образования более сложного комплекса [Hg(NH3)2]Cl2 и, как результат, более полному растворению ртути. + приведет к дальнейшему снижению окислительного потенциала ртути за счет образования более сложного комплекса [Hg(NH3)2]Cl2 и, как результат, более полному растворению ртути.
Таким образом, растворение ртути перхлоратом аммония в присутствии хлорида аммония NH4Cl можно выразить следующими вероятными химическими реакциями:
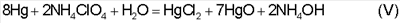
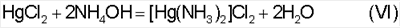
Введение в водный раствор хлорид ионов также может приводить к образованию ряда хлоридных комплексов, общая константа образования которых составляет  mo=1,66×1015, что способствует повышению эффективности демеркуризации. mo=1,66×1015, что способствует повышению эффективности демеркуризации.
Эффективность демеркуризации при проведении экспериментов проверялась по разработанному способу отбора и обработки проб ртути с поверхностей [10], в основе которого лежит метод Полежаева. Ртуть, оставшаяся после демеркуризации, собиралась ватным тампоном, смоченным поглотительным раствором – раствором йода в йодиде калия (Фото 1). После этого остатки поглотительного раствора собирались вторым (сухим) ватным тампоном. Обработка обоих тампонов осуществлялась их перетиранием в поглотительном растворе (Фото 2) и отжимом стеклянной палочкой на боковой поверхности стекла пробирки (Фото 3). Общая оценка величины загрязненности проводилась в соответствии с методикой Полежаева: путем построения шкалы и сравнения образовавшейся окраски осадка с цветом шкалы.
Для сравнительной оценки эффективности демеркуризации растворами перхлоратов и другими растворами демеркуризаторов была разработана методика равномерного нанесения ртути на поверхность (Методика  1). Методика заключалась в заливке капли ртути массой 5 г 100 мл хлористого метилена, взбалтывании хлористого метилена с ртутью в течение 2-3 минут, отстаивании капель ртути (Фото 4), отборе 1 мл хлористого метилена в мерную пипетку (Фото 5) и равномерном нанесении на ограниченную поверхность чашки Петри площадью 64 см2 (Фото 6). Хлористый метилен испаряется в течение 2-3 минут, обеспечивая равномерную и воспроизводимую загрязненность поверхности ртутью. 1). Методика заключалась в заливке капли ртути массой 5 г 100 мл хлористого метилена, взбалтывании хлористого метилена с ртутью в течение 2-3 минут, отстаивании капель ртути (Фото 4), отборе 1 мл хлористого метилена в мерную пипетку (Фото 5) и равномерном нанесении на ограниченную поверхность чашки Петри площадью 64 см2 (Фото 6). Хлористый метилен испаряется в течение 2-3 минут, обеспечивая равномерную и воспроизводимую загрязненность поверхности ртутью.
После испарения хлористого метилена последовательно несколькими ватными тампонами, смоченными стандартным поглотительным раствором, была собрана ртуть с поверхности с эталонной загрязненностью. Тампоны помещались в пробирку и заливались поглотительным раствором объемом 1 мл, после чего перетирались стеклянной палочкой, отжимались на боковой поверхности пробирки, извлекались и анализировались до отрицательного результата. Суммарная величина загрязнения ртутью поверхности оценивается приблизительно в 20 мкг ртути на поверхности 64 см2 [10].
Для определения погрешности собирания ртути с поверхностей 1 мл хлористого метилена с растворенной ртутью залили непосредственно в пробирку, в которой проводилась реакция определения величины концентрации. Хлористый метилен в пробирке испарили в струе воздуха, после чего определили массу ртути в пробирке: масса ртути составила 20±0,5 мкг. Полученный результат сравним с результатом определения массы ртути методом снятия мазков с площади чашки Петри. Искусственно загрязненные таким образом поверхности с равной площадью были залиты различными демеркуризаторами с целью определения в равных условиях эффективности демеркуризации при низких температурах.
Пример 1. Температура -2°С.
На поверхности чашек Петри, искусственно загрязненных ртутью, содержащейся в объеме 1 мл хлористого метилена, были нанесены водные растворы демеркуризаторов: 20% водный раствор хлорного железа, 0,2% водный раствор марганцовокислого калия KMnO4, подкисленный соляной кислотой (из расчета 5 мл соляной кислоты плотностью 1,19 г/см3 на 1 л 0,2% раствора), 5%, 10% и 15% водные растворы перхлората аммония NH4ClO4 с 10%-ным содержанием хлорида аммония в растворе.
Время демеркуризации – 2, 4, 8 часов.
Через 1 час раствор марганцовокислого калия 0,2%, подкисленный соляной кислотой из расчета 5 мл соляной кислоты плотностью 1,19 г/см3 на 1 л 0,2% раствора, замерз (Фото 7).
Через 2, 4, 8 часов демеркуризаторы удалялись ватным тампоном, остатки демеркуризатора удалялись фильтровальной бумагой. Остаточное количество ртути на поверхности определялось по методике, приведенной в [10]. Результаты демеркуризации приведены в таблице 1.
| Таблица 1 |
| Остаточное количество ртути, установленное после проведения демеркуризации со стеклянной поверхности через 2, 4, 8 часов (температура -2°С). |
| Время (час) |
Демеркуризатор |
Остаточное количество ртути после демеркуризации, мкг |
Примечание |
| 1 |
2 |
3 |
4 |
| 2 |
20% водный раствор хлорного железа (FeCl3) |
11,4±0,2 |
Раствор имеет светлый желто-зеленый цвет, кристаллы не выпадают |
| 2 |
0,2% водный раствор KMnO4, подкисленный соляной кислотой |
8,2±0,2 |
Демеркуризатор замерз через 1 час |
| 2 |
5% NH4ClO4
10% NH4Cl на 100 г раствора |
0,2±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 2 |
10% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 2 |
15% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшего в осадок |
| 4 |
20% водный раствор хлорного железа (FeCl3) |
9,0±0,2 |
Раствор имеет светлый желто-зеленый цвет, кристаллы не выпадают |
| 4 |
0,2% водный раствор KMnO4, подкисленный соляной кислотой |
7,8±0,2 |
Демеркуризатор замерз через 1 час |
| 4 |
5% NH4C1O4
10% NH4C1 на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 4 |
10% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 4 |
15% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 8 |
20% водный раствор хлорного железа (FeCl3) |
7,0±0,2 |
Раствор имеет светлый желто-зеленый цвет, кристаллы не выпадают |
| 8 |
0,2% водный раствор KMnO4, подкисленного соляной кислотой |
8,0±0,2 |
Демеркуризатор замерз через 1 час |
| 8 |
5% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 8 |
10% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 8 |
15% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
Пример 2. Температура -5°С
На поверхности чашек Петри, искусственно загрязненных ртутью, содержащейся в объеме 1 мл хлористого метилена, были нанесены растворы демеркуризаторов: 20% водный раствор хлористого железа, водный раствор марганцовокислого калия 0,2%, подкисленный соляной кислотой из расчета 5 мл соляной кислоты плотностью 1,19 г/см3 на 1 л 0,2% раствора, 5%, 10% и 15% водные растворы перхлората аммония NH4ClO4 с 10%-ным содержанием хлорида аммония в растворе.
Время демеркуризации – 2, 4, 8 часов.
Через 30 мин раствор марганцовокислого калия 0,2%, подкисленный соляной кислотой из расчета 5 мл соляной кислоты плотностью 1,19 г/см3 на 1 л 0,2% раствора, замерз.
Через 2, 4, 8 часов демеркуризаторы удалялись ватным тампоном, остатки демеркуризатора удалялись фильтровальной бумагой. Остаточное количество ртути на поверхности определялось по методике, приведенной в [10]. Результаты демеркуризации приведены в таблице 2. Общий вид растворов демеркуризаторов в течение 2, 4, 8 часов был похожим. 10% и 15% растворы ПХА отличались количеством выпавшего в осадок кристаллического ПХА. Общий вид растворов демеркуризаторов спустя 4 часа приведен на Фото 8, 9.
| Таблица 2 |
| Остаточное количество ртути, установленное после проведения демеркуризации со стеклянной поверхности через 2, 4, 8 часов (температура -5°С). |
| Время (час) |
Демеркуризатор |
Остаточное количество ртути после демеркуризации, мкг |
Примечание |
| 1 |
2 |
3 |
4 |
| 2 |
20% водный раствор хлорного железа (FeCl3) |
13,4±0,2 |
Раствор имеет светлый желто-зеленый цвет, кристаллы не выпадают |
| 2 |
0,2% водный раствор KMnO4, подкисленный соляной кислотой |
12,0±0,2 |
Демеркуризатор замерз через 30 мин |
| 2 |
5% NH4ClO4
10% NH4Cl на 100 г раствора |
5±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 2 |
10% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 2 |
15% NH4ClO4 10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшего в осадок |
| 4 |
20% водный раствор хлорного железа (FeCl3) |
10,0±0,2 |
Раствор имеет светлый желто-зеленый цвет, кристаллы не выпадают |
| 4 |
0,2% водный раствор KMnO4, подкисленный соляной кислотой |
11,8±0,2 |
Демеркуризатор замерз через 30 мин |
| 4 |
5% NH4ClO4
10% NH4Cl на 100 г раствора |
3,2±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 4 |
10% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 4 |
15% NH4ClO4
10% NH4CL на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 8 |
20% водный раствор хлорного железа (FeCl3) |
9,0±0,2 |
Раствор имеет светлый желто-зеленый цвет, кристаллы не выпадают |
| 8 |
0,2% водный раствор KMnO4, подкисленный соляной кислотой |
11,6±0,2 |
Демеркуризатор замерз через 30 мин |
| 8 |
5% NH4ClO4
10% NH4Cl на 100 г раствора |
2±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри – кристаллы ПХА, выпавшие в осадок |
| 8 |
10% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 8 |
15% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
Пример 3. Температура -10°С
На поверхности чашек Петри, искусственно загрязненных ртутью, содержащейся в объеме 1 мл хлористого метилена, были нанесены растворы демеркуризаторов: 20% водный раствор хлористого железа, водный раствор марганцовокислого калия 0,2%, подкисленный соляной кислотой из расчета 5 мл соляной кислоты плотностью 1,19 г/см3 на 1 литр 0,2% раствора, 5%, 10% и 15% водные растворы перхлората аммония NH4ClO4 с 10%-ным содержанием хлорида аммония в растворе.
Время демеркуризации – 2, 4, 8 часов.
Через 10 мин раствор марганцовокислого калия 0,2%, подкисленный соляной кислотой из расчета 5 мл соляной кислоты плотностью 1,19 г/см3 на 1 литр 0,2% раствора, замерз. Общий вид растворов в течение 2, 4, 8 часов был похожим. Растворы приобретали вязкий вид, местами покрывались коркой замерзшего демеркуризатора. 5%, 10% и 15% растворы ПХА отличались количеством выпавшего в осадок кристаллического ПХА. Общий вид растворов спустя 2, 4 часа приведен на Фото 10, 11, 12, 13.
Через 2, 4, 8 часов демеркуризаторы удалялись ватным тампоном, остатки демеркуризатора удалялись фильтровальной бумагой. Остаточное количество ртути на поверхности определялось по методике, приведенной в [10]. Результаты демеркуризации приведены в таблице 3.
| Таблица 3 |
| Остаточное количество ртути, найденное после проведения демеркуризации со стеклянной поверхности через 8 часов (температура -10°С). |
| Время (час) |
Демеркуризатор |
Остаточное количество ртути после демеркуризации, мкг |
Примечание |
| 1 |
2 |
3 |
4 |
| 2 |
20% водный раствор хлорного железа (FeCl3) |
14,0±0,2 |
Раствор имеет светлый желто-зеленый цвет, кристаллы не выпадают |
| 2 |
0,2% водный раствор KMnO4, подкисленный соляной кислотой |
14,4±0,2 |
Демеркуризатор замерз через 15-20 мин |
| 2 |
5% NH4ClO4
10% NH4Cl на 100 г раствора |
2±0,2 |
Демеркуризатор бесцветный, покрылся коркой замерзшего раствора, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 2 |
10% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, покрылся тонкой коркой замершего раствора, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 2 |
15% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 4 |
20% водный раствор хлорного железа (FeCl3) |
12,0±0,2 |
Раствор имеет светлый желто-зеленый цвет, кристаллы не выпадают |
| 4 |
0,2% водный раствор KMnO4, подкисленный соляной кислотой |
14,2±0,2 |
Демеркуризатор замерз через 15-20 мин |
| 4 |
5% NH4ClO4
10% NH4Cl на 100 г раствора |
1,4±0,2 |
Демеркуризатор бесцветный, покрылся коркой замершего раствора, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 4 |
10% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, покрылся тонкой коркой замершего раствора, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 4 |
15% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, сверху покрылся тонкой коркой замершего раствора, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 8 |
20% водный раствор хлорного железа (FeCl3) |
10,4±0,2 |
Раствор имеет светлый желто-зеленый цвет, кристаллы не выпадают |
| 8 |
0,2% водный раствор KMnO4, подкисленный соляной кислотой |
14,0±0,2 |
Демеркуризатор замерз через 15-20 мин |
| 8 |
5% NH4ClO4
10% NH4Cl на 100 г раствора |
0,2±0,2 |
Демеркуризатор бесцветный, покрылся коркой замершего раствора, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 8 |
10% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, покрылся тонкой коркой замершего раствора сверху, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 8 |
15% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, покрылся тонкой коркой замершего раствора, сверху, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
Для изучения особенностей демеркуризации при больших загрязненностях поверхностей ртутью разработана методика нанесения металлической ртути на ограниченную поверхность (Методика  2). 2).
Стеклянная поверхность ограничивалась стенками чашки Петри. Металлическую ртуть наносили на чашку Петри следующим образом: каплю ртути диаметром 8-10 мм помещали в мерный цилиндр объемом 25 мл или пробирку. Затем к мерному цилиндру плотно прижимали внутреннюю часть чашки Петри (Фото 14) и аккуратно, не допуская удара ртути (!) по поверхности чашки Петри (Фото 15), переворачивали (Фото 16). Таким образом, капля ртути находилась в чашке Петри на поверхности, ограниченная стенками мерного цилиндра (пробирки). Плотно прижимая мерный цилиндр к чашке Петри, передвигали каплю ртути по кругу внутренней поверхности чашки. После этого цилиндр с чашкой Петри переворачивали в обратном порядке. В итоге – исходная капля ртути оставалась в мерном цилиндре, а на внутренней поверхности чашки Петри – относительно равномерно нанесенная ртуть. Следует отметить, что после нанесения ртути данным методом на стекле остаются одиночные капли ртути диаметром около 0,1 мм, которые «забираются» основной каплей при круговом перемещении. К сожалению, данный способ не обеспечивает хорошо воспроизводимых значений загрязненности. Аналогичным способом загрязнялась поверхность алюминиевой и медной фольги (Фото 17). Степень загрязненности алюминиевых и медных поверхностей получается выше, чем у стеклянных, что, видимо, связано со степенью ватости их поверхностей. Загрязнение ртутью стеклянной поверхности составило около 80 мкг. Для более точного определения загрязненности тампоны обрабатывали в 10 мл поглотительного раствора до отрицательной реакции, а анализировался 1 мл поглотительного раствора с последующим умножением полученной загрязненности на 10.
После загрязнения стеклянных поверхностей по методике  2 были проведены эксперименты по демеркуризации стекла при отрицательных температурах. Сравнение предлагаемой демеркуризирующей рецептуры – водного раствора перхлората аммония NH4ClO4 с добавлением 10%-го водного раствора хлорида аммония NH4Cl, с другими демеркуризаторами не проводилось. 2 были проведены эксперименты по демеркуризации стекла при отрицательных температурах. Сравнение предлагаемой демеркуризирующей рецептуры – водного раствора перхлората аммония NH4ClO4 с добавлением 10%-го водного раствора хлорида аммония NH4Cl, с другими демеркуризаторами не проводилось.
Пример 4. Температура -5°С
Чашки Петри загрязнялись ртутью по методике  2, после чего заливались водными растворами демеркуризирующих рецептур (5%, 10% и 15% водные растворы перхлората аммония NH4ClO4 с 10%-ным содержанием хлорида аммония в растворе) так, чтобы демеркуризатор тонким слоем покрыл поверхность. 2, после чего заливались водными растворами демеркуризирующих рецептур (5%, 10% и 15% водные растворы перхлората аммония NH4ClO4 с 10%-ным содержанием хлорида аммония в растворе) так, чтобы демеркуризатор тонким слоем покрыл поверхность.
Методом, приведенным в [10], определили загрязненность чашек Петри через 2, 4, 8 часов. Результаты демеркуризации представлены в таблице 4.
| Таблица 4 |
| Остаточное количество ртути, определенное после проведения демеркуризации со стеклянной поверхности через 2, 4, 8 часов при температуре -5°С. |
| Время (час) |
[Остаточное количество Демеркуризатор ртути после демеркуризации, мкг |
Примечание |
| 1 |
2 |
3 |
4 |
| 2 |
5% NH4ClO4
10% NH4Cl на 100 г раствора |
3,0±0,2 |
Демеркуризаторы бесцветные, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 2 |
10% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
| 2 |
15% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризаторы бесцветные, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 4 |
5% NH4ClO4
10% NH4Cl на 100 г раствора |
2,2±0,2 |
Демеркуризаторы бесцветные, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 4 |
10% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
| 4 |
15% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
| 8 |
5% NH4ClO4
10% NH4Cl на 100 г раствора |
1,6±0,2 |
Демеркуризатор бесцветный, покрылся коркой замершего раствора, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 8 |
10% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризаторы бесцветные, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 8 |
15% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Как видно из таблицы, уже через 2 часа демеркуризирующие рецептуры, состоящие из 10% и 15% ПХА в 10% ХА, обеспечивают надежное удаление с поверхности ртути массой около 80 мкг. Демеркуризатор 5% ПХА в 10% ХА не обеспечивает полного удаления ртути ни за один опытный промежуток времени.
Пример 5. Температура -10°С
Чашки Петри загрязнялись ртутью по методике  2, после чего заливались водными растворами демеркуризирующих рецептур (5%, 10% и 15% водные растворы перхлората аммония NH4ClO4 с 10%-ным содержанием хлорида аммония в растворе) так, чтобы демеркуризатор тонким сдоем покрыл поверхность. 2, после чего заливались водными растворами демеркуризирующих рецептур (5%, 10% и 15% водные растворы перхлората аммония NH4ClO4 с 10%-ным содержанием хлорида аммония в растворе) так, чтобы демеркуризатор тонким сдоем покрыл поверхность.
Методом [10] определили загрязненность чашек Петри через 2, 4, 8 часов. Результаты демеркуризации представлены в таблице 5.
| Таблица 5 |
| Остаточное количество ртути, определенное после проведения демеркуризации со стеклянной поверхности через 2, 4, 8 часов при температуре -10°С. |
| Время (час) |
Демеркуризатор |
Остаточное количество ртути после демеркуризации, мкг |
Примечание |
| 1 |
2 |
3 |
4 |
| 2 |
5% NH4ClO4
10% NH4Cl на 100 г раствора |
5,0±0,2 |
Демеркуризатор бесцветный, покрылся коркой замершего раствора, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 2 |
10% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, покрылся тонкой коркой замершего раствора, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 2 |
15% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 4 |
5% NH4ClO4
10% NH4Cl на 100 г раствора |
3,8±0,2 |
Демеркуризатор бесцветный, покрылся коркой замершего раствора, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 4 |
10% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, покрылся тонкой коркой замершего раствора, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 4 |
15% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, покрылся тонкой коркой замершего раствора, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 8 |
5% NH4ClO4
10% NH4Cl на 100 г раствора |
2,4±0,2 |
Демеркуризатор бесцветный, покрылся коркой замершего раствора сверху, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 8 |
10% NH4ClO4
10% NH4Cl на 100 г раствора |
0,0±0,2 |
Демеркуризатор бесцветный, покрылся тонкой коркой замершего раствора сверху, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
| 8 |
Водный раствор 15% NH4ClO4 с добавлением 10% NH4Cl |
0,0±0,2 |
Демеркуризатор бесцветный, покрылся тонкой коркой замершего раствора, сверху, на дне чашки Петри видны кристаллы ПХА, выпавшие в осадок |
Как и в примере  4, уже через 2 часа демеркуризаторы 15% ПХА в 10% ХА обеспечивают надежное удаление с поверхности ртути массой около 80 мкг на демеркуризируемой поверхности. Демеркуризатор 5% ПХА в 10% ХА не обеспечивает полного удаления ртути ни за один опытный промежуток времени. 4, уже через 2 часа демеркуризаторы 15% ПХА в 10% ХА обеспечивают надежное удаление с поверхности ртути массой около 80 мкг на демеркуризируемой поверхности. Демеркуризатор 5% ПХА в 10% ХА не обеспечивает полного удаления ртути ни за один опытный промежуток времени.
При понижении температуры до -12°С демеркуризаторы замерзают в течение 30 минут (Фото 18).
Сходные результаты, описанные в примерах 1-6, были получены для медных, алюминиевых, пластиковых поверхностей.
При проведении демеркуризации капельной ртути при отрицательных температурах от -2 до -10°С перхлорат аммония не способен растворять их. При наличии на поверхности капельной ртути она подлежит сбору механическим способом.
Предлагаемый способ может найти широкое применение в промышленности, в ВС РФ, МЧС, так как отличается простотой реализации и высокой эффективностью демеркуризации.
Краткое описание фотографий.
Фото 1. Сбор ртути, оставшейся после демеркуризации, ватным тампоном, смоченным поглотительным раствором – раствором йода в йодиде калия.
Фото 2. Обработка ватных тампонов в поглотительном растворе.
Фото 3. Отжим ватных тампонов стеклянной палочкой на боковой поверхности пробирки.
Фото 4. Вид раствора хлористого метилена с ртутью после встряхивания и отстаивания.
Фото 5. Отбор 1 мл раствора хлористого метилена, загрязненного ртутью.
Фото 6. Нанесение 1 мл раствора хлористого метилена, загрязненного ртутью, на чашку Петри.
Фото 7. Общий вид замерзшего 0,2% водного раствора марганцовокислого калия, подкисленного соляной кислотой из расчета 5 мл соляной кислоты плотностью 1,19 г/см3 на 1 л 0,2% раствора.
Фото 8. Общий вид водного раствора ПХА 5% + ХА 10% через 4 ч при -5°С.
Фото 9. Общий вид водного раствора ПХА 10% + ХА 10% через 4 ч при -5°С.
Фото 10. Общий вид водного раствора ПХА 5% + ХА 10% через 2 ч при -10°С.
Фото 11. Общий вид водного раствора ПХА 10% + ХА 10% через 2 ч при -10°С.
Фото 12. Фото 12. Общий вид водного раствора ПХА 10% + ХА 10% через 4 ч при -10°С
Фото 13. Общий вид водного раствора ПХА 5% + ХА 10% через 4 ч при -10°С.
Фото 14. Способ нанесения ртути на поверхность: приготовление.
Фото 15. Способ нанесения ртути на поверхность: подвод капли ртути к поверхности
Фото 16. Способ нанесения ртути на поверхность: переворачивание.
Фото 17. Способ нанесения ртути на алюминиевую поверхность.
Фото 18. Общий вид водного раствора ПХА 15% + ХА 10% через 0,5 ч при -12°С
Литература
1. Ртуть. Нормативные и методические документы. Справочник – С-Пб. 1999 г. «Методические рекомендации по контролю за организацией текущей и заключительной демеркуризации и оценке ее эффективности» стр.44.
2. Яворская С.Ф. «Новости медицины»  26. 72 (1952). 26. 72 (1952).
3. Яворская С.Ф. «Гигиена и санитария»  2.38.1965 г. 2.38.1965 г.
4. «Гигиена и санитария»  4.48.1953 г. 4.48.1953 г.
5. А.С.  266727, Бюл. изобр. 266727, Бюл. изобр.  12 (1970 г.). 12 (1970 г.).
6. Патент РФ  2083709. 2083709.
7. Патент РФ  2318617. 2318617.
9. Справочник химика. В 3 т. / Под ред. Б.П.Никольского. – 2-е изд., перераб. и доп. – М-Л.: Химия, 1965. – Т.3. Химическое равновесие и кинетика. Свойства растворов. Электродные процессы / Б.П.Никольский, О.Н.Григорьев, М.Е.Позин и др. – 1008 с.
10. Патент РФ  2229109. 2229109.
Формула изобретения
Способ демеркуризации поверхностей, загрязненных металлической ртутью, включающий удаление капель механическим путем, нанесение водного раствора демеркуризатора, выдержку демеркуризатора на поверхности, при этом на поверхность наносят 10-15%-ный водный раствор перхлората аммония, в 100 г которого содержится 10% хлорида аммония, с временем демеркуризации не менее 2 ч в интервале температур от +4 до -10°С.
РИСУНКИ
|
|