Патент на изобретение №2354395
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) ПРОФИЛАКТИЧЕСКАЯ КОМПОЗИЦИЯ НА ОСНОВЕ ВЕЩЕСТВ ФЕНОЛЬНОЙ ПРИРОДЫ
(57) Реферат:
Изобретение относится к фармацевтической промышленности, в частности композиции для предупреждения или лечения патологических процессов и поддержания высокого уровня функциональной активности организма. Профилактическая композиция для предупреждения или лечения патологических процессов и поддержания высокого уровня функциональной активности организма, включающая комбинации одного или нескольких экстрактов лекарственных растений, содержащих вещества фенольной природы, и носитель, в качестве носителя используют биосовместимый полимер с определенным размером частиц, при этом композиция имеет определенное соотношение вещество фенольной природы: биосовместимый полимер. 1 з.п. ф-лы, 5 табл.
Изобретение относится к области фармакологии и медицины, конкретно к новой композиции, полученной с использованием нанотехнологии, характеризующейся высокой гидрофильностью, улучшенными биодоступностью и терапевтическими свойствами по сравнению со свободными биофлафоноидами и другими составами, включающими вещества фенольной природы и биополимер. Вещества фенольной природы в качестве действующих начал содержатся в широком спектре лекарственных растений, применяемых для профилактики и лечения различных патологий. Фенольные соединения обладают широким спектром биологической активности. В настоящее время хорошо изучены и задокументированы такие фармакологические свойства фенольных соединений, как антиоксидантная, периферическая, вазодилаторная активности, вазопротекторная активность (влияние на хрупкость и проницаемость капилляров), противовоспалительное, антиспазмолитическое, антигистаминное и противоопухолевое действия. Фенольные соединения представляют собой вещества ароматической природы, которые содержат одну или несколько гидроксильных групп, связанных с атомами углерода ароматического кольца, и встречаются в растениях в виде мономеров, димеров, олигомеров и полимеров. Одним из существенных препятствий для эффективного терапевтического применения веществ фенольной природы является их низкая растворимость в воде и, как следствие, низкая биодоступность. Для повышения биодоступности многими научными коллективами предпринимались усилия по изменению свойств молекул фенольной природы путем получения их производных с помощью химического модифицирования или взаимодействия с определенными агентами. Однако получаемые препараты обладают целым рядом недостатков, таких как повышенная иммуногенность, нестабильность, снижение активности действующего вещества, нежелательные токсические эффекты. Существует также опасность, что, несмотря на улучшенную всасываемость производных в кишечнике, их действие может существенно отличаться от действия исходного природного препарата. Терапевтическое применение веществ фенольной природы растительного происхождения в основном ограничено их пероральным применением вследствие низкой растворимости. Ранее предлагалось увеличить биодоступность веществ фенольной природы путем включения их в состав липосом или липидных комплексов. Однако такие препараты отличаются низкой стабильностью в растворах, и существует опасность возникновения эмболий при их внутривенном введении пациенту. Поскольку вещества фенольной природы растительного происхождения практически нерастворимы в воде, их парентеральное применение также оказывается затруднительным. Для целей практической медицины несомненную актуальность приобретает поиск путей повышения биодоступности и терапевтической эффективности таких препаратов. Одним из таких путей является применение липофильных комплексов, содержащих вещества фенольной природы растительного происхождения, а именно флавоноидов с фосфолипидами (патент США Хотя безусловной заслугой авторов этого патента является некоторое повышение биодоступности флавоноидов за счет улучшения их абсорбции в кишечнике при применении per os, высокая липофильность комплексов служит серьезным препятствием для парентерального применения препаратов, необходимого для более радикальной терапии ряда патологий. В патенте РФ Известна профилактическая композиция, применяемая для предупреждения или лечения патологических процессов и поддержания высокого уровня функциональной активности организма, включающая комбинации одного или нескольких экстрактов лекарственных растений, содержащих вещества фенольной природы, и фосфолипид (пат. РФ Таким образом, авторами приведенных выше работ частично решена задача повышения биодоступности фенольных соединений за счет увеличения их абсорбции в кишечнике в виде комплексов с фосфолипидами, однако проблема повышения растворимости фенольных соединений в водных растворах с целью создания инъекционных форм остается нерешенной. Наиболее близким техническим решением является профилактическая композиция, применяемая для предупреждения или лечения патологических процессов и поддержания высокого уровня функциональной активности организма, включающая комбинации одного или нескольких экстрактов лекарственных растений, содержащих вещества фенольной природы, и наполнитель, в качестве которого применяли фосфолипид. Вещества фенольной природы заключены в оболочку из фосфолипида, выбраного из группы: фосфолипиды из бычьего или свиного мозга или кожи, фосфатидилхолин, фосфатидилсерин, фосфатидилэтаноламин, содержащие одинаковые или различные ацильные группы, яичный лецитин, при этом оболочка выполнена в форме липосом, содержащих холестерол в количестве 11-40% (пат. РФ При этом вещества фенольной природы выбраны из группы: 5, 6, 7, 4′-тетраоксифлавон, 5, 6, 7-триоксифлавон, g-схизандрин, апигенин, астрагалин, ауреузидин, виснагин, виснадин, гесперидин, гиперозид, дезоксисхизандрин, дигидросамидин, дигидросилибин, изоликвиритигенин, изорамнитин, инокостерон, кверцетин. кверцитрин, квинквелозид, келлин, кемпферол, лептозидин, ликвиритигенин, лютеолин, мирицетин, нарингенин, пиранокумарин, розавин, рутин, салидрозид, силидианин, силибинин, силикристин, скополетин, сульфуретин, схизандрин, схизандрол, тилирозид, трицин, умбеллиферон, 6-метокси-7, 8-диоксикумарин, фурокумарин, экдистерон, энтеграстероны, 6,7-диоксикумарин и их производные. Значительного повышения эффективности терапевтического действия веществ фенольной природы можно достичь путем включения их в состав гидрофильных комплексов с различными биосовместимыми полимерами. Такие комплексы могут служить основой для создания обладающих повышенной терапевтической эффективностью и безопасностью инъекционных форм, включающих вещества растительного происхождения. Задачей настоящего изобретения является создание безопасной, с повышенной биодоступностью, эффективной композиции для профилактики и лечения патологий на основе веществ растительного происхождения фенольной природы и биосовместимых полимеров. Для решения этой задачи предлагается профилактическая композиция, применяемая для предупреждения или лечения патологических процессов и поддержания высокого уровня функциональной активности организма, включающая комбинации одного или нескольких экстрактов лекарственных растений, содержащих вещества фенольной природы, и носитель. В качестве носителя используют биосовместимый полимер с размерами частиц от 10-4 до 10-8 м, при этом соотношение вещество фенольной природы: биосовместимый полимер составляет от 1:99 до 1:0,25 мас.%. Профилактическая композиция содержит в качестве биосовместимого полимера полиэтиленгликоль, поливиниловый спирт, полиалкилметакрилат, полилактид и его сополимеры с гликолевой кислотой, поливинилпирролидон, полиэтиленоксид, глицирризиновая кислота, циклодекстрин, декстран. В основе изобретения лежит новая композиция, которая может содержать одно или несколько веществ фенольной природы или один или несколько содержащих данные вещества экстрактов лекарственных растений и биосовместимый полимер, отличающаяся способностью к образованию стабильных водных микродисперсий, которая, в отличие от ранее предлагаемых липофильных препаратов, может быть использована для парентерального введения и обладает более высокой терапевтической активностью. Композиция может быть получена методом упаривания эмульсий, методом преципитации наночастиц в присутствии смешиваемого с водой растворителя, методом высаливания раствора, содержащего полимерный компонент и активное вещество, методом ступенчатого полимерного синтеза, методом распределения активного вещества между цепями расплавленного полимера с последующим охлаждением и измельчением твердой дисперсии, методом самосборки, при этом необходимый размер частиц достигается с применением методов ультразвуковой обработки, экструзии или механического измельчения. В качестве веществ фенольной природы использовали 5,6,7,4′-тетраоксифлавон, 5,6,7-триоксифлавон, g-схизандрин, апигенин, астрагалин, ауреузидин, бергаптен, виснагин, виснадин, галлоэрготаннины, гесперидин, гиперозид, дезоксисхизандрин, дигидрокверцетин, дигидросамидин, дигидросилибин, изоликвиритигенин, изопимпинеллин, изорамнитин, инокостерон, кверцетин, кверцитрин, квинквелозид, келлин, кемпферол, ксантотоксин, 2-C-B-D-глюкопиранозид-1,3,6,7-тетраоксиксантон, лептозидин, ликвиритигенин, лютеолин, мирицетин, нарингенин, пиранокумарин, розавин, рутин, салидрозид, сангвинарин, силидианин, силибинин, силикристин, скополетин, сульфуретин, схизандрин, схизандрол, тилирозид, тритерпеноиды, трицин, умбеллиферон, 6-метокси-7,8-диоксикумарин, фурокумарин, хелеритрин, экдистерон, энтеграстероны, 6,7-диоксикумарин и их производные. В качестве биосовместимого полимера использовали полиэтиленгликоль (мол. масса 200-100000), поливиниловый спирт (мол. масса 15000-100000), полиметилметакрилат (мол. масса 600-800000), полиэтилметакрилат (мол. масса 1500-500000), полибутилметакрилат (мол. масса 1500-800000), полилактид (мол. масса 10000-150000) и его сополимеры с гликолевой кислотой (соотношение лактид/гликолевая кислота от 50/50 до 85/15, мол. масса 5000-120000), поливинилпирролидон (мол. масса 10000-360000), полиэтиленоксид (мол. масса 50000-500000), глицирризиновая кислота, Пример 1. Состав предлагаемой композиции и способ ее получения. Использовали метод распределения активного вещества между цепями расплавленного полимера с последующим охлаждением и измельчением твердой дисперсии ультразвуком. Носитель нагревали на водяной бане до расплавленного состояния, затем в расплав носителя постепенно добавляли при постоянном перемешивании мелко диспергированное действующее вещество. Полученный раствор немедленно охлаждали до комнатной температуры и подвергали обработке ультразвуком с помощью ультразвукового дезинтегратора (Германия). Образование частиц и их размеры детектировали методом микроскопии.
Аналогично были получены композиции с остальными веществами фенольной природы и заявленными биополимерами, указанные выше. Заявляемая композиция, включающая комплексы исходных веществ фенольной природы или содержащих их растительных экстрактов и наполнитель, отличается способностью в водных растворах образовывать стабильные микродисперсионные растворы. Стабильность и гидрофильность заявляемой композиции подтверждается отсутствием осадка при длительном хранении, а также данными микроскопии. Пример 2. Антиоксидантная активность заявляемой композиции Антиоксидантную активность заявляемой композиции оценивали по ее влиянию на генерацию активных форм кислорода у макрофагов, вызванную хризотил-асбестом. В измерительную кювету хемилюминометра помещали 0,85 мл среды, содержащей 110 мМ NaCl, 10 мМ трис-HCl, рН 7.4, 5 мМ глюкозы, 2.5 мМ MgCl2, 0.65 мМ люминола, рН 7.4. Затем в кювету добавляли 0,1 мл суспензии макрофагов (5·106 клеток/мл) и регистрировали интенсивность хемилюминесценции клеток при 37°С и постоянном перемешивании. Через 5 мин измеряли уровень спонтанной хемилюминесценции макрофагов. Затем в кювету вводили 0,05 мл исследуемой композиции (концентрация вещества фенольной природы во всех случаях составляла 0,1 мг/мл), а через 3 мин добавляли 0,05 мл физ. раствора, содержащего 0,3 мг хризотил-асбеста. Через 5 мин измеряли максимальный уровень люминесценции макрофагов (ХЛоп). В качестве контрольного образца использовали аналогичную систему, не содержащую исследуемых препаратов (ХЛк). Антиоксидантную активность исследуемой композиции оценивали в процентах по формуле: Результаты исследования приведены в таблице 2.
Как видно из таблицы 2, антиоксидантная активность веществ фенольной природы или содержащих их экстрактов может быть значительно повышена при включении их в состав заявляемой композиции. При этом антиоксидантная активность заявляемой композиции существенно выше активности препарата-прототипа, включающего соответствующие действующие вещества. Аналогичные результаты были получены при исследовании антиоксидантной активности других вышеперечисленных веществ фенольной природы с биополимерами, входящих в состав заявляемой композиции. Пример 3. Специфическая гепатозащитная активность композиции, включающей силибинин и глицирризиновую кислоту. Исследование специфической гепатозащитной активности композиции проводили на модели острого токсического гепатита у мышей. В экспериментах были использованы белые беспородные мыши в половозрелом возрасте. Водный раствор композиции вводили внутрижелудочно с помощью зонда в дозе 100 мг/кг по силибинину. В качестве гепатотропного средства использовали парацетамол (модель лекарственного гепатита). Животным вводили препарат впервые за 1 ч до введения парацетамола, а затем еще 5 раз ежедневно. В качестве препарата сравнения использовали препарат-прототип, включающий силибинин и фосфатидилхолин. Контрольным животным вводили только парацетамол. Через сутки после последнего введения препаратов животных декапитировали и проводили вскрытие и изучение биохимических показателей крови. Активность аланинаминотрансферазы (АЛАТ) и аспартатаминотрансферазы (АСАТ) определяли по методу Райтмана-Френкеля. Общий белок определяли с помощью биуретового реактива. Результаты исследования приведены в таблице 3.
Таким образом, степень выраженности воспалительных процессов у животных, получавших заявляемую композицию, заметно снижалась, и применение предлагаемого препарата положительно влияло на дезинтоксикационные функции печени животных с острым лекарственным гепатитом. При этом эффект от заявляемой композиции существенно превышал эффект от препарата-прототипа. Пример 4. Противоопухолевая активность заявляемой композиции, включающей экстракты расторопши пятнистой, эхинацеи и чаги и полибутилметакрилат Исследование противоопухолевой активности заявляемой композиции проводили на модели меланомы линии В16 у мышей С57В 1/6. Для индукции солидных опухолей мышам вводили подкожно клеточную суспензию (2·105 клеток в 0,1 мл физиологического раствора). Экспериментальным животным внутривенно вводили композицию в физ. растворе. В качестве препарата сравнения использовали препарат-прототип, содержащий те же экстракты и соевый лецитин. Препараты вводили один раз в неделю, всего три приема, начиная с 3 дня после прививки опухоли. Объем опухоли вычисляли по формуле
где Роп – средний размер опухолей в опытной группе, Рк – средний размер опухолей у контрольных животных. Увеличение продолжительности жизни леченых животных по сравнению с контролем определяли по формуле: Результаты исследования приведены в таблице 4. Как видно из таблицы, противоопухолевая активность заявляемой композиции заметно превышает активность препарата-прототипа.
Пример 5. Изучение антимикробной активности композиции (на модели сальмонеллезной инфекции у мышей) Белым мышам вводили внутрибрюшинно смыв суточной культуры сальмонелл в смеси с агаром. Одновременно внутривенно в растворе для инъекций вводили исследуемые препараты. Эффективность действия композиции оценивали по увеличению средней продолжительности жизни (УСПЖ) экспериментальных животных. В качестве препарата сравнения использовали препарат-прототип на основе соответствующих действующих веществ. Результаты приведены в таблице 5.
Таким образом, заявляемая композиция обладает выраженной противомикробной активностью.
Формула изобретения
1. Профилактическая композиция для предупреждения или лечения патологических процессов и поддержания высокого уровня функциональной активности организма, включающая комбинации одного или нескольких экстрактов лекарственных растений, содержащих вещества фенольной природы, и носитель, отличающаяся тем, что в качестве носителя используют биосовместимый полимер с размерами частиц от 10-4 до 10-8 м, при этом соотношение вещество фенольной природы: биосовместимый полимер составляет от 1:99 до 1:0,25, мас.%. 2. Профилактическая композиция по п.1, отличающаяся тем, что биосовместимый полимер выбран из группы: полиэтиленгликоль, поливиниловый спирт, полиалкилметакрилат, полилактид и его сополимеры с гликолевой кислотой, поливинилпирролидон, полиэтиленоксид, глицирризиновая кислота, циклодекстрин, декстран.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 5043323).
5043323). -циклодекстрин,
-циклодекстрин,  -циклодекстрин,
-циклодекстрин,  -циклодекстрин, декстран (мол. масса 324-500000).
-циклодекстрин, декстран (мол. масса 324-500000).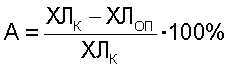 (0% – отсутствие антиоксидантной активности). В качестве препарата сравнения использовали комплексный препарат-прототип на основе соответствующего действующего вещества.
(0% – отсутствие антиоксидантной активности). В качестве препарата сравнения использовали комплексный препарат-прототип на основе соответствующего действующего вещества.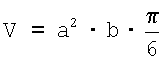 , где а – короткий, b – длинный диаметр опухоли. Относительный размер опухолей (ОРО) определяли по формуле:
, где а – короткий, b – длинный диаметр опухоли. Относительный размер опухолей (ОРО) определяли по формуле: 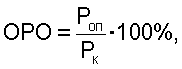
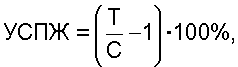 где Т – СПЖ леченых животных, дни, С – СПЖ контрольных животных, дни.
где Т – СПЖ леченых животных, дни, С – СПЖ контрольных животных, дни.