|
|
(21), (22) Заявка: 2007128393/15, 23.07.2007
(24) Дата начала отсчета срока действия патента:
23.07.2007
(46) Опубликовано: 27.03.2009
(56) Список документов, цитированных в отчете о
поиске:
SU 1081487 A1, 23.03.1984. SU 989411 A1, 15.01.1983. SU 883720 A1, 23.11.1981. SU 1059491, 07.12.1983.
Адрес для переписки:
414056, г.Астрахань, Татищева, 20-а, Астраханский государственный университет, отдел интеллектуальной собственности, к.209
|
(72) Автор(ы):
Алыков Нариман Мирзаевич (RU),
Алыкова Тамара Владимировна (RU),
Салмахаева Альфия Манцуровна (RU)
(73) Патентообладатель(и):
Государственное образовательное учреждение высшего профессионального образования “Астраханский государственный университет” (АГУ) (RU)
|
(54) СПОСОБ ЭКСПРЕССНОГО СОРБЦИОННО-ЦВЕТОМЕТРИЧЕСКОГО ОПРЕДЕЛЕНИЯ ТЕТРАЦИКЛИНА В МОЧЕ
(57) Реферат:
Изобретение относится к аналитической химии и касается количественного определения тетрациклина в моче человека и животных. Предложен способ экспрессного сорбционно-цветометрического определения тетрациклина в биологических средах, основанный на сорбционном концентрировании тетрациклина на минеральном сорбенте и формировании на сорбенте окрашенного соединения при участии тетрациклина, хлорида железа (III) и [Fe(CN)6]4-. Предложен экспресс-метод. Метод позволяет повысить чувствительность оценки содержания тетрациклина в моче. 1 табл., 1 ил.
Изобретение относится к аналитической химии и касается количественного определения тетрациклина в моче человека и животных.
Тетрациклины – традиционные популярные антибиотики широкого спектра действия, применяемые в медицине, ветеринарии и пищевой промышленности.
Тетрациклиновые антибиотики занимают также важное место среди средств хемиотерапии различных заболеваний и для создания методов диагностики при возникновении ряда заболеваний.
Это диктует необходимость определения наличия и концентрации тетрациклина в биологических объектах.
Известен фотометрический способ определения тетрациклина путем обработки анализируемой пробы раствором хлорамина и последующим фотометрированием полученного раствора [1].
Недостатками способа являются низкая чувствительность (0,05 мг/см3) и недостаточная селективность, т.к. невозможно проводить определение в окрашенных растворах и в присутствии других антибиотиков.
Известен также способ определения тетрациклина путем обработки анализируемой пробы раствором гидроксида натрия при рН 9-10,5 с последующим фотометрированием полученного раствора [2].
Недостатком данного способа является то, что в щелочной среде тетрациклин неустойчив. В зависимости от концентрации тетрациклина скорость деструкции будет настолько различной, что количественное определение с установленным доверительным интервалом на уровне 10% практически невозможно. Это означает, что в одной и той же пробе найденная концентрация тетрациклина может быть в 10 раз больше или в 10 раз меньше. Это обстоятельство является препятствием к применению данной методики.
Среди разработанных способов определения тетрациклина наиболее надежным является иммуноферментный анализ (ИФА) с использованием спорообразующих тест-культур Bacillus subtilis вар L2 [3].
К достоинствам ИФА следует отнести высокую чувствительность и возможность учета результатов через несколько часов от момента начала исследования.
К недостаткам метода относятся сложность осуществления самого анализа, трудности оценки специфичности полученных результатов и высокая стоимость.
Целью изобретения является создание высокочувствительного экспресс-метода оценки содержания тетрациклина в моче.
Метод основан на формировании координационных соединений, в которых один и тот же элемент находится в виде ионов с различной степенью окисления. Известно, что такие координационные соединения обладают высокой поглотительной способностью в видимом диапазоне спектра.
Изобретение включает стадии: а) пробоподготовка – удаление из мочи белков, б) сорбция тетрациклина силикагелем КСМГ, в) формирование на сорбенте окрашенного соединения при участие тетрациклина и ионов железа в степенях окисления +3 и +2.
Следующий пример представлен для того, чтобы наиболее полно проиллюстрировать изобретение.
Пример 1. Первая стадия определения тетрациклина (ТЦ) в моче человека и животных включает пробоподготовку – удаление из мочи белков. Для этого в 10 см3 отобранной мочи вносят 0,1 см3 20% раствора трихлоруксусной кислоты (ТХУ), перемешивают 5 мин, центрифугируют 5 мин при 3000 об/мин. Центрифугат переносят в другую центрифужную пробирку.
Вторая стадия: сорбция тетрациклина. В полученный центрифугат вносят 0,2 г силикагеля КСМГ, перемешивают 20 мин, центрифугируют 5 мин и центрифугат отбрасывают. К сорбенту вносят 10 см3 0,1 М уксусной кислоты, перемешивают, центрифугируют и центрифугат отбрасывают.
Третья стадия: формирование на сорбенте окрашенного соединения. К сорбенту после промывания вносят 0,1 см3 10-4 М раствора хлорида железа (III), доводят объем до 10 см3 0,1 М раствором уксусной кислоты, перемешивают 10 мин, центрифугируют 5 мин при 3000 об/мин, осадок дважды промывают 10 см3 0,1 М раствора уксусной кислоты. К осадку приливают 5 см3 0,1 М раствора уксусной кислоты, 1 см3 10-2 М раствора K4[Fe(CN)6], все тщательно перемешивают и через 20 мин определяют концентрацию ТЦ в пробе по тест-шкале, которую строят с ориентировкой на возможные концентрации ТЦ в моче.
Колористическая тест-шкала. В 10 центрифужных пробирок вносят 0; 0,05; 0,1; 0,2; 0,3; 0,4; 0,5; 1,0; 1,5; 2,0 см3 10-3 М раствора ТЦ, по 5 см3 мочи, не содержащей ТЦ, по 0,1 см3 20% ТХУ и доводят объемы растворов до 10 см3 0,1 М раствором уксусной кислоты. Перемешивают 5 мин, центрифугируют 5 мин при 3000 об/мин, центрифугат переносят в другие центрифужные пробирки. В полученные центрифугаты вносят по 0,2 г силикагеля КСМГ, содержимое пробирок перемешивают 20 мин и центрифугируют 10 мин при 3000 об/мин. Центрифугат отбрасывают, а к осадкам добавляют по 0,1 см3 10-4 М раствора хлорида железа (III), доводят до 10 см3 0,1 М раствором уксусной кислоты, перемешивают 10 мин, центрифугируют, центрифугат отбрасывают, осадки дважды промывают 0,1 М раствором уксусной кислоты. К промытым осадкам приливают по 5 см3 0,1 М раствора уксусной кислоты, по 1 см3 10-2 М К4[Fe(CN)6], доводят объемы до 10 см3 0,1 М раствором уксусной кислоты, все тщательно перемешивают и через 20 минут оценивают окраску силикагеля, которая меняется от бледно-голубой до зеленой см.чертеж. Окраска устойчива длительное время.
Результаты определения тетрациклина в моче методом «введено-найдено» по предлагаемой методике и методике сравнения представлены в таблице.
| Результаты определения тетрациклина в моче (n=6, р=0,95, tp=2,57) |
| Внесено в мочу тетрациклина, мкг/см3 |
Найдено, мкг/см3 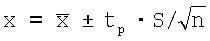 |
| Данным методом |
С использованием метода сравнения* |
| 0,00 |
– |
– |
| 0,25 |
0,25±0,02 |
0,20±0,03 |
| 0,5 |
0,50±0,05 |
0,45±0,05 |
| 1,0 |
1,00±0,01 |
0,95±0,09 |
| 1,5 |
1,50±0,10 |
1,45±0,10 |
| 2,0 |
2,00±0,20 |
2,00±0,30 |
| 2,5 |
2,50±0,30 |
2,40±0,30 |
| 5,0 |
5,00±0,50 |
4,50±0,50 |
| 7,5 |
7,5±0,80 |
7,0±0,90 |
| 10,0 |
10,0±1,00 |
10,0±1.50 |
| *Методические указания МУК. 4.2.026-95 |
Следует отметить, что тест-шкала с образованием окрашенного соединения тетрациклина с хлоридом железа (III) и K4[Fe(CN)6] на поверхности силикагеля КСМГ позволяет быстро оценить содержание тетрациклина в моче. В случае, если содержание тетрациклина не укладывается в шкалу, можно построить другую, для большего или меньшего интервала концентраций.
СПИСОК ЛИТЕРАТУРЫ
1. Соловей Н.В., Сааведра Н.Ф. Фотометрическое определение тетрациклина гидрохлорида. – Фармация, 1974, Т.23, №4, С.72-73.
2. Соболева О.Н. Способ определения тетрациклина: A.c. SU 1081487 A1; заявл. 1982.08.02; опубл. 1984.03.23.
3. Экспресс-метод определения антибиотиков в пищевых продуктах. Методические указания МУК 4.2.026-95, с.8.
Формула изобретения
Способ экспрессного определения тетрациклина в моче, характеризующийся тем, что тетрациклин концентрируют путем нанесения пробы мочи, из которой удалены белки, на сорбент, представляющий собой силикагель, формируют на нем окрашенное соединение при участии хлорида железа (III) и K4[Fe(CN)6] с последующим определением тетрациклина по колористической тест-шкале.
РИСУНКИ
|
|