|
|
(21), (22) Заявка: 2007139442/04, 25.10.2007
(24) Дата начала отсчета срока действия патента:
25.10.2007
(46) Опубликовано: 27.03.2009
(56) Список документов, цитированных в отчете о
поиске:
JP 58-059996, 09.04.1983. SU 204498, 30.11.1979. GB 1,152,748, 21.05.1969.
Адрес для переписки:
119021, Москва, ул. Б.Пироговская, 11, Государственное учреждение научно-исследовательский институт по изысканию новых антибиотиков им. Г.Ф. Гаузе Российской академии медицинских наук
|
(72) Автор(ы):
Преображенская Мария Николаевна (RU),
Олсуфьева Евгения Николаевна (RU),
Тевяшова Анна Николаевна (RU),
Бухман Владимир Михайлович (RU),
Штиль Александр Альбертович (RU),
Деженкова Любовь Георгиевна (RU)
(73) Патентообладатель(и):
Государственное учреждение научно-исследовательский институт по изысканию новых антибиотиков им. Г.Ф. Гаузе Российской академии медицинских наук (RU),
Государственное учреждение Российский онкологический научный центр им. Н.Н. Блохина Российской академии медицинских наук (RU)
|
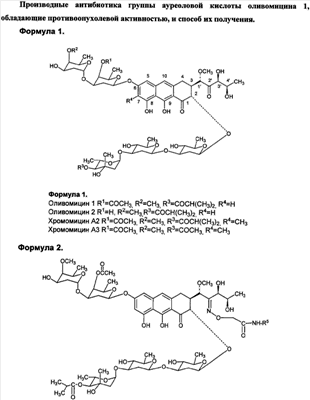
(54) ПРОИЗВОДНЫЕ АНТИБИОТИКА ГРУППЫ АУРЕОЛОВОЙ КИСЛОТЫ ОЛИВОМИЦИНА 1, ОБЛАДАЮЩИЕ ПРОТИВООПУХОЛЕВОЙ АКТИВНОСТЬЮ, И СПОСОБ ИХ ПОЛУЧЕНИЯ
(57) Реферат:
Изобретение относится к обладающим противоопухолевой активностью производным антибиотика группы ауреоловой кислоты оливомицина I, соответствующим структурной формуле, приведенной ниже, в которых R5 представляет собой водород, С3-С10-циклоалкил или C1-C4-алкил с прямой или разветвленной углеводородной цепью, необязательно замещенный одним или несколькими гидроксилами. Изобретение относится также к способу получения указанных производных, заключающемуся в селективной модификации 2′-карбонильной группы оливомицина 1 реакцией с аминооксиуксусной кислотой, с последующим проведением реакции амидирования полученного ключевого интермедиата 2′-(карбоксиметоксим)оливомицина 1 с соответствующими аминами в присутствии конденсирующего агента. 2 н.п. ф-лы, 5 табл.
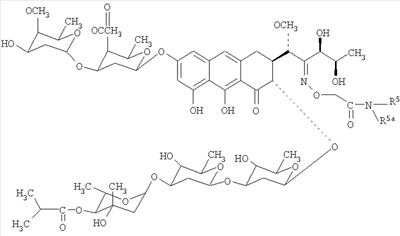
Изобретение относится к фармацевтической промышленности и касается новых производных противоопухолевого антибиотика группы ауреоловой кислоты оливомицина 1 и способа их получения.
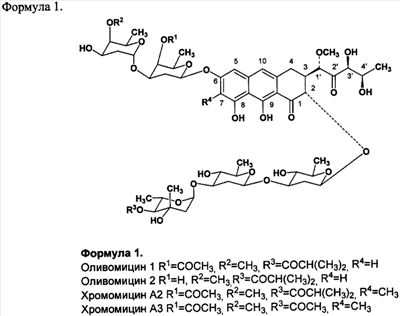
Антибиотики группы ауреоловой кислоты являются высокоэффективными природными противоопухолевыми препаратами, некоторые из которых разрешены к применению в качестве антинеопластических агентов для лечения ряда опухолевых заболеваний. Важнейшими представителями этой группы являются: оливомицин 1 (оливомицин А) (формула 1, R1=СОСН3, R2=СН3, R3=COCH(CH3)2, R4=H), оливомицин 2 (формула 1, R1=H, R2=СН3, R3=COCH(CH3)2, R4=H), хромомицин А2 (формула 1, R1=СОСН3, R2=СН3, R3=COCH(CH3)2, R4=CH3), хромомицин A3 (формула 1, R1=СОСН3, R2=СН3, R3=COCH3, R4=CH3), митрамицин.
Механизм действия антибиотиков группы ауреоловой кислоты основан на взаимодействии их с GC-парами в малой бороздке ДНК и нарушении структуры и функции нуклеиновых кислот, в том числе генной транскрипции [Симонова B.C., Самусенко А.В., Филиппова Н.А., Тевяшова А.Н., Лынив Л.С., Кулик Г.И., Чехун В.Ф., Штиль А.А. «Оливомицин вызывает апоптоз опухолевых клеток и подавляет р53-индуцированную транскрипцию». Бюллетень экспериментальной биологии и медицины, 2005, том 139, № 4, стр.451-455]. Антибиотики группы ауреоловой кислоты наряду с ценными свойствами имеют ряд недостатков, основными из которых являются высокая токсичность, мутагенность, канцерогенность, миело- и иммунодепрессивное действие.
Настоящее изобретение призвано получить новые производные антибиотика группы ауреоловой кислоты оливомицина 1, обладающие противоопухолевой активностью и низкой токсичностью. Изобретение включает соединения, соответствующие формуле 2.
Формула 2.
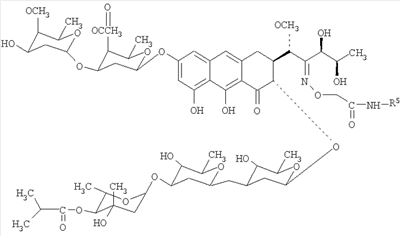
где R5 представляет собой водород, С3-С10-циклоалкил или С1-С4-алкил с прямой или разветвленной углеводородной цепью, необязательно замещенный одним или несколькими гидроксилами.
Хотя химическая модификация природных антибиотиков, в том числе противоопухолевых, является важнейшим способом получения новых препаратов, обладающих преимуществами перед исходными антибиотиками, химическая модификация антибиотиков группы ауреоловой кислоты практически не проводилась.
Известен полный синтез антибиотика оливомицина 1 [Roush W.R., Hartz R.A., Gustin D.J. «Total synthesis of olivomycin A», Journal of American Chemical Society, 1999, vol. 121, pp.1990-1991]. Описаны подходы к модификации оливомицина 1 по 2′-карбонильной группе и по ароматической части агликона. Авторами были описаны основные типы модификации оливомицина 1 по 2′-карбонильной группе: имин, оксимы, гидразон, семикарбазон. Все известные производные оливомицина 1 по карбонильной группе обладают цитотоксичностью, сравнимой с исходным оливомицином 1 [Kumar V., Remers W.A. “Preparation and antitumor activity of olivomycin A analogues”. Journal of Medicinal chemistry, 1980, vol.23, pp.376-379].
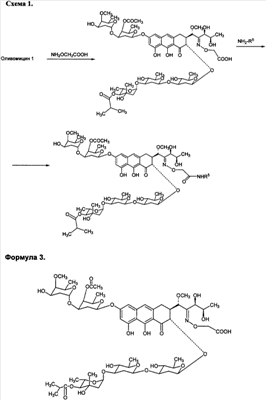
Изобретение также включает в себя способ получения производных антибиотика группы ауреоловой кислоты оливомицина 1 (формула 2), заключающийся в селективной модификации 2′-карбонильной группы оливомицина 1 реакцией с аминооксиуксусной кислотой (Схема 1), с последующим проведением реакции амидирования полученного ключевого интермедиата 2′-(карбоксиметоксим)оливомицина 1 (формула 3) с соотвествующими аминами в присутствии конденсирующего агента.
Реакцию амидирования 2′-(карбоксиметоксим)оливомицина 1 (формула 3) амином с получением соединения формулы 2 проводят в присутствии конденсирующих агентов, известных из уровня техники и применяемых для образования амидной связи, например бензотриазол-1-ил-окси-триспирролидинофосфоний гексафторфосфата (РуВОР) или O-(бензотриазол-1-ил)-N,N,N’,N’-бис(тетраметилен)) гексафторфосфат мочевины (HBPyU). Реакцию амидирования 2′-(карбоксиметоксим)оливомицина 1 (формула 3) амином с получением соединения формулы 2 проводят в растворителе, выбираемом из метанола, этанола, N,N-диметилформамида, диметилсульфоксида, толуола, ксилола и хлороформа.
Соединения формулы 2 обладают выраженной противоопухолевой активностью и сниженной токсичностью по сравнению с исходным оливомицином 1 (см. Примеры 4-6) и могут быть использованы для лечения онкологических заболеваний.
Вспомогательные средства.
Полугидрохлорид аминооксиуксусной кислоты, бензотриазол-1-ил-окси-триспирролидинофосфоний гексафторфосфат (РуВОР), O-(бензотриазол-1-ил)-N,N,N’,N’-бис(тетраметилен)) гексафторфосфат мочевины (HBPyU) были коммерческими продуктами фирмы Acros. Гидрохлорид 2-адамантиламина, триэтиламин были коммерческими продуктами фирмы Aldrich (США).
Тонкослойную хроматографию осуществляли на пластинках с силикагелем G60 (Merck) в смесях растворителей: хлороформ-метанол-муравьиная кислота: 9:1:0.05 (А). Для препаративной очистки использовали колоночную хроматографию на силикагеле Merck G60 с размером частиц 0.040-0.063  м. м.
ВЭЖХ проводили на приборе Shimadzu HPLC LC 10 на колонке Diaspher С18 № 1500, элюент: 0.01 н. Н3PO4 – MeCN, pH 2.6, в градиенте ацетонитрила от 40% до 80%, скорость потока 1.1 мл/мин. Регистрация велась на длине волны 274 нм, при температуре 20°С.
ИК-спектры снимали в таблетке КВг на спектрофотометре DTGS.
1H ЯМР и 13С ЯМР спектры регистрировали на спектрометрах Varian VXR-400 (США) при частоте 400 МГц.
Масс-спектры при ионизации электрораспылением (ESI) получали на приборе Finnigan MAT 900S (Германия), масс-спектры, полученные при ионизации методом MALDI (матричная лазерная десорбционная ионизация), получены на приборе Brucker BIFLEX III.
Примеры получения производных антибиотика группы ауреоловой кислоты оливомицина 1 по настоящему изобретению и изучение их противоопухолевой активности.
Пример 1.
Получение 2′-(карбоксиметоксим)оливомицина 1 (LCTA 1295) (Формула 3).
К раствору оливомицина I (0.100 мг, 0.084 ммоль) в МеОН (3 мл) добавляли полугидрохлорид аминооксиуксусной кислоты (4.5 мг, 0.42 ммоль). Реакционную смесь выдерживали при 37°С в течение 50 ч. Реакционную смесь упаривали, наносили на колонку с силикагелем, элюировали смесью CHCl3-МеОН-НСООН (9:1:0.05). Фракции, содержащие целевое вещество объединяли, удаляли растворитель на роторном вакуумном испарителе до минимального объема и добавляли петролейный эфир. Выпавший осадок отфильтровывали, промывали петролейным эфиром, высушивали.
Выход: 53 мг (50%). Rf(A) 0.42, Rt 12.38.
Тпл 140-142°С (с разложением).
13С-ЯМР (DMSO-d6) спектр 2′-(карбоксиметоксим)оливомицина 1 полностью соответствует 13С-ЯМР спектру исходного оливомицина (DMSO-d6) [отнесение сигналов см. Yoshimura Y., Koenuma M., Matsumoto К., Tori К., Terui Y. “MNR studies of Chromomycins, olivomycins and their derivatives”. The Journal of Antibiotics, 1988, vol. XLI, № 1, pp.53-67], за исключением: отсутствует сигнал 211.81 м.д., соответствующий 2′-карбонильной группе в оливомицине 1; появляются сигналы: 171.203 (-СООН), 158.815 (-C=N-), 70.45 (-ОСН2).
MS MALDI: MW вычислено для С60Н87HO28 1269.54, найдено 1292.63 (M+Na)+.
Пример 2.
Общая методика амидирования 2′-(карбоксиметоксим)оливомицина 1.
К раствору 2′-(карбоксиметоксим)оливомицина 1 (0.039 ммоль) в МеОН (3 мл) добавляли гидрохлорид амина (0.078 ммоль). Значение рН реакционной смеси доводили до 8-8.8 добавлением триэтиламина. Несколькими порциями добавляли конденсирующий реагент (0.058 ммоль), контролируя рН реакционной смеси добавлением триэтиламина. Реакционную смесь перемешивали в течение 2 ч, удаляли растворитель на роторном вакуумном испарителе. Остаток растворяли в CHCl3 и наносили на колонку с силикагелем. Вещество элюировали сначала CHCl3, а затем смесью CHCl3-МеОН-НСООН (9:1:0.05). Фракции, содержащие целевое вещество, объединяли, удаляли растворитель на роторном вакуумном испарителе до минимального объема и добавляли петролейный эфир. Выпавший осадок отфильтровывали, промывали петролейным эфиром, высушивали.
Чистота полученных соединений изучалась методами ТСХ и ВЭЖХ. Структура полученных соединений была подтверждена данными масс-спектрометрии.
Пример 3.
Получение 2-адамантиламид 2′-(карбоксиметоксим)оливомицина 1 (LCTA-1297).
К раствору 2′-(карбоксиметоксим)оливомицина 1 (50 мг, 0.039 ммоль) в МеОН (3 мл) добавляли гидрохлорид 2-адамантиламина (14.6 мг, 0.078 ммоль). Значение рН реакционной смеси доводили до 8-8.8 добавлением триэтиламина. Несколькими порциями добавляли РуВОР (30 мг, 0.058 ммоль), контролируя рН реакционной смеси добавлением триэтиламина. Реакционную смесь перемешивали в течение 2 ч, удаляли растворитель на роторном вакуумном испарителе. Остаток растворяли в CHCl3 и наносили на колонку с силикагелем. Вещество элюировали сначала CHCl3, а затем смесью CHCl3-МеОН-НСООН (9:1:0.05). Фракции, содержащие целевое вещество, объединяли, удаляли растворитель на роторном вакуумном испарителе до минимального объема и добавляли петролейный эфир. Выпавший осадок отфильтровывали, промывали петролейным эфиром, высушивали.
Выход: 30 мг (55%). Rf(A) 0.27, Rt 19.46.
Тпл 155-157°С (с разложением).
MS MALDI: MW вычислено для C70H102N2O27 1402.67, найдено 1425.47 (M+Na)+.
Аналогичным образом были получены в том числе следующие соединения: LCTA 1296 (амид 2′-(карбоксиметоксим)оливомицина 1), LCTA 1298 (этаноламид 2′-(карбоксиметоксим)оливомицина 1), LCTA 1344 (трет-бутиламид 2′-(карбоксиметоксим)оливомицина 1), LCTA 1345 (ди-(гидроксиметил)-метил-метил амид 2′-(карбоксиметоксим)оливомицина 1). Данные соединения соответствуют Формуле 2, где значения R5 представлены в таблице 1.
| Таблица 1 |
| Соединение |
R5 |
| LCTA 1296 |
H |
| LCTA 1297 |
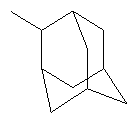 |
| LCTA 1298 |
 |
| LCTA 1344 |
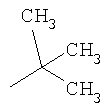 |
| LCTA 1345 |
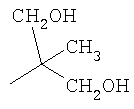 |
Пример 4.
Изучение антипролиферативной активности заявленных новых производных оливомицина 1 проводилось на культуре опухолевых клеток мышиного лейкоза L1210/0. Данные об антипролиферативной активности изученных производных оливомицина 1 представлены в Таблице 2.
| Таблица 2 |
| Антипролиферативная активность оливомицина 1 и новых производных оливомицина 1 в отношении опухолевых клеток линии (L1210/0). |
| Соединение |
IC50 * ( М) М) |
| L1210/0 |
| Оливомицин 1 |
0.034±0.002 |
| LCTA 1295 |
6.5±2.8 |
| LCTA 1296 |
3.6±3.1 |
| LCTA 1297 |
0.19±0.01 |
| LCTA 1298 |
18±5 |
| LCTA 1344 |
0.20±0.01 |
| LCTA 1345 |
20±11 |
IC50 – концентрация соединения, вызывающая гибель 50% клеток
Изучение антипролиферативной активности производных оливомицина 1 проводилось также на культурах опухолевых клеток линий лейкоза человека К562, рака толстой кишки НСТ116 и рака молочной железы MCF-7. Данные этих экспериментов представлены в таблице 3.
Таблица 3. Антипролиферативная активность оливомицина 1 и новых производных оливомицина 1 в отношении опухолевых клеток линии MCF-7, К562, НСТ116.
| Соединение |
IC50 * (nM) |
| MCF-7 |
К562 |
НСТ116 |
| Оливомицин 1 |
35 |
25 |
46 |
| LCTA 1344 |
950 |
1200 |
1250 |
| LCTA 1345 |
850 |
1000 |
1000 |
IC50 – концентрация соединения, вызывающая гибель 50% клеток
Пример 5.
Изучение противоопухолевой активности препарата LCTA 1297 (2-адамантиламид 2′-(карбоксиметоксим)оливомицина 1) при однократном введении проводили на мышах с лимфомой Р388. Самцы мышей B6D2F1 привиты внутрибрюшинно по 106 клеток асцитной лимфомы Р388 в день 0. Препарат LCTA 1297 растворяли в 0,1% ДМСО, разводили физиологическим раствором поваренной соли и вводили однократно внутрибрюшинно в день 3 (Таблица 4).
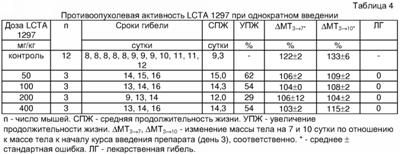
Как видно из представленных данных, при введении соединения в дозах от 50 до 400 мг/кг внутрибрюшинно наблюдалось выраженное противоопухолевое действие препарата при отсутствии токсической гибели мышей. Продолжительность жизни леченых мышей была выше по сравнению с контрольной группой (УПЖ до 62%). Введение препарата LCTA 1297 тормозило накопление асцита, что выражалось в высоко достоверном замедлении увеличения массы тела, масса тела у контрольных мышей увеличилась к 7 суткам до 122% за счет накопления асцита.
Пример 6.
Изучение противоопухолевой активности препарата LCTA 1297 при многократном введении проводили на мышах с лимфомой Р388. Самцы мышей B6D2F1 привиты внутрибрюшинно по 106 клеток асцитной лимфомы Р388 в день 0. Препарат LCTA 1297 растворяли в 0,1% ДМСО, разводили физиологическим раствором поваренной соли и вводили курсом с 3 по 7 сутки внутрибрюшинно (Таблица 5).
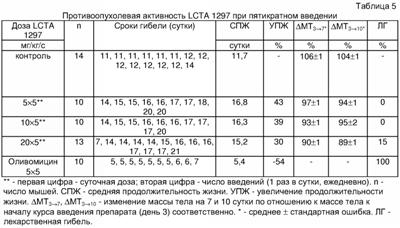
Как видно из представленных данных, при введении соединения LCTA 1297 в дозах от 5 до 10 мг/кг в сутки внутрибрюшинно отмечено выраженное противоопухолевое действие препарата и отсутствие токсической гибели мышей. Продолжительность жизни леченых мышей превышала таковую у контрольных мышей (УПЖ до 43%). Введение LCTA 1297 тормозило накопление асцита, что выражалось в высокодостоверном замедлении увеличения массы тела. Масса тела у контрольных мышей увеличилась к 7 и 10 суткам до 106% и 104% соответственно за счет накопления асцита. При применении препарата в дозе 20 мг/кг в сутки внутрибрюшинно наблюдалась токсическая гибель 2 из 13 мышей на фоне значительного снижения веса животных. При применении оливомицина 1 в дозе до 5 мг/кг в сутки внутрибрюшинно наблюдалась токсическая гибель всех мышей, причем в большинстве случаев после трех инъекций.
Таким образом, предложенный новый способ модификации антибиотика группы ауреоловой кислоты оливомицина 1 позволяет получать новые производные оливомицина 1, обладающие преимуществами перед исходным антибиотиком оливомицином 1, а именно: высокой противоопухолевой активностью и низкой токсичностью соединений.
Формула изобретения
1. Производные антибиотика группы ауреоловой кислоты, соответствующие формуле: 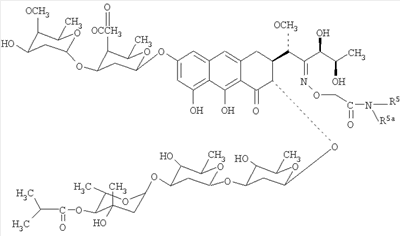
где R5 представляет собой водород, С3-С10-циклоалкил или С1-С4-алкил с прямой или разветвленной углеводородной цепью, необязательно замещенный одним или несколькими гидроксилами.
2. Способ получения производных антибиотика группы ауреоловой кислоты оливомицина 1 по п.1, заключающийся в селективной модификации 2′-карбонильной группы оливомицина 1 реакцией с аминооксиуксусной кислотой, с последующим проведением реакции амидирования полученного ключевого интермедиата 2′-(карбоксиметоксим)оливомицина 1 с соответствующими аминами в присутствии конденсирующего агента.
|
|