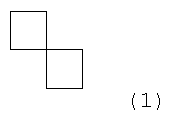Патент на изобретение №2350595
|
||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ СПИРО[3.3]ГЕПТАНА
(57) Реферат:
Изобретение относится к области органического синтеза, конкретно к способу получения спиро[3,3]гептана, который может найти применение в тонком органическом синтезе, в производстве жидкокристаллических систем, а также биологически активных веществ. Сущность предложенного способа заключается во взаимодействии метиленциклобутана с триэтилалюминием в присутствии катализатора – цикронацендихлорида в атмосфере аргона при комнатной температуре в гексане в течение 5-7 ч с последующим добавлением трифенилфосфина, ацетилацетоната палладия, свежеперегнанного аллилхлорида и перемешиванием реакционной массы 5 ч. Технический результат – упрощение способа и получение целевого соединения с высокой селективностью. 1 табл.
Предлагаемое изобретение относится к области органической химии, в частности к способу получения спиро[3.3]гептана общей формулы (1):
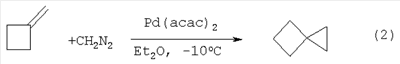
Спиро[3.3]гептан может найти применение в тонком органическом синтезе, в производстве жидкокристаллических систем, а также биологически активных веществ. Известен способ [У.М.Джемилев, В.А.Докичев, С.З.Султанов, Р.И.Хуснутдинов, Ю.В.Томилов, О.М.Нефедов, Г.А.Толстиков. Взаимодействие диазоалканов с непредельными соединениями. Сообщение 6. Каталитическое циклопропанирование различных непредельных углеводородов и их производных с диазометаном. Известия АН СССР. Сер.хим., №8, 1989, 1861-1869] получения спирогексана (2) взаимодействием метиленциклобутана с эфирным раствором диазометана в присутствии катализатора Pd(acac)2 с выходом 48% по схеме: Известный способ не позволяет синтезировать спиро[3.3]гептан формулы (1). Известен способ [B.Weinstein, A.H.Fenselau, J.G.Thoene. Syntesis of Spiro[3.3]heptane. J.Chem.Soc., 1965 (March), 2281] получения спиро[3.3]гептана (1) с выходом 50% двустадийной реакцией исходя из спирогептанкарбоновой кислоты, ацетата свинца Pb(ОАс)4, иода 12 и лития Li по схеме: Известный способ синтеза спиро[3.3]гептана (1) предполагает использование дорогостоящей и труднодоступной спирогептанкарбоновой кислоты, токсичного тетраацетата свинца, процесс проходит в две технологические стадии с выделением промежуточного продукта. Предлагается усовершенствованный способ синтеза спиро[3.3]гептана (1). Сущность способа заключается во взаимодействии метиленциклобутана с триэтилалюминием (Et3Al) в присутствии катализатора цирконацендихлорида (Ср2ZrCl2), взятых в мольном соотношении метиленциклобутан: Et3Al: Cp2ZrCl2=10: (10-14): (0.4-0.6), предпочтительно 10:12:0.5, в атмосфере аргона при комнатной температуре (20°С) и атмосферном давлении в алифатическом (гексан) растворителе в течение 5-7 ч с последующим добавлением к реакционной массе при -10°С диэтилового эфира в объеме, равном объему алифатического растворителя, затем трифенилфосфина (Ph3Р) и ацетилацетоната палладия (Pd(acac)2) в эквимольном к Cp2ZrCl2 количестве, затем свежеперегнанного аллилхлорида в трехкратном избытке на взятый Et3Al, перемешивают реакционную массу еще 5 ч. Получают целевой продукт (1) с выходом 69-78%. Реакция протекает по схеме: Целевой продукт (1) образуется только лишь с участием в качестве исходных реагентов метиленциклобутана, триэтилалюминия, аллилхлорида и комплексных катализаторов Cp2ZrCl2, Pd(acac)2 – Ph3Р. В присутствии других олефинов (например, 4-винилциклогекс-1-ена, метиленалканов, циклоолефинов), других соединений алюминия (например, EtAlCl2, изо-Bu3Al, изо-Bu2AlCl, изо-Bu2AlH) или других комплексов переходных металлов (например, Zr(acac)4, Ср2TiCl2, Ni(acac)2, Fe(асас)3) целевой продукт (1) не образуется. Проведение реакции в присутствии катализатора Cp2ZrCl2 больше 0.6 ммоль на 10 ммоль метиленциклобутана не приводит к существенному увеличению выхода целевого продукта (1). Использование в реакции катализатора Cp2ZrCl2 менее 0.4 ммоль на 10 ммоль метиленциклобутана снижает выход спиро[3.3]гептана (1), что связано с уменьшением каталитически активных центров в реакционной массе. Изменение соотношения исходных реагентов в сторону увеличения содержания Et3Al по отношению к метиленциклобутану не приводит к значительному повышению выхода целевого продукта (1). Снижение количества Et3Al по отношению к метиленциклобутану уменьшает выход спиро[3.3]гептана (1). Существенные отличия предлагаемого способа В предлагаемом способе используются в качестве исходных соединений производимые в промышленных масштабах метиленциклобутан, Et3Al и аллилхлорид, а также доступные катализаторы Cp2ZrCl2 и Pd(acac)2. Процесс проходит в одну технологическую стадию без выделения промежуточных подуктов. В известном способе спиро[3.3]гептан (1) получают из дорогостоящей и труднодоступной спирогептанкарбоновой кислоты и токсичного тетраацетата свинца Pb(ОАс)4, процесс проходит в две технологические стадии с выделением промежуточного продукта. Предлагаемый способ обладает следующими преимуществами: 1. Способ позволяет получать с высокой селективностью спиро[3.3]гептан (1) без использования труднодоступной спирогептанкарбоновой кислоты и высокотоксичного тетраацетата свинца Pb(ОАс)4. Способ поясняется следующими примерами: ПРИМЕР 1. В стеклянный реактор, установленный на магнитной мешалке, в атмосфере аргона помещают 2 мл гексана, 0.5 ммоль Cp2ZrCl2, 10 ммолей метиленциклобутана, при температуре 0°С 12 ммолей Et3Al, перемешивают при комнатной температуре 6 ч. Далее реакционную массу охлаждают до -10°С, добавляют диэтиловый эфир 2 мл, 0.5 ммоль Ph3Р, 0.5 ммоль Pd(acac)2 и 36 ммолей свежеперегнанного аллилхлорида. Температуру доводят до комнатной и перемешивают еще 5 часов. Получают индивидуальный спиро[3.3]гептан (1) с выходом 72%.
Другие примеры, подтверждающие способ, приведены в таблице 1.
Все опыты проводили при комнатной температуре (20°С) в гексане.
Формула изобретения
Способ получения спиро[3.3]гептана общей формулы (1)
отличающийся тем, что метиленциклобутан брутто-формулы C5H8 подвергают взаимодействию с триэтилалюминием Et3Al в присутствии катализатора цирконацендихлорида Ср2ZrCl2 в мольном соотношении метиленциклобутан:Et3Al:Ср2ZrCl2=10:(10-14):(0,4-0,6) в атмосфере аргона при нормальном давлении в гексане, в течение 5-7 ч с последующим добавлением при -10°С диэтилового эфира в объеме, равном взятому гексану, трифенилфосфина Ph3Р и ацетилацетоната палладия Pd(acac)2 в эквимольном к Cp2ZrCl2 количестве, затем прибавляют свежеперегнанный аллилхлорид в трехкратном избытке на взятый Et3Al, температуру доводят до комнатной и перемешивают еще 5 ч.
|
||||||||||||||||||||||||||||||||||||||||||

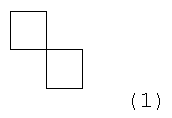


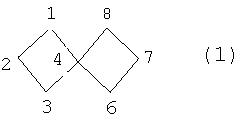
 , м.д.) спиро[3.3]гептана (1): 16.34 (С2,7), 35.19 (С1,3,6,8), 44.21 (С4)
, м.д.) спиро[3.3]гептана (1): 16.34 (С2,7), 35.19 (С1,3,6,8), 44.21 (С4)