Патент на изобретение №2162714
|
||||||||||||||||||||||||||
(54) РАДИОФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ
(57) Реферат: Изобретение относится к медицине, а именно к радиофармацевтическим препаратам, содержащим радионуклид самарий-153, и может быть использовано для лечения метастазов злокачественных новообразований в кости и ревматоидных артритов. Изобретение заключается в том, что заявленное средство представляет собой радиофармацевтическую композицию, содержащую самарий-153, самарий в виде комплекса с окса-бис(этиленнитрило)тетраметиленфосфоновой кислотой или ее физиологически приемлемой солью, натрия хлорид, воду для инъекций при определенном соотношении ингредиентов, при этом объемная активность самария-153 составляет 240-740 МБк/мл, а pH композиции 5-7. Изобретение обеспечивает простоту приготовления, повышение терапевтического эффекта, исключение токсических реакций при введении в организм пациента. 2 табл. Изобретение относится к медицине, а именно к радиофармацевтическим препаратам, содержащим радионуклид 153Sm, и может быть использовано для лечения метастазов злокачественных новообразований в кости и ревматоидных артритов. Радионуклид самарий-153 испускает гамма-кванты с энергией 69,7 и 106 кэВ и выходами 5,4 и 28% соответственно и бета-излучение 650, 720 и 820 КэВ с выходами 20, 40 и 40% соответственно. Период полураспада самария-153 составляет 46,2 ч. Комплексы 153Sm с полиметиленфосфоновыми кислотами обладают способностью к избирательному накоплению в метастатических и воспалительно-деструктивных очагах костной ткани. Благодаря наличию гамма-излучения 153Sm препараты на основе указанных комплексов воздействуют на клетки метастатическоого или воспалительного очага и окружающие его нервные окончания, вызывая одновременно обезболивающий и антипролиферативный эффект. Наличие гамма-излучения позволяет регистрировать распределение накопления препарата в организме при помощи гамма-камеры. В настоящее время известно несколько препаратов, содержащих 153Sm, для лечения метастазов злокачественных новообразований в кости. Так, известны комплексы органических аминофосфоновых кислот для лечения кальцифицированных опухолей [1]. Для создания композиции используют радионуклиды 153Sm, 166Ho, 175Yb, 177Lu, 159Gd и органические аминофосфоновые кислоты, в которых аминный азот и фосфор связаны между собой через алкиленовые группы 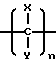 где X и Y независимо друг от друга – водород, гидроксил, карбоксил, фосфоновая группа, углеводородный радикал, имеющие 1 – 8 углеродных атомов и их физиологически приемлемые соли, а n = 1 – 3. При этом, если n>1, каждый X и Y могут быть одинаковыми или различаться количеством углеродных атомов. Структурные формулы соединений могут быть изображены следующим образом: 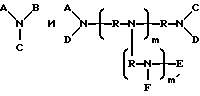 где заместители A, B, C, D, E и F независимо друг от друга – водород и кислотные радикалы физиологически приемлемой соли; 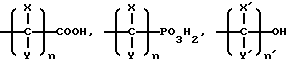 где X, Y и n, а также X’ и Y’ – независимый водород, метиловый или этиловый радикал, n’ составляет 2 или 3; m и m’ каждый независимо могут быть 0 – 10, при этом по крайней мере один атом азота может замещаться преимущественно фосфорсодержащей группой; где R – углеводородный радикал, который может быть линейным, ветвистым, циклическим, гетероциклическим или иметь кольцевую замкнутую структуру, при этом, если m или m’>1, то заменители E и F – одинаковые или отличаются от других заменителей количеством атомов азота, а также R могут быть одинаковыми или различными. Конкретно описана композиция, включающая 25 – 35 мг ЭДТМФ (этилендиаминтетраметиленфосфоновая кислота) и 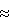 10 мКи 153Sm и имеющая pH 7 – 8, а также аналогичные композиции для других кислот.
Недостатком описанных композиций является установленный к настоящему времени факт образования продуктов радиационного разложения органических кислот в случае использования высоких активностей радионуклида и возможность их нежелательного взаимодействия с компонентами крови при введении препарата в организм.
Наиболее близким аналогом к заявляемому техническому решению являются замороженные радиофармацевтические композиции, представляющие собой комплекс по крайней мере одного радионуклида с лигандом или его физиологически приемлемой солью, особенно 153Sm-ЭДТМФ (этилендиаминтетраметиленфосфоновая кислота), которые могут содержать ионы металла (Ca2+) и которые замораживают, оттаивают и затем используют для инъекции [2]. В данном случае ионы Ca2+ вводятся в состав композиции с целью предотвращения связывания кальция крови ЭДТМФ, а замораживание производится с целью замедления реакций радиолиза в растворе препарата и соответственно снижения содержания продуктов радиолиза в препарате. При этом ионы двухвалентного металла (Ca2+) вводят перед замораживанием композиции в мольных соотношениях Me:лиганд 0,25:1; 0,5:1; 0,75: 1; 0,9: 1. Возможно использование также Fe2+, Mn2+ или ионов щелочноземельных элементов Be2+, Mg2+, Sr2+, Ba2+. После размораживания препарат вводится парентерально, внутривенно, внутримышечно или подкожно.
Недостатки аналога: 10 мКи 153Sm и имеющая pH 7 – 8, а также аналогичные композиции для других кислот.
Недостатком описанных композиций является установленный к настоящему времени факт образования продуктов радиационного разложения органических кислот в случае использования высоких активностей радионуклида и возможность их нежелательного взаимодействия с компонентами крови при введении препарата в организм.
Наиболее близким аналогом к заявляемому техническому решению являются замороженные радиофармацевтические композиции, представляющие собой комплекс по крайней мере одного радионуклида с лигандом или его физиологически приемлемой солью, особенно 153Sm-ЭДТМФ (этилендиаминтетраметиленфосфоновая кислота), которые могут содержать ионы металла (Ca2+) и которые замораживают, оттаивают и затем используют для инъекции [2]. В данном случае ионы Ca2+ вводятся в состав композиции с целью предотвращения связывания кальция крови ЭДТМФ, а замораживание производится с целью замедления реакций радиолиза в растворе препарата и соответственно снижения содержания продуктов радиолиза в препарате. При этом ионы двухвалентного металла (Ca2+) вводят перед замораживанием композиции в мольных соотношениях Me:лиганд 0,25:1; 0,5:1; 0,75: 1; 0,9: 1. Возможно использование также Fe2+, Mn2+ или ионов щелочноземельных элементов Be2+, Mg2+, Sr2+, Ba2+. После размораживания препарат вводится парентерально, внутривенно, внутримышечно или подкожно.
Недостатки аналога:– уровень кальция в крови пациента является достаточно индивидуальным показателем, и введение его в состав препарата не всегда необходимо и желательно; механизм действия препаратов на основе полиметиленфосфоновых кислот предполагает в первую очередь декальцинацию патологического очага, что может быть затруднено, если значительная часть координационных групп в молекуле лиганда будет связана с ионами металлов; кроме того, использование в основе препарата больших количеств таких металлов, как Fe, Mn, Be, Sr, Ba, может вызвать токсическую реакцию у пациента; наконец, соли двухвалентных металлов с ЭДТМФ имеют ограниченную растворимость в области pH выше 5, поэтому в ряде случаев возможно образование коллоидов или взвесей в растворе препарата, которое приводит к повышенному накоплению его в печени; следует отметить, что в примерах текста прототипа имеются указания на факты повышенного накопления препарата в печени, которое авторы относят к неинтерпретированным результатам; – проведение процедуры замораживания и оттаивания радиоактивного препарата является серьезным усложнением технологии; при этом гарантировать сохранность препарата в замороженном виде при транспортировании от производства в клинику практически нереально, а необходимость оттаивания в клинике связано с дополнительными временными затратами и лучевыми нагрузками на медицинский персонал. Эти обстоятельства поставили перед авторами задачу разработки препарата, представляющего собой физиологически приемлемый раствор 153Sm, обладающего способностью повышенного накопления в воспалительных очагах костной ткани и сохраняющего свои свойства в течение срока годности, который в соответствии с периодом полураспада радионуклида был выбран в 4 суток. Поставленная задача достигается тем, что в качестве препарата для лечения костных метастазов и ревматоидных артритов предлагается композиция, представляющая собой раствор, содержащий самарий-153, самарий в виде комплекса с окса-бис(этиленнитрило)тетраметиленфосфоновой кислотой (оксабифор) или ее натриевой солью, а также натрия хлорид 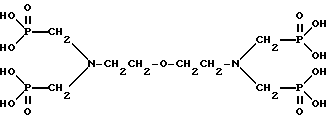 Препарат приготавливают следующим образом. Самарий-153 получают, облучая в ядерном реакторе 1-2 мг обогащенного самария-152 в форме хлорида. После облучения последний растворяют в 0,1 М растворе соляной кислоты и постепенно смешивают с заранее приготовленным вспомогательным раствором, содержащим 15,0-25,0 мг/мл натрия оксабифора и 4,0-6,0 мг/мл натрия хлорида. Объемная активность полученного препарата на время изготовления составляет от 240 до 740 МБк/мл. Полученный препарат фасуют во флаконы для лекарственных средств порциями от 925 до 3700 МБк и стерилизуют. Предельные значения концентраций компонентов установлены на основании экспериментальных данных, полученных при анализе ряда образцов препарата, и представлены ниже, мг: Натрий окса-бис(этиленнитрило)тетраметиленфосфоновой кислоты – 15 – 25 Самарий в виде комплекса самария с окса-бис(этиленнитрило)тетраметиленфосфоновой кислотой – 0,025 – 0,100 Натрия хлорид – 4 – 6 Вода для инъекций, мл – До 1 При этом объемная активность самария-153 составляет 240-740 МБк/мл. Препарат стерилен и апирогенен и имеет pH 5-7. Клинические испытания препарата проведены [в соответствии с решением Фармакологического государственного комитета N 1 от 12.01.95 г] в Медицинском радиологическом научном центре РАМН в течение 1996-1999 гг. С целью стойкого снижения интенсивности болевого синдрома, вызванного наличием метастатической ткани в костных очагах, препарат вводят в количестве 55,5 МБк/кг веса тела больного внутривенно. В ревматологической практике используют активность из расчета 18,5 МБк/кг веса тела. При этом с целью уменьшения лучевой нагрузки на персонал и безопасности при выполнении процедуры (декальцинирования крови, которое может наблюдаться при быстром введении препарата и которое может вызывать судороги пациента) используют методику капельного внутривенного введения с предварительным разведением порции препарата в 50-100 мл физиологического раствора. Для этого устанавливают систему для внутривенных вливаний и начинают капельное введение физиологического раствора. Затем, временно перекрыв зажимом трубку системы, вводят во флакон с физиологическим раствором все требуемое количество препарата, после чего продолжают капельное вливание. Всего в период клинических испытаний изучено поведение препарата у 50 больных с метастазами злокачественных новообразований в кости и у 20 ревматологических больных. После внутривенного введения препарата 153Sm-оксабифор в течение первых 2 ч накапливается в почках, мочевом пузыре, небольшое включение (до 5% от введенной дозы) может наблюдаться в печени, проекции носовых пазух. Через 2 ч препарат начинает активно фиксироваться в костях, преимущественно в пораженных участках (метастатические очаги, зоны воспаления). В течение первых суток с мочой выводится от 28 до 42% от введенной активности. Максимум выведения приходится на первые 8-12 ч. Уровень экскреции зависит от функции почек, объема поражения костей и активности фиксации препарата в патологических очагах. Уровень накопления препарата в метастатических очагах по сравнению с симметричными участками здоровой кости – коэффициент дифференциального накопления (КДН) – обычно составляет 2,0-3,0, достигая в отдельных случаях значения 5,0. Наиболее активное накопление отмечалось у больных раком предстательной железы, молочной железы, легкого. У больных ревматоидным артритом в связи с множественным характером суставных поражений было сложно точно определить процентное соотношение накопления больной/здоровый сустав. В тех случаях когда это определение представлялось возможным, соотношение достигало 4,8. Клинический эффект обычно проявлялся спустя 2 недели. Он носит стойкий характер (свыше 3 месяцев, а у некоторых больных – свыше 6 месяцев после однократного введения). При наличии показаний введение препарата можно выполнять повторно через 3 месяца. Радионуклидную терапию предложенным препаратом можно сочетать с химио- и гормонотерапией, другими видами лечения, контролируя общее состояние больного и показатели периферической крови. Техническая сущность изобретения заключается в следующем. Окса-бис(этиленнитрило)тетраметиленфосфонат образует более прочный комплекс с самарием-153, по сравнению с ЭДТМФ за счет реализации дополнительных коррдинационных связей с мостиковым атомом кислорода в молекуле оксабифора. Вместе с тем указанное соединение образует менее прочные по сравнению с ЭДТМФ комплексы с кальцием. Поэтому препарат на основе комплекса 153Sm-оксабифор обладает более высокой химической и радиационной устойчивостью при относительно меньшей способности связывать кальций крови. Использование предложенной композиции в сочетании с методом капельного введения препарата позволяет полностью исключить возможность негативных последствий введения препарата пациентам при получении положительного клинического эффекта лечения. Изобретение поясняется следующими примерами. Пример 1. Навеску 1 мг самария хлорида, обогащенного по самарию-152 до 99%, помещают в блок-контейнер, герметизируют и облучают тепловыми нейтронами ядерного реактора в потоке (5-6)  1013 нейтрон/см2 с продолжительностью 80-72 ч соответственно. Удельная активность самария-153 на конец облучения составляет 22-37 ГБк/мг.
Облученный самарий хлорид растворяют в 0,1 М HCl. К полученному раствору добавляют реагент, содержащий 645 1013 нейтрон/см2 с продолжительностью 80-72 ч соответственно. Удельная активность самария-153 на конец облучения составляет 22-37 ГБк/мг.
Облученный самарий хлорид растворяют в 0,1 М HCl. К полученному раствору добавляют реагент, содержащий 645 5 мг оксабифор-кислоты, 9 мл дистиллированной воды, 65 5 мг оксабифор-кислоты, 9 мл дистиллированной воды, 65 0,1 мл 1 М раствора NaOH и 60 0,1 мл 1 М раствора NaOH и 60 1 мг NaCl. Перемешивают смесь 5 мин барботированием воздуха, сливают готовый препарат 153Sm-оксабифор в сосуд для фасовки и фасуют во флаконы для лекарственных средств порциями по 925, 1850, 2775, 3700 МБк. Флаконы с препаратом укупоривают закатыванием и стерилизуют в автоклаве при температуре 119 – 121oC (1,0 – 1,1) ати в течение 8 мин. Концентрация лиганда в препарате составляет 0,05 моль/л, мольное соотношение Sm:L 1 мг NaCl. Перемешивают смесь 5 мин барботированием воздуха, сливают готовый препарат 153Sm-оксабифор в сосуд для фасовки и фасуют во флаконы для лекарственных средств порциями по 925, 1850, 2775, 3700 МБк. Флаконы с препаратом укупоривают закатыванием и стерилизуют в автоклаве при температуре 119 – 121oC (1,0 – 1,1) ати в течение 8 мин. Концентрация лиганда в препарате составляет 0,05 моль/л, мольное соотношение Sm:L 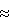 3 3 10-2.
Пример 2.
Для получения сравнительных данных по биологическому распределению были приготовлены препараты на основе оксабифора, ЭДТМФ – контроль и НТФ (нитрилотриметилфосфоновая кислота) по способу, описанному в примере 1. Препараты вводили внутривенно крысам – самкам весом 160-180 г в хвостовую вену в количестве 0,2 мл.
В табл. 1 представлены данные по распределению препаратов в организме крыс, где 1 – ЭДТМФ-контроль; 2 – предложенная композиция; 3 – НТФ.
Из данных табл. 1 следует, что использование композиции на основе НТФ (также описанное в [1 и 2]) практически неприемлемо из-за высокого накопления препарата в печени. Распределение комплексов 153Sm-ЭДТМФ и 153Sm-оксабифор практически одинаково; при этом соотношение кость/кровь; кость/печень несколько выше для оксабифора.
Пример 3.
Радиохимическую чистоту препарата, приготовленного по методике, описанной в примере 1, контролировали методом хроматографии на бумаге Ватман N 1 с использованием в качестве растворителя смеси этанол-пиридин-вода (1:2: 4). В указанной системе значение Rf комплекса 153Sm-оксабифор составляет 0,75.
Как следует из данных, представленных в табл. 2, содержание комплекса в препарате составляет не менее 95% в течение 4 суток (срок годности, установленный проектом Временной Фармакопейной статьи на препарат), что является свидетельством радиационной устойчивости композиции.
Пример 4.
Препарат в количестве 37 МБк/кг (1 МКи/кг) веса вводили капельным методом больной К. (41 год, рак молочной железы). Отмечено высокое накопление 153Sm в метастатических очагах (КДН свыше 2). Препарат обеспечил ярко выраженное уменьшение болей, возможность отмены наркотиков в течение 4 месяцев, после чего выполнено повторное введение препарата в количестве 55,5 МБк/кг (1,5 МКи/кг) веса; через месяц после повторного введения наблюдалось дальнейшее уменьшение болей.
Пример 5.
Больной М. (63 года, рак щитовидной железы, рак предстательной железы) получил препарат в количестве 45 МБк/кг (1,2 МКи/кг) веса. Боли купированы полностью, отмечено улучшение функции опорно-двигательного аппарата. Клинический эффект в течение 6 месяцев.
Пример 6.
Больная И. (34 года, ревматоидный артрит полиартрит, асептический некроз головки бедра справа). После капельного введения препарата 18,5 МБк/кг (0,5 МКи/кг) веса отмечено накопление активности в пораженных суставах с КДН до 5,6. Клинический эффект проявлялся через 10 суток и сохранялся в течение 5 месяцев.
Таким образом, технический результат при использовании изобретения заключается в простоте приготовления, в повышении терапевтического эффекта, в исключении токсических реакций при введении в организм пациента.
Список литературы 10-2.
Пример 2.
Для получения сравнительных данных по биологическому распределению были приготовлены препараты на основе оксабифора, ЭДТМФ – контроль и НТФ (нитрилотриметилфосфоновая кислота) по способу, описанному в примере 1. Препараты вводили внутривенно крысам – самкам весом 160-180 г в хвостовую вену в количестве 0,2 мл.
В табл. 1 представлены данные по распределению препаратов в организме крыс, где 1 – ЭДТМФ-контроль; 2 – предложенная композиция; 3 – НТФ.
Из данных табл. 1 следует, что использование композиции на основе НТФ (также описанное в [1 и 2]) практически неприемлемо из-за высокого накопления препарата в печени. Распределение комплексов 153Sm-ЭДТМФ и 153Sm-оксабифор практически одинаково; при этом соотношение кость/кровь; кость/печень несколько выше для оксабифора.
Пример 3.
Радиохимическую чистоту препарата, приготовленного по методике, описанной в примере 1, контролировали методом хроматографии на бумаге Ватман N 1 с использованием в качестве растворителя смеси этанол-пиридин-вода (1:2: 4). В указанной системе значение Rf комплекса 153Sm-оксабифор составляет 0,75.
Как следует из данных, представленных в табл. 2, содержание комплекса в препарате составляет не менее 95% в течение 4 суток (срок годности, установленный проектом Временной Фармакопейной статьи на препарат), что является свидетельством радиационной устойчивости композиции.
Пример 4.
Препарат в количестве 37 МБк/кг (1 МКи/кг) веса вводили капельным методом больной К. (41 год, рак молочной железы). Отмечено высокое накопление 153Sm в метастатических очагах (КДН свыше 2). Препарат обеспечил ярко выраженное уменьшение болей, возможность отмены наркотиков в течение 4 месяцев, после чего выполнено повторное введение препарата в количестве 55,5 МБк/кг (1,5 МКи/кг) веса; через месяц после повторного введения наблюдалось дальнейшее уменьшение болей.
Пример 5.
Больной М. (63 года, рак щитовидной железы, рак предстательной железы) получил препарат в количестве 45 МБк/кг (1,2 МКи/кг) веса. Боли купированы полностью, отмечено улучшение функции опорно-двигательного аппарата. Клинический эффект в течение 6 месяцев.
Пример 6.
Больная И. (34 года, ревматоидный артрит полиартрит, асептический некроз головки бедра справа). После капельного введения препарата 18,5 МБк/кг (0,5 МКи/кг) веса отмечено накопление активности в пораженных суставах с КДН до 5,6. Клинический эффект проявлялся через 10 суток и сохранялся в течение 5 месяцев.
Таким образом, технический результат при использовании изобретения заключается в простоте приготовления, в повышении терапевтического эффекта, в исключении токсических реакций при введении в организм пациента.
Список литературы1. Патент US N 4898724, МПК A 61 K 43/00 U.S.CI. 424/1.1, 1987, опубл. 1990. 2. Патент US N 5762907, МПК A 61 K 51/04 U.S.CI. 424/1.77, 1993, опубл. 1998. Формула изобретения
Самарий в виде комплекса с окса-бис(этиленнитрило)-тетраметиленфосфоновой кислотой или ее натриевой солью – 0,025 – 0,100 Натрия хлорид – 4 – 6 Вода для инъекций – До 1 при этом объемная активность самария – 153 составляет 240 – 740 МБк/мл, а pH композиции 5 – 7. РИСУНКИ
QB4A Регистрация лицензионного договора на использование изобретения
Лицензиар(ы): Федеральное государственное унитарное предприятие Государственный научный центр – Институт биофизики Федерального медико-биологического агентства
Вид лицензии*: НИЛ
Лицензиат(ы): Федеральное государственное унитарное предприятие “Завод медицинских радиоактивных препаратов” Федерального медико-биологического агентства
Договор № РД0011365 зарегистрирован 18.08.2006
Извещение опубликовано: 27.09.2006 БИ: 27/2006
* ИЛ – исключительная лицензия НИЛ – неисключительная лицензия
PD4A – Изменение наименования обладателя патента СССР или патента Российской Федерации на изобретение
(73) Новое наименование патентообладателя:
Адрес для переписки:
Извещение опубликовано: 10.01.2009 БИ: 01/2009
QZ4A – Регистрация изменений (дополнений) лицензионного договора на использование изобретения
Лицензиар(ы): Федеральное государственное учереждение “Федеральный медицинский биофизический центр имени А.И.Бурназяна”
Вид лицензии*: НИЛ
Лицензиат(ы): Федеральное государственное унитарное предприятие «Завод медицинских радиоактивных препаратов» Федерального медико-биологического агентства
Характер внесенных изменений (дополнений):
Дата и номер государственной регистрации договора, в который внесены изменения:
Извещение опубликовано: 27.08.2009 БИ: 24/2009
* ИЛ – исключительная лицензия НИЛ – неисключительная лицензия
|
||||||||||||||||||||||||||
