|
|
(21), (22) Заявка: 2007136817/15, 05.10.2007
(24) Дата начала отсчета срока действия патента:
05.10.2007
(46) Опубликовано: 27.02.2009
(56) Список документов, цитированных в отчете о
поиске:
US 6518028, 11.02.2003. RU 2161309 С2, 27.12.2000. RU 2249820 C1, 10.04.2005. US 7229774, 12.06.2007. WO 2006056766, 01.06.2006.
Адрес для переписки:
141100, Московская обл., г. Щелково, ул. Зубеева, 9, кв.56, А.А. Ляшенко
|
(72) Автор(ы):
Ляшенко Алла Анатольевна (RU),
Северин Евгений Сергеевич (RU),
Савватеева Мария Владимировна (RU),
Васильева Евгения Борисовна (RU)
(73) Патентообладатель(и):
Автономная некоммерческая организация “Центр медицинских биотехнологий” (RU)
|
(54) СПОСОБ ДИАГНОСТИКИ ОНКОЛОГИЧЕСКИХ ЗАБОЛЕВАНИЙ ПРЕДСТАТЕЛЬНОЙ ЖЕЛЕЗЫ
(57) Реферат:
Изобретение относится к области генетических исследований, молекулярной биологии, клинической биохимии, медицины, ветеринарии, фармакологии, эндокринологии. Способ включает сочетанное определение активности сериновой протеиназы-хепсина и метилированного гена глютатион-S-трансферазы класса PI (GSTP1) в опухолевых клетках, обнаруживаемых в моче пациентов, и при значении активности хепсина выше, чем 42% по отношению к контролю, и выявлении метилированного гена GSTP1 диагностируют онкологическое заболевание. Изобретение может применяться для дифференциальной диагностики заболеваний простаты, таких как аденома (доброкачественная гиперплазия) предстательной железы, простатит, интраэпителиальная гиперплазия простаты, рак предстательной железы, и обеспечивает неинвазивность и увеличение вероятности постановки правильного диагноза. 3 ил.
Область техники, к которой относится изобретение
Изобретение относится к области генетических исследований, молекулярной биологии, клинической биохимии, медицины, ветеринарии, фармакологи эндокринологии и может быть использовано с целью неинвазивной диагностики рака предстательной железы. Изобретение предусматривает сочетанную детекцию активности сериновой протеиназы хепсина и метилированного гена глютатион-S-трансферазы типа P1 (GSTP1) в опухолевых клетках, обнаруживаемых в моче пациентов. Изобретение может применяться также для дифференциальной диагностики заболеваний простаты, таких как аденома (доброкачественная гиперплазия) предстательной железы, простатит, интраэпителиальная гиперплазия простаты, рак предстательной железы.
Уровень техники
Известен способ детекции хепсина с целью ранней диагностики рака простат (патент США №6,518,028, прототип). Авторами предлагается способ детекции хепсина как маркера опухолей через ПЦР-диагностику гиперэкспрессии гена хепсина в тканях, жидкостях человека. Предложенный метод предусматривает изолирование мРНК в образцах нормальной и патологической ткани и сравнение транскрипционного уровня мРНК в образцах тканей, на основании чего делается вывод о разнице в уровне мРНК степени гиперэкспрессии гена. Недостатком предложенного способа являете необходимость в получении образцов тканей, что предусматривает инвазивность и связанные с этим ограничения в широком распространении метода.
Известен способ диагностики рака предстательной железы на основе детекции метилирования гена GSTP1 в биологических жидкостях и тканях человека, в том числе моче пациентов (патент США №7,049,062). Недостатками такого определения являются традиционно низкая прогностическая ценность при использовании одного маркера, а также отсутствие необходимости в наличии истинных объектов анализа – т.е. опухолевых клеток предстательной железы.
Наряду с диагностикой, основанной на разнице в экспрессии уровня гена хепсина (оценка его транскрипционной регуляции), в диагностике может применяться оценка активности хепсина как фермента, т.е учет его ферментативной активности как сериновой протеиназы с применением субстрата.
Сочетанное использование определения ферментативной активности хепсина и метилирования гена GSTP1 для диагностики рака предстательной железы и дифференциальной диагностики других заболеваний предстательной железы не известно из уровня техники.
Сущность изобретения
Задачей изобретения является создание метода диагностики, использующего в качестве маркеров рака предстательной железы сочетанное определение ферментативной активности хепсина и метилирования гена GSTP1 в опухолевых клетках предстательной железы в образцах мочи пациентов. Технический результат заключается в повышении прогностической ценности в сочетании с неинвазивностью способа.
Перечень чертежей
Фиг 1. Кинетика амидолитической активности хепсина в моче пациентов с аденокарциномой предстательной железы. Условные обозначения: OD – оптическая плотность.
Фиг 2. Измерение активности хепсина в моче пациентов с аденокарциномой предстательной железы. Показан «уровень отсечения» (линия), превышение которого позволяет с высокой долей вероятности отнести пациента к группе с диагнозом «рак предстательной железы».
Фиг 3. Определение метилирования промотерной области гена GSTP1 в моче пациентов с аденокарциномой предстательной железы. Обозначения дорожек: 1 – маркер 100 bp ladder; 2,3 – отрицательный контроль; 4,5 – положительный контроль; 6,7 – аденокарцинома предстательной железы; 8,9 – аденома предстательной железы.
Сведения, подтверждающие возможность осуществления изобретения
Хепсин – трансмембранная сериновая протеиназа, которая в норме экспрессируется на некоторых тканях, включая печень, почки, простату, щитовидную железу (Tsuji et al., 1991). Физиологическая функция хепсина в настоящее время четко не установлена. Показано, что в норме хепсин принимает участие в процессе коагуляции, регулируя активность некоторых факторов свертывающей системы (VII, XII, IX, проурокиназный тип плазминоген-активатора), а также активирует созревание фактора роста гепатоцитов HGF (Kazama et al., 1995; Moran et al., 2006; Wu & Parry, 2007).
Было показано, что хепсин является одним из наиболее частых генов, экспрессируемых на клетках рака предстательной железы, при этом степень экспрессии гена тесно коррелирует с прогрессией заболевания (Stephan et al., 2004; Tanimoto et al., 1997; Dhanasekaran et al., 2001). Патофизиологическая роль хепсина при раке сводится, по мнению большинства исследователей, к активации матриксных металлопротеиназ, что усиливает инвазивность опухоли и риск метастазирования.
Эти примеры говорят о том, что хепсин является отличным кандидатом на опухоль – специфический маркер, и его активность как фермента может быть использована в качестве диагностического критерия при дифференциальной диагностике между аденокарциномой и неопухолевыми заболеваниями предстательной железы. Показано, что на ранних стадиях заболевания иммуногистохимическое окрашивание антителами на хепсин было гораздо слабее, чем на поздних (Xuan et al., 2006). Способ детекции является несложным и применим для скрининга большого количества пациентов.
Глутатион-S-трансферазы (GSTs) составляют суперсемейство ферментов, отвечающих за II фазу детоксикации, что предотвращает образование опасных метаболитов внутри клетки. Биохимической функцией GSTs является образование коньюгатов восстановленного глютатиона с различными электрофильными компонентами, а также изоформами реактивного кислорода (т.н. свободными радикалами). Отсюда их название – антиоксидантные ферменты. В ряде случаев, особенно на фоне патологического метаболизма, экспрессия генов GST в клетке отсутствует (феномен т.н. «молчания генов»). Молекулярной этого феномена является метилирование промоторной области этих генов (Bernardini et al., 2004). Показано, что при РПЖ также наблюдается снижение антиоксидантной активности за счет вышеуказанного механизма (Bastian et al., 2004).
Поскольку изменения метаболизма при патологии предстательной железы, в частности при раке простаты, наблюдаются для обоих маркеров, то совместная детекция ферментативной активности хепсина и выявление метилирования гена GST класса Р1 (GSTP1) позволяют увеличить вероятность постановки правильного диагноза и дифференцировать онкологический процесс.
Примеры осуществления изобретения
Изобретение иллюстрируется следующими примерами.
Пример 1. Определение активности хепсина в опухолевых клетках предстательной железы.
Активность хепсина исследовали на клетках предстательной железы в моче, полученной от пациентов с заболеваниями простаты. Клетки предстательной железы обнаруживаются в моче после пальцевого исследования либо массажа простаты.
Суспензию клеток, полученных из мочи пациентов, трижды промывали в фосфатно-солевом буфере, рН 7,2-7,4, при комнатной температуре и лизировали в RIPAтм буфере 15 минут при + 4°С. Полученные лизаты центрифугировали при 14000 об/мин в течение 30 мин, супернатант отбирали на анализ. Количество белка в препарате определялось спектрофотометрически при длинах волн 260 и 280 нм. Расчет концентрации производился по формуле:
С1=(1,55·А280-0,76·А260),
где A280 и А260 – поглощение раствора при 280 и 260 нм, соответственно.
Определение активности хепсина основано на повышении оптической плотности реакционной смеси при длине волны 415 нм, обусловленное отщеплением паранитроаналина от Spectrozymeтм, имеющего сродство к хепсину. Инкубационная смесь содержала 130 нм Spectrozymeтм в 0,01М трис-имидазольном буфере, рН 8,4, инкубация при+37°С и 15-20 мкг белка клеточных лизатов. В качестве контроля использовали лизат 1,5 ×105 клеток линии LnCAP в 0,01М трис-имидазольном буфере, рН 8,4. Активность фермента определяли по начальной скорости реакции при 415 нм в течение 30-45 минут. Активность хепсина (А) рассчитывалась по следующей формуле:
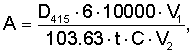
где D415 – рост поглощения за время t; С – концентрация общего белка в мг/мл; V1 – объем инкубации в мл; V2 – объем добавленной пробы; t – время инкубации; 103.63 – оптическая плотность, которую дает 1 мкмоль Spectrozymeтм.
Проведенный статистический анализ позволил установить предел отсечения, при котором вероятность постановки диагноза (отнесения индивида к той или другой группе) была наиболее высокой. Для математического анализа применялась следующая методика. Сильно отклоняющиеся варианты были исключены. Отсутствующие значения заменены на средние. Предел отсечения устанавливался по уровню среднего значения активности хепсина в «отсекаемой» группе пациентов (с диагнозом «аденома предстательной железы»). Если величина активности хепсина была больше, чем ее среднее в «отсекаемой группе», пациент относился к группе с диагнозом «рак предстательной железы». С учетом этого были подсчитаны частоты и сформирована таблица сопряженности бинарных признаков. Статистический анализ проводился с применением непараметрического критерия Хи-квадрат с поправкой Йетса. Уровень значимости был выбран р<0.05. Было показано, что группы пациентов достоверно различаются по активности хепсина по отношению к контролю (на клетках LnCap), если таковая превышала значение 42% (р=0.02). Полагаем, что данная величина и является тем пределом отсечения, превышение которого позволяет с высокой долей вероятности отнести пациента к группе с диагнозом «рак предстательной железы». Пополнение количества исследований (увеличение числа степеней свободы) не изменяет эту величину, поэтому в дальнейшем в качестве положительных рассматриваются только те образцы, дающие не менее чем 42% активности хепсина от таковой на клетках LnCap (Фиг 2).
Было обнаружено присутствие хепсина на клетках, полученных из образцов мочи пациентов с РПЖ, в 71% случаев (р=0.020). У здоровых доноров хепсин, с учетом чувствительности тест-системы и специфичности хромогенного субстрата, детектируется в минимальных количествах на уровне, гораздо ниже отсекаемого. Полагаем, что данный тест обладает возможностью детекции некоторых фоновых значений, что свидетельствует о возможном присутствии небольшого количества других сериновых протеиназ, с которыми взаимодействует используемый хромогенный субстрат, на исследуемых клетках здоровых доноров. Издержки данного определения не вносят существенных изменений в анализ получаемых данных и влияют на общие выводы по прогнозу. Обучающая выборка с известными диагнозами позволяет контролировать правильность отнесения к той или иной группе по данному маркеру.
Пример 2. Определение метилирования промоторной области гена GSTP1 в опухолевых клетках.
Забор мочи у пациентов (в объеме около 50 мл) проводили троекратно: утром; непосредственно после пальцевого исследования и после биопсии предстательной железы. Затем пробы собирали и центрифугировались Joan при 900 g в течение 10 мин. Надосадочную жидкость сливали. Осадок, содержащий клетки, промывали 1 или 2 раза фосфатно-солевым буфером, центрифугировали в тех же условиях, а затем замораживали при -35°С для последующего использования. Выделение ДНК проводили фенольным методом после предварительной обработки протеиназой К по стандартной методике (Sambrook et al, 1993).
ДНК подвергалась метабисульфитной модификации по стандартной методике. Для проведения ПЦР использовались две пары праймеров для определения метилированной и неметилированной ДНК в образцах:
Unmeth Sense 5′ – GCGTCGAGGGGATCTAGAATGT;
Antisense 5′ – TAGTCACATTGTACCTAGCCT;
Meth Sense 5′ – ACTGTGTGAACAGTGTACCTTG;
Antisense 5′ – CATCCTGGATACAGGTAACAAC.
ПЦР осуществляли на матрице геномной ДНК с использованием 10 пмоль праймеров в буфере, содержащем 50 mM трис-HCl (рН 9.2), 16 mM (NH2)2SO4, 175 mM MgCl2, 0.2 mM раствор каждого дезоксинуклеозидтрифосфата, 0.5 ед. Taq-полимеразы, 2% формальдегида. 30 циклов амплификации состояли из преденатурации при 95°С в течение 3 мин, денатурации при 95°С в течение 1 мин, отжига праймеров при 60°С в течение 1 мин и элонгации цепей при 72°С в течение 1 минуты. Полученные фрагменты разделяли в 2% агарозе, окрашивали бромидом этидия и затем визуализировали в УФ-свете. В качестве положительного контроля метилирования промоторной области гена GSTP1 использовалась ДНК, полученная из клеток линии LnCaP (клеточная линия РПЖ человека).
Согласно полученным данным, метилирование гена GSTP1 при РПЖ наблюдается в 45% случаев. При этом при простатите, аденоме и ПИН ген GSTP1 экспрессируется в 33% случаев. С другой стороны, было установлено, что у здоровых доноров метилирование гена GSTP1 не наблюдается. Таким образом, определение метилирования гена GSTP1 в сочетании с определением активности хепсина может использоваться в качестве молекулярных маркеров патологических процессов, имеющих место в предстательной железе. Т.о., данный подход может применяться для мониторинга состояния предстательной железы. При этом сочетанное использование определения метилирования гена GSTP1 и активности хепсина позволяет диагностировать РПЖ у пациентов с высокой долей вероятности, а также проводить диагностику нарушений метаболизма в клетках предстательной железы.
Пример 3. Оценка прогноза рака предстательной железы по простат-специфическому антигену в сравнении с предложенными маркерами.
Параллельно анализировался уровень простат-специфического антигена (ПСА) – популярного маркера для диагностики рака предстательной железы. Было получено, что повышение ПСА за пределы т.н. «серой шкалы» (4-10 нг/мл) при РПЖ наблюдается лишь в 58% случаев, что существенно уступает по диагностической ценности предсказаний по хепсину (в предложенном варианте 71%). Сочетанное использование обоих маркеров повышает диагностическую ценность неинвазивного метода диагностики и доводит вероятность предсказаний до 0,88. Подсчет условной вероятности проводился стандартными математическими способами.
Пример 4. Сочетанное определение маркеров в динамике.
В феврале 2006 года пациент Г. обратился в урологическую клинику. Традиционные диагностические манипуляции и лабораторные тесты (тест на ПСА, биопсия) установили диагноз – аденома предстательной железы. Клетки предстательной железы были взяты у пациента в соответствии с описанным способом. Было обнаружено метилирование гена GSTP1 и отсутствие активности хепсина. Через год пациент обратился повторно по причине ухудшения симптоматики. Был поставлен диагноз «аденокарцинома предстательной железы», причем на клетках предстательной железы, на фоне выявления метилирования гена GSTP1, уже детектировалась активность хепсина, составляющая 62% по отношению к контролю. Этот пример характеризует прогностическую важность неспецифичного для рака маркера – метилированного гена GSTP1 и доказывает необходимость учета обоих маркеров, что повышает вероятность при постановке онкологического диагноза.
Литература
1. Bignotti Е, Tassi RA, Calza S, Ravaggi A, Bandiera E, Rossi E, Donzelli C, Pasinetti B, Pecorelli S, Santin AD. Gene expression profile of ovarian serous papillary carcinomas: identification of metastasis-associated genes. Am J Obstet Gynecol. 2007 Mar; 196(3):45. el-ll.
2. Tanimoto H, Yan Y, Clarke J, Korourian S, Shigemasa K, Parmley TH, Parham GP,O’Brien TJ. Hepsin, a cell surface serine protease identified in hepatoma cells, is overexpressed in ovarian cancer. Cancer Res. 1997 Jul 15; 57(14):2884-7.
3. Xuan, J.A., D.Schneider, P.Toy, R.Lin, A.Newton, Y.Zhu, S.Finster, D.Vogel, B.Mintzer, H.Dinter, D.Light, R.Parry, M.Polokoff, M.Whitlow, Q.Wu & G.Parry: Antibodies neutralizing hepsin protease activity do not impact cell growth but inhibit invasion of prostate and ovarian tumor cells in culture. 2006 Cancer Res, 66, 3611-9.
4. Wu Q, Parry G. Hepsin and prostate cancer. Front Biosci. 2007 Sep 1; 12:5052-9.
5.Stephan C, Yousef GM, Scorilas A, Jung K, Jung M, Kristiansen G, Hauptmann S, Kishi T, Nakamura T, Loening SA, Diamandis EP. Hepsin is highly over expressed in and a new candidate for a prognostic indicator in prostate cancer. J Urol. 2004 Jan; (l):187-91.
6. Tanimoto H, Yan Y, Clarke J, Korourian S, Shigemasa K, Parmley TH, Parham GP, O’Brien TJ. Hepsin, a cell surface serine protease identified in hepatoma cells, is overexpressed in ovarian cancer. Cancer Res. 1997 Jul 15; 57(14):2884-7.
7. Dhanasekaran SM, Barrette TR, Ghosh D, Shah R, Varambally S, Karachi K, Pienta KJ, Rubin MA, Chinnaiyan AM. Delineation of prognostic biomarkers in prostate cancer. Nature. 2001 Aug 23; 412(6849):822-6.
8. Kazama Y, Hamamoto T, Foster DC, Kisiel W. Hepsin, a putative membrane-associated serine protease, activates human factor VII and initiates a pathway of blood coagulation on the cell surface leading to thrombin formation. J Biol Chem. 1995 Jan 6; 270(l):66-72.
9. Moran P, Li W, Fan B, Vij R, Eigenbrot C, Kirchhofer D. Pro-urokinase-type plasminogen activator is a substrate for hepsin. J Biol Chem. 2006 Oct 13; 281(41):30439-46.
10. Tsuji A, Torres-Rosado A, Aral T, Le Beau MM, Lemons RS, Chou SH, Kurachi K. Hepsin, a cell membrane-associated protease. Characterization, tissue distribution, and gene localization. J Biol Chem. 1991 Sep 5; 266(25):16948-53.
11. Sambrook J, MacCallum P. Cancer Institute, Melbourne, Australia; David Russell, University of Texas Southwestern Medical Center, Dallas Molecular Cloning: A Laboratory Manual (Third Edition)
12. Bernardini S, Miano R, lori R, Finazzi-Agro E, Palmieri G, Ballerini S, Angeloni C, Orlandi A, Bellincampi L, Cortese C, Federici G. Hypermethylation of the CpG islands in the promoter region of the GSTP1 gene in prostate cancer: a useful diagnostic and prognostic marker? Clin Chim Acta. 2004 Dec; 350(l-2):181-8.
13. Bastian PJ, Ellinger J, Schmidt D, Wernert N, Wellmann A, Muller SC, von Rucker A. GSTP1 hypermethylation as a molecular marker in the diagnosis of prostatic cancer: is there a correlation with clinical stage, Gleason grade, PSA value or age? Eur J Med Res. 2004 Nov 29; 9(ll):523-7.
14. Cairns P, Esteller M, Herman JG, Schoenberg M, Jeronimo C, Sanchez-Cespedes M, Chow NH, Grasso M, Wu L, Westra WB, Sidransky D. Molecular detection of prostate cancer in urine by GSTP1 hypermethylation. Clin Cancer Res. 2001 Sep; 7(9):2727-30.
Формула изобретения
Способ диагностики онкологических заболеваний предстательной железы (ПЖ), характеризующийся тем, что исследуют клетки ПЖ, выделенные из мочи пациента, после массажа или пальцевого ректального исследования, в которых определяют уровень активности хепсина и метилирование гена GSTP1, и при значении активности хепсина выше чем 42% по отношению к контролю и выявлении метилирования гена GSTP1 диагностируют онкологическое заболевание.
РИСУНКИ
PC4A – Регистрация договора об уступке патента СССР или патента Российской Федерации на изобретение
Прежний патентообладатель:
Автономная некоммерческая организация “Центр медицинских биотехнологий”
(73) Патентообладатель:
Автономная некоммерческая организация “Институт молекулярной диагностики”
Договор № РД0058510 зарегистрирован 21.12.2009
Извещение опубликовано: 10.02.2010 БИ: 04/2010
|
|