Патент на изобретение №2347785
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ КОМПЛЕКСОВ ТРИКРЕЗИЛ-, ТРИ(1,3-ДИХЛОРПРОПИЛ)- И ТРИ(2-ЭТИЛГЕКСИЛ)ФОСФАТОВ С ХЛОРИДАМИ Sn И Ti
(57) Реферат:
Изобретение относится к способу получения комплексов трикрезил-, три(1,3-дихлорпропил) и три(2-этилгексил)фосфатов с хлоридами Sn или Ti общей формулы 2(RO)3Р=O·ЭCl4, где R=-С4Н6СН3, -СН(Cl)СН2СН2(Cl) или -СН2СН(С2Н5)(СН2)3СН3, Э=Sn, Ti, и может быть использован в органическом синтезе. Способ характеризуется тем, что он предусматривает взаимодействие трикрезил-, три(1,3-дихлорпропил)- или три(2-этилгексил)фосфата с тетрахлоридами Sn или Ti при комнатной температуре и мольном соотношении фосфат:тетрахлорид 2:1. 2 табл.
Настоящее изобретение относится к элементоорганической химии, а именно к способам получения комплексов тетрахлоридов Sn или Ti, конкретно к способам получения соединений общей формулы
где Э=Sn или Ti; R=-С6Н4СН3, – CH(Cl)СН2СН2(Cl) или -СН2СН(С2Н5)(СН2)3СН3, которые могут использоваться в качестве катализаторов в органическом синтезе, а также в качестве катализаторов полимеризации и поликонденсации олигомерных композиций. Известны комплексы 2Et2P(OR)·SnX4, полученные взаимодействием Et2P(OR) (R=Et, Pr, n-С3Н13) и SnX4 Известны комплексы 2RP(OR’)2·SnCl4 и 2PhP(OR’)2·SnCl4, полученные взаимодействием 2RP(OR’)2 и PhP(OR’)2 с SnCl4 Однако установлено, что комплексы тетрахлоридов металлов с эфирами трехвалентного фосфора являются нестабильными соединениями: медленно на холоде и быстро при нагревании они претерпевают дальнейшие превращения (внутрикомплексная изомеризация, а также окислительно-восстановительные процессы). Кроме того, для выделения комплексов в индивидуальном состоянии требуется их дополнительная очистка: многократное промывание соответствующими растворителями с последующей осушкой под вакуумом при пониженной температуре, что отрицательно сказывается на выход продуктов и дополнительно усложняет технологию получения. Известны комплексы алкилфосфатов, в частности, триметил-, триэтил- и трибутилфосфатов с хлоридами олова и титана. Получение комплексов триметил- и триэтилфосфатов в результате взаимодействия соответствующего фосфата и тетрахлорида металла описано в работах: Turin Eric et all, Inorganica chimica acta, 1987, 134 (1), 67-78; Сумарокова Т.Н. и др. Известия АН Казахской ССР, серия химическая, 1976, 26(3), 52-53, Paul R.C. et all, Indian journal of chemistry, 1975, 13(7), 692-694, Bridgland B.E. et all, Journal of inorganic and nuclear chemistry, 1970, 32(5), 1729-1735, Teichmann Herbert et all, Chemische Berichte, 1965, 98(3), 856-863. Известно получение комплексов трибутилфосфата с тетрахлоридом олова при мольном соотношении 2:1. Корцев Г.Н. и др. Изв. АН СССР, Серия Химическая, 1973, 9, 1972-1973. Известно образование комплексов состава 2(BuO)3Р=O·SnCl4 и 2(BuO)3Р=O·TiCl4 в результате взаимодействия соответствующих хлоридов металлов с трибутилфосфатом. Ибраева Т.Д. и др. Теория растворов, 1971, 306-308 (РЖХимия, 1972, абстр. 5Б1479). Известно образование комплексов трибутилфосфата с тетрахлоридом титана обсуждается в документах Rolang G. Et all, Spectrochimica acta, part A: molecular and bimolecular spectroscopy, 1972, 28(5), 835-844, Старцев В.Н. и др. Журнал неорганической химии, 1965Б, 10(10), 2367-2371. В литературе отсутствуют данные о способах получения комплексов тетрахлоридов Sn или Ti с трикрезил-, три(1,3-дихлорпропил)- и три(2-этилгексил)фосфатами. Задачей заявляемого изобретения является получение новых, ранее не изученных, комплексов тетрахлоридов Sn или Ti с полными органическими эфирами ортофосфорной кислоты общей формулы: 2(RO)3РО·ЭCl4 (I): Э=Sn или Ti, R=-С6Н4СН3, -СН(Cl)СН2СН2(Cl) или -СН2СН(С2Н5)(СН2)3СН3 с улучшенными технологическими характеристиками, расширяющими арсенал комплексов данного назначения. Техническим решением задачи является получение новых комплексов тетрахлоридов Sn или Ti с полными органическими эфирами ортофосфорной кислоты, расширяющих арсенал средств данного назначения. Это достигается тем, что способ получения комплексов трикрезил-, три(1,3-дихлорпропил) и три(2-этилгексил)фосфатов с тетрахлоридами Sn или Ti общей формулы (I): 2(RO)3Р=O·ЭCl4, где R=-С6Н4СН3, – CH(Cl)CH2CH2(Cl) или – СН2СН(С2Н5)(СН2)3СН3, характеризующийся тем, что трикрезил-, три(1,3-дихлорпропил)- и три(2-этилгексил)фосфат соответственно подвергают взаимодействию с тетрахлоридами Sn или Ti при мольном соотношении фосфат:тетрахлорид 2:1 и комнатной температуре. Способ осуществляется следующим образом: при интенсивном перемешивании реакционной смеси тетрахлорид Sn или Ti постепенно прибавляют к соответствующему фосфату в мольном соотношении 1:2. Получение комплексов приведено в примерах конкретного выполнения 1-6. Данный способ получения комплексов, не описанных в источниках информации, отличается простотой аппаратурного оформления, а именно реакция протекает в отсутствии растворителей, инертной атмосферы и нагревания. Оптимальным мольным соотношением является соотношение фосфатов с тетрахлоридами металлов как 2:1. При меньшем содержании фосфата происходит выделение тетрагалогенида в отдельную фазу, а при большем образуется раствор комплекса в соответствующем фосфате, что снижает выход целевого комплекса. Следует отметить, что комплексы образуются с количественным выходом, в химически чистом виде и не нуждаются в выделении и дополнительной очистке. Кроме того, синтезированные соединения отличаются стабильностью при хранении. Для синтеза комплексов использовали следующие соединения: трикрезилфосфат (ГОСТ 5728-76), три(1,3-дихлорпропил)фосфат (бц. вязкая ж., d4 20=1,513; Ткип=200°С (1 мм рт.ст.)), три(2-этилгексил)фосфат (бц. вязкая ж., d4 20=0,925; Ткип=200°С (2 мм рт.ст.)), тетрахлорид олова (бц. дым. ж., d4 20=2,232 г/л, Ткип.=113,7°С) и тетрахлорид титана (бц. дым. ж., d4 20=1,726 г/л, Ткип.=136,5°С). Пример 1. В герметично закрывающуюся колбу поместили 10,00 г (0,0272 моль) трикрезилфосфата. Затем при постоянном перемешивании порциями добавили через капельную воронку 3,54 г (0,0136 моль) тетрахлорида олова. Реакция протекает самопроизвольно с выделением тепла, при этом повышается вязкость реакционной системы и образуется светло-коричневый комплекс бис(трикрезилфосфат)тетрахлороолова (I). Спектр ЯМР31P в м.д.: Пример 2. В герметично закрывающуюся колбу поместили 10,00 г (0,0272 моль) трикрезилфосфата. Затем при постоянном перемешивании порциями добавили через капельную воронку 2,57 г (0,0136 моль) тетрахлорида титана. Реакция протекает самопроизвольно с выделением тепла, при этом повышается вязкость реакционной системы и образуется темно-коричневый комплекс бис(трикрезилфосфат)тетрахлоротитана (II). Спектр ЯМР31P в м.д.: Пример 3. В герметично закрывающуюся колбу поместили 10,00 г (0,02 моль) три(1,3-дихлорпропил)фосфата. Затем при постоянном перемешивании порциями добавили через капельную воронку 3,02 г (0,01 моль) тетрахлорида олова. Реакция протекает самопроизвольно с выделением тепла, при этом повышается вязкость реакционной системы и образуется бесцветный комплекс бис(три(1,3-дихлорпропил)фосфат)тетрахлоролова (III). Спектр ЯМР31P в м.д.: Пример 4. В герметично закрывающуюся колбу поместили 10,00 г (0,02 моль) три(1,3-дихлорпропил)фосфата. Затем при постоянном перемешивании порциями добавили через капельную воронку 2,2 г (0,01 моль) тетрахлорида титана. Реакция протекает самопроизвольно с выделением тепла, при этом повышается вязкость реакционной системы и образуется светло-коричневый комплекс бис(три(1,3-дихлорпропил)фосфат)тетрахлоротитана (IV). Спектр ЯМР31P в м.д.: два стереоизомера с Пример 5. В герметично закрывающуюся колбу поместили 10,00 г (0,024 моль) три(2-этилгексил)фосфата. Затем при постоянном перемешивании порциями добавили через капельную воронку 3,0 г (0,012 моль) хлорида олова. Реакция протекает самопроизвольно с выделением тепла, при этом повышается вязкость реакционной системы и образуется бесцветный комплекс бис(три(2-этилгексил)фосфат)тетрахлоролова (V). Спектр ЯМР31P в м.д.: Пример 6. В герметично закрывающуюся колбу поместили 10,00 г (0,024 моль) три(2-этилгексил)фосфата. Затем при постоянном перемешивании порциями добавили через капельную воронку 2,18 г (0,012 моль) хлорида титана. Реакция протекает самопроизвольно с выделением тепла, при этом повышается вязкость реакционной системы и образуется светло-желтый комплекс бис(три(2-этилгексил)фосфат)тетрахлоротитана (VI). Спектр ЯМР1Н в м.д.: 0,92-0,87 м (СН3), 1,40-1,29 м (СН2), 1,58 м (СН), 3,54-3,52 м (СН2). Температура саморазогрева, показатель преломления (nd 20), плотность (d4 20), фактор замедления (Rf) и цвет приведены в табл.1. Данные ИК-спектроскопии и элементного анализа на фосфор приведены в табл.2. Состав и строение синтезированных комплексов подтверждены методами ИК-спектроскпии, ЯМР31P, ЯМР1Н и элементным анализом на фосфор. ИК-спектры снимали на приборе спектрофотометр SPECORD-IR 75 в тонком слое. Спектры ЯМР регистрировали на Bruker Avance-600 (1H, 600 МГц) и Bruker CXP-100 (31P, 36,48 МГц) относительно внутреннего стандарта – ГМДС или внешнего 85%-ной Н3PO4, растворители – дейтерохлороформ (31P) и дейтерированный метанол (1H). Содержание фосфора определяли фотометрическим методом с помощью фотоэлектрического колориметра типа КФС-2 при В спектрах ЯМР31P комплексов наблюдается смещение химических сдвигов фосфора по сравнению с исходными эфирами фосфорной кислоты в более сильное поле. Мы полагаем, что такое смещение свидетельствует об образовании P=O….Me-связи. Данные ЯМР1Н также указывают на образование координационных соединений фосфатов с хлоридами металлов. Данные ИК-спектров, подтверждающих образование комплексных соединений, представлены в табл.2. Для наглядности в табл.2 приведены характеристические полосы исходных фосфатов. ИК-спектры комплексов отличаются от спектров исходных эфиров. Основные изменения в спектрах комплексов (1-6) по сравнению со спектрами исходных эфиров наблюдаются в области поглощения Р=O и Р-О-С-связей. В ИК-спектрах комплексов наблюдается смещение полосы поглощения фосфорильной группы (Р=O) в сторону меньших частот и изменение ее интенсивности, полоса поглощения Р-О-С-связи также меняет свою интенсивность. Наблюдаемые изменения в ИК-спектрах дают возможность предположить, что комплексные соединения образуются за счет донорно-акцепторной связи, в которой роль донора выполняет атом кислорода. Анализ полученных соединений на фосфор методом элементного анализа показывает, что в комплексах на одну молекулу хлорида металла приходится две молекулы эфира ортофосфорной кислоты. Таким образом, все полученные данные свидетельствуют об образовании комплексов следующего строения: (RO)3Р=O: где Э=Sn или Ti; R=-С6H4СН3, – СН(Cl)СН2СН2(Cl) или -СН2СН(С2Н5)(СН2)3СН3.
Формула изобретения
Способ получения комплексов трикрезил-, три(1,3-дихлорпропил)- и три(2-этилгексил)фосфатов с хлоридами Sn или Ti общей формулы (I): 2(RO)3Р=O·ЭCl4, где R=-С6Н4СН3, -СН(Cl)СН2СН2(Cl) или -СН2СН(С2Н5)(СН2)3СН3, Э=Sn, Ti, характеризующийся тем, что трикрезил-, три(1,3-дихлорпропил)- или три(2-этилгексил)фосфат соответственно, подвергают взаимодействию с тетрахлоридами Sn или Ti при мольном соотношении фосфат:тетрахлорид 2:1 и комнатной температуре.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

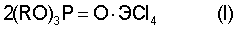
 р=-29,0 (для ТКФ
р=-29,0 (для ТКФ  max=597 нм в кюветах при толщине поглощающего слоя 10 мм относительно контрольного раствора.
max=597 нм в кюветах при толщине поглощающего слоя 10 мм относительно контрольного раствора. ЭCl4
ЭCl4  :O=Р(OR)3
:O=Р(OR)3 (P=O), см-1
(P=O), см-1 TiCl4
TiCl4