Патент на изобретение №2347561
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СРЕДСТВА, ОБЛАДАЮЩИЕ ГЕМОРЕОЛОГИЧЕСКОЙ, АНТИАГРЕГАНТНОЙ И АНТИТРОМБОГЕННОЙ АКТИВНОСТЬЮ
(57) Реферат:
Предложено использование 2-метил-6-изоборнилфенола, 4-метил-2,6-диизоборнилфенола или 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорида в качестве средств, обладающих гемореологической, антиагрегантной и антитромбогенной активностью. Показано, что заявленные соединения ограничивали усиление агрегации эритроцитов на модели гипервязкости крови, проявляли выраженную антиагрегантную активность при АДФ-индуцированной агрегации тромбоцитов и снижали массу тромба на 75% или 97% по сравнению с контролем при снижении кровотока в артерии. 5 табл.
(56) (продолжение): CLASS=”b560m”(Журнал российского химического общества им. Д.И.Менделеева), 2004, 48, №3, с.21-38.
Изобретение относится к медицине, конкретно к фармакологии, и касается средств, обладающих антирадикальной, гемореологической, антитромбоцитарной и антитромбогенной активностью. Известны средства, обладающие антирадикальной активностью: ионол (ди-бунол), аскорбиновая кислота, токоферола ацетат, эмоксипин, Известны средства, обладающие гемореологической активностью пентоксифиллин, дигидрокверцетин, танакан [3, 4, 5, 6]. Известны средства, обладающие антитромбоцитарной активностью: пентоксифилин, ацетилсалициловая кислота, тиклопидин, дипиридамол [3, 7]. Известны средства, обладающие антитромбогенной активностью: пентоксифиллин, ингибиторы циклооксигеназы и витамин С [8, 9, 10]. По этим трем видам активности наиболее близким (прототипом) является пентоксифиллин, обладающий гемореологической, антитромбоцитарной и антитромбогенной активностью [3, 11, 12]. Задачей изобретения является расширение номенклатуры средств, обладающих антирадикальной, гемореологической, антитромбоцитарной и антитромбогенной активностью. Поставленная задача достигается использованием ряда производных о-изоборнилфенола: 2-метил-6-изоборнилфенола, 4-метил-2,6-диизоборнилфенола, 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорида в качестве антирадикальных, гемореологических, антитромбоцитарных и антитромбогенных средств. Использование 2-метил-6-изоборнилфенола, 4-метил-2,6-диизоборнилфенола и 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорида, в качестве антирадикальных, гемореологических, антитромбоцитарных и антитромбогенных средств в литературе не описано [20, 21, 22, 23]. Принципиально новым в предлагаемом изобретении является то, что в качестве антирадикальных, гемореологических, антитромбоцитарных и антитромбогенных средств используются 2-метил-6-изоборнилфенол, 4-метил-2,6-диизоборнилфенол и 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорид. Данные виды активности соединений явным образом не вытекает для специалиста из уровня техники. Производные о-изоборнилфенола: 2-метил-6-изоборнилфенол, 4-метил-2,6-диизоборнилфенол и 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорид можно использовать для лечения больных с сердечно-сосудистыми и другими заболеваниями для уменьшения повышенной вязкости крови, спонтанной агрегации эритроцитов, а также снижения агрегационной способности тромбоцитов и внутрисосудистого тромбообразования. Таким образом, данное техническое решение соответствует критериям изобретения: “новизна”, “изобретательский уровень”, “промышленно применимо”. Исследования антирадикальной активности 2-метил-6-изоборнилфенола, 4-метил-2,6-диизоборнилфенола и 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорида проводили с использованием метода, основанного на способности веществ с антирадикальной активностью нейтрализовать свободные радикалы [13]. Донором свободных радикалов выступал 2,2-дифенил-1-пикрилгидразил (ДФПГ). Регистрацию изменений оптической плотности проводили на спектрофотометре СФ-46 (Россия) в течение 60 минут с интервалом пять минут при длине волны 520 нм в кварцевых кюветах с толщиной поглощающего слоя 10 мм. Антирадикальную активность соединений оценивали по уровню снижения оптической плотности, выраженного в процентах, для конечной точки периода измерения (60 минут) относительно исходного значения оптической плотности и показателю эффективного времени. Показатель эффективного времени ЕТ50% – это значение времени, выраженное в минутах, при котором происходит уменьшение исходной оптической плотности (концентрации свободных радикалов) на 50%. Данный показатель является одной из определяющих характеристик антирадикальной активности и обратно пропорционален ей. Растворы исследуемых соединений: 2-метил-6-изоборнилфенола, 4-метил-2,6-диизоборнилфенола и 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорида, раствор ионола и раствор ДФПГ использовали в эквимолярных концентрациях, равных 0,25·10-3 ммоль/л. Во всех случаях в качестве растворителя использовался 95% спирт этиловый. Измерение оптической плотности исследуемых соединений проводили каждые пять минут в течение часа после смешивания 1,5 мл 0,25·10-3 ммоль/л растворов исследуемых соединений и 1,5 мл 0,25·10-3 ммоль/л раствора ДФПГ. В качестве контроля выступал раствор, состоящий из 1,5 мл 0,25·10-3 ммоль/л раствора ДФПГ и 1,5 мл 95% спирта этилового. Эксперименты по изучению гемореологической, антитробоцитарной и антитромбогенной активностей проводили на крысах Вистар. Эксперименты по изучению гемореологических свойств 2-метил-6-изоборнилфенола, 4-метил-2,6-диизоборнилфенола и 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорида проводили на 25 крысах-самцах Вистар массой 250-300 г. Животные были разделены на 5 групп: 5 животных получили внутрижелудочно крахмальную слизь (контроль), 5 животных получали внутрижелудочно пентоксифиллин (400 мг/кг) (группа I); 5 животных получили внутрижелудочно 2-метил-6-изоборнилфенол (100 мг/кг) (группа II), 5 животных получили внутрижелудочно 4-метал-2,6-диизоборнилфенола (100 мг/кг) (группа III) и 5 животных получили внутрижелудочно 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорид (100 мг/кг) (группа IV). Соединения и эквиобъемное количество крахмальной слизи (1 мл) вводили внутрижелудочно через зонд за один час до забора крови. Влияние соединений на вязкость крови оценивали с использованием модели гипервязкости крови in vitro. Кровь забирали из общей сонной артерии под эфирным наркозом. В качестве стабилизатора использовали 3,8% раствор цитрата натрия в соотношении с кровью 1:9. Вязкость крови измеряли на ротационном вискозиметре АКР-2 в диапазоне скоростей сдвига от 5 до 300 с-1 до и после инкубации образцов при температуре 20,0±0,4°С в течение 60 минут. В этой же серии экспериментов было исследовано влияние соединений на агрегацию эритроцитов. Спонтанную агрегацию эритроцитов исследовали с помощью силлектометрического метода [3] в нашей модификации [14]. Для установления интенсивности фотометрического сигнала использовали микроколориметр МКМФ-1 с графической регистрацией на графопостроителе Н306. Критерием агрегационной активности эритроцитов служил полупериод агрегации Т1/2 – время, за которое величина фотометрического сигнала снижается в два раза. Эксперименты по изучению антитромбоцитарной активности 2-метил-6-изоборнилфенола, 4-метил-2,6-диизоборнилфенола и 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорида проводили на 25 крысах-самцах Вистар массой 250-280 г. Животные были разделены на 5 групп: 5 животных получили внутрижелудочно крахмальную слизь (контроль), 5 животных получили внутрижелудочно пентоксифиллин (400 мг/кг) (группа V); 5 животных получили внутрижелудочно 2-метил-6-изоборнилфенол (100 мг/кг) (группа VI), 5 животных получили внутрижелудочно 4-метил-2,6-диизоборнилфенол (100 мг/кг) (группа VII) и 5 животных получили внутрижелудочно 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорид (100 мг/кг) (группа VIII). Соединения и эквиобъемное количество крахмальной слизи (1 мл) вводили внутрижелудочно через зонд за один час до забора крови. Кровь забирали из общей сонной артерии под эфирным наркозом. В качестве стабилизатора использовали 3,8% раствор цитрата натрия в соотношении с кровью 1:9. Агрегацию тромбоцитов в богатой тромбоцитами плазме (БТП) определяли нефелометрическим методом по Born [15]. Получение богатой (БТП) и бедной (БеТП) тромбоцитами плазмы и подсчет числа тромбоцитов проводили по стандартному методу [16]. Из проб крови получали БТП и БеТП методом центрифугирования при 400 g и 1800 g соответственно на центрифуге РС-6. В полученной БТП подсчитывали количество тромбоцитов микроскопическим методом при фазовом контрасте в камере Горяева. Так как в норме число тромбоцитов в крови у крысы колеблется в широких пределах – от 430000 до 1 млн в 1 мм3 – после определения числа тромбоцитов в БТП проводили стандартизацию числа тромбоцитов, для чего БПТ разводили необходимым количеством БеТП до 400±30 тыс.тромбоцитов в 1 мм3 в пробе [17, 18]. Агрегацию тромбоцитов оценивали в стандартизованной плазме на приборе АТ-02, агрегатограммы регистрировали с помощью самописца Recorder 2210. После добавления индуктора агрегации регистрировали изменение уровня оптической плотности БТП. В качестве критерия агрегационной активности тромбоцитов использовали показатель степени агрегации (в %), характеризуемый изменением оптической плотности БТП после добавления в кювету индуктора агрегации. При этом за 100% принимали величину оптической плотности БеТП, а за 0% – величину оптической плотности БТП. В качестве индуктора агрегации использовали АДФ в конечной концентрации 4·10-6 M. Эксперименты по изучению антитромбогенной активности 2-метил-6-изоборнилфенола, 4-метил-2,6-диизоборнилфенола и 2-(дибуталамино)метил-4-метил-6-изоборнилфенола гидрохлорида проводили на 25 крысах-самцах Вистар массой 220-240 г. Животные были разделены на 5 групп: 5 животных получили внутрижелудочно крахмальную слизь (контроль), 5 животных получили внутрижелудочно пентоксифиллин (400 мг/кг) (группа IX); 5 животных получили внутрижелудочно 2-метал-6-изоборнилфенол (100 мг/кг) (группа X), 5 животных получили внутрижелудочно 4-метил-2,6-диизоборнилфенол (100 мг/кг) (группа XI) и 5 животных получили внутрижелудочно 2-(дибутиламино)метил-4-метил-6-изоборнилфенол гидрохлорид (100 мг/кг) (группа XII). Соединения и эквиобъемное количество крахмальной слизи (1 мл) вводили внутрижелудочно через зонд в течение трех суток. На третьи сутки эксперимента – через 1 час после последнего введения – животных наркотизировали (тиопентал натрия в дозе 60 мг/кг, внутрибрюшинно), выделяли левую общую сонную артерию и воспроизводили модель внутрисосудистого тромбоза [19]. На отпрепарированную сонную артерию накладывали манжеточные датчики и регистрировали величину кровотока по сосуду с помощью электромагнитного расходомера крови MFV-1100 (Nihon Kohden, Япония). Затем под сонную артерию подкладывали полоску фильтровальной бумаги и полоску полиэтиленовой пленки. Сверху на эту артерию накладывали полоску фильтровальной бумаги, на которую наносили 1 каплю 10% раствора FeCl2. Измеряли величину кровотока в артерии, время от момента нанесения хлорида железа на левую сонную артерию до полной остановки кровотока в ней (время образования тромба). Кроме того, производили расчет снижения кровотока относительно исходной величины кровотока в процентах. Массу тромба оценивали гравиметрическим методом. Статистическую обработку проводили с помощью пакета программного обеспечения “Statistica 6.0”. Рассчитывали среднее значение, стандартную ошибку, для выявления межгрупповых различий использовали t-критерий Стьюдента. Результаты исследований антирадикальной активности 2-метил-6-изоборнилфенола, 4-метил-2,6-диизоборнилфенола, 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорида представлены в примерах 1-5. Пример 1. Определение исходной оптической плотности раствора ДФПГ. К 1,5 мл 0,25·10-3 ммоль/л раствора ДФПГ добавляли 1,5 мл 95% спирта этилового. В качестве контрольного раствора использовали 95% спирт этиловый. Измеренное значение оптической плотности далее в расчетах принимали за 100%. Пример 2. Определение изменения оптической плотности ДФПГ под действием радикалсвязывающего агента ионола. Снижение оптической плотности на 60 минуте составило 70% относительно исходного, и ЕТ50% было равно 26,56±1,64 мин (табл.1). Пример 3. Определение изменения оптической плотности ДФПГ под действием 2-метил-6-метилизоборнилфенола. Снижение значения оптической плотности на 60 минуте составило 82% относительно исходного, и ЕТ50% было равно 5,89±1,22 мин. 2-Метил-6-метилизоборнилфенол вызвал снижение значения оптической плотности на 60 минуте на 12% больше, чем прототип, и значение показателя ЕТ50% было на 20,67 минут меньше, чем у прототипа. Полученные данные свидетельствуют о наличии высокой антирадикальной активности 2-метил-6-метилизоборнилфенола, превышающей активность прототипа (табл.1). Пример 4. Определение изменения оптической плотности ДФПГ под действием 4-метил-2,6-диизоборнилфенола. Снижение значения оптической плотности на 60 минуте составило 89% относительно исходного, и ET50% было равно 3,88±0,87 мин. 4-Метил-2,6-диизоборнилфенол вызвал снижение значения оптической плотности на 60 минуте на 19% больше, чем прототип, и значение показателя ЕТ50% было на 22,68 минут меньше, чем у прототипа. Полученные данные свидетельствуют о наличии высокой антирадикальной активности 2-метил-6-метилизоборнилфенола, превышающей активность прототипа (табл.1). Пример 5. Определение изменения оптической плотности ДФПГ под действием 2-(дибутиламино)метил-4-метил-6-изоборнилфенол гидрохлорида. Снижение значения оптической плотности на 60 минуте составило 52% относительно исходного, и ЕТ50% было равно 57,02±6,74 мин. 4-Метил-2,6-диизоборнилфенол вызвал снижение значения оптической плотности на 60 минуте на 18% меньше, чем прототип, значение показателя ЕТ50% было на 30,46 минут больше, чем у прототипа. Полученные данные свидетельствуют о наличии выраженной антирадикальной активности 2-(дибутиламино)метил-4-метил-6-изоборнилфенола, но уступающей прототипу (табл.1). Результаты исследований гемореологической активности 2-метал-6-изоборнилфенола, 4-метил-2,6-диизоборнилфенола, 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорида представлены в примерах 6-15. Пример 6. Инкубирование крови в течение 60 мин при температуре 20,0±0,4°С приводило к значимому повышению вязкости крови при скоростях сдвига 5 с-1, 10 с-1, 50 с-1, 100 с-1 и 300 с-1 на 31%, 19%, 27%, 26% и 14% соответственно (табл.2, контроль). Таким образом, на модели гипервязкости крови in vitro в контрольной группе отмечено достоверно возрастание вязкости в широком диапазоне скоростей сдвига. Пример 7. У опытных крыс в группе I вязкость крови до инкубации была достоверно ниже, чем в контроле при скоростях сдвига 5, 10 и 50 с-1 на 9%, 16% и 6% соответственно. Инкубирование крови крыс этой группы в течение 60 мин при температуре 20,0±0,4°С приводило к повышению вязкости крови при скоростях сдвига 5 с-1, 10 с-1, 50 с-1, 100 с-1 и 300 с-1 на 10%, 14%, 12%, 9% и 7% соответственно. После инкубации вязкость крови при скоростях сдвига 5 с-1,10 с-1, 50 с-1, 100 с-1, 300 с-1 была ниже, чем в контроле, на 24%, 17%, 17%, 15% и 8% соответственно (табл.2, группа I). Таким образом, на модели гипервязкости крови in vitro пентоксифиллин ограничивает возрастание вязкости крови в широком диапазоне скоростей сдвига. Пример 8. У опытных крыс в группе II исходные значения вязкости крови при скоростях сдвига 5 с-1, 10 с-1, 50 с-1 были ниже на 13%, 10% и 6% соответственно, чем в контроле. Инкубирование крови крыс этой группы в течение 60 мин при температуре 20,0±0,4°С приводило к повышению вязкости крови во всем диапазоне исследуемых скоростей сдвига на 11-26%. После инкубирования вязкость крови крыс группы II была ниже, чем в контроле при скоростях сдвига 5 с-1, 10 с-1, 50 с-1, 100 с-1 и 300 с-1 на 16%, 8%, 15%, 10% и 2% соответственно (табл.2, группа II). Таким образом, на модели гипервязкости крови in vitro 2-метил-6-изоборнилфенол ограничивает возрастание вязкости крови в широком диапазоне скоростей сдвига. Выраженность гемореологической активности 2-метил-6-изоборнилфенола сопоставима с таковым у прототипа – пентоксифиллина. Пример 9. У опытных крыс в группе III до инкубации вязкость крови была ниже, чем в контроле при скоростях сдвига 5 с-1, 10 с-1 и 50 с-1 на 14%, 10% и 6% соответственно. Инкубирование крови крыс этой группы в течение 60 мин при температуре 20,0±0,4°С приводило к повышению вязкости крови при скоростях сдвига 5 с-1, 10 с-1, 50 с-1, 100 с-1 и 300 с-1 на 14%, 12%, 12%, 11% и 7% соответственно. После инкубирования вязкость крови была ниже, чем в контроле, при скоростях сдвига 5 с-1, 10 с-1, 50 с-1, 100 с-1 и 300 с-1 на 25%, 14%, 17%, 14% и 6% соответственно (табл.2, группа III). Таким образом, на модели гипервязкости крови in vitro 4-метил-2,6-диизоборнилфенол ограничивает возрастание вязкости крови в широком диапазоне скоростей сдвига. Выраженность гемореологической активности 4-метил-2,6-диизоборнилфенола сопоставима с таковой у прототипа – пентоксифиллина. Пример 10. У опытных крыс в группе IV до инкубации вязкость крови была ниже, чем в контроле, при скоростях сдвига 5 с-1, 10 с-1, 50 с-1 и 100 с-1 на 15%, 10%, 6% и 2% соответственно. Инкубирование крови крыс этой группы в течение 60 мин при температуре 20,0±0,4°С приводило к повышению вязкости крови при скоростях сдвига 5 с-1, 10 с-1, 50 с-1, 100 с-1 и 300 с-1 на 15%, 11%, 10%, 7% и 7% соответственно. После инкубирования вязкость крови была ниже, чем в контроле, при скоростях сдвига 5 с-1, 10 с-1, 50 с-1, 100 с-1 и 300 с-1 на 25%, 15%, 18%, 17% и 6% соответственно (табл.2, группа IV). Таким образом, на модели гипервязкости крови in vitro 2-(дибутиламино)метил-4-метил-6-изоборнилфенол гидрохлорид ограничивает возрастание вязкости крови в широком диапазоне скоростей сдвига. Выраженность гемореологической активности 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорида сопоставима с таковой у прототипа – пентоксифиллина. Пример 11. Полупериод агрегации эритроцитов у крыс контрольной группы составил 18,6±1,1 с. Инкубирование крови в течение 60 мин при температуре 20,0±0,4°С приводило к уменьшению полупериода агрегации эритроцитов на 35% (табл.3, контроль). Таким образом, на модели гипервязкости крови in vitro в контрольной группе установлено уменьшение полупериода агрегации эритроцитов, что свидетельствовало об усилении агрегации эритроцитов. Пример 12. Полупериод агрегации эритроцитов у крыс группы I составил 19,6±2,1 с. Инкубирование крови в течение 60 мин при температуре 20,0±0,4°С не вызывало значимых сдвигов в значении полупериода агрегации эритроцитов. После инкубации полупериод агрегации эритроцитов был выше на 52% по сравнению с показателем контрольной группы (табл.3, группа I). Таким образом, на модели гипервязкости крови in vitro пентоксифиллин предотвращает усиление агрегации эритроцитов. Пример 13. Полупериод агрегации эритроцитов у крыс группы II составил 16,9±2,2 с. Инкубирование крови в течение 60 мин при температуре 20,0±0,4°С не вызывало существенных сдвигов в значении полупериода агрегации эритроцитов. После инкубации полупериод агрегации эритроцитов был выше на 31% по сравнению с показателем контрольной группы (табл.3, группа II). Таким образом, на модели гипервязкости крови in vitro 2-метил-6-изоборнилфенол ограничивает усиление агрегации эритроцитов. Выраженность гемореологической активности 2-метил-6-изоборнилфенола сопоставима с таковой у прототипа – пентоксифиллина. Пример 14. Полупериод агрегации эритроцитов у крыс группы III составил 18,5±1,8 с. Инкубирование крови в течение 60 мин при температуре 20,0±0,4°С не вызывало существенных сдвигов в значении полупериода агрегации эритроцитов. После инкубации полупериод агрегации эритроцитов был выше на 33% по сравнению с показателем контрольной группы (табл.3, группа III). Таким образом, на модели гипервязкости крови in vitro 4-метил-2,6-диизоборнилфенол ограничивает усиление агрегации эритроцитов. Выраженность гемореологической активности 4-метил-2,6-диизоборнилфенола сопоставима с таковой у прототипа – пентоксифиллина. Пример 15. Полупериод агрегации эритроцитов у крыс группы IV составил 16,5±1,1 с. Инкубирование крови в течение 60 мин при температуре 20,0±0,4°С не вызывало существенных сдвигов в значении полупериода агрегации эритроцитов. После инкубации полупериод агрегации эритроцитов был выше на 31% по сравнению с показателем контрольной группы (табл.3, группа IV). Таким образом, на модели гипервязкости крови in vitro 2-(дибутиламино)метил-4-метил-6-изоборнилфенол гидрохлорид ограничивает усиление агрегации эритроцитов. Выраженность гемореологической активности 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорида сопоставима с таковой у прототипа – пентоксифиллина. Результаты исследований антитромбоцитарной активности 2-метил-6-изоборнилфенола, 4-метил-2,6-диизоборнилфенола, 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорида представлены в примерах 16-20. Пример 16. В контрольной группе животных амплитуда АДФ-индуцированной агрегации тромбоцитов в стандартизованной плазме составила 28±1% (табл.4, контроль). Пример 17. После однократного внутрижелудочного введения пентоксифиллина в дозе 400 мг/кг амплитуда АДФ-индуцированной агрегации тромбоцитов в стандартизированной плазме составила 19±1%, что на 32% ниже показателя у крыс контрольной группы (табл.4, группа V). Таким образом, пентоксифиллин в дозе 400 мг/кг внутрижелудочно однократно обладает выраженной антиагрегантной активностью. Пример 18. После однократного внутрижелудочного введения 2-метил-6-изоборнилфенола в дозе 100 мг/кг амплитуда АДФ-индуцированной агрегации тромбоцитов в стандартизованной плазме составила 17±1% (табл.4, группа VI). Амплитуда агрегации тромбоцитов была на 39% ниже, чем в контроле, и была близка к значению показателя у крыс в группе V. Таким образом, 2-метал-6-изоборнилфенол в дозе 100 мг/кг внутрижелудочно однократно обладает выраженной антиагрегантной активностью, сравнимой по выраженности с пентоксифиллином в дозе 400 мг/кг. Пример 19. После однократного внутрижелудочного введения 4-метил-2,6-диизоборнилфенола в дозе 100 мг/кг амплитуда АДФ-индуцированной агрегации тромбоцитов в стандартизованной плазме составила 17±2% (табл.4, группа VII). Амплитуда агрегации тромбоцитов была на 39% ниже, чем в контроле и была близка к значению показателя у крыс в группе V. Таким образом, 4-метил-2,6-диизоборнилфенол в дозе 100 мг/кг внутрижелудочно однократно обладает выраженной антиагрегантной активностью, сравнимой по выраженности с пентоксифиллином в дозе 400 мг/кг. Пример 20. После однократного внутрижелудочного введения 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорида в дозе 100 мг/кг амплитуда АДФ-индуцированной агрегации тромбоцитов в стандартизованной плазме составила 18±1% (табл.4, группа VIII). Амплитуда агрегации тромбоцитов была на 36% ниже, чем в контроле, и была близка к значению показателя у крыс в группе V. Таким образом, 2-(дибутиламино)метил-4-метил-6-изоборнилфенол гидрохлорид в дозе 100 мг/кг внутрижелудочно однократно обладает выраженной антиагрегантной активностью, сравнимой по выраженности с пентоксифиллином в дозе 400 мг/кг. Результаты исследований антитромбогенной активности 2-метил-6-изоборнилфенола, 4-метил-2,6-диизоборнилфенола, 2-(дибутиламино)метил-4-метал-6-изоборнилфенола гидрохлорида представлены в примерах 21-25. Пример 21. В контрольной группе животных после аппликации хлорида железа на поверхность сонной артерии у всех животных происходило полное прекращение кровотока по сосуду. Среднее время полной остановки кровотока до нуля составило 20±2 минуты. Масса тромба, определяемая через сутки после аппликации хлорида железа, составила 1,2±0,2 мг (табл.5, контроль). Пример 22. У опытных крыс в группе IX к концу периода наблюдения (90 мин с момента аппликации хлорида железа) происходило снижение кровотока в сонной артерии на 31±12%. На следующие сутки в просвете сонной артерии не выявлено тромбов ни у одного животного (табл.5, группа IX). Таким образом, пентоксифиллин в дозе 400 мг/кг внутрижелудочно обладает выраженной антитромбогенной активностью. Пример 23. У опытных крыс группы к концу периода наблюдения (90 мин с момента аппликации хлорида железа) происходило снижение кровотока в сонной артерии на 20±8%. Через сутки у трех животных из пяти были обнаружены тромбы в просвете сонной артерии. Средняя масса тромба составила 0,33±0,24 мг, что было на 75% ниже, чем в контроле (табл.5, группа X). Таким образом, 2-метил-6-изоборнилфенол в дозе 100 мг/кг внутрижелудочно обладает умеренной антитромбогенной активностью. Пример 24. У опытных крыс группы XI к концу периода наблюдения (90 мин с момента аппликации хлорида железа) происходило снижение кровотока в сонной артерии на 13±9%. На следующие сутки в просвете сонной артерии не выявлено тромбов ни у одного животного (табл.5, группа XI). Таким образом, 4-метил-2,6-диизоборнилфенол в дозе 100 мг/кг внутрижелудочно обладает выраженной антитромбогенной активностью. Пример 25. У опытных крыс группы XII к концу периода наблюдения (90 мин с момента аппликации хлорида железа) происходило снижение кровотока в сонной артерии на 23±6%. Через сутки у двух животных из пяти были обнаружены тромбы в просвете сонной артерии. Средняя масса тромба составила 0,04±0,02 мг, что было на 97% ниже, чем в контроле (табл.5, группа XII). Таким образом, 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорид в дозе 100 мг/кг внутрижелудочно обладает антитромбогенной активностью. Предлагаемое изобретение расширяет арсенал средств, обладающих одновременно антирадикальной, гемореологической, антитромбоцитарной и антитромбогенной активностью. Источники информации 1. Меньщикова Е.Б., Ланкин В.З., Зенков Н.К., Бондарь И.А. и др. Окислительный стресс. Прооксиданты и антиоксиданты. – М.: Фирма «Слово», 2006. – С.193-196. 3. Габриэлян Э.С., Акопов С.Э. Клетки крови и кровообращение. – Ереван: Айастан, 1985. – С.71, 326. 4. Машковский М.Д. Лекарственные средства. – Харьков: Торсинг, 1998. – Т.1. – С.196, 441. 5. Плотников М.Б.. Алиев О.И., Маслов М.Ю. и др. Коррекция синдрома повышенной вязкости крови в условиях ишемии мозга у крыс комплексом диквертина и аскорбиновой кислоты / Эксперим. и клинич. фармакология. – 1999. – № 6. – С.45-47. 16. Баркаган З.С., Момог А.П. Основные методы лабораторной диагностики нарушений системы гемостаза. – Барнаул, 1998. – С.10-11. 18. Западнюк И.П., Западнюк В.И., Захария Е.А. Лабораторные животные. – Киев, 1974. – 303 с. 21. Патент РФ № 2233262. “Способ получения орто-терпенофенолов”. 2004. 23. Ежегодник Института химии Коми НЦ УрО РАН. – Сыктывкар, 2007. – С.31, 33.
Формула изобретения
Применение 2-метил-6-изоборнилфенола, 4-метил-2,6-диизоборнилфенола или 2-(дибутиламино)метил-4-метил-6-изоборнилфенола гидрохлорида в качестве средств, обладающих гемореологической, антиагрегантной и антитромбогенной активностью.
|
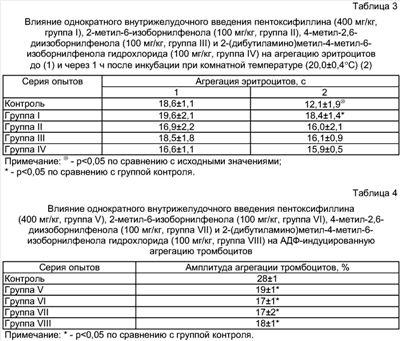
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 -каротин [1]. Наиболее близким средством (прототипом) является 4-метил-2,6-диизобутилфенол (ионол), как соединение близкое по структуре, относящееся к пространственно-затрудненным фенолам и обладающее выраженной антирадикальной активностью [2].
-каротин [1]. Наиболее близким средством (прототипом) является 4-метил-2,6-диизобутилфенол (ионол), как соединение близкое по структуре, относящееся к пространственно-затрудненным фенолам и обладающее выраженной антирадикальной активностью [2].