Патент на изобретение №2346937
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) ЗАМЕЩЕННЫЕ О-[
(57) Реферат:
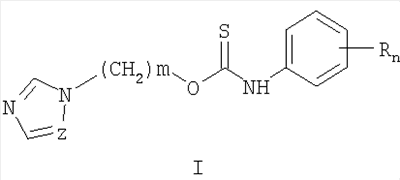
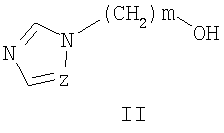
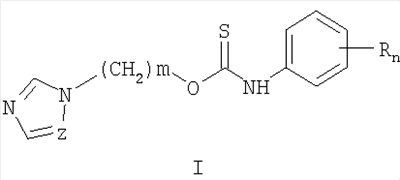
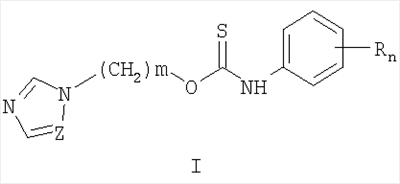
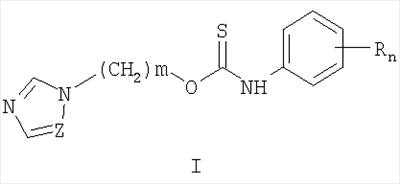
Описываются замещенные O-[ где Z=CH, N, R=H, Alk, AlkO, Hal и др., m=1, 2, 3, n=0-5, которые получают ацилированием
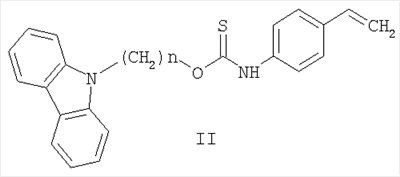
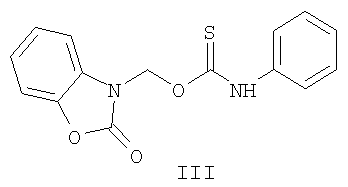
Изобретение относится к химии гетероциклических соединений, а именно к замещенным O-[ где Z означает атом азота или СН-группу; n означает целое число от 1 до 5; m означает целое число от 1 до 3; R одинаковые или разные означают атом водорода, галогена, алкильную группу с числом атомов углерода от 1 до 4, алкоксигруппу с числом атомов углерода от 1 до 4, алкоксикарбонильную группу числом атомов углерода от 1 до 4, алкилсульфанильную группу с числом атомов углерода от 1 до 4, перфторалкильную группу с числом атомов углерода от 1 до 4; обладающим фунгицидной активностью. Соединения общей формулы I могут найти применение в качестве сельскохозяйственных, промышленных, медицинских или ветеринарных фунгицидов. Изобретение относится также к способам получения соединений общей формулы I, к использованию этих соединений в композициях с другими активными и вспомогательными соединениями для борьбы с грибковыми болезнями сельскохозяйственных культур, животных и человека. Наиболее близким к заявленным O-[
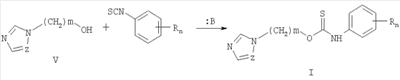
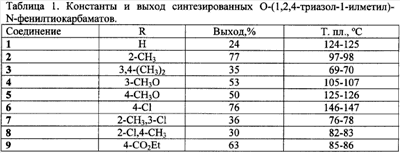
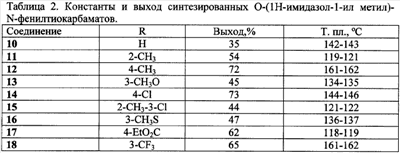
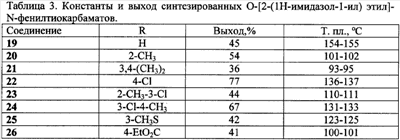
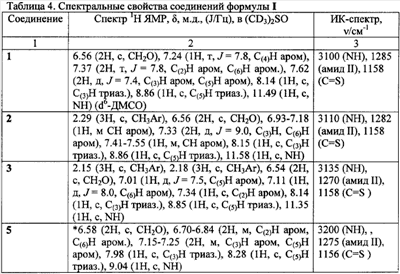
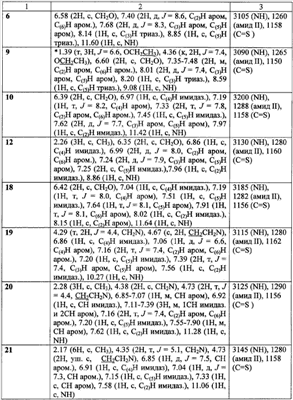
Задача, решаемая данным изобретением, состоит в увеличении эффективности борьбы с вредоносными грибами и расширении ассортимента фунгицидных препаратов. Поставленная задача решается получением соединений общей формулы I, обладающих фунгицидной активностью, а также увеличением эффективности фунгицидных средств за счет применения замещенных O-[ Согласно настоящему изобретению замещенные O-[ Техническим результатом изобретения являются новые соединения – замещенные O-[ Успешное применение пестицидов для борьбы с различными вредными организмами в большой степени зависит от препаративной формы препарата и условий, при которых действующее вещество контактирует с вредителями и возбудителями заболеваний растений. В зависимости от физико-химических свойств препарата, его назначения и способа применения выбирается наиболее эффективная и экономичная препаративная форма (композиция), это могут быть, например, дусты, гранулы, микрокапсулированные препараты, смачивающиеся порошки, концентраты эмульсий, мази, вододиспергируемые гранулы, суспензионные концентраты. Препаративные формы помимо действующего вещества могут включать в свой состав вспомогательные вещества: наполнители, растворители, поверхностно-активные вещества, умягчители воды, синергические добавки и др. Известен препарат цинеб, который применяют в виде 70 и 80%-ного смачивающегося порошка для борьбы с болезнями яблони, сливы, картофеля, томатов, огурцов, капусты в период вегетации, а также как протравитель семян. [Пестициды и регуляторы роста растений: Справ, изд. / Н.Н.Мельников, К.В.Новожилов, С.Р.Белан. – М.: Химия, 1995, с.24, с.316.] Техническим результатом изобретения также является разработка фунгицидных композиций, состоящих из замещеных O-[ Изобретение может быть проиллюстрировано следующими примерами: Пример 1. O-(1,2,4-Триазол-1-илметил)-N-фенилтиокарбамат (1) К раствору 0,99 г (0,01 моль) (1,2,4-триазол-1-ил)метанола в 10 мл абсолютного ацетонитрила добавляют 1,35 г (0,01 моль) фенилизотиоцианата и 0.1 мл (0.7 ммоль, 0.072 г) триэтиламина. Реакционную массу кипятят в течение 2 часов при температуре 80°С, растворитель удаляют в вакууме водоструйного насоса, остаток кристаллизуют из диэтилового эфира. Кристаллы отфильтровывают, промывают 2 мл холодного ацетонитрила, 2 мл диэтилового эфира и получают 0,57 г (24%) O-(1,2,4-триазол-1-илметил)-N-фенилтиокарбамата (1) с т.пл. 124-125°С. Пример 2. Этил 4-(1,2,4-триазол-1-илметокситиокарбониламино)бензоат (9) К 0,99 г (0,01 моль) (1,2,4-триазол-1-ил)метанола в 10 мл абсолютного тетрагидрофурана добавляют 2,07 г (0,01 моль) этил 4-изотиоцианатобензоата и 0.1 мл (0.7 ммоль, 0.072 г) триэтиламина. Реакционную массу кипятят в течение 4 часов при температуре 67°С, растворитель удаляют в вакууме водоструйного насоса, остаток перекристаллизовывают из метанола и получают 1,93 г (63%) этил 4-(1,2,4-триазол-1-илметокситиокарбонил-амино)бензоата (9) с т.пл. 85-86°С. Аналогично получают другие замещенные O-(1,2,4-триазол-1-илметил)-N-фенилтиокарбаматы. (Таблица 1). Пример 3. O-(Имидазол-1-илметил)-N-фенилтиокарбамат (10) К 0,98 г (0,01 моль) (имидазол-1-ил)метанола в 10 мл абсолютного ацетонитрила добавляют 1,35 г (0,01 моль) фенилизотиоцианата и 0.05 мл (0.4 ммоль, 0.036 г) триэтиламина. Реакционную массу кипятят в течение 2 часов при температуре 80°С, растворитель удаляют в вакууме водоструйного насоса, остаток кристаллизуют из диэтилового эфира. Кристаллы отфильтровывают, промывают 2 мл холодного ацетонитрила, 2 мл диэтилового эфира и получают 0,81 г (35%) O-(имидазол-1-илметил)-N-фенилтиокарбамата (10) с т.пл. 142-143°С. Пример 4. Этил 4-(имидазол-1-илметокситиокарбониламино)бензоат (17) К 0,98 г (0,01 моль) (имидазол-1-ил)метанола в 10 мл абсолютного ацетонитрила добавляют 2,07 г (0,01 моль) 4-изотиоцианатобензоата и 0.1 мл (0.7 ммоль, 0.072 г) триэтиламина. Реакционную массу кипятят в течение 3 часов при температуре 80°С, растворитель удаляют в вакууме водоструйного насоса, остаток перекристаллизовывают из изопропанола и получают 1,89 г (62%) этил 4-(имидазол-1-илметокситиокарбонил-амино)бензоата (17) с т.пл. 118-119°С.Аналогично получают другие замещенные O-(имидазол-1-илметил)фенилтио-карбаматы. (Таблица 2). Пример 5. O-[2-(Имидазол-1-ил) этил]-N-фенилтиокарбамат(19) К 1,12 г (0,01 моль) 2-(имидазол-1-ил)этанола в 10 мл абсолютного ацетонитрила добавляют 1,35 г (0,01 моль) фенилизотиоцианата и 0.1 мл (0.7 ммоль, 0.072 г) триэтиламина. Реакционную массу перемешивают в течение 24 часов при комнатной температуре, растворитель упаривают наполовину в вакууме водоструйного насоса, добавляют 20 мл диэтилового эфира, охлаждают до 0°С, кристаллы отфильтровывают и промывают 2 мл диэтилового эфира. Получают 1,11 г (45%) O-[2-(имидазол-1-ил)этил]-фенилтиокарбамата (19)с т.пл. 154-155°С. Пример 6. Этил 4-[2-(имидазол-1-ил)этокситиокарбониламино]бензоат (26) К 1,12 г (0,01 моль) 2-(имидазол-1-ил)этанола в 10 мл абсолютного ацетонитрила добавляют 2,07 г (0,01 моль) 4-изотиоцианатобензоата и 0.05 мл (0.3 ммоль, 0.046 г) диазобицикло[5.4.0]ундец-7-ена (ДБУ). Реакционную массу кипятят в течение 6 часов при температуре 80°С, растворитель удаляют в вакууме водоструйного насоса, остаток перекристаллизовывают из изопропанола и получают 1,31 г (41%) этил 4-[2-(имидазол-1-ил)этокситиокарбониламино]бензоата (26) с т.пл. 100-101°С.Аналогично получают другие замещенные O-[2-(1H-имидазол-1-ил)этил]-N-фенилтиокарбаматы. (Таблица 3). Данные о выходе и температуре плавления полученных продуктов приведены в таблицах 1,2,3 спектральные характеристики – в таблице 4. 1Н ЯМР-спектры записаны на приборе «Bruker AC-200» (рабочая частота 200 МГц), сдвиги измерены относительно тетраметилсилана, в качестве растворителя использовали d6-DMSO. ИК-спектры регистрировали с призмами NaCl в тонкой пленке в вазелиновом масле на приборе «Specord M80». Пример 7. Композиция концентрата эмульсии Действующее вещество (замещений O-[ Пример 8. Испытания на фунгицидную активность соединений проводили в экспериментах in vitro. [Методические рекомендации по определению фунгицидной активности новых соединений. Черкассы: НИИТЭХИМ. 1984. 34 с.]. Действие препаратов на радиальный рост мицелия определяли растворением композиции соединения в ацетоне и внесением аликвоты в картофелесахарозный агар при 50°С до концентрации 30 мг/л по действующему веществу. Конечная концентрация ацетона в контрольных растворах с действующими веществами составили 1%. В чашки Петри, содержащие 15 мл агаровой среды, наносили иглой культуры грибов на агаровую поверхность. Образцы выдерживали в инкубаторе при 25°С и измеряли радиальный рост через 3 суток. Процент ингибирования рассчитывали по Эбботу по отношению к необработанному контролю. В качестве эталона использовали коммерческий фунгицид триадимефон в той же концентрации. Результаты испытаний представлены в таблице 5.
Применение соединений общей формулы I как в индивидуальном виде, так и в композициях с другими активными и вспомогательными соединениями, позволяет более эффективно бороться с грибковыми заболеваниями сельскохозяйственных культур в сравнении, например, с таким широко используемым фунгицидом, как триадимефон.
Формула изобретения
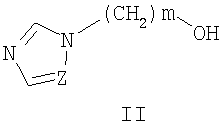
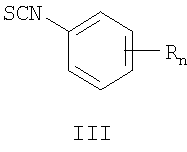
1. Замещенные O-[ где Z означает атом азота или СН-группу, n означает целое число от 1 до 5, m означает целое число атомов от 1 до 3, R одинаковые или разные означают атом водорода, галогена, алкильную группу с числом атомов углерода от 1 до 4, алкоксигруппу с числом атомов углерода от 1 до 4, алкоксикарбонильную группу числом атомов углерода от 1 до 4, алкилсульфанильную группу с числом атомов углерода от 1 до 4, перфторалкильную группу с числом атомов углерода от 1 до 4. 2. Способ получения замещенных O-[ где Z означает атом азота или СН-группу, n означает целое число от 1 до 5, m означает целое число атомов от 1 до 3, R одинаковые или разные означают атом водорода, галогена, алкильную группу с числом атомов углерода от 1 до 4, алкоксигруппу с числом атомов углерода от 1 до 4, алкоксикарбонильную группу числом атомов углерода от 1 до 4, алкилсульфанильную группу с числом атомов углерода от 1 до 4, перфторалкильную группу с числом атомов углерода от 1 до 4, заключающийся в том, что
в полярных апротонных растворителях в присутствии оснований при температуре от 20 до 80°С. 3. Способ по п.2, отличающийся тем, что в качестве оснований используют третичные амины или четвертичные аммонийные основания, выбираемые, например, из группы: триэтиламин, диазобицикло[5.4.0]ундец-7-ен, гидроксид тетрабутиламмония. 4. Фунгицидная композиция, содержащая фунгицид в концентрации 0,1-99% и вспомогательные вещества, отличающаяся тем, что в качестве фунгицида используют замещенные O-[
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 -(АЗОЛ-1-ИЛ)АЛКИЛ]-N-ФЕНИЛТИОКАРБАМАТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФУНГИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ
-(АЗОЛ-1-ИЛ)АЛКИЛ]-N-ФЕНИЛТИОКАРБАМАТЫ, СПОСОБ ИХ ПОЛУЧЕНИЯ, ФУНГИЦИДНАЯ КОМПОЗИЦИЯ НА ИХ ОСНОВЕ