|
|
(21), (22) Заявка: 2005137151/15, 29.04.2004
(24) Дата начала отсчета срока действия патента:
29.04.2004
(30) Конвенционный приоритет:
30.04.2003 EP 03009705.9
(43) Дата публикации заявки: 10.06.2006
(46) Опубликовано: 10.02.2009
(56) Список документов, цитированных в отчете о
поиске:
US 5985173 A, 16.11.1999. МАРКОВСКИЙ Л.Я. Люминофоры. – М. – Л.: Химия, 1966, с.10-12. JP 1318078 А, 22.12.1989. JP 5251008 А, 28.09.1993. JP 11043669 А, 16.02.1999. CN 1303814 А, 18.07.2001. ЕР 0333053 А2, 20.09.1989. GB 6311415 А, 02.11.1949. US 3764554 А, 09.10.1973. RU 2008318 С1, 28.02.1994. DE 10131173 А1,16.01.2003. US 2001/0024088 А,
(85) Дата перевода заявки PCT на национальную фазу:
30.11.2005
(86) Заявка PCT:
EP 2004/004573 (29.04.2004)
(87) Публикация PCT:
WO 2004/096943 (11.11.2004)
Адрес для переписки:
129090, Москва, ул. Б.Спасская, 25, стр.3, ООО “Юридическая фирма Городисский и Партнеры”, пат.пов. Е.Е.Назиной, рег. № 517
|
(72) Автор(ы):
МЕЙЕР Кристиане (DE),
ХААЗЕ Маркус (DE)
(73) Патентообладатель(и):
ЦЕНТРУМ ФЮР АНГЕВАНДТЕ НАНОТЕХНОЛОГИ (ЦАН) ГМБХ (DE)
|
(54) ЛЮМИНЕСЦЕНТНЫЕ НАНОЧАСТИЦЫ С ЯДРОМ И ОБОЛОЧКОЙ
(57) Реферат:
Изобретение может быть использовано в устройствах или материалах для генерации света, печати или маркировки. Люминесцентные наночастицы включают ядро, полученное из люминесцирующей соли металла, выбранной из фосфатов, сульфатов или фторидов, которое окружено оболочкой, полученной из соли или оксида металла, способных предотвращать или уменьшать перенос энергии от ядра после его электронного возбуждения к поверхности наночастицы. Для получения люминесцентных наночастиц согласно изобретению готовят первую смесь, содержащую наночастицы необязательно легированного люминесцирующего сульфата, фосфата или фторида металла в органической среде. Затем полученную смесь подвергают взаимодействию при 50-350°С с источником анионов для формируемой оболочки и второй смесью, содержащей формирующие оболочку ионы металла и органический комплексообразователь. Изобретение позволяет повысить квантовый выход. 4 н. и 18 з.п. ф-лы, 2 ил.
(56) (продолжение):
CLASS=”b560m”27.09.2001. US 6207229 В1, 27.03.2001. М.HAASE et al. Synthesis and properties of colloidal lanthanide-doped nanocrystals, J. Alloys and Compounds, 2000, v.303-304, p.p.191-197.
Настоящее изобретение относится к люминесцентным, в частности к фотолюминесцентным наночастицам с ядром из люминесцентного вещества, окруженным особой оболочкой, и к их получению.
Уровень техники
Наночастицы, т.е. частицы, размеры которых не превышают 1 микрометра, благодаря своим уникальным свойствам вот уже более десятилетия остаются в центре внимания как исследователей, так и промышленных разработчиков. В исследованиях и разработках в области оптоэлектроники внимание на люминесцентных частицах фокусируется ввиду их возможного применения в светоизлучающих диодах (LED), дисплеях, оптоэлектронных устройствах для нанометрических измерений или как источника излучения в лазерах с низким порогом возбуждения.
Среди люминесцирующих (люминесцентных) веществ часто различают полупроводники и не полупроводники.
Полупроводниковые наночастицы, такие как полупроводники II-VI или III-V, которые могут быть легированными или нелегированными, характеризуются квантовыми ограничениями как для электрона, так и для дырки во всех трех измерениях, что приводит к увеличению эффективной ширины запрещенной (энергетической) зоны вещества с уменьшением размеров кристаллов. Следовательно можно получать сдвиг как оптического поглощения, так и эмиссии полупроводниковых наночастиц в сторону голубой части спектра (более высоких энергий) по мере уменьшения размеров наночастиц. Однако зависимость эмиссии от размеров является нежелательной в ряде применений, поскольку она требует очень строгого контроля на стадиях распределения частиц по размеру или селекции по размеру, прежде чем рассматривать вопрос о промышленном применении.
Водорастворимые полупроводниковые нанокристаллы с ядром/оболочкой описаны, например, в WO 00/17655.
В патенте раскрывается, что особая привлекательность люминесцирующих веществ на основе нанокристаллических не полупроводников, в частности, легированных лантаноидами окислов или солей металлов, состоит в том, что их флуоресцентное излучение относительно узкое и не зависит в большой степени от вещества-хозяина (носителя), а также от размеров наночастиц. Цвет излучения, скорее, зависит лишь от типа лантаноидного металла. Документ PCT/DE 01/03433, переданный авторам, описывает общеприменимый способ получения легированных лантаноидами наночастиц указанного типа. Эти наночастицы можно получать таких размеров (не более 30 нм), при которых более не происходит взаимодействия с длиной волны видимого света, что ведет к образованию прозрачных дисперсных систем, например, в органических или водных растворителях.
Важной характеристикой для легированных лантаноидами наночастиц, определяющей степень их пригодности к применению, является их квантовый выход. Под квантовым выходом авторы понимают отношение числа испускаемых фотонов к числу поглощаемых фотонов.
Как правило, желательно получать нанокристаллические вещества с квантовым выходом такого же порядка, который соответствует люминесцирующему макрокристаллическому веществу. Например, суммарный показатель квантового выхода у коммерчески доступного макрокристаллического зеленого люминесцирующего фосфора (La0,45,Ce0,40)PO4:Tb0,15 составляет порядка 93% (включая УФ-излучение).
Однако за счет значительно большей величины соотношения поверхность/объем у нанокристаллических веществ возрастает вероятность явления гашения поверхностной люминесценции.
K.Riwotzky et al. в J. Phys. Chem. B 2000, 104, 2824-2828, “Liquid phase synthesis doped nanoparticles: colloids of luminescent LaPO4:Eu and CePO4:Tb particles with a narrow particle size distribution” сообщают, например, о квантовом выходе у LaPO4:Eu, составившем менее 10%, при возбуждении при 277 нм и о 16% квантовом выходе у CePO4:Tb, с учетом эмиссии церия, и об 11% выходе при учете эмиссии одного только тербия. Наблюдаемые значения весьма далеки от теоретических значений квантового выхода 89% и 38%, рассчитанных соответственно для нанокристаллических LaPO4:Eu и CePO4:Tb. Авторы названной статьи полагают, что возбужденное состояние основного вещества убывает за счет переноса энергии не только к люминесцирующим центрам, но также и к центрам, в которых имеет место безизлучательная рекомбинация. Вероятно, центрами безизлучательной рекомбинации могут быть те же самые гасящие ионы, к которым осуществляется перенос энергии от люминесцирующих ионов, или же состояния поверхности наночастиц. В этом контексте авторы отмечают, что наращивание оболочки из инертного материала вокруг каждой наночастицы уже применялось с успехом для полупроводниковых наночастиц, посредством чего достигалось увеличение у них квантового выхода люминесценции до значений 30-60% и более (ссылки 37-44 у K. Riwotzki и др.).
Jan W. Stouwdam and Frank C. J. M. van Veggel, Nano Letters, ASAP article, web release May 15, 2002, “Near-infrared emission of redispersible Er3+, Nd3+ and Ho3+ doped LaF3 nanoparticles” раскрывают получение наночастиц, которые могут быть перспективным материалом для основанных на полимерах оптических компонентов, поскольку им свойственна люминесценция и они имеют длину волны в диапазоне 1300-1600 нм, в котором оптические волокна на основе кремния обладают максимальной светопроницаемостью. Эти авторы проводили количественные измерения биэкспоненциального распада при люминесценции этих наночастиц и в этой связи высказывают предположение, что возможным путем усиления люминесценции ионов, локализующихся на поверхности или вблизи от нее, может оказаться наращивание слоя нелегированного LaF3 вокруг частиц.
K. Riwotzki et al., J. Phys. Chem. B 2001, 105, 12709-12713, “Colloidal YVO4:Eu and YO0,95V0,05О4:Eu particles: Luminescence and Energy transfer process” рассматривают вероятность покрытия из YPO4 для ядер из YVO4:Eu как возможного средства по увеличению низкого квантового выхода в 15%, наблюдаемого у нанокристаллического YVO4:Eu.
Получение частиц с ядром и оболочкой наталкивается, однако, на существенные трудности. Во-первых, необходимо предотвращать независимый (самостоятельный) рост исходных веществ, используемых для оболочки, так как он приводит к сосуществованию гомогенных наночастиц различного состава. Одновременно необходимо подавлять процессы обмена между отдельными наночастицами и созревание Оствальда. Созревание Оствальда представляет собой явление, имеющее место в дисперсионных системах малых частиц при повышенных температурах и включающее рост больших частиц за счет более малых частиц. Этот механизм также ведет к рандомизации различных композиций, используемых для ядра и оболочки.
M. Haase et al., Journal of Alloys and Compounds, 303-304 (2000) 191-197, “Synthesis and properties of colloidal lanthanide-doped nanocrystals” сравнивают свойства легированных лантаноидами нанокристаллов, которые были получены гидротермальным способом (в водном растворе) и в высококипящих органических растворителях (трибутилфосфате), соответственно. Авторы сообщают о 15% люминесцентном квантовом выходе при комнатной температуре у наночастиц YVO4:Eu.
Люминесцентные квантовые выходы такого же порядка (15%) приводятся также в G. A. Hebbink et al., Advanced Materials 2002, 14, №16, pages 1147-1150, “Lanthanide (III)-doped nanoparticles that emit in the near-infrared” для LaPO4-частиц, легированных Nd3+ и Er3+.
Таким образом, на сегодняшний день еще не получены не полупроводниковые частицы состава ядро/оболочка.
Соответственно, целью настоящего изобретения является разработка получения особых не полупроводниковых частиц с ядром и оболочкой (ядро/оболочка).
Кроме того, в настоящем изобретении ставится цель увеличения квантового выхода гомогенных люминесцирующих не полупроводниковых частиц.
Сущность настоящего изобретения
Указанные технические задачи решаются следующим образом:
с помощью люминесцентных наночастиц, включающих
(а) ядро, полученное из необязательно легированной люминесцирующей соли металла, выбранной из фосфатов, сульфатов, или фторидов, и окруженное
(b) оболочкой, полученной из соли или окисла металла, способных предотвращать или уменьшать перенос энергии от ядра к поверхности наночастиц после его электронного возбуждения,
а также с помощью способа получения этих наночастиц, где указанный способ включает следующие стадии:
получение первой смеси, содержащей наночастицы легированных люминесцирующих сульфата, фосфата или фторида металлов в органической среде,
взаимодействие указанной первой смеси, источника анионов для оболочки, которую необходимо сформировать, и второй смеси, содержащей формирующие оболочку ионы металлов и органическое комплексообразующее вещество для указанных ионов металлов, при температуре от 50 до 350°С до тех пор, пока вокруг указанных люминесцирующих наночастиц не образуется оболочка.
Фигуры
Фиг.1 показывает спектры флуоресценции гомогенных наночастиц CePO4:Tb (сплошная линия) и частиц ядра и оболочки по настоящему изобретению (пунктирная линия), где LaPO4-оболочка выращена вокруг CePO4:Tb-ядра.
Фиг.2 показывает результаты TEM (просвечивающий электронный микроскоп)-анализа одной частицы ядро/оболочка по настоящему изобретению, а именно, (D) Хельфельдово (Hellfeld) изображение одной наночастицы CePO4:Tb, окруженной LaPO4-оболочкой (диаметром около 7 нм); (E) изображение спектра при 860 эВ-ной потере энергии, а также профили поверхности частицы (A,C) и центра (B).
Детальное описание настоящего изобретения
I. Люминесцирующие наночастицы
Люминесцирующие, в особенности, фотолюминесцирующие наночастицы по настоящему изобретению включают ядро, полученное из необязательно легированной люминесцирующей неорганической соли металла, выбранной из фосфатов, сульфатов или фторидов.
“Люминесценция” характеризует свойство заявленных наночастиц поглощать энергию (например, в виде фотонов, пучков электронов, рентгеновских лучей и т.п.), которая затем выделяется в виде света с меньшей энергией. Следует понимать, что в описании и в формуле изобретения термин “люминесцирующий” включает более конкретное и предпочтительное значение “фотолюминесцирующий”.
Под “фотолюминесценцией” авторы понимают способность неорганической соли металла поглощать фотоны конкретной энергии (например, УФ, видимого света) и излучать свет с меньшей энергией (с большей длиной волны, например, УФ, видимый спектр, инфракрасное излучение) в течение определенного периода времени. Период светового излучения может соответствовать продолжительности возбужденного состояния вплоть до 10-7 или 10-8 сек, который обычно называется флуоресценцией, но возможны также и более длительные периоды. Для легированных лантаноидами сульфатов, фосфатов или фторидов обычно длительность возбужденного состояния составляет, по наблюдениям, величины порядка миллисекунд (например, 1-20 мс).
“Легирование” следует понимать в широком смысле. Верхний предел используемой легирующей добавки должен быть достаточно низким для того, чтобы генерируемая люминесценция не уменьшалась за счет явления концентрационного гашения. Соответственно, этот верхний предел зависит от факторов, подобных расстоянию в кристаллической решетке между ионами легирующего металла, которые являются специфическими для каждого материала ядра. Предпочтительно, вещество-хозяин замещается легирующей добавкой в количестве вплоть до 50 мол.%, предпочтительно 0,1-45 мол.%, например, 0,5-40 мол.%, или 1-20 мол.%.
В соответствии с первым вариантом осуществления настоящего изобретения предпочтительно легированное вещество ядра покрывают нелюминесцирующими солями металлов, в частности, фосфатами, сульфатами или фторидами.
Для вещества-хозяина, используемого для ядра, особых ограничений не имеется. Оно может быть выбрано из числа известных сульфатов, фосфатов или фторидов в зависимости от легирующей добавки, которая должна быть внедрена в решетку. Поскольку большинство люминесцирующих легирующих добавок представляют собой ионы двух- или трехвалентных металлов, предпочтительно использовать сульфаты, фосфаты или фториды нелюминесцирующих двух- или трехвалентных металлов, таких как металлы группы 2 (щелочноземельные металлы, такие как Mg, Ca, Sr или Ba) или группы 3 (Sc, Y или La) или группы 13 (например, Al, Ga, In или Tl) или Zn. При выборе подходящего вещества-хозяина для конкретной легирующей добавки следует, кроме того, учитывать, что, как известно в уровне техники, металл-хозяин и металл легирующей добавки предпочтительно должны иметь, одинаковую валентность и сходные (допустимое отклонение, например, ±20%) или идентичные ионные диаметры. Одновременно, это обычно повышает совместимость легирующей добавки и металла-хозяина в случаях, когда они способны к формированию, с определенным анионом, кристаллов с тем же самым или сходным типом решетки, имеющих одинаковые или сходные параметры кристаллических решеток (допустимое отклонение, например, ±20%).
В качестве металла вещества-хозяина для ядра указанным критериям могут отвечать Ba и Sr, поскольку диаметры ионов этих металлов очень близки к диаметрам двухвалентных (+II) лантаноидных легирующих добавок. По этой же причине, соли La и Y являются подходящими веществами-хозяевами для легирующих добавок на основе трехвалентных (+III) лантаноидов.
Не имеется также никаких специальных ограничений в отношении типа вводимого легирующего металла, пока он обладает способностью преобразовывать поглощаемые фотоны в люминесцентное излучение. Так, например, можно использовать такие металлы, как Cr, Ag, Cu, Co или Mn (например, в сочетании с цинком в качестве металла-хозяина). Из их числа предпочтительными в качестве легирующих добавок для атомов металла-хозяина групп 13 и 2 являются соответственно Cr3+ и Mn2+. Однако легирование с помощью металлов-лантаноидов является предпочтительным, поскольку люминесценция лантаноидных металлов особенно не зависит от окружения решетки. Как правило, предпочтительным является использование двух- или трехвалентных легирующих добавок, в особенности, лантаноидных легирующих добавок. Двухвалентные лантаноиды (+II состояния окисления) характеризуются относительно сильным поглощением, но относительно широкими полосами излучения. По этой причине их удобно использовать в качестве сенсибилизаторов, переносящих энергию к другим люминесцирующим металлам (например, Eu2+ к Mn2+). Способность трехвалентных лантаноидов (состояние окисления +III) к световому излучению в форме относительно отчетливых полос также делает их особенно желательными для применения в качестве легирующих добавок в конкретных применениях. Эти легирующие добавки можно использовать в качестве единственного легирующего металла или в комбинации, как раскрывается ниже для некоторых сочетаний трехвалентных лантаноидов.
Легирующие лантаноидные ионы (ион) можно подходящим образом выбирать из Ce (порядковый номер 58), Pr (59), Nd (60), Sm (62), Eu (63), Gd (64), Tb (65), Dy (66), Ho (67), Er (68), Tm (69) или Yb (70). Предпочтительными легирующими добавками являются Ce, Nd, Eu, Tb, Dy, Ho, Er и Yb. Er3+, Nd3+ и Ho3+ представляют особый интерес для области телекоммуникации, поскольку они излучают в диапазоне 1300-1600 нм. Ce используется предпочтительно в сочетании с другим легирующим веществом, таким как Nd, Dy или Tb. Как известно, Ce хорошо поглощает УФ-излучение с длиной волны 250-300 нм и характеризуется довольно широкой полосой люминесценции приблизительно 330 нм в зависимости от окружения решетки (например, в фосфатной решетке). Если использовать Ce в сочетании с другими легирующими добавками, которым можно передать поглощенную энергию, то можно получить очень эффективные люминесцирующие системы. Еще одну интересную комбинацию легирующих металлов представляет Yb и Er, имеющая большое значение для Er3+-легированных оптических усилителей, где Er3+ накачивается косвенно, через Yb3+, имеющий в десять раз большее поперечное сечение поглощения и значительно более широкий пик при 980 нм, чем у Er3+.
Как отмечалось выше, указанные сочетания лантаноидных металлов можно использовать не только как легирующие добавки для ядра. В равной мере выгодно использовать в качестве металла-хозяина ион металла-лантаноида (например, Ce3+, Yb3+), который имеет большее поперечное сечение поглощения, и при замещении его части меньшими количествами другого металла (например, 0,1-40 мол.%, предпочтительно, 0,5-30 мол.%). “Другим” металлом предпочтительно является Nd3+, Dy3+ или Tb3+ для основанных на Ce3+ веществ-хозяев и Er3+ для основанных на Yb3+ веществ-хозяев. По этой причине, в качестве вещества-хозяина для ядра можно использовать также сульфаты, фосфаты или фториды лантаноидов (например, Ce3+, Yb3+). Их можно комбинировать с такими же веществами для оболочки, как это далее детально будет разъяснено, предпочтительно, с сульфатами, фосфатами или фторидами металлов группы 2, в особенности, сульфатами, фосфатами или фторидами La. Особенно предпочтительными вариантами осуществления изобретения являются частицы ядро/оболочка типа CePO4:Tb/LaPO4 и CePO4:Nd/LaPO4.
В соответствии с настоящим изобретением вещество оболочки, а именно, соль или оксид металла, способно предотвращать или уменьшать перенос энергии от ядра, в его электронном возбужденном состоянии, к поверхности частицы ядро/оболочка, где она будет гаситься. Как полагают, эти явления гашения (тушения), наблюдаемые у люминесцирующих ядер наночастиц, не имеющих оболочки, вызваны либо взаимодействием центров люминесценции на поверхности с молекулами из окружающей среды (например, растворителя), контактирующими с поверхностью или связанными с нею, либо состояниями ненасыщенности поверхности. Что касается последнего воздействия, то, как полагают, свободные валентности поверхностных металлических атомов обусловливают низкоэнергетические состояния, которым энергия, поглощенная атомами металла, расположенными ниже поверхности, легко может быть передана.
Задачу предотвращения или уменьшения переноса энергии всегда можно решить с помощью солей или оксидов металла, в которых энергетическое расстояние между основным состоянием электронов и первоначальным возбужденным состоянием электронов больше, чем соответствующее энергетическое расстояние выбранного ядра. При таких обстоятельствах энергия (например, УФ, видимого света, инфракрасного излучения), поглощенная ядром, не может быть передана оболочке, в особенности, атомам металла оболочки. Достигаемая таким образом локализация энергии в ядре предотвращает явления поверхностного гашения и увеличивает квантовый выход. В соответствии с указанным первым вариантом осуществления настоящего изобретения соль или оксид оболочки является нелюминесцирующим и таким образом отсутствуют низкоэнергетические состояния электронов, которым могла бы передаваться энергия от возбужденного ядра.
В соответствии со вторым вариантом осуществления настоящего изобретения ядро состоит из люминесцирующего сульфата, фосфата или фторида лантаноида, а оболочка состоит из соли или окиси лантаноида, отличающихся от вещества ядра и предотвращающих или уменьшающих перенос энергии от ядра после возбуждения его электронов к поверхности наночастицы. Ядро и атом лантаноидного металла можно подходящим образом выбирать из числа Ce (порядковый номер 58), Pr (59), Nd (60), Sm (62), Eu (63), Gd (64), Tb (65), Dy (66), Ho (67), Er (68), Tm (69) или Yb (70) при условии, согласно вышеприведенному объяснению, что относительные энергетические расстояния между основным состоянием электронов и первоначальным возбужденным состоянием не позволят передать энергию возбуждения от ядра к оболочке. Предпочтительно, ядро состоит из сульфата, фосфата или фторида Nd, а оболочка состоит из соли или окиси Gd. Данное сочетание атомов этих металлов особенно желательно, так как Gd-оболочка не только способствует увеличению квантового выхода сульфата, фосфата или фторида Nd, но также обеспечивает прекрасные контрастные свойства ЯМР, что обусловлено, как полагают, местонахождением Gd на поверхности частиц. Способность люминесцировать и давать ЯМР-контрастность вместе делают особенно привлекательным использование данного варианта осуществления в диагностических целях.
Что касается химического состава оболочки, то любой подходящий анион или оксид можно использовать, пока он способен расти на частицах ядра вместе с выбранным атомом металла.
Подходящие анионы для получения оболочки включают, но не ограничиваются ими, фосфаты, галофосфаты, арсенаты, сульфаты, бораты, алюминаты, галлаты, силикаты, германаты, оксиды, ванадаты, ниобаты, танталаты, вольфраматы, молибдаты, алкалгалогенаты, прочие галогениды, нитриды, сульфиды, селениды, сульфоселениды или оксисульфиды. Соли металлов в виде наночастиц такого типа описаны в PCT/DE 01/03433.
В соответствии с настоящим изобретением единственным критерием, определяющим выбор атомов металла для оболочки, является отсутствие способности передавать энергию люминесценции от возбужденного ядра к поверхности после облучения. Предпочтительными ионами металлов, которые можно использовать для этой цели, являются те же ионы металлов, что упомянуты выше для материалов ядра. Они включают, но не ограничиваются ими, металлы группы 2 (щелочноземельные металлы, такие как Mg, Ca, Sr или Ba), металлы группы 3 (как Sc, Y или La), металлы группы 13 (как Al, Ga, In или Tl). Для увеличения способности вещества оболочки расти на поверхности вещества ядра предпочтительно также, но совершенно не обязательно, выбирать в качестве вещества оболочки сульфат, фосфат или фторид того же металла, что составляет вещество-хозяина ядра. Если это условие не выполняется, то предпочтительно, чтобы вещество-хозяин ядра и вещество оболочки принадлежали к одному и тому же типу решетки и имели бы очень схожие (допустимое отклонение, например, ±20%) или идентичные параметры решетки.
Частицы ядро/оболочка по настоящему изобретению образуют предпочтительно кристаллические вещества. Это может быть подтверждено порошковыми рентгенограммами.
Частицы ядро/оболочка по настоящему изобретению могут иметь форму, например, иглоподобную, эллипсоидную или сферическую, последние два варианта являются предпочтительными.
Наночастицы ядро/оболочка по настоящему изобретению предпочтительно имеют средний размер, измеренный по самой длинной оси, 1-100 нм, более предпочтительно 1-50 нм. Еще более желательны средние размеры, составляющие самое большее 30 нм, самое большее 20 нм, самое большее 10 нм, например, 2-8 нм или 4-6 нм. Для каждого случая стандартное отклонение составляет предпочтительно менее 30%, особенно, менее 10%.
Размер частиц и их распределение может быть определено с помощью технологий, описанных также в уже упомянутых статьях K.Riwotzki et al. и M. Haase et al., например, с использованием просвечивающего электромикрографа (TEM).
Средняя толщина оболочки предпочтительно соответствует по меньшей мере одному или двум монослоям. С другой стороны, излишняя толщина оболочки может отрицательно сказаться на суммарных фотолюминесцентных свойствах частицы ядро/оболочка. Предпочтительный верхний предел толщины оболочки равняется таким образом диаметру ядра, более предпочтительно 2/3 диаметра, еще более предпочтительно 1/2 диаметра.
II. Получение наночастиц ядро/оболочка
Указанные наночастицы ядро/оболочка по настоящему изобретению получены по способу, раскрываемому далее в пунктах формулы и включающему по меньшей мере две следующих стадии:
1. Получение так называемой “первой смеси”, содержащей наночастицы (ядра) необязательно легированного, люминесцирующего сульфата, фосфата или фторида металла в органической среде.
2. Взаимодействие указанной первой смеси, источника анионов для оболочки, которую необходимо сформировать, в частности, фосфатным, сульфатным или фторидным источником, и “второй смеси”, содержащей ионы металла, образующего оболочку, и органическое комплексообразующее вещество для указанных ионов металла при температуре 50-350°С до тех пор, пока вокруг указанных люминесцирующих наночастиц не образуется оболочка.
II.1 Первая стадия способа и получение частиц ядра.
Наночастицы, обеспеченные в качестве материала ядра и присутствующие в так называемой “первой смеси”, можно синтезировать (получать) способами, известными в уровне техники. Как правило, жидкостная технология предпочтительней, чем “сухая”, поскольку она позволяет лучше контролировать размер частиц. Кроме того, при жидкостных способах получения легче подавлять агрегирование получаемых наночастиц.
Из известных технологий жидкостного получения можно использовать золь-гель процессы, гидротермальный синтез или органический синтез с комплексообразователями, которые регулируют рост кристаллов. Кроме того, конкретно фториды можно получать по методике получения, описанной у J. W. Stouwdam и F. C. J. M. Van Veggel. Так, наночастицы LaF3 и другие фториды могут быть получены нагреванием раствора ди-н-октадецилдитиофосфата аммония и NaF в смеси этанол/вода. Затем водные растворы нитратов соответствующих металлов добавляют по каплям и перемешивают раствор в течение двух часов при 75°С с последующим охлаждением до комнатной температуры. Недостатком этого способа является то, что получаемые частицы все еще отличаются довольно широким распределением частиц по размеру, что требует дополнительных стадий очистки путем центрифугирования.
“Гидротермальный синтез” фосфатов, легированных лантаноидами, описан, например, в “Wet-chemical synthesis of doped colloidal nanomaterials: particles and fibres of LaPO4:Eu, LaPO4:Ce, LaPO4:Ce,Tb” у H. Meyssamy et al., Advanced Materials (1999), Vol. 11, No. 10, pages 840 et seq. В качестве исходных веществ для сульфатных, фосфатных или фторидных наночастиц, предпочтительно использовались хлориды, нитраты или ацетаты металлов. Взаимодействие проводили в воде в качестве реакционной среды в автоклаве, чтобы поддерживать высокое давление, предпочтительно, давление от 10-20 бар во время реакции.
В результате гидротермального синтеза получаются частицы относительно большие по размеру, часто имеющие игольчатую форму. Помимо этого, для получаемого вещества, как правило, характерно относительно широкое распределение частиц по размерам. При указанном способе H. Meyssamy et al. процент наночастиц с диаметром менее 25 нм составляет, например, всего лишь около 20%. Они могут быть выделены на последующих стадиях центрифугирования.
Кроме того, необязательно легированные сульфаты можно получать при давлении окружающей среды в органических средах, выбираемых из полиолов (высокомолекулярных спиртов) и сульфоксидов, которые, как полагают, способны регулировать рост кристаллов за счет способности образовывать металлокомплексы. Далее здесь этот способ будет называться как “полиол- или сульфоксид-способ”.
Используемые полиолы предпочтительно содержат две или три гидроксильные группы, в качестве примера можно назвать глицерин, этиленгликоль или полиэтиленгликоль, где предпочтительно использовать полиэтиленгликоль с низкой молекулярной массой (предпочтительное среднее число звеньев этиленгликоля вплоть до 4). В качестве сульфоксида можно использовать диметилсульфоксид (DMSO). Данный способ получения предпочтительно используется при получении сульфатов щелочноземельных металлов, таких как сульфат магния, кальция, стронция или бария как легированного вещества-хозяина.
Предпочтительными источниками атомов металла являются соответствующие хлориды и их гидраты. Как исходное вещество для сульфата предпочтительно использовать сульфаты щелочных металлов, сульфаты аммония или сульфаты, имеющие органические катионы. В равной степени приемлемы соответствующие гидросульфаты.
Органический катион выбирают предпочтительно из основных N-содержащих алифатических, ароматических и алифатических/ароматических веществ, имеющих предпочтительно от 4 до 30 атомов углерода, предпочтительно, от 4 до 20 атомов. Приемлемые катионы включают, например, четвертичный аммоний или четвертичный фосфоний, где 4 замещающие группы могут быть независимо выбраны из алкила, имеющего предпочтительно от 1 до 10 атомов углерода (предпочтительно, 1-5), или бензила, или протонированных ароматических оснований, таких как гидразин, амантадин, пиридин или коллидин.
Соответственно, сульфатные наночастицы можно получать из исходных материалов, таких как тетрабутиламмоний гидросульфат, тетраметиламмоний сульфат, бис-тетрабутиламмоний сульфат или триэтиламмоний гидросульфат. Другими приемлемыми исходными материалами являются аммоний гидросульфат, аммоний сульфат, гидросульфаты щелочных металлов, сульфаты амантадина, этилендиаммоний сульфат и гидразиний сульфат.
Для легирования сульфатного вещества-хозяина можно использовать нитраты или галогениды соответствующей легирующей добавки, особенно хлорида соответствующего металла.
Если в исходном материале содержатся гидросульфаты, то предпочтительно добавлять в реакционную среду органические основания, такие как имидазол, в качестве кислотного акцептора. Реакцию предпочтительно проводят при температуре от 50 до 240°С, при этом для глицерина предпочтительна более низкая температура в интервале 50-100°С, а для других полиол- или сульфоксидных растворителей предпочтительна более высокая температура в интервале 160-240°С, в частности, наиболее приемлема температура от 160 до 180°С. Средний диаметр получаемых частиц составляет порядка 0,2-50 нм, эти частицы легко диспергируют в водной среде.
Ядра наночастиц, получаемые по золь-гелевому способу, гидротермальным синтезом или так называемым “полиол- или сульфоксид-синтезом”, являются иногда диспергируемыми в органической среде, используемой на первой стадии способа по изобретению, особенно, когда реакционная среда для ядра и среда в способе по изобретению (при получении оболочки), соответственно, значительно различаются по своей полярности. По этой причине может оказаться необходимым подвергать наночастицы последующей обработке приемлемым полярным органическим соединением для увеличения их диспергируемости. Предпочтительно осуществлять эту последующую обработку с использованием той же органической среды, что будет использоваться при получении оболочки или с помощью органических сред сходной полярности.
Если, например, необходимо осуществлять получение оболочки в N- или P-содержащих средах, то последующая обработка может подходящим образом включать подвергания частиц, полученных золь-гелевым способом, гидротермальным синтезом или так называемым “полиол- или сульфоксид-способом”, последующей обработке в N- или P-содержащих средах.
Указанная последующая обработка включает нагревание наночастиц в соответствующем органическом соединении. Результатом этого является замещение водных или других гидрофильных остатков, связанных с поверхностью наночастиц, полярным органическим соединением. По причинам, указанным выше, полярное органическое соединение выбирают предпочтительно из N- или P-содержащих комплексообразователей для ионов металла, что будет описано далее в тексте в связи с “органическим синтезом” и в связи со второй стадией способа. Однако можно использовать также и другие функционализированные полярные органические соединения.
Указанная последующая обработка для сульфатов не требуется, когда они получены по “полиол- или сульфоксид-” способу, если последующие стадии получения выполнялись в полиолах и/или сульфоксидах.
В соответствии с дополнительной и предпочтительной методикой, называемой здесь и далее “органический синтез”, способ получения люминесцирующих ядер наночастиц включает следующие стадии:
а) взаимодействие в органической реакционной среде, содержащей по крайней мере один агент, образующий комплекс с металлом, и необязательно по меньшей мере один дополнительный растворитель, растворимый или диспергируемый в реакционной среде источник металла и растворимый или диспергируемый в реакционной среде источник фосфата, сульфата или фторида,
b) необязательно отделение реакционной среды от образовавшихся при этом наночастиц фосфата, сульфата или фторида металла, и
c) необязательно извлечения наночастиц соли.
Под “органической средой” понимаются органические растворители, которые, кроме неизбежных остатков, не содержат воды. Точка кипения этой органической среды предпочтительно выше, чем приводимые ниже температуры реакции. Она составляет, например, от 150 до 400°С, предпочтительно выше 180°С, и особенно выше 210°С (при давлении окружающей среды).
В зависимости от подверженности источника металла к окислению предпочтительно осуществлять реакцию в атмосфере газа, такого как азот или аргон.
Учитывая степень чистоты исходных веществ, можно рекомендовать использовать соли металлов, чистота которых составляет по меньшей мере 99,9%. Все используемые реагирующие вещества и растворители предпочтительно не содержат воды и/или их высушивают до использования. Однако хлориды металлов, часто применяемые в качестве гидроксида, предпочтительно, не следует подвергать слишком длительной процедуре сушки, так как это может способствовать увеличению образования нерастворимых в реакционной среде оксихлоридов.
Реакцию предпочтительно осуществлять при температуре от 50 до 350°С, например, от 120 до 320°С, особенно, от 180 до 290°С. Специалист в данной области техники легко сможет установить приемлемую температуру путем мониторинга реакции реагирующих веществ при постепенно возрастающих температурах, определяя при этом минимальную температуру реакции, при которой реакция протекает с достаточной скоростью. Для этой цели можно, например, осаждать наночастицы из образцов (проб) реакционной среды, что позволит исследовать рост частиц при увеличении продолжительности реакции.
Аналогичным образом можно установить приемлемое время реакции и предпочтительный интервал от 10 мин до 48 час, особенно от 30 мин до 20 час.
После завершения реакции реакционную смесь можно охлаждать до комнатной температуры. Если наночастицы в ходе реакции или после охлаждения осели все еще не полностью, то можно добавить метанол к реакционной среде или наоборот, для того чтобы получить максимальный выход.
Вне связи с теорией, считается, что агент, образующий комплекс с металлом, используемый в “органическом синтезе”, координируется с атомами металла на поверхности образованных наночастиц и ограничивает этим их рост после того, как исходные вещества прореагировали. Как полагают, указанный агент, образующий комплекс с металлом, остается на границе с поверхностью частицы и таким образом предотвращает или снижает процессы агломерации и обмена между частицами, подобные созреванию Оствальда. Таким образом, органический синтез приводит к довольно маленьким частицам, со средним диаметром, измеренным по самой большой оси, составляющим, предпочтительно, 1-10 нм, особенно, 2-8 нм, например, 4-6 нм при узких распределениях по размерам (стандартное отклонение <30%, в частности, <10%). Агент, образующий комплекс с металлом, характеризуется наличием полярной группы, способной координироваться с ионом металла и по меньшей мере еще с одним фрагментом молекулы (менее полярным, предпочтительно, гидрофобным), например, с алифатическим, ароматическим/алифатическим, или чисто ароматическим фрагментом молекулы, содержащим предпочтительно 4-20, в частности, 6-14 атомов углерода.
Агент, образующий комплекс с металлом, представляет собой предпочтительно фосфорорганическое соединение или моно- или двузамещенный амин.
Из последних наиболее предпочтительными вариантами являются моно- или диалкиламины, алкильная группа у которых имеет предпочтительно от 4 до 20, в частности, от 6 до 14 атомов углерода, например, додециламин или бис(этилгексил)амин.
Что касается фосфорорганических соединений, то предпочтительно использовать по меньшей мере одно из следующих веществ:
a) эфиры фосфиновой кислоты
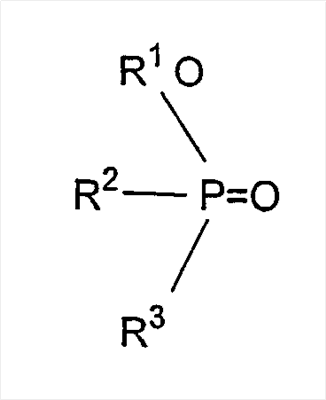
b) диэфиры фосфиновой кислоты
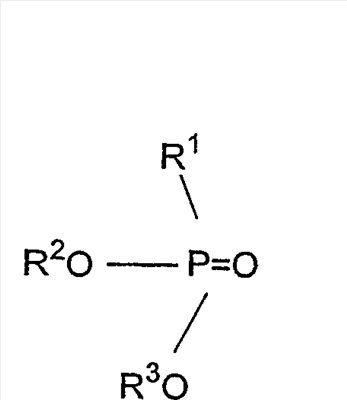
c) триэфиры фосфорной кислоты, наиболее предпочтительны такие триалкилфосфаты, как трибутилфосфат или три(этилгексил)фосфат,
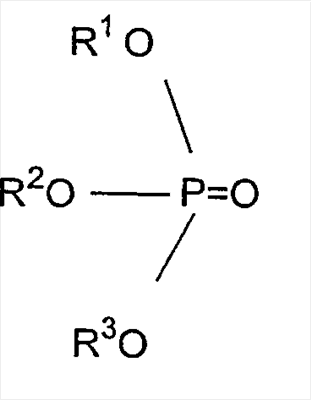
d) триалкилфосфины, такие как триоктилфосфин (ТОР),
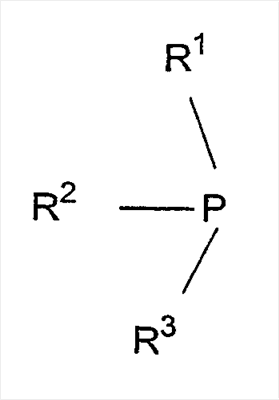
или
e) окиси триалкилфосфина, такие как окись триоктилфосфина (ТОРО)
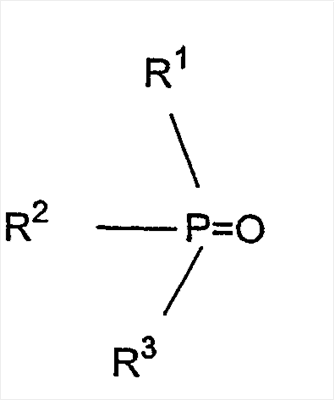
в которых R1, R2 и R3 выбраны независимо из разветвленных или неразветвленных алифатических (предпочтительно, алкильных), алифатических/ароматических или ароматических групп, содержащих от 4 до 20, более предпочтительно, от 4 до 14, в частности, от 4 до 10 атомов углерода. В качестве примеров ароматических остатков можно привести фенил, а алифатических/ароматических остатков – толил, ксилил или бензил.
Использование фосфорорганических соединений (a)-(c) и (e), в особенности, (a)-(c), особенно предпочтительно.
Агент, образующий комплекс с металлом, может быть только растворителем в органической реакционной среде. Предпочтительно использовать его в количестве по меньшей мере 10 молей, основываясь на молярном количестве атомов(атома) металла, используемых как источник металла, если он является единственным растворителем. Предпочтительный верхний предел составляет приблизительно 1000 моль.
В зависимости от того, какой агент, образующий комплекс с металлом, выбран и особенно в зависимости от длины гидрофобного фрагмента молекулы, использование больших количеств может оказаться неприемлемым, поскольку это может мешать полному осаждению получаемых наночастиц.
Поэтому предпочтительным является использование дополнительно “по меньшей мере, одного дополнительного растворителя”. В этом варианте осуществления агент, образующий комплекс с металлом (“первый растворитель”), использован предпочтительно в молярном количестве менее 10 моль, более предпочтительно, 0,9-6 моль из расчета на один моль ионов металла (использованных как источник металла). Количество “дополнительного растворителя (растворителей)” составляет предпочтительно 5-100 моль из расчета на один моль атомов металла (использованных как источник металла).
“Дополнительный растворитель (растворители)” должны смешиваться с агентом, образующим комплекс с металлом, и иметь температуру кипения выше минимальной температуры реакции получения, предпочтительно, температуру кипения выше 150°С, более предпочтительно, выше 180°С, наиболее предпочтительно, выше 210°С. Температура кипения выше 400°С может оказаться нежелательной.
“Дополнительный растворитель (растворители)” может быть на углеводородной основе или содержать по меньшей мере одну полярную группу. Использование последнего предпочтительно, когда в исходных для соли металла веществах присутствует кристаллизационная вода и указанную воду следует замещать растворителем, который способен к координации с металлом.
“Дополнительный растворитель (растворители)” выбирают предпочтительно из следующих:
– растворители, имеющие по меньшей мере одну функциональную простую эфирную группу; в частности, диалкиловые эфиры, имеющие от 5 до 10 атомов углерода на алкильную группу, такие как дипентиловый эфир, дигексиловый эфир, дигептиловый эфир, диоктиловый эфир или диизоамиловый эфир; диариловый эфир или диаралкиловый эфир, имеющий в сумме от 12 до 18 атомов углерода, например, как дифениловый эфир или дибензиловый эфир; или диалкиловый эфир моно- или полиэтиленгликоля (PEG) (в котором каждая алкильная группа содержит предпочтительно от 1 до 4 атомов углерода, а среднее количество PEG-звеньев, предпочтительно составляет до 10), например, как дибутиловый эфир диэтиленгликоля, дибутиловый эфир триэтиленгликоля и/или диметиловый эфир тетраэтиленгликоля;
– разветвленные или неразветвленные алканы, имеющие, предпочтительно, от 10 до 18 атомов углерода, в частности, 12-16 атомов углерода, как, например, додекан или гексадекан; и/или
– органическое основание с высокой точкой кипения, предпочтительно, N-содержащее алифатическое основание, наиболее предпочтительно, трехзамещенный амин, в частности, триалкиламиновые соединения, содержащие от 5 до 10 атомов углерода на алкильную группу, как, например, триоктиламин или три(2-этилгексил)амин или N-содержащее ароматическое основание, содержащее, предпочтительно, от 3 до 20 атомов углерода, как, например, имидазол.
Эти растворители можно также использовать в сочетании. Органическое высококипящее основание может служить не только растворителем, но также и как акцептор кислоты. Например, в случаях, когда кислота, например, фосфорная кислота, используется в качестве ионного источника, то предпочтительно использовать основание в приблизительно эквимолярном количестве (например, приблизительно 0,6-1,4 моль) относительно атомов водорода в кислоте.
“Источник катиона” может быть выбран из любой приемлемой (в достаточной степени реактивной) соли металла и предпочтительно представляет хлорид металла, алкоголят металла (у которого число углеродных атомов, предпочтительно, составляет 1-6 атомов, в частности, 1-4 углеродных атома), нитрат металла или ацетат металла. Особенно предпочтительно использовать хлориды металлов. Можно использовать также соли металлов в форме гидратов. Однако, предпочтительно, до реакции удалять кристаллизационную воду.
“Источник анионов” предпочтительно выбирать из следующих веществ:
a) серная кислота, фосфорная кислота или HF;
b) фосфатные, сульфатные или фторидные соли, растворимые или по крайней мере диспергируемые в реакционной смеси, в частности, соли, содержащие органические катионы, или соли щелочных металлов.
Что касается выбора b), то предпочтительно выбирать катион из основных N-содержащих алифатических, ароматических и алифатических/ароматических веществ, которые имеют, предпочтительно, от 4 до 30, предпочтительно, от 4 до 20 атомов углерода. В число приемлемых катионов входят, например, четвертичный аммоний или фосфоний, описанные выше, или протонированные ароматические основания, как, например, пиридин или коллидин. Для получения фосфатных наночастиц в качестве источника анионов можно использовать тетрабутиламмония дигидрофосфат, тетраметиламмония дигидрофосфат или триэтиламмония дигидрофосфат. Соответственно, сульфатные наночастицы можно получать из исходных веществ, таких как тетрабутиламмония гидросульфат, тетраметиламмония гидросульфат, бис-тетрабутиламмония сульфат или триэтиламмония гидросульфат. Для получения наночастиц с фторсодержащими анионами можно использовать триэтиамин-трисгидрофторид, тетрабутиламмония фторид, тетрабутиламмония гидродифторид, додециламингидрофторид или менее растворимые пиридингидрофторид или коллидингидрофторид.
Если ион металла (источник катионов) растворяется слишком медленно в органической среде, то предпочтительно растворить его в низшем спирте, предпочтительно, в метаноле, перед добавлением агента, образующего комплекс с металлом и реакционного растворителя. Метанол и кристаллизационную воду потом удаляют с помощью дистилляции и высушивания до того, как добавлять другие реагенты.
В соответствии со способом по изобретению наночастицы, получаемые по одному из указанных выше способов, обеспечиваются в виде дисперсной системы в органической среде (так называемая “первая смесь”).
Органическая среда основана предпочтительно на одном или более полярных растворителях, имеющих температуру кипения выше 120°С, в частности, выше 180°С, но ниже 400°С. Предпочтительно выбирать ее из “агентов, образующих комплекс с металлом”, в частности, указанных моно- или диалкиловых аминов, алкильная группа которых имеет 4-20 атомов С, фосфорорганических соединений, полиолов и сульфоксидов. Предпочтительно, органическая среда содержит агент, образующий комплекс с металлом, и, необязательно, “по крайней мере один дополнительный растворитель”, раскрытый в контексте органического синтеза.
Соответственно, возможно и предпочтительно использовать наночастицы, полученные по “органическому” способу или по “полиол- или сульфоксид-способу”, на первой стадии способа по изобретению без их выделения.
Следует подчеркнуть, что органическая среда выступает в качестве дисперсионной среды для ядер-наночастиц. Таким образом, благодаря свойству органической среды координироваться с атомом металла, наночастицы сохраняются в своем коллоидном (нерастворенном) состоянии до того, как на них может нарасти оболочка.
II.2. Вторая стадия способа
На второй стадии
– описанная выше первая смесь,
– источник анионов для формируемой оболочки, в частности, фосфатный, сульфатный или фторидный источник, и
– так называемая “вторая смесь”, содержащая формирующие оболочку ионы металла (и их противоионы), и органическое комплексообразующее вещество для указанных ионов металла
взаимодействуют при температуре 50-350°С до получения формирования оболочки вокруг указанных люминесцирующих наночастиц.
Как правило, предпочтительно, во избежание преждевременной реакции, поддерживать анионный источник отдельно от первой смеси.
Вторую стадию способа можно осуществлять в соответствии со следующими тремя вариантами осуществления (А), (В) и (С).
Вариант получения (А) включает следующие стадии:
получение первой смеси, содержащей наночастицы необязательно легированного люминесцирующего сульфата, фосфата или фторида металла в органической среде,
нагревание указанной первой смеси до температуры в пределах 50-350°С,
добавление, по каплям и отдельно, к указанной первой смеси при указанной температуре анионного источника для формируемой оболочки, и второй смеси, содержащей формирующие оболочку ионы металла и органическое комплексообразующее вещество для указанных ионов металла, и
взаимодействия полученной смеси при указанной температуре до формирования оболочки вокруг указанных люминесцирующих наночастиц.
Раздельное, но одновременное добавление анионного источника и второй смеси, например, посредством двух капельных воронок снижает концентрацию активных исходных веществ для оболочки и таким образом повышает селективность реакции путем уменьшения независимого роста частиц из исходных веществ для оболочки.
Вариант получения (В) включает следующие стадии:
получение первой смеси, содержащей наночастицы необязательно легированного люминесцирующего сульфата, фосфата или фторида металла в органической среде,
добавление формирующего оболочку анионного источника к указанной первой смеси,
нагревание полученной смеси до температуры в пределах 50-350°С,
добавление туда по каплям второй смеси, содержащей формирующие оболочку ионы металла и органическое комплексообразующее вещество для указанных ионов металла, и
взаимодействие полученной смеси при указанной температуре до формирования оболочек вокруг указанных люминесцирующих наночастиц.
По вариантам (А) и (В) получаются, как правило, более однородные частицы и, кроме того, имеется меньший процент независимо выращенных частиц из формирующих оболочку веществ.
Вариант получения (С) включает следующие стадии:
получение первой смеси, содержащей наночастицы необязательно легированного люминесцирующего сульфата, фосфата или фторида металла в органической среде,
объединение указанной первой смеси, анионного источника для формируемой оболочки, и второй смеси, содержащей ионы металла, формирующие оболочку, и органическое комплексообразующее вещество для указанных ионов металла, предпочтительно путем добавления указанной первой смеси и указанного анионного источника к указанной второй смеси, и
нагревание полученной смеси до температуры в пределах 50-350°С до формирования оболочки вокруг указанных люминесцирующих наночастиц.
Неожиданно было обнаружено, что постепенное, например, по каплям, добавление исходных веществ не является абсолютно необходимым. Хотя, в соответствии с вариантом (С), исходные вещества можно объединять путем смешивания целых порций, желаемый материал ядро/оболочка формируется высокой степенью селективности и малым независимым ростом частиц. Вариант получения (С), таким образом, является более простым в исполнении в сравнении с вариантами (А) и (В).
Если не оговорено иначе, то следующие предпочтительные варианты осуществления относятся ко всем трем вариантам (А), (В) и (С).
Как источник ионов металла можно использовать любую достаточно реактивную соль металла, предпочтительно, хлориды или алкоксиды ионов металла оболочки. Алкоксидная группа имеет, предпочтительно, от 1 до 4 углеродных атомов.
Любой приемлемый анионный источник можно использовать, пока он способен к формированию оболочки вокруг ядер частиц, полученных на первой стадии.
Приемлемые анионы, формирующие оболочку, включают, но не ограничиваются, фосфаты, галогенфосфаты, арсенаты, сульфаты, бораты, алюминаты, галлаты, силикаты, германаты, оксиды, ванадаты, ниобаты, танталаты, вольфраматы, молибдаты, алкалгалогенаты, другие галоиды, нитриды, сульфиды, селениды, сульфоселениды или оксисульфиды.
Предпочтительно использовать для формирования оболочки анионы, которые приемлемо реагируют в органической среде при сходных или идентичных условиях, как это описано в PCT/DE 01/03433/. В число примеров входят силикаты, бораты, арсенаты, сульфиды, сульфаты, фосфаты и фториды, в особенности, сульфаты, фосфаты и фториды. В данном документе раскрывается также, какой из анионных источников можно использовать для получения соответствующего вещества наночастиц.
Что касается приемлемого источника фосфата, сульфата и фторида, то дается ссылка также на источники анионов, описанные выше в связи с первой стадией способа по изобретению, в частности, источники, используемые при “полиол- или сульфоксид-способе” и/или при “органическом” синтезе.
Источник анионов предпочтительно добавлять в форме тонкодисперсной системы или в виде раствора в по крайней мере одном из растворителей, описанных для “полиол- или сульфоксид-способа” или для “органического” синтеза.
Источник анионов, в частности, фосфатный, сульфатный или фторидный, используется предпочтительно в количестве 0,75-3 моль, в частности, 0,75-2, относительно стехиометрически требуемого молярного количества для взаимодействия со всеми добавляемыми атомами, формирующими оболочку. Для двойных солей (АВ) отношение В (анион) к А (металл) будет таким образом колебаться от 0,75:1 до 2:1.
Фосфатные и фторидные источники, такие как фосфорная кислота или HF, используются предпочтительно в избыточных количествах при “органическом” способе получения частиц ядра или ядро/оболочка, получаемых из фосфатов или фторидов. Избыточное молярное количество предпочтительно составляет по меньшей мере 1,05 моль, более предпочтительно, 1,1-2 моль, в особенности, 1,2-1,6 моль относительно стехиометрически требуемого молярного количества.
Подобным же образом предпочтительно использовать в избыточном количестве источники сульфатов, такие как (гидро)сульфатные соли четвертичного аммония при получении сульфатных ядер или частиц ядро/оболочка по способу “полиол- или сульфоксид-синтеза”. Избыточное молярное количество составляет, предпочтительно, по меньшей мере 1,05 моль, более предпочтительно, 1,1-3 моль, в частности, 1,2-2 моль относительно стехиометрически требуемого молярного количества.
Органическое комплексообразующее вещество, входящее в состав второй смеси, также можно выбирать из числа органических комплексообразующих веществ, о которых говорилось выше в связи с органическим способом получения наночастиц или растворителей, описанных в разделе по “полиол- или сульфоксид-синтезу”.
Обычно желательно поддерживать эффективную концентрацию формирующих оболочку ионов на по возможности низком уровне. В соответствии с настоящим изобретением это достигается путем использования агента, образующего комплекс с металлом. Вне связи с теорией считается, что только очень малая концентрация реакционноспособных (не связанных в) ионов металла способствует росту оболочки по отношению к независимому образованию новых частиц.
В соответствии с предпочтительным вариантом осуществления органическая среда, используемая для первой смеси, и комплексообразователь, присутствующий во второй смеси, представляют собой одно и то же органическое полярное соединение, например, одно из указанных выше фосфорорганических соединений, моно-/двузамещенных аминов, полиолов или сульфоксидов.
Кроме того, предпочтительно также использовать вышеупомянутый “по меньшей мере один дополнительный растворитель” в той же самой пропорции к органическому комплексообразующему веществу. Это дает возможность использования агента, образующего комплекс с металлом в меньших количествах, как если бы он был единственным растворителем. В данном случае молярное соотношение агента, образующего комплекс с металлом и формирующих оболочку ионов металла, вновь составляет предпочтительно от 0,9:1 до 6:1.
Если источник анионов для вещества оболочки содержит кислотные водородные атомы, то предпочтительно использовать указанные выше основания. Вышеописанное высококипящее органическое основание (например, триалкиламин) предпочтительно использовать, например, как кислотный акцептор для анионных источников, подобных фосфорной кислоте или HF при условиях, описанных выше. В соответствии со способом (А) или (В), предпочтительно добавлять основание как ингредиент “второй смеси”, содержащей источник металла и комплексообразующее вещество.
Специалист в данной области легко определит общее количество растворителя (растворителей), включая агент, образующий комплекс с металлом, так как обычно предпочтительным является гомогенное растворение или диспергирование всех исходных веществ. При способе (А) и (В) предпочтительным является использование растворителей для растворения источника анионов и источника металла (вторая смесь) в приблизительно одинаковых количествах.
В целом реакция может протекать в таких же или в схожих условиях, как описаны выше в разделе II.1 в связи с “полиол- или сульфоксид-синтезом” или с “органическим” синтезом, если не делается других оговорок. Это относится также к использованию защитного инертного газа и сушки реагирующих веществ.
Количество ядер наночастиц, которое должно быть объединено с оставшимися исходными веществами, специально не ограничивается и определяется, в первую очередь, желаемой толщиной оболочки.
В соответствии со способом по настоящему изобретению, реакционная среда нагревается до температуры в пределах 50-350°С, в частности, 120-320°С до формирования оболочки вокруг люминесцирующих ядер наночастиц, полученных на первой стадии способа.
Предпочтительно осуществлять реакцию при температуре в пределах 160-240°С, в частности, 180-220°С для фторидов и фосфатов и 160-180°С для сульфатов. При получении сульфатных оболочек в глицерине допустимы также значительно более низкие температуры (например, 50-100°С). Специалисту в данной области техники легко установить приемлемую температуру путем мониторинга роста оболочки при постепенно возрастающей температуре, определяя при этом минимальную температуру синтеза, при которой реакция протекает с достаточной скоростью, но без нежелательных побочных реакций, подобных образованию новых частиц из исходных веществ, предназначенных для оболочек.
При таких вариантах получения (А) и (В), где исходные вещества добавляются по каплям, время добавления изменяется предпочтительно в пределах 0,5-10 час, в частности, 1-5 час.
Предпочтительная продолжительность реакции колеблется в пределах от 30 мин до 48 час, в частности, от 1 час до 20 час, особенно от 1,5 до 16 час. Опять-таки, контролирование реакции, например, путем осаждения наночастиц из проб, которые берутся из реакционной среды, и путем исследования распределения частиц по размерам на ТЕМ-микрографах, дает возможность установить приемлемую продолжительность реакции. Прекращать реакцию следует, например, с помощью охлаждения, сразу же, как только обнаружится Оствальдово созревание, т.е. когда начинается рост более крупных частиц за счет частиц меньшего размера.
После завершения реакции реакционная среда охлаждается до комнатной температуры. Это уже способствует осаждению полученных наночастиц ядро/оболочка. Если осаждение является неполным, то добавление осаждающих растворителей (например, метанола) к реакционной среде, или наоборот, позволяет полностью выделить продукт реакции. Альтернативно, возможна отгонка избытка органических растворителей, в их числе, органического комплексообразующего вещества, или проведение ультрафильтрации через мембраны, предпочтительные размеры пор которых соответствуют Дальтоновым значениям порядка от 5000 до 10000. Эти значения соответствуют отсечке приблизительно 3 нм, которые в большинстве случаев оказываются достаточно большими для того, чтобы пропустить растворитель, и в то же самое время достаточно малыми, чтобы предотвратить прохождение и потерю наночастиц. Обычно для обмена растворителей в соответствующих ячейках ультрафильтрации необходимо давление от 2 до 5 бар.
Кроме того, предпочтительно промывать полученные наночастицы, например, метаном, этаном или изопропаном.
Действительное наличие роста оболочек можно подтвердить способом, приводимым ниже.
Один способ заключается в постоянном контролировании реакции путем осаждения малых проб и анализа распределения частиц по размеру, например, на ТЕМ-микрографах. Полученные таким образом образцы покажут, происходит ли наращивание оболочек в течение всего реакционного периода или может наблюдаться также независимое образование более мелких частиц. С помощью EDX-анализа (анализ рентгеновского спектра рассеивания энергии) можно проверить общий состав наночастиц. С помощью XPS (рентгеноэлектронной)-спектроскопии возможно получить дополнительную информацию относительно распределения состава от внешних до внутренних частей частиц, если XPS выполняют с различными энергиями возбуждения. Более того, квантовые выходы частиц ядро/оболочка можно с легкостью отличить от ядер-наночастиц, используемых в реакции.
Если оболочка нелюминесцирующего вещества наращивается вокруг необязательно легированного люминесцирующего ядра наночастицы, то квантовый выход последних будет увеличиваться. Это следует из Фиг.1, отражающей спектр флуоресценции однородных наночастиц CePO4:Tb (сплошная линия) и частиц ядро/оболочка по настоящему изобретению (пунктирная линия), где оболочка LaPO4 была выращена вокруг ядер CePO4:Tb. Оба спектра измеряли при одинаковой оптической плотности (10-3 мас.%) в изопропаноле (exc=274 нм).
Как видно из Фиг.1, интенсивность флуоресценции ядер CePO4:Tb значительно увеличилась за счет покрытия оболочкой из LaPO4.
III. Использование частиц ядро/оболочка
Частицы ядро/оболочка по изобретению могут использоваться в различных промышленных устройствах и продуктах, где требуется фотолюминесценция.
Частицы ядро/оболочка такого предназначения обычно получают в форме дисперсии в жидкой или твердой среде.
Приемлемые жидкостные среды содержат, например, органическую или водную дисперсионную среду, состав для покрытия, краску или краситель, полимерную композицию или аэрозоль. Приемлемые органические дисперсионные среды включают, но не ограничиваются ими, толуол, ксилол, CHCl3 или CH2Cl2.
Получение с N- или P-содержащей средой/комплексообразующими веществами в соответствии с приведенным выше описанием обеспечивает высокая степень дисперсности в органической среде частиц ядро/оболочка по настоящему изобретению.
При получении водной дисперсной системы может потребоваться последующая обработка, при которой остатки органических веществ, используемых для получения, замещаются растворителями, имеющими одну функциональную связь с поверхностью частиц и один гидрофильный фрагмент молекулы, обеспечивающий необходимую совместимость в воде, необязательно в сочетании с водосмешиваемыми растворителями.
Твердофазную дисперсионную среду можно выбирать из покрытия, краски или красителя, полимерной композиции, в частности, полимерной пленки.
Наночастицы как таковые или, обычно, жидкофазная или твердофазная среда, их содержащая, могут использоваться, например, в устройствах для генерации света, печатающих и маркировальных изделиях и средствах.
Такие применения включают, например, светоизлучающие диоды, дисплеи, оптоэлектронные устройства, например, усилители нм-диапазона и источники света в лазерах с нулевым порогом генерации. Их можно использовать также как печатную краску в печатающих устройствах, что представляет особый интерес для маркировки в целях безопасности документов или бумажных денег.
IV. ПРИМЕРЫ
Пример 1: Ядра наночастиц CePO4:Tb, имеющие оболочку из LaPO4.
В 100 мл круглодонной колбе, снабженной высокоэффективным обратным охладителем, датчиком температуры и нагревательной рубашкой, растворяли в примерно 10 мл этанола 2,79 г (7,5 ммоль) CeCl3×7H2O и 0,934 г (2,5 ммоль) TbCl3×6H2O с последующим добавлением к раствору 10,9 мл (40 ммоль) трибутилфосфата. После этого удаляли метанол в вакууме при температуре 20-30°С. Затем добавляли 30 мл дифенилового эфира (дифенилоксида) и отгоняли оставшиеся летучие компоненты, главным образом кристаллизационную воду в вакууме при температуре 80°С.
Во второй колбе растворяли сухую ортофосфорную кислоту (20 ммоль) в 10 мл диметилового эфира тетраэтиленгликоля.
10,2 мл (30 ммоль) тригексиламина и 7,0 мл (14 ммоль фосфорной кислоты) раствора ортофосфорной кислоты/диметилового эфира тетраэтиленгликоля добавляли к указанному выше раствору CeCl3/TbCl3 с последующим нагреванием с обратным холодильником до 200°С в течение 24 час. По истечении этого времени получали прозрачную дисперсию (“первая смесь”) наночастиц CePO4:Tb.
Во второй 100 мл круглодонной колбе, снабженной высокоэффективным обратным охладителем, датчиком температуры и нагревательной рубашкой, растворяли приблизительно в 10 мл метанола 3,71 г LaCl3×7H2O (10 ммоль) с последующим добавлением к раствору 10,9 мл трибутилфосфата (40 ммоль). После этого удаляли метанол при комнатной температуре в вакууме. Затем к полученному раствору добавляли 30 мл дифенилового эфира и удаляли оставшиеся летучие компоненты, главным образом кристаллизационную воду при температуре около 80°С в вакууме для получения так называемой “второй смеси”.
К полученному раствору LaCl3 (“вторая смесь”) добавляли 13,1 мл (30 ммоль) тригексиламина, 7 мл (14 ммоль фосфорной кислоты) раствора ортофосфорной кислоты/диметилового эфира тетраэтиленгликоля и 14,5 мл дисперсной CePO4:Tb (охлажденной до 20-30°С), которые затем нагревали до 200°С в течение не менее 16 час.
Для полной выработки реакционной смеси вначале отгоняли дифениловый эфир в вакууме при 80-150°С с последующим добавлением к остатку приблизительно 200 мл этанола, чтобы осадить наночастицы. Осадок центрифугировали (5500 об/мин), промывали метанолом и сушили.
При этом получались частицы ядро/оболочка со средним диаметром по большей оси около 7 нм, как было установлено по ТЕМ-микрографам.
Их спектр фотолюминесценции показан на Фиг.1. Эти частицы давали очень интенсивную люминесценцию зеленого оттенка. На основании спектральных показателей подсчитали, что квантовый выход составлял 70%.
Кроме того, для полученных частиц ядро/оболочка выполняли следующий спектроскопический анализ. Для чего помещали частицы на углеродную пленку с отверстиями и исследовали под микроскопом Philipps CM300UT.
a) EELS (спектроскопия энергетических потерь электронов) показала, что средний химический состав катионов представлен Ce/La=0,34±0,05, Tb/La=0,12±0,03, из чего следует, что La/Ce=3,0±0,4 и Ce/Tb=2,8±0,8, последние значения приблизительно соответствуют молярному соотношению используемых Ce/Tb (3,14/1).
b) HREM (электронная микроскопия высокого разрешения) подтвердила кристалличность полученных частиц ядро/оболочка.
c) Кроме того, было получено Хельфельдово (Hellfeld) изображение, сделанное не совсем в фокусе при скорости сканирования 0,48 нм/тчк отражения, для того чтобы охватить также более мелкие частицы. Анализ отображения показал, что основной класс частиц характеризуется с точки зрения объема диаметрами от 5 до 9 нм. Шесть таких частиц подвергли исследованию EFTEM (просвечивающая электронная микроскопия с фильтрацией энергий) конкретно так называемым “методом отображения спектра”, разработанным для целей количественного анализа в Германии в Бонне в “Landeszentrum für Hochleistungsspektroskopie, Institut für Anorganische Chemie”. Для этой цели шесть кристаллических частиц помещали в центре (CCD) камеры (прибор с зарядовой связью) с очень сильным увеличением позади фильтра отображения энергий. Затем вставляли самый маленький экран объектива (4,6 мрад) и самый большой экран на входе (3 мм) и использовали энергетический фильтр в его спектроскопическом режиме. При этом интенсивность прохождения входного экрана полностью, линия за линией, отображалась на детекторе. Из-за хроматической аберрации линзы этот процесс давал отображение высокой четкости (менее нм) только для диапазона примерно ±40 эВ, так что в фокусе его находился LaM5,4, а по краям CeM5,4 при 832, 849, 884 и 902 эВ. При выборочном первичном увеличении 99К диаметр экрана на входе был всегда равен 11,2 нм.
Фиг.2 показывает (D) Хельфельдово отображение (при помощи входного экрана) одной наночастицы CePO4:Tb, окруженной оболочкой LaPO4 (диаметр около 7 нм), (Е) спектральное изображение при потере энергии 860 эВ, а также профили поверхности частиц (А, С), центра (В). Профили (А, В и С) показывают пики LaM5,4 и CeM5,4, относительная интенсивность которых приблизительно соответствует локальной композиции.
Различные профили подтверждают существование структуры ядро/оболочка с высоким содержанием Ce в ядре и высоким содержанием La в оболочке. У шести выбранных частиц средний диаметр равнялся 7,5±1,9 нм, состоящий из 4,0±1,1 нм диаметра ядра с высоким содержанием Ce и 1,9±0,7 нм толщины оболочки с высоким содержанием La (Tb при данном анализе не исследовался).
Пример 2: Ядра наночастицы BaSO4:Eu (II) с оболочкой из BaSO4.
В 50 мл круглодонной колбе, снабженной высокоэффективным обратным охладителем, датчиком температуры и нагревательной рубашкой, растворяли в смеси метанол/вода (5 мл, 50/50 об./об.) 540 мг (2,2 ммоль) BaCl2×2H2O. Затем добавляли 10 мл DMSO и 540 мг имидазола (8 ммоль). После установления вакуума в круглодонной колбе сначала удаляли метанол и воду при комнатной температуре (от 1 до 2 час), а затем при 35°С (2 час).
В другой колбе растворяли 1,32 г (3,9 ммоль) гидросульфата тетрабутиламмония в 10 мл DMSO.
К указанному выше раствору BaCl2 добавляли 0,401 г (1,8 ммоль) EuCl2 c последующим добавлением вышеуказанного раствора гидросульфата тетрабутиламмония в DMSO. Реакционную смесь нагревали до 170°С не менее 30 мин, что приводило к получению прозрачной дисперсии (“первая смесь”) ядер наночастиц BaSO4:Eu (II).
Во второй 100 мл круглодонной колбе, снабженной высокоэффективным обратным охладителем, датчиком температуры и нагревательной рубашкой, растворяли 977 мг (4 ммоль) BaCl2×2H2O в смеси метанол/вода (8 мл, 50/50 об./об.) с последующим добавлением 10 мл диметилсульфоксида (DMSO) и 545 мл (8 ммоль) имидазола. После установления вакуума в круглодонной колбе сначала удаляли метанол и воду при комнатной температуре (от 1 до 2 час), а затем при 35°С (2 час). При атмосфере азота и при перемешивании охлажденную дисперсную систему BaSO4:Eu и раствор гидросульфата тетрабутиламмония (2,64 г, 7,8 ммоль) в 10 мл DMSO добавляли к полученному ранее раствору BaCl2 (“вторая смесь”) с последующим нагреванием реакционной смеси в течение 1 час выше 170°С. После охлаждения до комнатной температуры реакционную смесь выливали в метанол. Полученный таким образом осадок центрифугировали (при 5500 об./мин), промывали метанолом и сушили.
Пример 3: Ядра наночастицы NdPO4 с оболочкой из GdPO4.
В 100 мл круглодонной колбе, снабженной высокоэффективным обратным охладителем, датчиком температуры и нагревательной рубашкой, растворяли 3,0 г (8,4 ммоль) NdCl3×7H2O в приблизительно 6 мл метанола с последующим добавлением к полученной в результате смеси 37 мл трис-2-этилгексилфосфата (TEHP). После установления вакуума в круглодонной колбе сначала удаляли метанол и кристаллизационную воду при комнатной температуре (от 1 до 2 час), а затем при 50°С (несколько часов).
Во второй колбе растворяли сухую ортофосфорную кислоту (20 ммоль) в 5 мл диметилового эфира тетраэтиленгликоля.
При атмосфере азота и при 50°С добавляли 12,0 мл (27,4 ммоль) триоктиламина и 2,1 мл смеси ортофосфорной кислоты/диметилового эфира тетраэтиленгликоля к раствору NdCl3 в TEHP. После этого смесь нагревали в течение 16 час до 200°С. По истечении этого времени получали прозрачную дисперсию (“первая смесь”) частиц NdPO4.
Во второй 100 мл круглодонной колбе, снабженной высокоэффективным обратным охладителем, датчиком температуры и нагревательной рубашкой, растворяли 1,45 г (6,6 ммоль) GdCl3×6H2O приблизительно в 10 мл метанола с последующим добавлением к раствору 17,6 мл трис-2-этилгексилфосфата (TEHP). После установления вакуума в этой круглодонной колбе удаляли метанол и кристаллизационную воду вначале при комнатной температуре (1-2 час), а затем при 50°С (несколько часов). Под слоем азота и при 50°С добавляли 5,3 мл (12,1 ммоль) триоктиламина и 0,99 мл (3,96 ммоль фосфорной кислоты) раствора ортофосфорной кислоты/диметилового эфира тетраэтиленгликоля, а также все количество диспергированного NdPO4 (охлажденного до примерно 20-30°С) к раствору GdCl3 (“вторая смесь”) с последующим нагреванием до 200°С в течение 16 час. После охлаждения до комнатной температуры реакционную смесь выливали в метанол (300 мл), для того чтобы осадить наночастицы ядро/оболочка. Осадок центрифугировали (при 5500 об./мин) и полученные в результате частицы промывали дважды метанолом и сушили.
Пример 4: Ядра наночастицы CePO4:Nd с оболочкой из LaPO4.
Сначала получали примерно 2 М раствор фосфорной кислоты в дигексиловом эфире из примерно 9,80 г сухой фосфорной кислоты и 40 мл дигексилового эфира в 100 мл круглодонной колбе, а затем наливали в мерную колбу до 50 мл. Если использовалась влагосодержащая H3PO4 (примерно 10-11 г), то влагу следовало удалять, используя роторный испаритель.
Исходный раствор для ядер:
3,61 г CeCl3×7H2O (9,7 ммоль) и 0,108 г NdCl3×6H2O (0,3 ммоль) растворяли примерно в 10 мл метанола р.а. в 100 мл трехгорлой колбе, добавляли в нее 10,98 мл (40 ммоль) трибутилфосфата и отгоняли метанол, используя роторный испаритель (при самое большее 40°С и 50 мбар). При помощи масляного насоса отгоняли кристаллизационную воду при 50°С и наконец поднимали температуру до 80°С. После охлаждения смеси до 50°С добавляли 30 мл дифенилового эфира и снова отгоняли воду масляным насосом (до тех пор пока не исчезали пузырьки).
10,87 мл этого раствора (что соответствовало 2,5 ммоль атомов металла) переливали в 250 мл четырехгорлую колбу (с холодильником и капельной воронкой).
Исходный раствор для оболочки:
5,57 г LaCl3×7H2O (15 ммоль) растворяли примерно в 15 мл метанола р.а. в 100 мл трехгорлой колбе, добавляли туда 16,36 мл (60 ммоль) трибутилфосфата и отгоняли метанол, используя роторный испаритель (при самое большее 40°С и 50 мбар). При помощи масляного насоса отгоняли кристаллизационную воду при 50°С и под конец поднимали температуру до 80°С. После охлаждения смеси до 50°С добавляли туда 45 мл дифенилового эфира и заново отгоняли воду масляным насосом до тех пор, пока не переставали образовываться пузырьки.
35,52 мл этого исходного раствора загружали в капельную воронку, подсоединенную к четырехгорлой колбе.
Получение ядерных частиц:
При 50°С добавляли 2,54 мл (7,5 ммоль) тригексиламина и такое количество полученного выше раствора фосфорной кислоты, которое соответствует 3,5 ммоль фосфорной кислоты, к раствору в четырехгорлой колбе и раствор снова эвакулировали, продували азотом и нагревали до 200°С по меньшей мере в течение одного часа (вплоть до 16 час).
Получение оболочки:
К раствору в четырехгорлой колбе добавляли раствор фосфорной кислоты в количестве, соответствующем 9,5 ммоль фосфорной кислоты. Содержащий LaCl3 раствор в капельной воронке добавляли по каплям в течение 1,5-2 час к раствору, нагретому до 200°С, с последующим перемешиванием смеси при 200°С в течение 16 час.
Смешивание составных частей:
После охлаждения реакционной смеси ниже 50°С полученный раствор разбавляли метанолом, для того чтобы осадить полученные частицы ядро/оболочка, которые затем можно было очищать далее путем многократного ультрафильтрования в смесительной камере (5000 D мембрана) с использованием метанола.
Формула изобретения
1. Люминесцирующие наночастицы, содержащие
a) ядро, полученное из люминесцирующей соли металла, выбранной из фосфатов, сульфатов или фторидов, окруженное
b) оболочкой, полученной из соли или оксида металла, способных предотвращать или уменьшать перенос энергии от ядра после его электронного возбуждения к поверхности наночастицы.
2. Люминесцирующие наночастицы по п.1, где соль ядра и оболочки содержат один и тот же анион, при этом указанный анион выбран из фосфатов, сульфатов или фторидов.
3. Люминесцирующие наночастицы по п.1, имеющие средний диаметр, основанный на их самой длинной оси, менее 30 нм.
4. Люминесцирующие наночастицы по п.1, где средняя толщина оболочки не превышает средний диаметр ядра.
5. Люминесцирующие наночастицы по п.1, где ядро получают из предпочтительно легированного люминесцирующего сульфата, фосфата или фторида металла, и оболочка состоит из нелюминесцирующего вещества.
6. Люминесцирующие наночастицы по п.5, где ядро получают из сульфата, фосфата или фторида легированного металла-хозяина, где металл-хозяин выбран из группы 2 (щелочноземельные металлы), группы 3 (Sc, Y или La), группы 13 (например, Al, Ga, In или Tl) или Zn, и легирующей добавкой является по меньшей мере один лантаноидный металл, выбранный из Се, Pr, Nd, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm или Yb или переходных металлов, выбранных из Cr и Mn.
7. Люминесцирующие наночастицы по п.5, где ядро получают из сульфата, фосфата или фторида легированного металла-хозяина, где металл-хозяин и легирующую добавку выбирают из Се, Pr, Nd, Sm, Eu, Gd, Tb, Dy, Ho, Er, Tm или Yb.
8. Люминесцирующие наночастицы по п.7, где ядро состоит из СеРО4:Tb или CePO4:Nd, и оболочка состоит из LaPO4.
9. Люминесцирующие наночастицы по любому из пп.1-4, где ядро состоит из люминесцирующего сульфата, фосфата или фторида лантаноидного металла, и оболочка состоит из соли или оксида лантаноидного металла, отличающихся от вещества ядра и предотвращающих или снижающих передачу энергии от ядра после его электронного возбуждения к поверхности наночастицы.
10. Люминесцирующие наночастицы по п.9, где ядро предпочтительно состоит из сульфата, фосфата или фторида Nd, и оболочка состоит из соли или оксида Gd.
11. Способ получения наночастиц по любому из пп.1-10, включающий следующие стадии: получение первой смеси, содержащей наночастицы необязательно легированного люминесцирующего сульфата, фосфата или фторида металла в органической среде, взаимодействие указанной первой смеси, источника анионов для формируемой оболочки, и второй смеси, содержащей формирующие оболочку ионы металла и органический комплексообразователь для указанных ионов металла, при температуре 50-350°С до формирования оболочки вокруг указанных люминесцирующих наночастиц.
12. Способ получения (А) по п.11, включающий стадии: получение первой смеси, содержащей наночастицы необязательно легированного люминесцирующего сульфата, фосфата или фторида металла в органической среде, нагревание указанной первой смеси до температуры 50-350°С, добавление к этой первой смеси при указанной температуре по каплям и по отдельности источника анионов для формируемой оболочки, и второй смеси, содержащей формирующие оболочку ионы металла и органический комплексообразователь для указанных ионов металла, и взаимодействие полученной в результате смеси при указанной температуре до формирования оболочки вокруг указанных люминесцирующих наночастиц.
13. Способ получения (В) по п.11, включающий стадии: получение первой смеси, содержащей наночастицы необязательно легированного люминесцирующего сульфата, фосфата или фторида металла в органической среде, добавление источника анионов к указанной первой смеси, нагревание полученной в результате смеси до температуры 50-350°С, добавление туда второй смеси, содержащей формирующие оболочку ионы металла и органический комплексообразователь для указанных ионов металла, и взаимодействие полученной в результате смеси при указанной температуре до формирования оболочки вокруг указанных люминесцирующих наночастиц.
14. Способ получения (С) по п.11, включающий стадии: получение первой смеси, содержащей наночастицы необязательно легированного люминесцирующего сульфата, фосфата или фторида металла в органической среде, объединение указанной первой смеси, источника анионов для формируемой оболочки и второй смеси, содержащей формирующие оболочку ионы металла и органический комплексообразователь для указанных ионов металла, и нагревание результирующей смеси до температуры 50-350°С до формирования оболочки вокруг указанных люминесцирующих наночастиц.
15. Способ по любому из пп.11-14, где органическая среда, присутствующая в первой смеси, идентична органическому комплексообразователю, присутствующему во второй смеси.
16. Способ по любому из пп.11-14, где органическая среда и комплексообразователь выбраны из моно- или диалкиламинов, алкильная группа которых содержит от 4 до 20 атомов С, фосфорорганических соединений, полиолов и сульфоксидов.
17. Способ по любому из пп.11-14, включающий стадии получения ядер наночастиц в указанной органической среде с последующим взаимодействием этих ядер без предварительного выделения.
18. Способ по любому из пп.11-14, где источник анионов, в частности фосфатный, сульфатный или фторидный источник, используют в избыточных молярных количествах относительно стехиометрически требуемого количества для взаимодействия с доступными атомами металла, формирующими оболочку.
19. Жидкая или твердая среда, содержащая наночастицы по любому из пп.1-10.
20. Жидкая среда по п.19, выбираемая из органической или водной дисперсионной среды, композиции для покрытия, краски или красителя, полимерной композиции или аэрозоля.
21. Твердая среда по п.19, выбираемая из покрытия, краски или красителя, полимерной композиции, в частности полимерной пленки.
22. Применение наночастиц по любому из пп.1-10 или среды по пп.19-21 для устройств и материалов для генерации света, изделий и материалов для печати или маркировки.
РИСУНКИ
|
|