|
|
(21), (22) Заявка: 2007126506/04, 11.07.2007
(24) Дата начала отсчета срока действия патента:
11.07.2007
(46) Опубликовано: 10.01.2009
(56) Список документов, цитированных в отчете о
поиске:
RU 2241541 C1, 10.12.2004. RU 2103057 C1, 27.01.1998. SU 803967 A, 15.02.1981. RU 2152255 С1, 10.07.2000. DE 2161623 В1, 14.06.1973. WO 9724184 А, 10.07.1997.
Адрес для переписки:
690022, г.Владивосток, 22, пр-кт 100-лет Владивостоку, 159, Институт химии ДВО РАН, отдел интеллектуальной собственности, О.Л. Ляховской
|
(72) Автор(ы):
Руднев Владимир Сергеевич (RU),
Тырина Лариса Михайловна (RU),
Лукьянчук Ирина Викторовна (RU)
(73) Патентообладатель(и):
Институт химии Дальневосточного отделения Российской академии наук (статус государственного учреждения) (Институт химии ДВО РАН) (RU)
|
(54) СПОСОБ ПОЛУЧЕНИЯ НИКЕЛЬ-МЕДНОГО ОКСИДНОГО КАТАЛИЗАТОРА
(57) Реферат:
Изобретение относится к получению никель-медных оксидных катализаторов на металлической подложке, которые могут быть использованы при конверсии СО в CO2 в высокотемпературных процессах очистки технологических и выхлопных газов, в частности в энергетике и автомобильной промышленности. Катализаторы на подложке, выполненной из алюминия или его сплава, получают плазменно-электрохимическим методом путем обработки подложки в щелочном электролите, содержащем ацетат никеля и ацетат меди и дополнительно включающем тринатрийфосфат, тетраборат и вольфрамат натрия при следующем соотношении компонентов, г/л: ацетат никеля Ni(СН3СОО)2·4Н2O-5-20; ацетат меди Cu(СН3СОО)2·Н2O-1,3-5,0; тринатрийфосфат Na3PO4·12H2O-20-30; тетраборат натрия Na2B4O7·10H2O-10-20; вольфрамат натрия Na2WO4·2H2O-1-3. Плазменно-электрохимическую обработку проводят в гальваностатическом режиме импульсным током, переменным либо переменным однополярным при длительности импульсов 0,0033-0,04 с, напряжении 240-400 В, эффективной плотности тока 5-20 А/дм2 и расходе количества электричества 1500-6000 Кл/дм2 формируемого каталитически активного слоя. Полученный катализатор является устойчивым в области температур 300-500° и обеспечивает степень конверсии СО в CO2 в широких пределах (от 37 до 97%). 2 ил., 1 табл.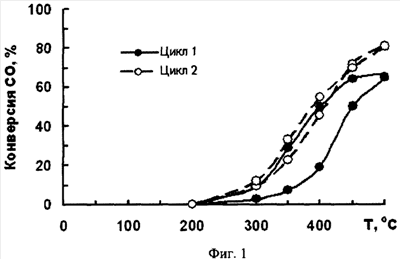
Изобретение относится к области технической химии, а именно к никель-медным оксидным катализаторам на металлическом носителе-подложке, которые могут быть использованы в реакциях конверсии СО в СО2, имеющих место в высокотемпературных процессах очистки технологических и выхлопных газов, в частности в энергетике и автомобильной промышленности.
Процессы очистки выхлопных и отходящих газов («дожигания»), в основе которых лежат процессы окисления, сопровождаются выделением тепла и характеризуются большими перепадами давления, что приводит к перегревам и дезактивации катализаторов, а также к механическому разрушению катализаторов.
Катализаторы на металлических носителях, обладающих высокой теплопроводностью и механической прочностью, испытывают меньший локальный перегрев, подвержены меньшему разрушению, при этом металлические носители могут быть изготовлены в виде сложных, например сотовых, структур.
Дефицит и высокая стоимость катализаторов, включающих благородные металлы, их безвозвратные потери в процессе эксплуатации делают актуальной задачу поиска и разработки катализаторов, не содержащих драгоценных металлов, в частности каталитически активных систем на основе оксидов других металлов.
Известен описанный в патенте РФ №2103057, опубл. 27.01.98, способ получения катализатора окисления углерода и углеводородов, в котором катализатор, содержащий металлический алюминий и оксидный композит, состоящий из оксида алюминия, оксидов переходных металлов и, дополнительно, оксидов редкоземельных элементов или их смеси и/или оксида фосфора, и/или оксида кремния, и/или смесей оксидов переходных металлов, получают в две стадии. На первой стадии подложку из металлического алюминия обрабатывают электрохимическим (анодным либо анодно-искровым) методом, при этом толщину и состав оксидного слоя варьируют, изменяя значения времени, плотности тока и напряжения электрохимического процесса, а также состав электролита. После стадии электрохимического окисления полученный керамометалл отмывают от примесей электролита, сушат и прокаливают при 400-600°С, а затем методом пропитки керамометалла в растворах азотно-кислых солей соответствующего состава совместно или раздельно в него вводят оксиды редкоземельных и переходных элементов с последующей сушкой и прокаливанием при 400-600°С. Недостатком известного способа является его сложность, обусловленная многостадийностью, а также высокие энергозатраты, связанные с неоднократным прокаливанием, и затраты времени.
Наиболее близким к заявляемому является способ получения оксидных, в частности никель-медных, катализаторов [пат. РФ №2241541, опубл. 10.12.2004] на носителе, выполненном из вентильного металла, преимущественно титана и его сплавов или алюминия и его сплавов, методом анодно-искрового осаждения (плазменно-электрохимическим методом) из щелочного электролита, содержащего ацетат двух и/или поливалентного металла, в гальваностатическом режиме при эффективной плотности тока 0,5-40 А/дм2 на постоянном, переменном либо переменном однополярном токе (импульсном однополупериодном выпрямленном) частотой 50 Гц или в режиме падающей мощности при напряжении на электродах не более 600 В.
По мере исследования процессов, происходящих на поверхности обрабатываемых металлов в электролитах под воздействием электрического тока, изменяется используемая в данной области терминология. Термин «плазменно-электрохимический метод» более точно отражает сущность происходящих процессов и является более употребительным в современной научной литературе.
Известный способ реализует общий принцип нанесения каталитически активных оксидных структур на металлическую подложку. Однако каждый конкретный химический процесс, протекающий в присутствии катализатора, нуждается в специфическом катализаторе с оптимально подобранным составом, обеспечивающим максимально полное протекание реакции, а также максимальную механическую и химическую устойчивость катализатора в условиях данного химического процесса.
Задачей изобретения является разработка способа получения оптимизированного по составу никель-медного (Ni-Cu) оксидного катализатора для процесса конверсии СО в СО2 на подложке, выполненной из алюминия или его сплава, обеспечивающего повышение степени конверсии и являющегося термоустойчивым в области температур 300-500°C.
Поставленная задача решается способом получения катализатора на подложке, выполненной из алюминия или его сплава, включающим обработку подложки плазменно-электрохимическим методом в щелочном электролите, содержащем ацетат никеля и ацетат меди, в гальваностатическом режиме на импульсном токе, переменном либо переменном однополярном, в котором, в отличие от известного способа, плазменно-электрохимическую обработку проводят при напряжении 240-400 В, эффективной плотности тока 5-20 А/дм2, длительности импульсов 0,0033-0,04 с и расходе количества электричества 1500-6000 Кл/дм2 формируемого каталитически активного слоя, при этом электролит дополнительно содержит тринатрийфосфат, тетраборат натрия и вольфрамат натрия при следующем соотношении компонентов, г/л:
| ацетат никеля Ni(СН3СОО)2·4 Н2O |
5-20 |
| ацетат меди Cu(СН3СОО)2·Н2О |
1,3-5,0 |
| тринатрийфосфат Na3PO4·12 H2O |
20-30 |
| тетраборат натрия Na2B4O7·10 H2O |
10-20 |
| вольфрамат натрия Na2WO4·2 H2O |
1-3 |
Способ осуществляют следующим образом.
Подложку из алюминия либо его сплава погружают в подготовленный электролит и проводят ее плазменно-электрохимическую обработку в гальваностатическом режиме при эффективной плотности импульсного тока, переменного либо переменного однополярного (однополупериодного выпрямленного), равной 5-20 А/дм2, и продолжительности импульсов (анодных и катодных) 0,0033-0,04 секунды. Величина напряжения плазменно-электрохимической обработки от 240 до 400 В, при этом время и параметры обработки выбирают таким образом, чтобы расход количества электричества на 1 дм2 обрабатываемой поверхности находился в пределах от 1500 до 6000 Кл.
Электролит готовят путем раздельного растворения компонентов в дистиллированной воде при комнатной температуре и последующего сливания полученных растворов.
Обработку ведут при постоянном перемешивании электролита, при этом в ходе обработки температуру электролита поддерживают в пределах 50°С.
В качестве противоэлектрода в процессе плазменно-электролитической обработки могут быть использованы сплавы никеля, титана, нержавеющая сталь, при этом противоэлектродом может служить внутренняя поверхность ванны, в которую помещен электролит.
В результате плазменно-электрохимической обработки подложки, выполненной из алюминия или его сплава, на ее поверхности получают оксидные слои, содержащие наряду с  -Al2О3 соединения никеля и меди и проявляющие каталитическую активность в высокотемпературных процессах окисления СО в СО2. -Al2О3 соединения никеля и меди и проявляющие каталитическую активность в высокотемпературных процессах окисления СО в СО2.
Данные фазового (рентгенофазовый анализ) и элементного (микрозондовый рентгеноспектральный анализ) состава полученного слоя и его поверхности (рентгено-электронная спектроскопия) показывают, что на поверхности оксидного слоя присутствуют более высокие, чем в его объеме, концентрации меди и никеля, более низкие концентрации алюминия. Никель и медь, по всей вероятности, входят в состав твердых растворов, образующихся в системе NiO-CuO, поскольку кристаллических фаз, содержащих никель и медь, в составе полученных оксидных слоев не обнаружено.
По данным рентгено-электронной спектроскопии, соотношение Ni2+/Cu++Cu2+) на поверхности обогащенных никелем и медью оксидных слоев составляет 1,6-3,2. При этом известно [В.Н.Ефремов, Е.З.Голосман. Основы приготовления никель-медных каталитических систем на различных носителях и промышленные катализаторы на их основе. Кинетика и катализ. 2006, том 47, №5, с.814-817], что для обеспечения максимальной каталитической активности никель-медных осажденных катализаторов в реакциях окисления оптимальным является соотношение 2,3-3,0.
Активности полученного катализатора также способствует формирование вторичного носителя  -Al2О3, в структуре которого присутствуют активные центры. Известно, что катализаторы на его основе проявляют более высокую каталитическую активность. Кроме того, -Al2О3, в структуре которого присутствуют активные центры. Известно, что катализаторы на его основе проявляют более высокую каталитическую активность. Кроме того,  -Al2О3 как носитель отличается термостабильностью и химической стойкостью, а также высокой прочностью сцепления с поверхностью инертной металлической подложки. -Al2О3 как носитель отличается термостабильностью и химической стойкостью, а также высокой прочностью сцепления с поверхностью инертной металлической подложки.
Проведенные эксперименты показали, что после катализа наблюдается повышение активности катализатора, которую характеризовали величиной конверсии СО в CO2 при температуре 300-500°С. Упомянутое повышение может найти свое объяснение в изменении соотношения между количеством Cu+ и Cu2+ на поверхности формируемого каталитического слоя (уменьшения содержания Cu2+ при сохранении количества Cu+). Экспериментально также показано, что катализатор активируется при высокотемпературном взаимодействии с газовой смесью (воздух +5% СО), при этом, по-видимому, активатором является СО.
Таким образом, для катализатора, полученного предлагаемым способом, характерно увеличение каталитической активности как при обратном ходе, так и при повторных циклах каталитических испытаний, о чем наглядно свидетельствует наличие петли гистерезиса на графике зависимости величины конверсии от температуры (фиг.1).
Кроме того, проведенные испытания показали, что полученный катализатор сохраняет свою активность при отжиге на воздухе (при 450°С в течение 2 ч), о чем наглядно свидетельствует график зависимости величины конверсии от температуры, показанный на фиг.2.
Таким образом, предлагаемый способ позволяет получить устойчивый в области температур 300-500° никельмедный оксидный катализатор на металлической подложке, обеспечивающий более высокую по отношению к прототипу степень конверсии СО в СО2 (до 90%), что является техническим результатом изобретения.
Примеры конкретного осуществления способа
В качестве носителя катализатора были использованы алюминий и его сплавы, плазменно-электрохимическую обработку которых осуществляли, используя в качестве источника тока тиристорный агрегат ТЕР4-100/460 с программным управлением.
Электролит получали сливанием соответствующих количеств водных растворов, каждый из которых содержал один компонент электролита. При сливании полученных растворов образуется суспензия, стабильность которой поддерживают непрерывным перемешиванием электролита в ходе обработки. В общем случае значение рН электролита было больше 8.
Поверхностный состав полученного каталитически активного слоя исследовали с помощью метода рентгеноэлектронной спектроскопии на сверхвакуумной установке фирмы Specs (Германия) с использованием 150 мм электростатического полусферического анализатора.
Микрозондовый рентгеноспектральный анализ в толщине каталитически активного слоя осуществляли на рентгеноспектральном микроанализаторе JXA 8100 (Япония) с энергодисперсионной приставкой INCA (Англия). Предварительно на пленки напыляли графит для предотвращения зарядки поверхности.
Данные по составу покрытия приведены в примере 5.
Рентгенограммы снимали на рентгеновском дифрактометре Д8 ADVANCE (Германия) в CuK -излучении. При выполнении рентгенофазового анализа использована программа поиска “EVA” с банком данных “PDF-2”. -излучении. При выполнении рентгенофазового анализа использована программа поиска “EVA” с банком данных “PDF-2”.
Полученные рентгенограммы для всех примеров показали присутствие  -Al2O3. -Al2O3.
Толщина покрытия, определенная с помощью вихретокового толщиномера, составляет 10-20 мкм.
Каталитическую активность образцов определяли на универсальной установке проточного типа BI-CATflow4.2A. В активную зону (диаметр 0,9 см, длина 3 см) трубчатого кварцевого реактора помещали образцы из сплава алюминия с нанесенным каталитическим покрытием (геометрическая площадь поверхности покрытия 20 см2). Исходная реакционная смесь содержала 5% СО и воздух. Скорость протока газа составляла 50 мл/мин. Концентрацию СО и CO2 на выходе определяли, используя ИК-газоанализатор “ПЭМ-2”. Интервал исследуемых температур 20-500°С.
Пример 1
Электролит содержит, г/л: Na3PO4·12H2O – 25, Na2B4O7·10H2O – 13, Na2WO4·2H2O – 2, Ni(СН3СОО)2·4Н2О – 20, Cu(СН3СОО)2·H2O – 5. Значение pH электролита составляет 8.5. Фольгу из алюминия марки о.с.ч. с площадью поверхности 20 см2 обрабатывают в анодном гальваностатическом режиме при эффективной плотности тока 10 А/дм2 и длительности импульса 0,0033 с в течение 10 мин. Конечное напряжение формирования 357 В. Количество электричества составляет 6000 Кл/дм2 поверхности формируемого катализатора.
Пример 2.
Состав электролита по примеру 1. Пластину из сплава алюминия АМцМ размерами 2×5×0.05 см обрабатывают аналогично примеру 1. Конечное напряжение формирования 335 В.
Пример 3.
Состав электролита по примеру 1. Пластину из сплава алюминия АМг2 размерами 0,12×0,2×31,2 см, свернутую в спираль, обрабатывают в анодном гальваностатическом режиме при эффективной плотности тока 10 А/дм2 и длительности импульса 0,006 с в течение 5 мин. Конечное напряжение формирования 337 В. Количество электричества составляет 3000 Кл/дм2 поверхности формируемого катализатора
Пример 4.
Состав электролита по примеру 1. Пластину из сплава алюминия Д16 размерами 0,12×0,2×31,2 см, свернутую в спираль, обрабатывают в анодном гальваностатическом режиме при эффективной плотности тока 10 А/дм2 и длительности импульса 0,006 с в течение 10 мин. Конечное напряжение формирования 344 В. Количество электричества составляет 6000 Кл/дм2 поверхности формируемого катализатора.
Пример 5.
Состав электролита по примеру 1. Спираль из сплава алюминия АМг5, выполненную из проволоки диаметром 0,15 см, с общей площадью поверхности 20 см2 обрабатывают в анодном гальваностатическом режиме при эффективной плотности тока 10 А/дм2 и длительности импульса 0,01 c в течение 10 мин. Конечное напряжение формирования 351 В. Количество электричества составляет 6000 Кл/дм2 поверхности формируемого катализатора.
Поверхностный состав полученного каталитического слоя, ат.%: Na – 4.4, Cu – 5.4 (в том числе Cu2+ – 1.1, Cu+ – 4.3), Ni – 12.6, О – 50.7, С – 15.6, Р – 5.9, Al – 5.2, W – 0.2, при этом соотношение Ni/Cu составляет 2.33, Cu2+/Cu – 0.20.
Состав каталитического слоя (глубина 3-5 мкм), ат.%: Ni – 2.1, Cu – 0.3, Р – 0.6, Al – 39.0, О – 56.1, W – 0.1, Mg – 1,8.
Пример 6.
Состав электролита по примеру 1. Спираль из сплава алюминия АМг5, выполненную из проволоки диаметром 0,15 см, с общей площадью поверхности 20 см2 обрабатывают в анодном гальваностатическом режиме при эффективной плотности тока 5 А/дм2 и длительности импульса 0,01 с в течение 15 мин. Конечное напряжение формирования 311 В. Количество электричества составляет 4500 Кл/дм2 поверхности формируемого катализатора.
Пример 7.
Электролит содержит, г/л: Na3PO4·12H2O – 20, Na2B4O7·10H2O – 15, Na2WO4·2H2O – 2, Ni(СН3СОО)2·4Н2O – 15, Cu(СН3СОО)2·H2О – 5. Спираль из сплава АМг5, выполненную аналогично примеру 6, обрабатывают в анодном гальваностатическом режиме при эффективной плотности тока 5 А/дм2 и длительности импульса 0,02 с в течение 10 мин. Конечное напряжение формирования 268 В. Количество электричества 3000 Кл/дм2 поверхности формируемого катализатора.
Пример 8.
Электролит содержит, г/л: Na3PO4·12Н2O – 25, Na2B4O7·10H2O – 10, Na2WO4·2H2O – 3, Ni(СН3СОО)2·4Н2O – 20, Cu(СН3СОО)2·Н2O – 5. Две спирали из сплава алюминия АМг5, выполненные аналогично примеру 6, завешивают параллельно в электролите и обрабатывают в течение 10 мин в гальваностатическом режиме при анодно-катодной поляризации с одинаковой эффективной плотностью анодного и катодного тока 10 А/дм2 при длительности анодных и катодных импульсов, равной 0.02 с. Образцы попеременно являются анодом и катодом. Конечное напряжение формирования UA=UK=380-390 В. Суммарное количество электричества 6000 Кл/дм2 поверхности формируемого катализатора.
Пример 9.
Электролит содержит, г/л: Na3PO4·12H2O – 30, Na2B4O7·10H2O – 10, Na2WO4·2H2O – 1, Ni(СН3СОО)2·4Н2O – 5, Cu(СН3COO)2·H2О – 1.25. Спираль из сплава АМг5, выполненную аналогично примеру 6, обрабатывают в анодном гальваностатическом режиме при эффективной плотности тока 10 А/дм2 и длительности импульса 0,03 с в течение 10 мин. Конечное напряжение формирования 360 В. Количество электричества 6000 Кл/дм2 поверхности формируемого катализатора.
Пример 10.
Электролит содержит, г/л: Na3PO4·12H2O – 25, Na2B4O7·10H2O – 13, Na2WO4·2H2O – 2, Ni(СН3СОО)2·4Н2O – 20, Cu(СН3СОО)2·Н2O – 5. Спираль из сплава АМг5, выполненную аналогично примеру 6, обрабатывают в анодном гальваностатическом режиме при эффективной плотности тока 20 А/дм2 и длительности импульса 0,03 с в течение 3 мин. Конечное напряжение формирования 360 В. Количество электричества 3600 Кл/дм2 поверхности формируемого катализатора.
Пример 11.
Электролит содержит, г/л: Na3PO4·12H2O – 25, Na2B4O7·10H2O – 13, Na2WO4·2H2O – 2, Ni(СН3СОО)2·4Н2О – 10, Cu(СН3СОО)2·Н2O – 5. Мольное отношение Ni/Cu=1.6. Спираль из сплава АМг5, выполненную аналогично примеру 6, обрабатывают в анодном гальваностатическом режиме при эффективной плотности тока 5 А/дм2 и длительности импульса 0,01 с в течение 5 мин. Конечное напряжение формирования 240 В. Количество электричества 1500 Кл/дм2 поверхности формируемого катализатора.
Пример 12.
Электролит содержит, г/л: Na3PO4·12H20 – 25, Na2B4O7·10H2O – 13, Na2WO4·2H2O – 2, Ni(СН3СОО)2·4Н2O – 20, Cu(СН3СОО)2·Н2O – 5. Две детали из сплава алюминия АМг5 завешивают параллельно в электролите и обрабатывают в течение 10 мин в гальваностатическом режиме при анодно-катодной поляризации с одинаковой плотностью анодного и катодного тока 10 А/дм2 при длительности анодных и катодных импульсов, равной 0.04 с. Конечное напряжение формирования UA=UK=310-320 В. Суммарное количество электричества 6000 Кл/дм2 поверхности формируемого катализатора.
Составы электролитов, режимы плазменно-электрохимической обработки, а также результаты каталитических испытаний (4 цикл конверсии СО в CO2 при 450 и 500°С) для алюминия и четырех его сплавов приведены в таблице.
Таблица
Условия обработки и результаты каталитических испытаний |
| Электролит, режимы обработки и результаты каталитических испытаний |
Примеры |
| 1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
12 |
| Na3PO4·12Н2O, г/л |
25 |
25 |
25 |
25 |
25 |
25 |
20 |
25 |
30 |
25 |
25 |
25 |
| Na2B4O7·10H2O, г/л |
13 |
13 |
13 |
13 |
13 |
13 |
15 |
10 |
10 |
13 |
13 |
13 |
| Na2WO4·2H2O, г/л |
2 |
2 |
2 |
2 |
2 |
2 |
2 |
3 |
1 |
2 |
2 |
2 |
| Ni(СН3СОО)2·4Н2O, г/л |
20 |
20 |
20 |
20 |
20 |
20 |
15 |
20 |
5 |
20 |
10 |
20 |
| Cu(СН3СОО)2·Н2O, г/л |
5 |
5 |
5 |
5 |
5 |
5 |
5 |
5 |
1.25 |
5 |
5 |
5 |
| Мольное отношение Ni/Cu |
3.2 |
3.2 |
3.2 |
3.2 |
3.2 |
3.2 |
2.4 |
3.2 |
3.2 |
3.2 |
1.6 |
3.2 |
| |
Материал анода (алюминий или сплав алюминия) |
| Al о.с.ч. |
АМцМ |
АМг2 |
Д16 |
АМг5 |
АМг5 |
АМг5 |
АМг5 |
АМг5 |
АМг5 |
АМг5 |
АМг5 |
| Эффективная плотность тока*, А/дм2 |
10 |
10 |
10 |
10 |
10 |
5 |
5 |
А=К 10 |
10 |
20 |
5 |
А=К 10 |
| Длительность импульсов**, с |
0,0033 |
0,0033 |
0,006 |
0,006 |
0,01 |
0,01 |
0,02 |
0,02 |
0,03 |
0,03 |
0,01 |
0,04 |
| Продолжительность обработки, мин |
10 |
10 |
5 |
10 |
10 |
15 |
10 |
10 |
10 |
3 |
5 |
10 |
| Количество электричества, Кл/дм2 |
6000 |
6000 |
3000 |
6000 |
6000 |
4500 |
3000 |
3000 |
6000 |
3600 |
1500 |
3000 |
| Напряжение, В |
357 |
335 |
337 |
344 |
351 |
311 |
268 |
400 |
360 |
360 |
240 |
320 |
| Конверсия СО при 450°С (4 цикл) |
21 |
22 |
37 |
67 |
66 |
70 |
31 |
25 |
23 |
54 |
23 |
20 |
| Конверсия СО при 500°С (4 цикл) |
37 |
41 |
64 |
95 |
91 |
97 |
61 |
59 |
54 |
77 |
58 |
48 |
| * В анодно-катодном режиме значения эффективной плотности анодного и катодного токов одинаковы. |
** В анодно-катодном режиме длительности анодных и катодных импульсов равны  а= а= к. к. |
Формула изобретения
Способ получения катализатора на подложке из алюминия или его сплава методом обработки подложки плазменно-электрохимическим методом в щелочном электролите, содержащем ацетат никеля и ацетат меди, в гальваностатическом режиме импульсным током, переменным либо переменным однополярным, отличающийся тем, что плазменно-электрохимическую обработку проводят при напряжении 240-400 В, эффективной плотности тока 5-20 А/дм2, длительности импульсов 0,0033-0,04 с и расходе количества электричества 1500-6000 Кл/дм2 формируемого каталитически активного слоя, при этом электролит дополнительно содержит тринатрийфосфат, тетраборат натрия и вольфрамат натрия при следующем соотношении компонентов, г/л:
| ацетат никеля Ni(СН3СОО)2·4Н2O |
5-20 |
| ацетат меди Cu(CH3СОО)2·Н2О |
1,3-5,0 |
| Na3PO4·12H2O |
20-30 |
| Na2B4O7·10H2O |
10-20 |
| Na2WO4·2H2O |
1-3 |
РИСУНКИ
|
|