Патент на изобретение №2342930
|
||||||||||||||||||||||||||||||||
(54) ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, СОДЕРЖАЩИЕ МАЛОНАМИДНЫЕ ПРОИЗВОДНЫЕ ДЛЯ УМЕНЬШЕНИЯ ПРОДУКЦИИ КОЖНОГО САЛА
(57) Реферат:
Изобретение относится к области медицины и фармацевтики и касается применения соединения, выбранного из группы, состоящей из N-бензил-N’-(2,6-диизопропилфенил)-N-изопропилмалонамида, N’-[2,6-бис(1-метилэтил)фенил]-N-(1-метилэтил)-N-[[4-(метилтио)фенил]метил]пропандиамида и N-[2,6-бис(1-метилэтил)фенил]-[
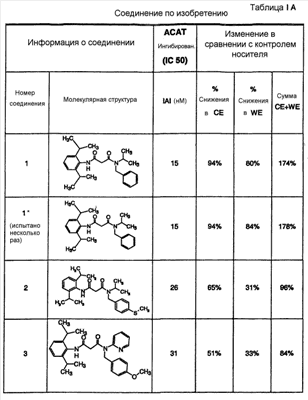
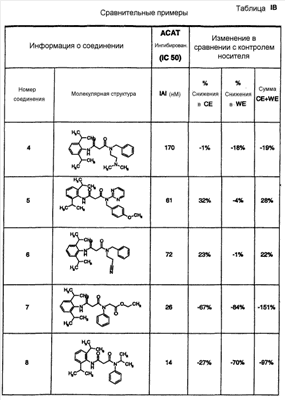
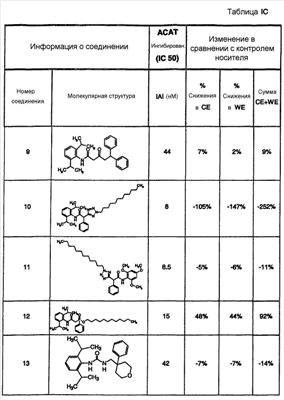
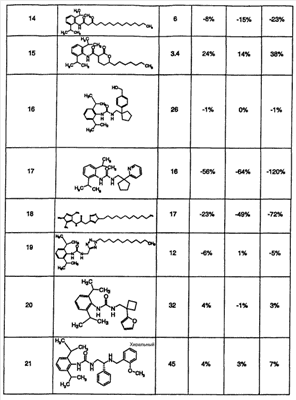
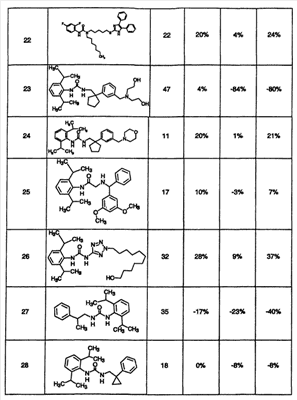
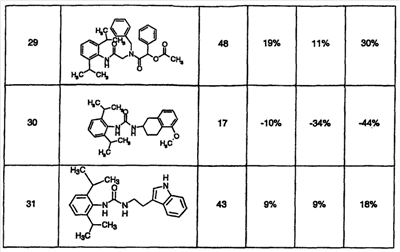
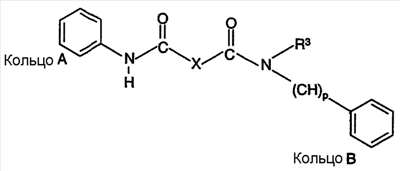
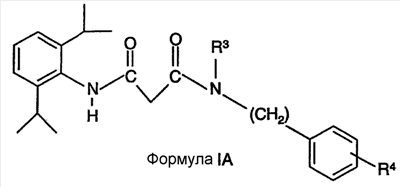
Область, к которой относится изобретение Настоящее изобретение направлено на местное применение ингибиторов АСАТ класса диамидов. Другие аспекты изобретения направлены на композиции этих диамидов для местного применения, их применение для лечения расстройств сальных желез и их применение для уменьшения жирности кожи. Предпосылки создания изобретения Кожа человека состоит из трех основных слоев роговидного слоя, эпидермиса и дермы. Наружный слой представляет собой роговидный слой. Его первостепенной функцией является роль барьера для внешней окружающей среды. Липиды секретируются на поверхность роговидного слоя. Эти липиды уменьшают проницаемость роговидного слоя для воды. Кожное сало обычно составляет 95% этих липидов (Abramovits et al, Dermatologic Clinic, Vol 18, Number 4, Oct. 2000). Кожное сало продуцируется в сальных железах. Эти железы присутствуют почти по всей поверхности тела. Самая высокая концентрация этих желез встречается на волосистой части головы, лбу и лице. Несмотря на важную физиологическую роль, которую играет кожное сало, у многих индивидуумов имеется избыточная продукция кожного сала, особенно в области лица. Избыток кожного сала связан с повышенной распространенностью угрей. Даже у индивидуумов без угрей кожное сало может вызвать сальный вид кожи, уменьшая ее привлекательность (см. Abramovits et al. выше). Современные способы лечения избыточной продукции кожного сала менее чем оптимальны. Аккутан (изотретиоин) снижает секрецию кожного сала до 90%. Однако изотретиоин связан с рядом серьезных побочных эффектов. Он вызывает тяжелые родовые дефекты и противопоказан женщинам детородного возраста. Таким образом, изотретиоин используется только по поводу тяжелых угрей. Этот препарат нецелесообразно использовать просто в качестве косметического средства. Ингибиторы ацил-СоА-холестеролацилтрансферазы (АСАТ) первоначально оценивали для лечения повышенного уровня холестерина. В патенте США № 6133326 раскрыто, что ингибиторы АСАТ также снижают секрецию кожного сала. Хотя патент ‘326 представляет собой ценный вклад в данную область, такие способы лечения в настоящее время не являются коммерчески доступными. В настоящее время наиболее практичным средством уменьшения избыточной продукции кожного сала является частое мытье. Таким образом, в данной области существует необходимость в новых способах лечения, которые снизят секрецию кожного сала сальными железами. Краткое описание сущности изобретения Был открыт новый способ уменьшения секреции кожного сала сальными железами. Был обнаружен класс ингибиторов АСАТ, которые проявляют более высокую активность ингибирования секреции кожного сала. Эти ингибиторы АСАТ могут быть представлены формулой I: в которой R1 и R2, каждый независимо, представлен водородом, С1-6алкилом, С1-6алкокси, галогеном, гидрокси, трифторметилом, трифторметокси, циано, NR5R6 или SR7; X представлен -CR8R9-(CH2)n; R3 представлен водородом, С1-6 алкилом, -(CH2)q-Ph или -(CH2)q-M, p равно целому числу от 1 до 4; R4 представлен заместителем, выбранным из группы, состоящей из водорода, С1-6алкила, С1-6алкокси, галогена, гидрокси, трифторметила, трифторметокси, циано, NR5R6 или SR7; R5, R6, R7, R8 и R9, каждый независимо, представлен водородом, С1-6алкилом; Ph представлен фенильным кольцом, которое может быть необязательно замещенным; М представлен 5- или 6-членным гетероарильным кольцом, содержащим 1 гетероатом, выбранный из группы N, S или O; n и q, каждый независимо, равен целому числу от 0 до 4; его фармацевтически приемлемой солью или его пролекарством. Соединения формулы I можно вводить пациенту для уменьшения количества кожного сала, секретируемого их сальными железами. Обычно соединения следует применять местно на области, проявляющие избыточную продукцию кожного сала. Уменьшение секреции кожного сала снизит количество дерматологических расстройств и косметических жалоб. Эти состояния включают жирную кожу, сальные волосы, лоснящуюся кожу, угри и себорейный дерматит. Изобретение также направлено на фармацевтические композиции, содержащие, по меньшей мере, одно из соединений формулы I в смеси с носителем, подходящим для местного применения. В дополнительном варианте осуществления изобретение направлено на промышленное изделие, включающее соединение формулы I, упакованное для розничного распространения, в сочетании с инструкциями, рекомендующими потребителям способ применения соединения для облегчения состояния, связанного с избытком продукции кожного сала. Дополнительный вариант осуществления направлен на применение соединения формулы I в качестве диагностического средства для выявления неадекватной продукции кожного сала. Другие аспекты изобретения направлены на применение соединения формулы I при изготовлении лекарственного средства, применяемого против себореи. Подробное описание изобретения Заголовки в данном описании используются для облегчения его анализа читателем. Их никоим образом не следует трактовать как ограничивающие изобретение или формулу изобретения. А) Определения и иллюстративные примеры Следующие термины, используемые во всех разделах настоящего описания, включая формулу изобретения, имеют определенные ниже значения, если специально не указано иное. Кроме случаев указания числа, множественное и единственное число следует трактовать как взаимозаменяемые. а. Термин «С1-6алкил» относится к алькильной группе с прямой или разветвленной цепью, содержащей от 1 до 6 атомов углерода, такой как метил, этил, н-пропил, изопропил, н-бутил, изобутил, н-пентил, изопентил, н-гескил, 1,1-диметилбутил, 2,3-диметилбутил и т.д. b. Термин «С1-6алкокси» относится алкоксигруппе с прямой или разветвленной цепью, содержащей от 1 до 6 атомов углерода, такой как метокси, этокси, н-пропокси, изопропокси, н-бутокси, изобутокси, н-пентокси, н-гексилокси и т.д. с. Термин «галоген» относится к атому хлора, фтора или брома. d. Термин «необязательно замещенный фенил» относится к фенилу (-С6Н5), который может быть замещен заместителями в количестве до 3, причем каждый заместитель независимо выбран из группы, состоящей из С1-6алкила, С1-6алкокси, галогена, гидрокси, трифторметила, трифторметокси, циано, NR5R6 или SR7. Эти заместители могут быть одинаковыми или различными и могут располагаться в любом из орто-, мета- или параположениях. е. Термин «гетероарил» относится к ароматическому кольцу, имеющему один гетероатом, выбранный из кислорода, азота и серы. Более конкретно, он относится к 5- или 6-членному кольцу, содержащему 1 атом азота, 1 атом кислорода или 1 атом серы. 5-членное кольцо имеет 2 двойные связи, и 6-членное кольцо имеет 3 двойные связи. Примеры таких гетероарильных кольцевых систем включают, но без ограничения, пирролил, фуранил, тиофенил и пиридинил. f. Термин «фармацевтически приемлемые соли» предназначен для обозначения или «фармацевтически приемлемых кислотно-аддитивных солей», или «фармацевтически приемлемых основно-аддитивных солей», в зависимости от действительной структуры соединения. g. Термин «фармацевтически приемлемые кислотно-аддитивные соли» относится к любой из нетоксичных солей добавления органических и неорганических кислот основных соединений, представленных формулой I, или любых из его промежуточных соединений. Иллюстративные неорганические кислоты, которые образуют подходящие соли, включают хлористо-водородную, бромисто-водородную, серную и фосфорную кислоту и кислотные соли металлов, такие как моногидроортофосфат натрия и гидросульфат калия. Иллюстративные органические кислоты, которые образуют подходящие соли, включают моно-, ди- и трикарбоновые кислоты. Примерами таких кислот являются, например, уксусная, гликолевая, молочная, пировиноградная, малоновая, янтарная, глутаровая, фумаровая, яблочная, винная, лимонная, аскорбиновая, малеиновая, гидроксималеиновая, бензойная, гидроксибензойная, фенилуксусная, циннамовая, салициловая, 2-феноксибензойная, п-толуолсульфоновая кислота и сульфоновые кислоты, такие как метансульфоновая кислота и 2-гидроксиэтансульфоновая кислота. Такие соли могут существовать в гидратированной или по существу безводной форме. В основном, кислотно-аддитивные соли этих соединений растворимы в воде и различных гидрофильных органических растворителях и по сравнению с их формами свободных оснований обычно демонстрируют более высокие температуры плавления. h. Термин «фармацевтически приемлемые основно-аддитивные соли» относится к любой из нетоксичных органических или неорганических основно-аддитивных солей соединений, представленных формулой I, или любых из его промежуточных соединений. Иллюстративные основания, которые образуют подходящие соли, включают гидроксиды щелочных металлов или щелочноземельных металлов, такие как гидроксиды натрия, калия, кальция, магния или бария; аммиак и алифатические, алициклические или ароматические органические амины, такие как метиламин, диметиламин, триметиламин и пиколин. i. Термин «пролекарство» относится к соединениям, которые быстро трансформируются in vivo для получения исходного химического соединения указанных выше формул, например, гидролизом в крови. Подробное обсуждение представлено в публикациях T.Higuchi and V.Stella, “Pro-drugs as Novel Delivery Systems,” Vol. 14 of A.C.S. Symposium Series, и в Bioreversible Carriers in Drug Design, ed. Edward B.Roche, American Pharmaceutical Association and Pergamon Press, 1987, которые включены в настоящее описание посредством ссылки. j. Термины «соединение формулы I», «соединения изобретения» и «соединения» во всем описании используются взаимозаменяемо и должны рассматриваться как синонимы. k. Термин «пациент» относится к теплокровным животным, таким как, например, морские свинки, свиньи, мыши, крысы, песчанки, кошки, кролики, собаки, обезьяны, шимпанзе и люди. l. Термин «лечить» относится к способности соединений облегчить, уменьшить или замедлить прогрессирование заболевания (или состояния) пациента или любого повреждения ткани, связанного с заболеванием. Некоторые из соединений формулы I могут существовать в виде оптических изомеров. Любая ссылка в данной заявке на одно из соединений, представленных формулой I, предназначена для охвата или конкретного оптического изомера, или смеси оптических изомеров (пока нет ясного их исключения). Конкретные оптические изомеры могут быть выделены и извлечены методами, известными в данной области, такими как хроматография на хиральных стационарных фазах или разделение посредством образования хиральной соли и последующего разделения селективной кристаллизацией. Альтернативно, использование конкретного оптического изомера в качестве исходного вещества даст соответствующий изомер в качестве конечного продукта. Кроме того, соединения по настоящему соединению могут существовать в несольватированных, а также сольватированных формах с фармацевтически приемлемыми растворителями, такими как вода, этанол и им подобные. В целом, в целях настоящего изобретения сольватированные формы считаются эквивалентными несольватированным формам. Любая ссылка в настоящем описании на соединение формулы I предназначена для охвата индивидуальных соединений в виде смесей, в виде солей, в виде сольватов или любых их комбинаций. Все из соединений формулы I имеют, по меньшей мере, 2 фенильных кольца, как изображено непосредственно ниже: Кольцо А может быть незамещенным или может быть замещено одним или двумя заместителями, как определено группами R1 и R2. R1 и R2 могут быть представлены одинаковыми или различными заместителями. В одном варианте осуществления R1 и R2 каждый представлен изопропильными группами, и оба расположены в ортоположениях фенильного кольца. Кольцо В также необязательно может быть замещенным, как указано для R4. Как описано выше, R4 может представлять собой до 3 заместителей, отличных от водорода. Эти заместители могут быть расположены в любом из орто-, мета- или параположений. R3 может также быть представлен фенильным кольцом или фенилалкиленовой группой. Как описано выше, любое такое фенильное кольцо может также быть замещенным заместителями в количестве до 3. Они могут быть расположены в любом из орто-, мета- или параположений. R3 может также быть представлен гетероарильным кольцом или гетероарилалкиленовой группой. Гетероарильное кольцо может быть присоединено к указанному атому азоту любым атомом углерода гетероарильного кольца. Аналогичным образом, если q равно 1, 2, 3 или 4, то гетероарильное кольцо может быть связано с алкиленовой группой через любой из ее атомов углерода. В дополнительном варианте осуществления изобретения формула IA иллюстрирует подгруппу формулы I, особенно пригодную для местного применения. в которой R1 и R2, каждый представляет собой изопропил (орто), р равен 1, и Х представляет собой метилен, как проиллюстрировано выше; R3 представлен С1-6алкилом или гетероарилом (более конкретно, изопропилом или пиридилом), и R4 представляет собой, как определено в формуле I. Более конкретные примеры соединений формулы Ia включают: а) N-бензил-N’-(2,6-диизопропилфенил)-N-изопропилмалонамид; b) N’-[2,6-бис(1-метилэтил)фенил]-N-(1-метилэтил)-N-[[4-(метилтио)фенил]метил]пропандиамид и с) N-[2,6-бис(1-метилэтил)фенил]-[ В) Синтез Соединения формулы I были ранее описаны в литературе. Внимание читателя обращается на Европейскую патентную заявку № 0433662, которая включена в данное описание посредством ссылки. В заявке ‘662 раскрыто, что соединения формулы I обладают ингибирующей активностью в отношении ацил-СоА-холестеролацилтрансферазы (АСАТ). В заявке ‘662 раскрыто, что эти соединения можно использовать для снижения возросших уровней холестерина и для лечения атеросклероза. В заявке ‘662 не раскрыто применение этих соединений для уменьшения секреции кожного сала. В заявке ‘662 раскрыто, как получить соединения формулы I. Внимание читателя обращается на стр.7-20, где описаны способы синтеза этих соединений. Способы получения фармацевтически приемлемых солей этих соединений описаны на стр.6 указанной заявки. С) Применение в медицине и косметике Ингибирование ацил-СоА-холестеролацилтрансферазы (АСАТ) блокирует этерификацию свободного холестерина в сложные эфиры холестерина. Сложные эфиры холестерина представляют собой первичную форму транспортировки и хранения холестерина у животных. Было показано, что в кишечнике ингибиторы АСАТ ингибируют всасывание холестерина из пищеварительного тракта. Было показано, что ингибирование АСАТ уменьшает образование и секрецию содержащих холестерин липопротеинов снижением массы сложного эфира холестерина липопротеинового ядра. По этим причинам ингибиторы АСАТ ранее оценивали в качестве средств для снижения уровней холестерина в сыворотке. Кожные сальные железы представляют собой голокринные железы, которые секретируют смесь липидов, известных как кожное сало. Кожное сало состоит из триглицеридов, воска, сложных стериновых эфиров и сквалена. Существует значительное различие состава кожного сала человека на основе индивидуальных переменных величин, таких как возраст, пол, рацион питания и патология. Кожное сало вырабатывается в ацинарных клетках сальных желез, накапливается по мере старения этих клеток и мигрирует в сторону центра железы. При созревании ацинарные клетки лизируются и высвобождают кожное сало в проток просвета, из которого секретируется кожное сало. Образование кожного сала регулируется разнообразными гормонами, которые действуют в основном для регуляции скорости липидного метаболизма. Воски и стерины превращаются внутри ацинарных клеток в устойчивую форму сложного эфира посредством активности разнообразных ацильных и жирно-кислотных трансфераз. Эти сложные эфиры затем хранятся в виде липидных капелек внутри ацинарных клеток перед высвобождением. Соединения формулы I блокируют превращение свободного холестерина в сложные эфиры холестерина, приводя к повышенным уровням свободного холестерина внутри ацинарных клеток. Хотя в настоящее время клеточный механизм не полностью понят, ацинарные клетки продуцируют меньше кожного сала при контакте с ингибитором АСАТ. Таким образом, соединения формулы I ингибируют секрецию кожного сала и, таким образом, уменьшают количество кожного сала на поверхности кожи. Соединения можно применять для лечения разнообразных кожных заболеваний, таких как угри или себорейный дерматит. В дополнение к лечению заболеваний, связанных с избыточной продукцией кожного сала, данные соединения можно также применять для достижения косметического эффекта. Некоторые потребители считают, что они поражены избыточной активностью сальных желез. Они считают, что их кожа жирная и, таким образом, непривлекательная. Эти индивидуумы могут использовать соединения формулы I для уменьшения количества кожного сала на их коже. Уменьшение секреции кожного сала снизит жирность кожи у индивидуумов, пораженных такими состояниями. Для проявления описанных выше биологических эффектов данные соединения необходимо вводить в количестве, достаточном для ингибирования продукции и/или секреции кожного сала сальными железами и ацинарными клетками. Это количество может варьироваться в зависимости от определенного подвергаемого лечению заболевания/состояния, тяжести заболевания/состояния пациента, пациента, конкретного вводимого соединения, пути введения и наличия других, лежащих в основе патологических состояний у пациента и т.д. При системном введении соединения обычно проявляют свой эффект в диапазоне доз от примерно 0,1 мг/кг/день до примерно 100 мг/кг/день для любого из перечисленных выше заболеваний или состояний. Может быть желательно повторное ежедневное введение, и оно будет варьироваться в соответствии с указанными выше условиями. Соединения настоящего изобретения можно вводить разнообразными путями. Одни эффективны при пероральном введении. Соединения можно также вводить парентерально (т.е. подкожно, внутривенно, внутримышечно, внутрибрюшинно или подоболочечно), ректально или местно. В конкретном варианте осуществления соединения вводят местно. Местное введение особенно пригодно для лечения угрей и по косметическим показаниям. Соединения следует наносить на те области кожи, которые поражены избыточной продукцией кожного сала. Доза должна варьироваться, но в качестве общей рекомендации, соединение должно присутствовать в дерматологически приемлемом носителе в количестве от 0,01 до 10 мас.%, и дерматологический препарат следует наносить на пораженную область от 1 до 4 раз/день. Термин «дерматологически приемлемый» относится к носителю, который можно наносить на кожу, волосы или волосистую часть головы и который позволит препарату диффундировать к участку действия (т.е. сальным железам и/или ацинарным клеткам). D) Совместное введение В дополнительном варианте осуществления изобретения соединения формулы I можно вводить совместно с другими соединениями для дополнительного усиления их активности или для минимизации потенциальных побочных эффектов. Например, для облегчения состояния при угревой сыпи применялись антибиотики, такие как тетрациклин и клиндамицин. Антибиотик искореняет микроорганизм, Propionbacterium acnes, приводя к уменьшению угрей у пациента. Соединения формулы I можно вводить совместно с любым антибиотиком, подходящим для лечения угрей. Было показано, что ретиноиды, такие как изотретиоин, уменьшают продукцию кожного сала и применяются для лечения угрей. Эти ретиноиды можно вводить совместно с соединением формулы I для уменьшения продукции кожного сала и/или лечения угрей. Было показано, что эстроген и прогестерон снижают продукцию кожного сала. Эти соединения или любой синтетический агонист рецепторов эстрогена или прогестерона можно вводить совместно с соединением формулы I для уменьшения продукции кожного сала. Было показано, что антиандрогены уменьшают секрецию кожного сала. Антиандрогены могут работать посредством ряда различных механизмов. Например, некоторые соединения блокируют превращение тестостерона в 5- Используемый в настоящем описании термин «вводимые совместно» относится к введению соединения формулы I со вторым лекарственным средством, обычно имеющим отличающийся механизм действия, с использованием схемы дозирования, которая способствует достижению желаемого результата. Он может относиться к одновременному дозированию, дозированию в различное время в течение одного дня или даже дозированию в разные дни. Соединения можно вводить отдельно или их можно объединять в одну композицию. Методики получения таких композиций описаны ниже. Е. Косметические и фармацевтические композиции При желании, соединения можно вводить непосредственно без какого-либо носителя. Однако для облегчения введения они обычно включаются в фармацевтические носители. Для перорального введения соединения могут составляться в твердые или жидкие препараты, такие как капсулы, пилюли, таблетки, пастилки, расплавы, порошки, суспензии или эмульсии. Твердые единичные дозированные формы могут представлять собой капсулы обычного желатинового типа, содержащие, например, поверхностно-активные вещества, лубриканты и инертные наполнители, такие как лактоза, сахароза и кукурузный крахмал, или они могут представлять собой препараты длительного высвобождения. В другом варианте осуществления соединения могут быть таблетированы с общепринятыми основами для таблеток, такими как лактоза, сахароза и кукурузный крахмал, в комбинации со связующими веществами, такими как акация, кукурузный крахмал или желатин, дезинтегрантами, такими как картофельный крахмал или альгиновая кислота, и лубрикантом, таким как стеариновая кислота или стеарат магния. Жидкие препараты получают растворением активного ингредиента в водном или неводном фармацевтически приемлемом растворителе, который может также содержать суспендирующие агенты, подслащивающие агенты, ароматизирующие агенты и консервирующие агенты, как известно в данной области. Для парентерального введения соединения могут быть растворены в физиологически приемлемом фармацевтическом носителе и вводиться в виде или раствора, или суспензии. Иллюстративными подходящими носителями являются вода, солевой раствор, растворы декстрозы, растворы фруктозы или масла животного, растительного или синтетического происхождения. Фармацевтический носитель может также содержать консерванты, буферы и т.д., как известно в данной области. Когда соединения вводятся подоболочечно, они также могут быть растворены в спинно-мозговой жидкости, как известно в данной области. Однако обычно соединения должны быть включены в композиции, подходящие для местного введения. Можно применять любую из местных композиций, известных в данной области. Примеры таких местных композиций включают лосьоны, аэрозоли, кремы, различные мази, гели и т.д. Действительные способы получения местных композиций известны или очевидны для специалистов в данной области, и они подробно описаны в указанном выше руководстве Remington’s Pharmaceutical Sciences, 1990; и Pharamaceutical Dopsage Forms and Drug Delivery Systems, 6th ed., Willams & Wilkins (1995). В дополнительном варианте осуществления описанные выше композиции могут быть упакованы для розничного распространения (т.е. в виде набора или промышленного изделия). Упаковка содержит инструкции, информирующие пациента, как применять продукт для облегчения таких состояний, как угри, жирная кожа и т.д. Такие инструкции могут быть напечатаны на коробке, могут представлять собой отдельный вкладыш или напечатаны на стороне контейнера, содержащего композицию, и т.д. Соединения формулы I могут быть также смешаны с любым инертным носителем и использоваться в лабораторных анализах для определения концентрации соединений в сыворотке, моче и т.д. пациента, как известно в данной области. Соединения можно также использовать в качестве инструмента исследований. Хотя изобретение было описано в связи с определенными вариантами его осуществления, следует понимать, что оно может быть подвергнуто дальнейшим модификациям, и данное описание предназначено для охвата любых вариантов, видов применения или адаптаций изобретения, следующих основным принципам изобретения и включающих такие отходы от настоящего описания, которые входят в известную или привычную практику в той области, к которой относится настоящее изобретение. Следующие примеры и биологические данные представлены для дальнейшей иллюстрации изобретения. Данное описание не следует рассматривать как ограничивающее изобретение. Пример 1 Luderschmidt et al. описывает экспериментальную животную модель для тестирования того, способны ли соединения модулировать секрецию кожного сала (Arch. Derm. Res. 258, 185-191 (1977)). В этой модели используются сирийские хомячки, уши которых содержат сальные железы. Соединения можно вводить этим животным для определения того, способно ли испытуемое соединение модулировать продукцию кожного сала. Был проведен скрининг ряда соединений, которые, как известно, ингибируют АСАТ, используя способы, аналогичные способам Luderschmidt et al. В таблице 1А показаны результаты, полученные с отобранными диамидами, охватываемыми указанной выше формулой I. В таблице 1В показаны результаты, полученные с рядом диамидов, не охватываемых формулой I. В таблице IC показаны результаты, полученные с другими активными ингибиторами АСАТ, которые не представляют собой диамиды. В таблицах 1А-1С также представлена аффинность соединения к крысиным АСАТ, измеренная в виде IC50. Эти величины определяли измерением опосредованного АСАТ переноса тритий содержащей олеиновой кислоты от ацил-СоА к холестерину для получения меченого холестерилолеата. Источником активности АСАТ были гомогенаты ткани кишечника крыс. Заданные концентрации: 1) кишечного гомогената, содержащего эндогенный холестерин, 2) испытуемого соединения и 3) [1-14C]олеил-СоА контактировали в течение заданного времени. Реакцию гасили и результаты определяли тонкослойной хроматографией. Аналогичные анализы с использованием кроличьего кишечника были описаны Roth et al в J. Med Chem. 35:1609-1617 (1992). Испытание на игибирование продукции кожного сала проводили следующим образом. Самцов сирийских хомячков в возрасте от 9 до 10 недель помещали в лабораторную окружающую среду и давали возможность акклиматизироваться в течение 2 недель перед использованием в исследовании. Каждая группа состояла из 5 животных, и параллельно исследовали действие носителя и положительные контроли. Перед введением 10 мг каждого соединения растворяли в 1 мл универсального растворителя (этанол/пропиленгликоль (70/30% об./об.) для достижения конечной концентрации 1% мас./об. Препараты наносили животным местно 2 раза в день, 5 дней в неделю, в течение 4 недель. Каждая доза составляет 25 мкл контроля носителя или лекарственного средства. Дозу наносили на вентральные поверхности правого и левого уха. Всех животных умерщвляли примерно через 18-24 ч после нанесения конечной дозы. Правое ухо брали у каждого животного и использовали для анализа кожного сала. Уши готовили для анализа ВЭЖХ следующим образом. Брали дистальную биопсию размером 8 мм пробойником непосредственно над анатомической отметкой “V” в ухе для нормализации области образца. Пункционный биоптат оттягивали в сторону. Вентральную поверхность биоптата (площадь, где непосредственно на сальные железы местно наносили дозу) удерживали для испытания и дорсальную поверхность пункционного биоптата удаляли. Образцы ткани продували газообразным N2 и хранили при -80°С в атмосфере азота до анализа ВЭЖХ. В дополнение к образцам ушей аликвотное количество каждого препарата и носителя (по меньшей мере, 250 мкл) также хранили при -80°С для включения в анализ ВЭЖХ. Анализ ВЭЖХ проводили на экстракте образца ткани. Обеспечивали контакт образцов ткани с 3 мл растворителя (смесь 4:1 2,2,4-триметилпентана и изопропилового спирта). Смесь встряхивали в течение 15 мин и хранили в течение ночи при комнатной температуре, защищая от света. На следующее утро к образцу добавляли 1 мл воды и встряхивали в течение 15 мин. Затем образец центрифугировали приблизительно при 1500 об/мин в течение 15 мин. 2 мл органической фазы (верхний слой) переносили в стеклянный флакончик, сушили при 37°С в атмосфере азота в течение приблизительно 1 ч и затем лиофилизировали в течение приблизительно 48 ч. Затем образцы удаляли из лиофилизатора и содержимое каждого флакончика восстанавливали 600 мкл растворителя А (триметилпентан/тетрагидрофуран (99:1)). Затем образцы снова закрывали и перемешивали в вихревой мешалке в течение 5 мин. Затем 200 мкл каждого образца переносили в предварительно маркированный флакончик емкостью 200 мкл для ВЭЖХ со стеклянными вкладышами по 200 мкл. Флакончики для ВЭЖХ помещали в кювету автосэмплера для блока ВЭЖХ серии Agilent 1100. Устройство ВЭЖХ серии Agilent 1100 состояло из термостатированного автосэмплера, четверного насоса, нагревателя колонки и модуля интерфейса A/D (переменного/постоянного тока). Все компоненты контролировались программным обеспечением Agilent ChemStation. Аналитическую колонку Waters Spherisorb S3W 4,6×100 мм поддерживали при 30°С блоком нагревателя колонки Agilent. Автосэмплер ВЭЖХ был запрограммирован для поддержания температуры образца 20°С в течение цикла. 10 мкл каждого образца инжектировали в трех повторах в колонку. Использовали 2 растворителя для градиента растворителей. Растворитель А представлял собой смесь триметилпентана и тетрагидрофурана (99:1). Растворитель В представлял собой этилацетат. Используемый градиент представлен в таблице ниже:
Детектор светорассеивания с испарением Sedex 75 (ELSD) действовал при 45°С с прибавкой по 5 и давлении N2, поддерживаемом при 3,1 бар. Аналоговый сигнал, полученный прибором, посылался к модулю интерфейса A/D, где он превращался в цифровой выходной сигнал. Превращение было основано на точке установки 10000 мАЕД/вольт, а частоту данных устанавливали на 10 Гц (0,03 мин). Затем полученный цифровой выходной сигнал подавали в устройство с программным обеспечением Agilent ChemStation для интегрирования площади пика. Результаты анализа ВЭЖХ представлены ниже в таблицах 1А-С. Результаты представлены в виде снижения уровня продукции сложного холестеринового эфира (СЕ) и сложного эфира воска (WE), по сравнению с контролем носителя. Отрицательное число указывает на то, что ингибитор АСАТ действительно увеличивал продукцию кожного сала. В таблицах 1А, 1В и 1С сведены результаты, полученные в описанных выше экспериментах. В таблице 1А показаны результаты, полученные с соединениями, охватываемыми формулой I (т.е. изобретения). Таблицы 1В и 1С представлены для сравнения и включают соединения, не описываемые формулой I. В таблице 1В показаны диамиды, структурно родственные соединения формулы I. В таблице 1С показаны результаты, полученные с известными ингибиторами АСАТ, структурно не родственными диамидам, но имеющими IC50 50 нм или меньше при измерении в описанном выше анализе АСАТ. Для проведения этого сравнения общий формат использовали в трех таблицах. Каждому соединению был присвоен произвольный номер соединения, который показан в левой крайней колонке (т.е. колонке 1). Во второй колонке показана структура испытуемого соединения, и в третьей колонке показана его активность в качестве ингибитора АСАТ в описанном выше анализе. В колонках 4-6 показаны результаты исследования влияния соединений на секрецию кожного сала. Результаты выражены в виде разницы с контролем. Положительное число отражает снижение продукции измеренного компонента кожного сала, т.е. сложного холестеринового эфира (СЕ) или сложного эфира воска (WE). Отрицательное число указывает на то, что соединение увеличивало продукцию СЕ или WE. В колонке 4 показана способность соединений снижать количество сложного холестеринового эфира в образце кожного сала. Ингибирование сложного холестеринового эфира имеет важное значение, потому что АСАТ ответственна за превращение холестерина в сложный холестериновый эфир. Эти результаты отражают способность или отсутствие способности соединения модулировать АСАТ в ткани-мишени (сальные железы хомячка). В колонке 5 показано действие, которое соединение оказывало на генерирование сложного эфира воска. Сложные эфиры воска представляют собой специфические маркеры сальных желез и оцениваемым образом не выявляются ни в одном слое кожи. Снижение уровня сложного эфира воска отражает уменьшение секреции кожного сала. Колонка 6 представляет собой суммирование результатов, представленных в колонках 4 и 5 (и она включена для дополнительного выяснения относительных различий активности). Как показано в таблице 1А, диамиды формулы I значимо снижали секрецию сложного холестеринового эфира, указывая на то, что АСАТ ингибировался в ткани-мишени. Содержание сложного эфира воска также снижалось, указывая на то, что общая секреция кожного сала уменьшалась при сравнении с контролем. Например, соединение 1 уменьшало уровень СЕ на 95% и WE – на 80%. Соединения 2 и 3 давали сравнимые результаты. Сравнение с таблицей 1В показывает значимые различия. Несмотря на структурное сходство, эти диамиды оказывали значимо меньшее воздействие на секрецию СЕ и WE. Сравнение с соединениями таблицы 1С также является иллюстративным. Все эти соединения являются мощными ингибиторами АСАТ. У всех соединений величина IC50 составляла 50 нм или менее. Несмотря на такую активность, они как группа оказывали значительно меньшее действие на секрецию кожного сала, чем соединение формулы I. Такие результаты были неожиданными.
Формула изобретения
1. Применение соединения, выбранного из группы, состоящей из N-бензил-N’-(2,6-диизопропилфенил)-N-изопропилмалонамида, N’-[2,6-бис(1-метилэтил)фенил]-N-(1-метилэтил)-N-[[4-(метилтио)фенил]метил]пропандиамида и N-[2,6-бис(1-метилэтил)фенил]-[ или его фармацевтически приемлемой соли при изготовлении лекарственного средства для жирной кожи. 2. Применение по п.1, при котором указанное соединение представляет собой N-бензил-N’-(2,6-диизопропилфенил)-N-изопропилмалонамид. 3. Фармацевтическая композиция для местного применения для лечения жирной кожи, расстройств сальных желез или для уменьшения секреции кожного сала, содержащая, по меньшей мере, один дерматологически приемлемый носитель в смеси с эффективным количеством, по меньшей мере, одного соединения, выбранного из группы, состоящей из N-бензил-N’-(2,6-диизопропилфенил)-N-изопропилмалонамида, N’-[2,6-бис(1-метилэтил)фенил]-N-(1-метилэтил)-N-[[4-(метилтио)фенил]метил]пропандиамида и N-[2,6-бис(1-метилэтил)фенил]-[ или его фармацевтически приемлемой соли. 4. Композиция для местного применения по п.3, в которой указанное соединение представляет собой N-бензил-N’-(2,6-диизопропилфенил)-N-изопропилмалонамид. 5. Применение соединения, выбранного из группы, состоящей из N-бензил-N’-(2,6-диизопропилфенил)-N-изопропилмалонамида, N’-[2,6-бис(1-метилэтил)фенил]-N-(1-метилэтил)-N-[[4-(метилтио)фенил]метил]пропандиамида и N-[2,6-бис(1-метилэтил)фенил]-[ или его фармацевтически приемлемой соли при изготовлении лекарственного средства для уменьшения секреции кожного сала. 6. Применение по п.5, при котором указанное соединение представляет собой N-бензил-N’-(2,6-диизопропилфенил)-N-изопропилмалонамид. 7. Применение соединения, выбранного из группы, состоящей из N-бензил-N’-(2,6-диизопропилфенил)-N-изопропилмалонамида, N’-[2,6-бис(1-метилэтил)фенил]-N-(1-метилэтил)-N-[[4-(метилтио)фенил]метил]пропандиамида и N-[2,6-бис(1-метилэтил)фенил]-[ или его фармацевтически приемлемой соли при изготовлении лекарственного средства против расстройств сальных желез. 8. Применение по п.7, при котором указанное соединение представляет собой N-бензил-N’-(2,6-диизопропилфенил)-N-изопропилмалонамид. 9. Применение по любому из п.7 или 8, при котором указанное расстройство представляет собой угри.
|
||||||||||||||||||||||||||||||||

 -[[(4-метоксифенил)метил](2-пиридинил)амино]]-
-[[(4-метоксифенил)метил](2-пиридинил)амино]]-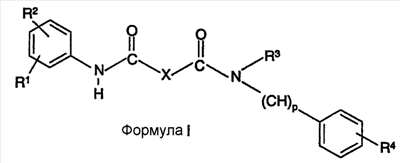
 -дигидротестостерон, который ответственен за биологический эффект во многих тканях. Было показано, что ингибиторы 5-альфа-редуктазы, такие как финастерид, уменьшают продукцию кожного сала. Финастерид коммерчески доступен от компании Merck под торговым названием Propecia®. Примеры других ингибиторов 5-
-дигидротестостерон, который ответственен за биологический эффект во многих тканях. Было показано, что ингибиторы 5-альфа-редуктазы, такие как финастерид, уменьшают продукцию кожного сала. Финастерид коммерчески доступен от компании Merck под торговым названием Propecia®. Примеры других ингибиторов 5-