Патент на изобретение №2342928
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) ПРИМЕНЕНИЕ ИНГИБИТОРА IBAT ДЛЯ ЛЕЧЕНИЯ ИЛИ ПРОФИЛАКТИКИ ЗАПОРА
(57) Реферат:
Описано применение ингибитора IBAT (транспорта желчных кислот в подвздошной кишке), выбранного из 1,2,5-бензотиадиазепинов в лечении и/или профилактике запора у теплокровных животных, таких как человек, соответствующие способ лечения и фармацевтическая композиция (варианты). Изобретение обеспечивает не только увеличение количества фекалий за счет усиления двигательной функции кишечника, но и увеличение количества воды в нижней части его содержимого. Это приводит к размягчению последнего и к снижению растяжения стенок кишечника, что уменьшает чувство боли. 4 н. и 12 з.п. ф-лы, 3 табл.
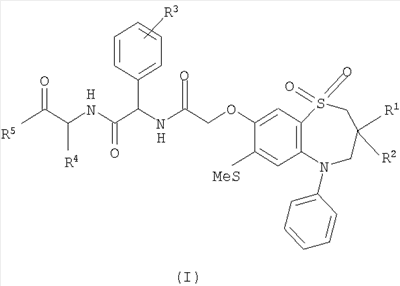
Настоящее изобретение относится к новому лечению и/или профилактике функциональных запоров и синдрома раздраженного кишечника с преобладанием запоров (C-IBS). Более конкретно изобретение относится к применению ингибитора транспорта желчных кислот в подвздошной кишке (IBAT) в лечении и/или профилактике этих нарушений и к фармацевтическим композициям, содержащим указанный ингибитор IBAT для применения в лечении и/или профилактике этих расстройств. Запор и/или ассоциированные с ним симптомы беспокоят многих людей в западном мире и чаще встречаются у детей и пожилых людей. До 20% (включительно) населения, в зависимости от демографических факторов, выборки и используемых определений, могут иметь запоры. При исследовании приблизительно 2000 человек в пяти разных европейских странах (Gastroenterology 118:A720, 2000) от 6 до 23% людей сказали, что в течение последних 12 месяцев у них был запор, приблизительно 20% людей принимали в этот период слабительное, и по меньшей мере 10% испытывали затруднения при дефекации по меньшей мере один раз в месяц. В ходе проводимого в 1991 г исследования-опроса по вопросам национального здравоохранения приблизительно 4,5 миллионов человек в США отметили, что страдают запорами все время или большую часть времени. Чаще всего о запорах сообщали женщины, дети и взрослые в возрасте 65 лет и старше. Беременные женщины также жалуются на запоры, которые также являются частой проблемой после родов или хирургического вмешательства. Женщины составляют самую большую группу пациентов с запорами, и согласно большинству исследований эта проблема усиливается с возрастом. Опросы жителей запада выявили IBS у 15-20% подростков и взрослых со значительным преобладанием среди женщин (у других популяций распространенность различалась). От 30 до 35% пациентов с IBS страдали запором в качестве основного симптома наряду с болью и/или дискомфортом в области живота (C-IBS). Причины запора различны и включают такие общие факторы, как пол, возраст, национальность, режим питания и физическая нагрузка; анатомия и функционирование толстой кишки, например содержимое просвета, поглощение воды и натрия, диаметр и длина толстой кишки и ее двигательная функция; дефекационная функция, такая как нормальная дисфункция, недостаточность расслабления комплекса анального сфинктера, неэффективные позывы, пониженная ректальная чувствительность, а также объем и консистенция стула; расстройства аноректальной области и тазового дна; психологические и поведенческие факторы. Запор может являться следствием или результатом некоторых медицинских состояний, например неврологических нарушений, таких как рассеянный склероз, болезнь Паркинсона; хронической идиопатической псевдонепроходимости кишечника; инсульта и повреждений спинного мозга; метаболических и эндокринных заболеваний, таких как диабет, недостаточная или избыточная активность щитовидной железы и уремия; и системных расстройств, таких как амилоидоз, волчанка и склеродермия. Причиной запоров также может являться лечение некоторыми лекарственными средствами, включая анальгетики, такие как опиаты, антихолинергические средства, такие как спазмолитики, трициклические антидепрессанты, фенотиазолины и антимускариновые средства; антагонисты рецепторов серотонина; и кальций/алюминий-содержащие антацидные средства. Функциональный запор включает группу функциональных нарушений, которые проявляются в виде постоянно затрудненной, редкой или, как может показаться, неполной дефекации. Он наиболее распространен у женщин и обычно склонен усиливаться с возрастом. IBS включает группу функциональных расстройств кишечника, при которых боль и дискомфорт в области живота связаны с дефекацией или изменением функции кишечника и с признаками расстройства дефекации. IBS имеет хроническое рецидивирующее течение и накладывается на другие функциональные желудочно-кишечные расстройства. Это приводит к высоким затратам на непосредственное лечение и косвенным издержкам, включая невыход на работу. Симптомы, ассоциированные с запором, включают редкий стул, отсутствие позывов на стул, затрудненный для прохождения стул, неэффективные позывы, необходимость помогать пальцем, ощущение неполного опорожнения, боль в анусе или в промежности, выпадение из ануса и загрязнение белья. Вздутие живота (растяжение), боль и дискомфорт также являются симптомами запора. Когда симптомом запора является боль, она может быть вызвана различными факторами, включая сильные сокращения и растяжение кишечного тракта. Также вероятно существует взаимосвязь между распространяющимися высокоамплитудными сокращениями и болью у пациентов с запорами (Dig Dis Sci 36, 827-862, 1991). Иногда для облегчения такой боли применяют спазмолитики, так как считается, что они уменьшают сильные сокращения, связанные с болью (Pharmacol. Ther., 80, 49-98, 1998). Обнаружено, что антимускариновые соединения атропин (Digestive Diseases & Sciences 40 (6); 1381-7, 1995) и замифенацин (Aliment. Pharmacol. Ther., 11, 561-8, 1997) также уменьшают боль при запорах. Существующие в настоящее время режимы лечения запора включают: 1) пищевую клетчатку; 2) другие объемные слабительные, такие как псиллиум, метилцеллюлоза и поликарбофил кальция; 3) раствор полиэтиленгликоля (PEG); 4) стимулирующие слабительные, такие как бисакодил, пикосульфат натрия или сеннозиды; 5) агонисты 5-гидрокситриптомина 4 (5-НТ4), такие как прукалоприд; 6) клизмы и суппозитории и 7) хирургическое вмешательство, – но терапевтические результаты этих способов лечения часто разочаровывают и могут привести к неприятным побочным эффектам. Например, увеличение пищевой клетчатки часто не уменьшает запор и в некоторых случаях фактически ухудшает симптомы, например усиливая ощущение растяжения (Gut 27:41, 1986). Другие объемные слабительные часто оказываются неэффективны по той же причине, и в общем случае объемные слабительные подходят только для длительного применения и не годятся для быстрого облегчения при временном запоре. Применение растворов PEG может быть эффективным, но при этом обычно требуется выпивать большие объемы жидкости (приблизительно литр в день в течение до трех дней включительно), что, кроме того что является неприятным, совершенно неприемлемо для пациентов, например детей, которым затруднительно выпивать такие количества. Лечение стимулирующими слабительными средствами имеет множество зафиксированных побочных эффектов и может привести к зависимости от слабительных средств и к злоупотреблению. Агонисты 5-НТ4, кроме оказания необходимого воздействия на толстую кишку, могут влиять на опорожнение желудка и на тонкую кишку (Clinical Pharmacology & Therapeutics, 67:2 (PII-33), 2000), что приводит к диарее. Клизмы и свечи могут вызывать серьезное повреждение слизистой оболочки прямой кишки, кроме того, если для клизмы используют большие объемы воды, когда клизму удерживают, может возникать серьезная водная интоксикация. Хирургическое вмешательство, например колэктомия, может быть эффективно, но были зафиксированы случаи неудовлетворительных результатов, например требовалось дополнительное хирургическое вмешательство, запоры могли не прекращаться или развивалась диарея с недержанием. Также был зафиксирован слабительный эффект желчных кислот (Br.J. Surg. 1979; 66; 776-9; Gut. 1975, 16, 894-902; и Gut. 1973, 14, 348-353), и хотя для лечения запоров можно вводить желчные кислоты перорально (Myo Clinic Proceedings, 1973, 48, 356), они оказывают нежелательное воздействие на тонкий кишечник, усиливая его двигательную функцию, что потенциально может приводить к таким побочным эффектам как недостаточное всасывание питательных веществ. Несомненно, существует необходимость в установлении дополнительных средств лечения запоров, и предпочтительно более эффективных или имеющих меньшее количество побочных эффектов. В литературе описано множество ингибиторов IBAT (см. ниже), и они определены как полезные в лечении дислипидемических состояний и нарушений, например гиперлипидемии, и как полезные в предупреждении и лечении разных сердечно-сосудистых клинических состояний, например атеросклероза. Обоснованием для лечения дислипидемического состояния при помощи ингибиторов IBAT является то, что посредством усиления выведения желчных кислот и холестерина можно достичь благоприятного отрицательного холестеринового баланса и улучшения атерогенного липопротеинового профиля. Применение ингибитора IBAT для лечения желудочно-кишечных (GI) расстройств не предлагалось и не рассматривалось в литературе. Фактически, в некоторых сообщениях предполагалось, что терапевтическое лечение дислипидемии при помощи ингибитора IBAT на самом деле является причиной желудочно-кишечных проблем, например результаты клинического исследования, опубликованные Glaxo SmithKline (abstract, DALM September 2001), указывали на побочные эффекты для желудочно-кишечного тракта (диарею и спастические боли в животе) при применении ингибитора IBAT у человека. Настоящее изобретение касается нового лечения и/или профилактики запоров при помощи ингибитора IBAT. Это лечение и/или профилактика заключается в доставке желчных кислот в толстую кишку, где они действуют как эндогенные слабительные. Местная доставка в толстую кишку позволяет избежать побочных эффектов (подробно описанных выше), присущих пероральному приему желчных кислот, так как желчные кислоты не будут воздействовать на части желудочно-кишечного тракта, предшествующие толстой кишке. Как ожидается, возможность избежать воздействия на желудочно-кишечный тракт выше толстой кишки путем введения ингибитора IBAT также будет давать преимущества над лечением посредством уже существующих фармацевтических средств, таких как агонисты 5-НТ4. Кроме того, некоторые ингибиторы IBAT обладают очень низкой биодоступностью (<2%), в этом случае системное воздействие невысоко, что снижает риск побочных эффектов. Более того, ингибиторы IBAT могут облегчать болевые симптомы посредством вторичного механизма, аналогичного антимускариновым средствам. Облегчение боли происходит из-за того, что ингибиторы IBAT усиливают двигательную функцию кишечника и количество воды в содержимом нижней части кишечника. Это в свою очередь ведет к размягчению содержимого, которое легче движется и не накапливается, следовательно растяжение стенок кишечника уменьшается, а хорошо известно, что растяжение кишечного тракта вызывает боль. Кроме того, для продвижения более мягкого содержимого кишечника требуется меньше высокоамплитудных распространяющихся сокращений, так что опять чувствуется меньшая боль. Таким образом, настоящее изобретение включает применение ингибитора IBAT или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или его пролекарства в лечении и/или профилактике запоров. В данном описании при использовании термина “запор” подразумевается, что этот термин, если не указано иное, относится к функциональному запору и C-IBS (синдрому раздраженного кишечника с преобладанием запоров). В одном аспекте данного изобретения “запор” относится к функциональному запору. В другом аспекте изобретения “запор” относится к C-IBS. Один аспект данного изобретения относится к лечению запора. Другой аспект относится к профилактике запора. Третий аспект относится к лечению и профилактике запора. Следует понимать, что в одном аспекте изобретения, который относится к лечению запора, и где запор относится к C-IBS, он включает в себя чередующийся (запор-диарея) синдром раздраженной прямой кишки. Также, когда в описании используют термины “функциональный запор” и “C-IBS”, следует понимать, что они определены в соответствии с “Rome 2 Criteria” (Gut.45 (Suppl.2):43, 1999, II43-II47). В литературе ингибиторы IBAT часто упоминаются под разные названия. Следует понимать, что когда в описании упоминаются ингибиторы IBAT, этот термин также включает в себя соединения, известные в литературе как: 1) ингибиторы апикальных натрий-ко-зависимых транспортеров желчных кислот в подвздошной кишке (ASBT); 2) ингибиторы транспортеров желчных кислот (ВАТ); 3) ингибиторы системы ко-транспортеров натрия/желчных кислот в подвздошной кишке; 4) ингибиторы апикальных ко-транспортеров натрия-желчных кислот; 5) ингибиторы натрий-зависимого транспорта желчных кислот в подвздошной кишке; 6) ингибиторы реабсорбции желчных кислот (BARI 7) ингибиторы натрий-желчнокислотного транспортера (SBAT), где они действуют посредством ингибирования IBAT. Описаны подходящие соединения, обладающие ингибиторной активностью в отношении IBAT, смотри, например, соединения, описанные в WO 93/16055, WO 94/18183, WO 94/18184, WO 94/24087, WO 96/05188, WO 96/08484, WO 96/16051, WO 97/33882, WO 98/07749, WO 98/38182, WO 98/40375, WO 98/56757, WO 99/32478, WO 99/35135, WO 99/64409, WO 99/64410, WO 00/01687, WO 00/20392, WO 00/20393, WO 00/20410, WO 00/20437, WO 01/34570, WO 00/35889, WO 00/47568, WO 00/61568, WO 01/68637, WO 01/68096, WO 02/08211, WO 00/38725, WO 00/38726, WO 00/38727, WO 00/38728, WO 00/38729, DE 19825804, JP 10072371, US 5070103, EP 251315, EP 417725, EP 489423, EP 549967, EP 573848, EP 624593, EP 624594, EP 624595, EP 869121, EP 864582 и EP 1070703, и содержание данных патентных заявок, в частности соединения, описанные в п.1 формулы изобретения и указанные в названиях примеров, включены в данное описание изобретения посредством ссылки. Отдельными классами ингибиторов IBAT, пригодными для применения в настоящем изобретении, являются бензотиепины. Другими подходящими классами ингибиторов IBAT являются любые из следующих: 1,2-бензотиазепины, 1,4-бензотиазепины и 1,5-бензотиазепины. Еще одним подходящим классом ингибиторов IBAT являются 1,2,5-бензотиадиазепины. Одним конкретным подходящим соединением, обладающим ингибиторной активностью в отношении IBAT, является (3R,5R)-3-бутил-3-этил-1,1-диоксидо-5-фенил-2,3,4,5-тетрагидро-1,4-бензотиазепин-8-ил-D-глюкопиранозидуроновая кислота (EP 864582). Еще одним подходящим соединением, обладающим ингибиторной активностью в отношении IBAT, является S-8921 (EP 597107). Кроме того, подходящим ингибитором IBAT является соединение: Другими подходящими соединениями по изобретению являются ингибиторы IBAT, описанные в WO 01/66533. Конкретное соединение по изобретению выбрано из любого соединения Примеров 1-39 в WO 01/66533 или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или его пролекарства, и соединения Примеров 1-39 включены в данное описание изобретения посредством ссылки. Пункты 1-6 из WO 01/66533 также включены в данное описание изобретение посредством ссылки. Дополнительными подходящими соединениями по изобретению являются ингибиторы IBAT, описанные в WO 02/50051. Конкретное соединение по изобретению выбрано из любого соединения Примеров 1-120 в WO 02/50051 или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или его пролекарства, и соединения Примеров 1-120 включены в данное описание изобретения посредством ссылки. Пункты 1-14 из WO 02/50051 также включены в данное описание изобретения посредством ссылки. Конкретное соединение по изобретению, выбранное из WO 02/50051, выбрано из любого из следующих соединений: 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)-1 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-(N-{(R)-1 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{ 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-(N-{ 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-(N-{ 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-{N-[(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-{N-[(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-[(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-[N-{(R)- или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или пролекарства. Дополнительными подходящими соединениями по изобретению являются ингибиторы IBAT, описанные в WO 03/020710. Конкретное соединение по изобретению выбрано из любого соединения Примеров 1-44 в WO 03/020710 или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или пролекарства, и соединения Примеров 1-44 включены в данное описание изобретения посредством ссылки. Пункты 1-10 формулы изобретения из WO 03/020710 также включены в данное описание изобретения посредством ссылки. Конкретное соединение по изобретению, выбранное из WO 03/020710, выбрано из любого из следующих соединений: 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-[N-((R)- 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-[N-((R)- 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-[N-((R)- 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3-бутил-3-этил-5-фенил-7-метилтио-8-(N-{(R)- или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или пролекарства. Дополнительными подходящими соединениями по изобретению являются ингибиторы IBAT, описанные в WO 03/022825. Конкретное соединение по изобретению выбрано из любого соединения Примеров 1-7 в WO 03/022825 или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или его пролекарства, и соединения Примеров 1-7 включены в данное описание изобретения посредством ссылки. Пункты 1-8 формулы изобретения из WO 03/022825 также включены в данное описание изобретения посредством ссылки. Конкретное соединение по изобретению, выбранное из WO 03/022825, выбрано из любого из следующих соединений: 1,1-диоксо-3(R)-3-бутил-3-этил-5-(R)-5-фенил-8-[N-((R)- 1,1-диоксо-3(S)-3-бутил-3-этил-5-(S)-5-фенил-8-[N-((R)- 1,1-диоксо-3(R)-3-бутил-3-этил-5-(R)-5-фенил-8-(N-{(R)- 1,1-диоксо-3(S)-3-бутил-3-этил-5-(S)-5-фенил-8-(N-{(R)- 3,5-транс-1,1-диоксо-3-этил-3-бутил-5-фенил-7-бром-8-(N-{(R)- 3,5-транс-1,1-диоксо-3-(S)-3-этил-3-бутил-4-гидрокси-5-(S)-5-фенил-7-бром-8-(N-{(R)- 3,5-транс-1,1-диоксо-3-(R)-3-этил-3-бутил-4-гидрокси-5-(R)-5-фенил-7-бром-8-(N-{(R)-б-[N-(карбоксиметил)карбамоил]бензил}карбамоилметокси)-2,3,4,5-тетрагидро-1,4-бензотиазепина; 3,5-транс-1,1-диоксо-3-этил-3-бутил-5-фенил-7-метилтио-8-(N-{(R)- 3,5-транс-1,1-диоксо-3-этил-3-бутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3-(S)-3-этил-3-бутил-5-(S)-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3-(R)-3-этил-3-бутил-5-(R)-5-фенил-7-метилтио-8-(N-{(R)- или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или пролекарства. Дополнительными подходящими соединениями по изобретению являются ингибиторы IBAT, описанные в WO 03/022830. Конкретное соединение по изобретению выбрано из любого соединения Примеров 1-4 в WO 03/022830 или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или его пролекарства, и соединения Примеров 1-4 включены в данное описание изобретения посредством ссылки. Пункты 1-8 формулы изобретения из WO 03/022830 также включены в данное описание изобретения посредством ссылки. Конкретное соединение по изобретению, выбранное из WO 03/022830, выбрано из любого из следующих соединений: 1,1-диоксо-3-бутил-3-этил-4-гидрокси-5-фенил-7-(N-{(R)- 1,1-диоксо-3-бутил-3-этил-4-гидрокси-5-фенил-7-(N-{(R)- 1,1-диоксо-3-бутил-3-этил-4-гидрокси-5-фенил-7-{N-[ 1,1-диоксо-3-бутил-3-этил-4-гидрокси-5-фенил-7-{N-[1-(карбокси)-1-(тиен-2-ил)метил]карбамоилметилтио}-2,3,4,5-тетрагидробензотиепина или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или пролекарства. Дополнительными соединениями в заявке являются ингибиторы IBAT, описанные в WO 03/022286. Конкретное соединение по изобретению выбрано из любого из Примеров 1-39 в WO 03/022286 или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или пролекарства, и соединения Примеров 1-39 включены в данное описание изобретения посредством ссылки. Пункты 1-10 формулы изобретения из WO 03/022286 также включены в данное описание изобретения посредством ссылки. Конкретное соединение по изобретению, выбранное из WO 03/022286, выбрано из любого из следующих соединений: 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или пролекарства. Еще одним конкретным соединением по изобретению, выбранным из WO 03/022286, является соединение, выбранное из любого из следующих соединений: 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-[N-((R)- или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или пролекарства. Кроме того, подходящими ингибиторами IBAT являются ингибиторы, имеющие следующую структуру: где: Ry выбран из водорода или C1-6алкила; один из R1 и R2 выбран из водорода или С1-6алкила, и другой выбран из С1-6алкила; Rx и Ry независимо выбраны из водорода, гидрокси, амино, меркапто, С1-6алкила, С1-6алкокси, N-(С1-6алкил)амино, N,N-(С1-6алкил)2амино, С1-6алкилS(O)а, где а равно 0-2; Rz выбран из галогено, нитро, циано, гидрокси, амино, карбокси, карбамоила, меркапто, сульфамоила, C1-6алкила, С2-6алкенила, С2-6алкинила, C1-6алкокси, C1-6алканоила, C1-6алканоилокси, N-(C1-6алкил) амино, N,N-(C1-6алкил)2амино, C1-6алканоиламино, N-(С1-6алкил)карбамоила, N,N-(С1-6алкил)2карбамоила, С1-6алкилS(O)а, где а равно от 0 до 2, C1-6алкоксикарбонила, N-(С1-6алкил)сульфамоила и N,N-(С1-6алкил)сульфамоила; v равно 0-5; один из R4 и R5 является группой формулы (IA):
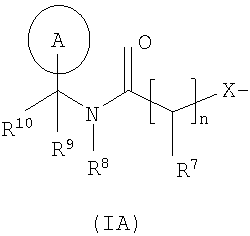
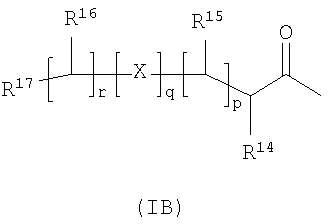
R3 и R6, и другой из R4 и R5 независимо выбраны из водорода, галогено, нитро, циано, гидрокси, амино, карбокси, карбамоила, меркапто, сульфамоила, С1-6алкила, С2-6алкенила, С2-6алкинила, C1-6алкокси, С1-6алканоила, C1-6алканоилокси, N-(С1-6алкил)амино. N,N-(С1-6алкил)2амино, C1-6алканоиламино, N-(С1-6алкил)карбамоила, N,N-(С1-6алкил)2карбамоила, С1-6алкилS(O)а, где а равно 0-2, С1-6алкоксикарбонила, N-(С1-6алкил)сульфамоила и N,N-(С1-6алкил)2сульфамоила; где R3 и R6 и другой из R4 и R5 возможно могут быть замещены по углероду одним или более R17; Х представляет собой -O-, -N(Ra)-, -S(O)b– или -CH(Ra)-; где Ra представляет собой водород или C1-6алкил и b равно 0-2; кольцо А представляет собой арил или гетероарил; где кольцо А возможно замещено по углероду одним или более заместителями, выбранными из R18; R7 представляет собой водород, C1-6алкил, карбоциклил или гетероциклил; где R7 возможно замещен по углероду одним или более заместителями, выбранными из R19; и где, если указанный гетероциклил содержит группу -NH-, азот этой группы возможно может быть замещен группой, выбранной из R20; R8 представляет собой водород или С1-6алкил; R9 представляет собой водород или С1-6алкил; R10 представляет собой водород, галогено, нитро, циано, гидрокси, амино, карбамоил, меркапто, сульфамоил, гидроксиаминокарбонил, С1-10алкил, С2-10алкенил, С2-10алкинил, С1-10алкокси, С1-10алканоил, С1-10алканоилокси, N-(С1-10алкил)амино, N,N-(С1-10алкил)2амино, N,N,N-(С1-10алкил)заммонио, С1-10алканоиламино, N-(С1-10алкил)карбамоил, N,N-(С1-6алкил)2карбамоил, С1-10алкилS(O)а, где а равно 0-2, N-(С1-10алкил)сульфамоил, N,N-(С1-10алкил)2сульфамоил, N-(С1-10алкил)сульфамоиламино, N,N-(С1-10алкил)2сульфамоиламино, С1-10алкоксикарбониламино, карбоксициклил, карбоксициклилС1-10алкил, гетероциклил, гетероциклилС1-10алкил, карбоциклил-(C1-10алкилен)p-R21-(C1-10алкилен)q– или гетероциклил-(C1-10алкилен)r-R22-(C1-10алкилен)s-; где R10 возможно замещен по углероду одним или более заместителями, выбранными из R23; и где, если указанный гетероциклил содержит группу -NH-, азот этой группы возможно может быть замещен группой, выбранной из R24; или R10 представляет собой группу формулы (IB):
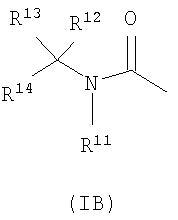
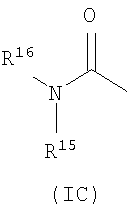
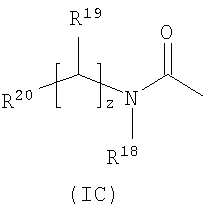
где: R11 представляет собой водород или C1-6алкил; R12 и R13 независимо выбраны из водорода, галогено, карбамоила, сульфамоила, С1-10алкила, С2-10алкенила, С2-10алкинила, С1-10алканоила, N-(С1-10алкил)карбамоила, N,N-(С1-10алкил)2карбамоила, С1-10алкилS(O)а, где а равно 0-2, N-(С1-10алкил)сульфамоила, N,N-(С1-10алкил)2сульфамоила, N-(С1-10алкил)сульфамоиламино, N,N-(С1-10алкил)2сульфамоиламино, карбоциклила или гетероциклила; где R12 и R13 независимо возможно могут быть замещены по углероду одним или более заместителями, выбранными из R25; и где, если указанный гетероциклил содержит группу -NH-, азот этой группы возможно может быть замещен группой, выбранной из R26; R14 выбран из водорода, галогено, карбамоила, сульфамоила, гидроксиаминокарбонила, С1-10алкила, С2-10алкенила, С2-10алкинила, С1-10алканоила, N-(С1-10алкил)карбамоила, N,N-(С1-10алкил)2карбамоила, С1-10алкилS(O)а, где а равно 0-2, N-(С1-10алкил)сульфамоила, N,N-(С1-10алкил)2сульфамоила, N-(С1-10алкил)сульфамоиламино, N,N-(С1-10алкил)2сульфамоиламино, карбоциклила, карбоциклилС1-10алкила, гетероциклила, гетероциклилС1-10алкила, карбоциклил-(C1-10алкилен)p-R27-(C1-10алкилен)q– или гетероциклил-(C1-10алкилен)r-R28-(C1-10алкилен)s-; где R14 возможно может быть замещен по углероду одним или более заместителями, выбранными из R29; и где, если указанный гетероциклил содержит группу -NH-, азот этой группы возможно может быть замещен группой, выбранной из R30; или R14 представляет собой группу формулы (IC):
R15 представляет собой водород или С1-6алкил; и R16 представляет собой водород или C1-6алкил; где R16 возможно может быть замещен по углероду одной или более группами, выбранными из R31; или R15 и R16 вместе с азотом, к которому они присоединены, образуют гетероциклил; где указанный гетероциклил возможно может быть замещен по углероду одним или более R37; и где, если указанный гетероциклил содержит группу -NH-, азот этой группы возможно может быть замещен группой, выбранной из R38; n равно 1-3; где значения R7 могут быть одинаковыми или разными. R17, R18, R19, R23, R25, R29, R31 и R37 независимо выбраны из галогено, нитро, циано, гидрокси, амино, карбамоила, меркапто, сульфамоила, гидроксиаминокарбонила, С1-10алкила, С2-10алкенила, С2-10алкинила, С1-10алкокси, С1-10алканоила, С1-10алканоилокси, N-(С1-10алкил)амино, N,N-(С1-10алкил)2амино, N,N,N-(С1-10алкил)3аммонио, С1-10алканоиламино, N-(С1-10алкил)карбамоила, N,N-(С1-10алкил)2карбамоила, С1-10алкилS(O)а, где а равно 0-2, N-(С1-10алкил)сульфамоила, N,N-(С1-10алкил)2сульфамоила, N-(С1-10алкил)сульфамоиламино, N,N-(С1-10алкил)2сульфамоиламино, С1-10алкоксикарбониламино, карбоциклила, карбоциклилС1-10алкила, гетероциклила, гетероциклилС1-10алкила, карбоциклил-(C1-10алкилен)p-R32-(C1-10алкилен)q– или гетероциклил-(C1-10алкилен)r-RЗЗ-(C1-10алкилен)s-; где R17, R18, R19, R23, R25, R29, R31 и R37 могут быть независимо возможно замещены по углероду одним или более R34; и где, если указанный гетероциклил содержит группу -NH-, азот этой группы возможно может быть замещен группой, выбранной из R35; R21, R22, R27, R28, R32 или R33 независимо выбраны из -O-, -NR36-, -S(O)x-, -NR36C(O)NR36-, -NR36C(S)NR36-, -OC(O)N=C-, -NR36C(O)-or-C(O)NR36-; где R36 выбран из водорода или C1-6алкила, и х равно 0-2; p, q, r и s независимо выбраны из 0-2; R34 выбран из галогено, гидрокси, циано, карбамоила, уреидо, амино, нитро, карбамоила, меркапто, сульфамоила, трифторметила, трифторметокси, метила, этила, метокси, этокси, винила, аллила, этинила, формила, ацетила, формамидо, ацетиламино, ацетокси, метиламино, диметиламино, N-метилкарбамоила, N,N-диметилкарбамоила, метилтио, метилсульфинила, мезила, N-метилсульфамоила, N,N-диметилсульфамоила, N-метилсульфамоиламино и N,N-диметилсульфамоиламино; R20, R24, R26, R30, R35 и R38 независимо выбраны из С1-6алкила, C1-6алканоила, С1-6алкилсульфонила, С1-6алкоксикарбонила, карбамоила, N-(С1-6алкил)карбамоила, N,N-(С1-6алкил)карбамоила, бензила, бензилоксикарбонила, бензоила и фенилсульфонила; или их фармацевтически приемлемая соль, сольват, сольват такой соли или пролекарство. Подходящие ингибиторы IBAT, имеющие приведенную выше структуру, выбраны из любого из следующих соединений: 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-[N-((R/S)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-{N-[(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-[N-((R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или пролекарства. Кроме того, подходящими ингибиторами IBAT являются ингибиторы, имеющие следующую структуру: где: R1 и R2 независимо выбраны из С1-4алкила; R3 представляет собой водород, гидрокси или галогено; R4 представляет собой С1-4алкил, возможно замещенный гидрокси, метокси и метилS(O)а, где а равно 0-2; R5 представляет собой гидрокси или НОС(O)CH(R6)NH-; R6 выбран из водорода и C1-3алкила, возможно замещенного гидрокси, метокси и метилS(O)а, где а равно 0-2; или их фармацевтически приемлемая соль, сольват, сольват такой соли или пролекарство; при условии что, когда R1 и R2 оба представляют собой бутил, R5 представляет собой гидрокси, и R4 представляет собой метилтиометил, метилсульфинилметил, 2-метилтиоэтил, гидроксиметил, метоксиметил; тогда R3 не является водородом; и при условии что, когда R1 и R2 оба представляют собой бутил, R5 представляет собой НОС(O)CH(R6)NH-, R6 представляет собой гидроксиметил, и R4 представляет собой гидроксиметил; тогда R3 не является водородом. Подходящие ингибиторы IBAT, имеющие указанную выше структуру, выбраны из любого из следующих соединений: 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или пролекарства. Дополнительные подходящие ингибиторы IBAT, имеющие указанную выше структуру, выбраны из: 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- Кроме того, подходящими ингибиторами IBAT являются ингибиторы, имеющие структуру:
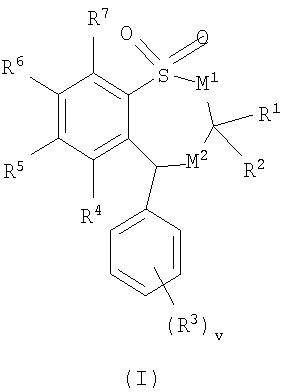
где М1 представляет собой -СН2– или -NR21-; М2 представляет собой -CR22R23– или -NR24-; при условии что, если М1 представляет собой -NR21-, то М2 представляет собой -CR22R23-; Один из R1 и R2 выбран из водорода, С1-6алкила или C2-6алкенила, а другой выбран из C1-6алкила или С2-6алкенила; R3 выбран из галогено, нитро, циано, гидрокси, амино, карбокси, карбамоила, меркапто, сульфамоила, C1-6алкила, С2-6алкенила, С2-6алкинила, C1-6алкокси, C1-6алканоила, С1-6алканоилокси, N-(С1-6алкил)амино, N,N-(С1-6алкил)2амино, С1-6алканоиламино, N-(С1-6алкил)карбамоила, N,N-(С1-6алкил)2карбамоила, С1-6алкилS(O)а, где а равно 0-2, C1-6алкоксикарбонила, N-(С1-6алкил)сульфамоила и N,N-(С1-6алкил)2сульфамоила; v равно 0-5; один из R5 и R6 представляет собой группу формулы (IA):
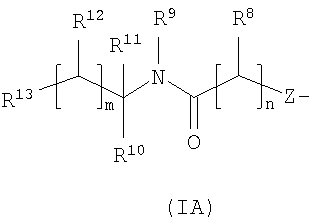
R4 и R7 и другой из R5 и R6 независимо выбраны из водорода, галогено, нитро, циано, гидрокси, амино, карбокси, карбамоила, меркапто, сульфамоила, С1-4алкила, С2-4алкенила, С2-4алкинила, С1-4алкокси, С1-4алканоила, С1-4алканоилокси, N-(С1-4алкил)амино, N,N-(С1-4алкил)2амино, С1-4алканоиламино, N-(С1-4алкил)карбамоила, N,N-(С1-4алкил)2карбамоила, С1-4алкилS(O)а, где а равно 0-2, С1-4алкоксикарбонила, N-(С1-4алкил)сульфамоила и N,N-(С1-4алкил)2сульфамоила; где R4 и R7 и другой из R5 и R6 возможно может быть замещен по углероду одним или более R25; Z представляет собой -O-, -N(Ra)-, -S(O)b– или -СН(Ra)-; где Ra является водородом или C1-6алкилом, и b равно 0-2; R8 представляет собой водород, С1-4алкил, карбоциклил или гетероциклил; где R8 возможно может быть замещен по углероду одним или более заместителями, выбранными из R26; и где, если указанный гетероциклил содержит группу -NH-, азот этой группы возможно может быть замещен группой, выбранной из R27; R9 представляет собой водород или С1-4алкил; R10 и R11 независимо выбраны из водорода, С1-4алкила, карбоциклила или гетероциклила; или R10 и R11 вместе образуют С2-6алкилен; где R10 и R11 или R10 и R11 вместе могут быть независимо возможно замещены по углероду одним или более заместителями, выбранными из R28; и где, если указанный гетероциклил содержит группировку -NH-, азот этой группировки возможно может быть замещен одним или более R29; R12 представляет собой водород, С1-4алкил, карбоциклил или гетероциклил; где R12 возможно может быть замещен по углероду одним или более заместителями, выбранными из R30; и где, если указанный гетероциклил содержит группировку -NH-, азот этой группировки возможно может быть замещен одним или более R31; R13 представляет собой водород, галогено, нитро, циано, гидрокси, амино, карбамоил, меркапто, сульфамоил, гидроксиаминокарбонил, С1-10алкил, С2-10алкенил, С2-10алкинил, С1-10алкокси, С1-10алкоксикарбонил, С1-10алканоил, С1-10алканоилокси, N-(С1-10алкил)амино, N,N-(С1-10алкил)2амино, N,N,N-(C1-10алкил)3аммонио, С1-10алканоиламино, N,N-(С1-10алкил)карбамоил, N,N-(С1-10алкил)2карбамоил, С1-10алкилS(O)а, где а равно 0-2, N-(С1-10алкил)сульфамоил, N,N-(С1-10алкил)2сульфамоил, N-(С1-10алкил)сульфамоиламино, N,N-(С1-10алкил)2сульфамоиламино, С1-10алкоксикарбониламино, карбоциклил, карбоциклилС1–10алкил, гетероциклическую группу, гетероциклилС1-10алкил, карбоциклил-(C1-10алкилен)e-R32-(C1-10алкилен)f– или гетероциклил-(С1-10алкилен)g-R33-(С1-10алкилен)h-; где R13 возможно может быть замещен по углероду одним или более заместителями, выбранными из R36; и где, если указанный гетероциклил содержит группу -NH-, азот этой группы возможно может быть замещен группой, выбранной из R37; или R13 представляет собой группу формулы (IB):
где: X представляет собой -N(R38)-, -N(R38)C(O)-, -О- и -S(O)a-, где а равно 0-2, и R38 представляет собой водород или С1-14алкил; R14 представляет собой водород или С1-14алкил; R15 и R16 независимо выбраны из водорода, галогено, нитро, циано, гидрокси, амино, карбамоила, меркапто, сульфамоила, C1-6алкила, С2-6алкенила, С2-6алкинила, C1-6алкокси, С1-6алканоила, С1-6алканоилокси, N-(С1-6алкил)амино, N,N-(С1-6алкил)2амино, C1-6алканоиламино, N-(С1-6алкил)карбамоила, N,N-(С1-6алкил)2карбамоила, С1-6алкилS(O)а, где а равно 0-2, C1-6алкоксикарбонила, N-(С1-6алкил)сульфамоила, N,N-(С1-6алкил)2сульфамоила, карбоциклила или гетероциклической группы;, где R15 и R16 могут быть независимо возможно замещены по углероду одним или более заместителями, выбранными из R41; и где, если указанный гетероциклил содержит группу -NH-, азот этой группы возможно может быть замещен группой, выбранной из R42; R17 выбран из водорода, галогено, нитро, циано, гидрокси, амино, карбамоила, меркапто, сульфамоила, гидроксиаминокарбонила, С1-10алкила, С2-10алкенила, С2-10алкинила, С1-10алкокси, С1-10алканоила, С1-10алканоилокси, N-(С1-10алкил)амино, N,N-(С1-10алкил)2амино, С1-10алканоиламино, N-(С1-10алкил)карбамоила, С1-10алкоксикарбонила, N,N-(С1-10алкил)2карбамоил, С1-10алкилS(O)а, где а равно 0-2, N-(С1-10алкил)сульфамоила, N,N-(С1-10алкил)2сульфамоила, N-(С1-10алкил)сульфамоиламино, N,N-(С1-10алкил)2сульфамоиламино, карбоциклила, карбоциклилС1-10алкила, гетероциклической группы, гетероциклилС1-10алкила, карбоциклил-(C1-10алкилен)e-R43-(C1-10алкилен)f– или гетероциклил-(C1-10алкилен)g-R44-(C1-10алкилен)h-; где R17 возможно может быть замещен по углероду одним или более заместителями, выбранными из R47; и где, если указанный гетероциклил содержит группу -NH-, азот этой группы возможно может быть замещен группой, выбранной из R48; или R17 представляет собой группу в формуле (IC):
где: R18 выбран из водорода или С1-4алкила; R19 выбран из водорода, галогено, нитро, циано, гидрокси, амино, карбамоила, меркапто, сульфамоила, С1-6алкила, С2-6алкенила, С2-6алкинила, C1-6алкокси, C1-6алканоила, C1-6алканоилокси, N-(С1-6алкил)амино, N,N-(С1-6алкил)2амино, С1-6алканоиламино, N-(С1-6алкил)карбамоила, N,N-(С1-6алкил)2карбамоила, С1-6алкилS(O)а, где а равно 0-2, С1-6алкоксикарбонила, N-(С1-6алкил)сульфамоила, N,N-(С1-6алкил)2сульфамоила, карбоциклила или гетероциклической группы; где R19 может быть независимо возможно замещен по углероду одним или более заместителями, выбранными из R51; и где, если указанный гетероциклил содержит группу -NH-, азот этой группы возможно может быть замещен группой, выбранной из R52; R20 выбран из галогено, нитро, циано, гидрокси, амино, карбамоила, меркапто, сульфамоила, гидроксиаминокарбонила, С1-10алкила, С2-10алкенила, С2-10алкинила, С1-10алкокси, С1-10алкоксикарбонила, С1-10алканоила, С1-10алканоилокси, N-(С1-10алкил)амино, N,N-(С1-10алкил)2амино, N,N,N-(С1-10алкил)3аммонио, С1-10алканоиламино, N-(С1-10алкил)карбамоила, N,N-(С1-10алкил)2карбамоила, С1-10алкилS(O)а, где а равно 0-2, N-(С1-10алкил)сульфамоила, N,N-(С1-10алкил)2сульфамоила, N-(С1-10алкил)сульфамоиламино, N,N-(С1-10алкил)2сульфамоиламино, C1-10алкоксикарбониламино, карбоциклила, карбоциклилС1-10алкила, гетероциклической группы, гетероциклилС1-10алкила, карбоциклил-(C1-10алкилен)e-R53-(C1-10алкилен)f– или гетероциклил-(С1-10алкилен)g-R54-(C1-10алкилен)h-; где R20 может быть независимо возможно замещен по углероду одним или более R57; и где, если указанный гетероциклил содержит группу -NH-, то азот этой группы возможно может быть замещен группой, выбранной из R58; р равно 1-3; где значения R15 могут быть одинаковыми или разными; q равно 0-1; r равно 0-3; где значения R16 могут быть одинаковыми или разными; m равно 0-2; где значения R12 могут быть одинаковыми или разными; n равно 1-2; где значения R8 могут быть одинаковыми или разными; z равно 0-3; где значения R19 могут быть одинаковыми или разными; R21 выбран из водорода или C1-6алкила; R22 и R23 независимо выбраны из водорода, гидрокси, амино, меркапто, C1-6алкила, С1-6алкокси, N-(С1-6алкил)амино, N,N-(С1-6алкил)2амино, С1-6алкилS(O)а, где а равно 0-2; R24 выбран из водорода, гидрокси, С1-6алкила, C1-6алкокси и C1-6алканоилокси; R25 выбран из галогено, нитро, циано, гидрокси, амино, карбокси, карбамоила, меркапто, сульфамоила, С1-4алкила, С2-4алкенила, С2-4алкинила, С1-4алкокси, С1-4алканоила, С1-4алканоилокси, N-(С1-4алкил)амино, N,N-(С1-4алкил)2амино, С1-4алканоиламино, N-(С1-4алкил)карбамоила, N,N-(С1-4алкил)2карбамоила, С1-4алкилS(O)а, где а равно 0-2, С1-4алкоксикарбонила, N-(С1-4алкил)сульфамоила и N,N-(С1-4алкил)2сульфамоила; где R25 может быть независимо возможно замещен по углероду одним или более R67; R26, R28, R30, R36, R41, R47, R51 и R57 независимо выбраны из галогено, нитро, циано, гидрокси, амино, карбамоила, меркапто, сульфамоила, гидроксиаминокарбонила, С1-10алкила, С2-10алкенила, С2-10алкинила, С1-10алкокси, С1-10алканоила, С1-10алканоилокси, С1-10алкоксикарбонила, N-(С1-10алкил)амино, N,N-(С1-10алкил)2амино, N,N,N-(С1-10алкил)3аммонио, C1-10алканоиламино, N-(С1-10алкил)карбамоила, N,N-(С1-10алкил)2карбамоила, С1-10алкилS(O)а, где а равно 0-2, N-(С1-10алкил)сульфамоила, N,N-(С1-10алкил)2сульфамоила, N-(С1-10алкил)сульфамоиламино, N,N-(С1-10алкил)2сульфамоиламино, C1-10алкоксикарбониламино, карбоциклила, карбоциклилС1-10алкила, гетероциклической группы, гетероциклилС1-10алкила, карбоциклил-(С1-10алкилен)е-R59-(C1-10алкилен)f– или гетероциклил-(C1-10алкилен)g-R60-(C1-10алкилен)h-; где R26, R28, R30, R36, R41, R47, R51 и R57 могут быть независимо возможно замещены по углероду одним или более R63; и где, если указанный гетероциклил содержит группу -NH-, азот этой группы возможно может быть замещен группой, выбранной из R64; R27, R29, R31, R37, R42, R48, R52, R58 и R64 независимо выбраны из С1-6алкила, C1-6алканоила, C1-6алкилсульфонила, сульфамоила, N-(С1-6алкил)сульфамоила, N,N-(С1-6алкил)2сульфамоила, С1-6алкоксикарбонила, карбамоила, N-(С1-6алкил)карбамоила, N,N-(С1-6алкил)2карбамоила, бензила, фенетила, бензоила, фенилсульфонила и фенила; R32, R33, R43, R44. R53, R54, R59 и R60 независимо выбраны из -O-, -NR65-, -S(O)x-, -NR65C(O)NR66-, -NR65C(S)NR66-, -OC(O)N=C-, -NR65C(O)-or-C(O)NR65-; где R65 и R66 независимо выбраны из водорода или С1-6алкила, и х равно 0-2; R63 and R67 независимо выбраны из галогено, гидрокси, циано, карбамоила, уреидо, амино, нитро, карбамоила, меркапто, сульфамоила, трифторметила, трифторметокси, метила, этила, метокси, этокси, винила, аллила, этинила, метоксикарбонила, формила, ацетила, формамидо, ацетиламино, ацетокси, метиламине, диметиламино, N-метилкарбамоила, N,N-диметилкарбамоила, метилтио, метилсульфинила, мезила, N-метилсульфамоила и N,N-диметилсульфамоила; и е, f, g и h независимо выбраны из 0-2; или их фармацевтически приемлемая соль, сольват, сольват такой соли или пролекарство. Дополнительными подходящими ингибиторами IBAT, имеющими приведенную выше структуру, выбраны из любого из следующих соединений: (+/-)-транс-1,1-диоксо-3-этил-3-бутил-5-фенил-7-метилтио-8-(N-{(R)- (+/-)-транс-1,1-диоксо-3-этил-3-бутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3-этил-3-бутил-4-гидрокси-5-фенил-7-(N-{ 1,1-диоксо-3-этил-3-бутил-4-гидрокси-5-фенил-7-(N-{1-[N В конкретном аспекте изобретения ингибитор IBAT или его фармацевтически приемлемая соль, сольват, сольват такой соли или пролекарство является ингибитором IBAT или его фармацевтически приемлемой солью. Подходящие фармацевтически приемлемые соли вышеуказанных соединений представляют собой, например, соль присоединения кислоты к соединению по изобретению, являющемуся достаточно основным, например солью присоединения, например, неорганической или органической кислоты, например соляной, бромисто-водородной, серной, фосфорной, трифторуксусной, лимонной, уксусной или малеиновой кислоты. Кроме того, подходящей фармацевтически приемлемой солью соединения, являющегося достаточно кислым, является соль щелочного металла, например соль натрия или калия, соль щелочноземельного металла, например соль кальция или магния, соль аммония или соль органического основания, которое представляет физиологически приемлемый катион, например соль метиламина, диметиламина, триметиламина, пиперидина, морфолина или трис(2-гидроксиэтил)амина. Соединения можно вводить в форме пролекарства, которое расщепляется в организме человека или животного с образованием родительского соединения. Примеры пролекарств включают in vivo гидролизуемые эфиры и in vivo гидролизуемые амиды. In vivo гидролизуемый эфир соединения, содержащего карбоксильную или гидроксильную группу, представляет собой, например, фармацевтически приемлемый эфир, который гидролизуется в организме человека или животного с образованием родительской кислоты или спирта. Подходящие фармацевтически приемлемые эфиры для карбоксигруппы включают C1-6алкоксиметиловые эфиры, например метоксиметил, C1-6алканоилоксиметиловые эфиры, например пивалоилоксиметил, фталидиловые эфиры, С3-8циклоалкоксикарбонилоксиС1-6алкиловые эфиры, например 1-циклогексилкарбонилоксиэтил; 1,3-диоксолен-2-онилметиловые эфиры, например 5-метил-1,3-диоксолен-2-онилметил; и С1-6алкоксикарбонилоксиэтиловые эфиры, например 1-метоксикарбонилоксиэтил, и могут быть образованы с любой карбоксильной группой в соединениях. In vivo гидролизуемый эфир соединения, содержащего гидроксигруппу, включает неорганические эфиры, такие как фосфатные эфиры и Подходящим in vivo гидролизуемым амидом соединения, содержащего карбоксигруппу, является, например, N-C1-6алкил или N,N-ди-С1-6алкиламид, такой как N-метил, N-этил, N-пропил, N,N-диметил, N-этил-N-метил или N,N-диэтиламид. Экспериментальная часть Как утверждалось выше в описании, соединения, описанные в настоящем изобретении, полезны в лечении функциональных запоров и C-IBS. Эти свойства можно оценить, например, используя модели, применяемые в данной области: Buenos модель запора на собаках (Hepato-gasteroenterology, 1980, 27, 381-389). При этом собак для того, чтобы вызвать запор, содержат на диете с низким содержанием клетчатки/высоким содержанием белка; Niwa модель запора, вызванного морфием (Bioscience Biotechnology and Biochemistry, 2002, 66, 6, 1233-1240); и удаление слепой кишки у крыс, которое также, как было показано, вызывает запор. После того, как вызван запор, животным можно ввести дозу ингибитора IBAT, чтобы оценить способность ингибитора IBAT облегчать запор. Следующие данные были получены с использованием Buenos модели на собаках (метод, описанный в указанной выше публикации) с тем изменением, что собаки получали 20 г мяса/кг массы/сутки. Результат рассчитывают как среднее значение увеличения количества фекалий в течение трех суток лечения за вычетом начального значения (за сутки перед началом лечения ингибитором IBAT). У собак признавался запор, если количество фекалий за сутки составляло менее 30 граммов.
Данные, полученные при использовании Buenos модели запора на собаках, показывают, что исследованные ингибиторы IBAT в данной модели могут реверсировать запор. Количество фекалий каждой собаки увеличивалось после лечения соединением 1, соединением 2 и соединением 3 на 38±7, 23±11 и 39±2 г/сутки соответственно. Таким образом, в еще одном аспекте изобретения предложена фармацевтическая композиция, содержащая ингибитор IBAT или его фармацевтически приемлемую соль, сольват, сольват такой соли или пролекарство в сочетании с фармацевтически приемлемым разбавителем или носителем для применения в лечении и/или профилактике запора. Фармацевтические композиции могут находится в форме, пригодной для перорального введения, например в виде таблетки или капсулы, для парентеральной инъекции (включая внутривенную, подкожную, внутримышечную, внутрисосудистую или инфузию) в виде стерильного раствора, суспензии или эмульсии, для местного введения в виде мази или крема или для ректального введения в виде суппозитория. В общем случае указанные выше композиции могут быть изготовлены обычным образом с использованием традиционных эксципиентов. Согласно еще одному аспекту изобретения предложено применение ингибитора IBAT или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или пролекарства в изготовлении лекарства для применения в лечении и/или профилактике запора у теплокровного животного, такого как человек. Следовательно, согласно настоящему изобретению предложен способ лечения и/или профилактики запора у теплокровного животного, такого как человек, нуждающегося в таком лечении и/или профилактике, включающий введение указанному животному эффективного количества ингибитора IBAT или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или пролекарства. В другом аспекте изобретения предлагается использование ингибитора IBAT или его фармацевтически приемлемой соли, сольвата, сольвата такой соли или пролекарства в лечении и/или профилактике запора у теплокровного животного, такого как человек. Ингибитор IBAT или его фармацевтически приемлемая соль, сольват, сольват такой соли или пролекарство обычно вводят теплокровному животному в разовой дозе в интервале 0,5-5000 мг на квадратный метр поверхности тела животного, т.е. приблизительно 0,001-50 мг/кг, и это количество, как ожидается, должно обеспечивать терапевтически эффективную дозу. Разовая доза из такой таблетки или капсулы обычно будет составлять, например, 0,05-250 мг активного ингредиента. В одном аспекте изобретения применяют суточную дозу в интервале 0,01-50 мг/кг. Однако суточная доза неизбежно будет меняться в зависимости от организма, который лечат, конкретного пути введения и тяжести заболевания, которое лечат. Соответственно, оптимальная дозировка может быть определена врачом, лечащим любого конкретного пациента.
Формула изобретения
1. Применение ингибитора IBAT (транспорта желчных кислот в подвздошной кишке), выбранного из 1,2,5-бензотиадиазепинов, в лечении и/или профилактике запора у теплокровного животного, такого как человек. 2. Применение по п.1, где запор представляет собой функциональный запор. 3. Применение по п.1, где запор представляет собой синдром раздраженного кишечника с преобладанием запоров. 4. Применение по п.1, где ингибитор IBAT выбран из: 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-металтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(-{N{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- или их фармацевтически приемлемой соли, сольвата, сольвата такой соли, или их гидролизуемых эфиров и гидролизуемых амидов. 5. Фармацевтическая композиция, содержащая ингибитор IBAT, выбранный из 1,2,5-бензотиадиазепинов, в сочетании с фармацевтически приемлемым разбавителем или носителем, для применения в лечении и/или профилактике запора. 6. Фармацевтическая композиция по п.5, где запор представляет собой функциональный запор. 7. Фармацевтическая композиция по п.5, где запор представляет собой синдром раздраженного кишечника с преобладанием запоров. 8. Фармацевтическая композиция по п.5, где ингибитор IBAT выбран из: 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- или их фармацевтически приемлемой соли, сольвата, сольвата такой соли, или их гидролизуемых эфиров и гидролизуемых амидов. 9. Применение ингибитора IBAT, выбранного из 1,2,5-бензотиадиазепинов, в изготовлении лекарства для применения в лечении и/или профилактике запора у теплокровного животного, такого как человек. 10. Применение по п.9, где запор представляет собой функциональный запор. 11. Применение по п.9, где запор представляет собой синдром раздраженного кишечника с преобладанием запоров. 12. Применение по п.9, где ингибитор IBAN выбран из 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- или их фармацевтически приемлемой соли, сольвата, сольвата такой соли, или их гидролизуемых эфиров и гидролизуемых амидов. 13. Способ лечения и/или профилактики запора у теплокровного животного, такого как человек, нуждающегося в таком лечении и/или профилактике, включающий введение указанному животному эффективного количества ингибитора IBAT, выбранного из 1,2,5-бензотиадиазепинов. 14. Способ по п.13, где запор представляет собой функциональный запор. 15. Способ по п.13, где запор представляет собой синдром раздраженного кишечника с преобладанием запоров. 16. Способ по п.13, где ингибитор IBAT выбран из 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- 1,1-диоксо-3,3-дибутил-5-фенил-7-метилтио-8-(N-{(R)- или их фармацевтически приемлемой соли, сольвата, сольвата такой соли, или их гидролизуемых эфиров и гидролизуемых амидов.
TK4A – Поправки к публикациям сведений об изобретениях в бюллетенях “Изобретения (заявки и патенты)” и “Изобретения. Полезные модели”
Напечатано: (57) 4. …1,1-диоксо- …-8-(N-{(R)-
Следует читать: (57) 4. …1,1-диоксо- …-8-(N-{(R)-
Номер и год публикации бюллетеня: 1-2009
Код раздела: FG4A
Извещение опубликовано: 10.05.2009 БИ: 13/2009
TK4A – Поправки к публикациям сведений об изобретениях в бюллетенях “Изобретения (заявки и патенты)” и “Изобретения. Полезные модели”
Напечатано: 12. …1,1-диоксо-… -1-[N-((8)-2-гидрокси-…
Следует читать: 12. …1,1-диоксо-… -1-[N-((S)-2-гидрокси-…
Номер и год публикации бюллетеня: 1-2009
Код раздела: FG4A
Извещение опубликовано: 10.05.2009 БИ: 13/2009
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 s); и
s); и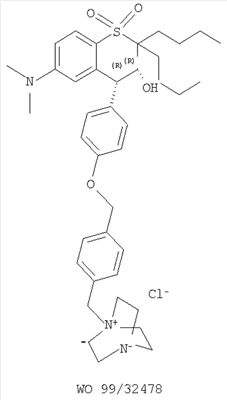
 -фенил-1
-фенил-1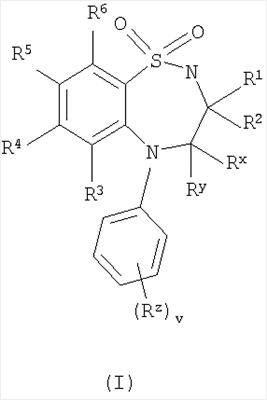

 0,01
0,01