Патент на изобретение №2342370
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ N-[1′,3′,5′-ДИТИАЗИНАН-5′-ИЛ-КАРБОНИЛ]-1,3,5-ДИТИАЗИНАН-5-КАРБОКСАМИДА
(57) Реферат:
Настоящее изобретение относится к способу получения N-[1
Предлагаемое изобретение относится к области органической химии, а именно к способу синтеза N-[1
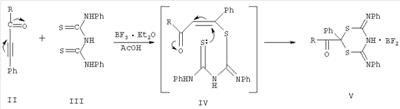
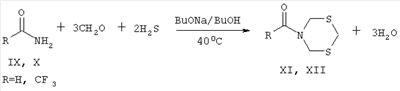
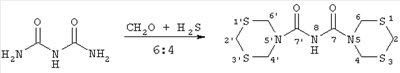
Представленное соединение может найти применение в качестве модифицированного селективного сорбента благородных и драгоценных металлов [Муринов Ю.И., Майстренко В.Н., Афзалетдинова Н.Г., Экстракция металлов S,N-органическими соединениями, М., Наука, 1993, с 192]. Синтез N-[1 Известно, что гетероциклизация на основе 1-ароил-2-фенилацетиленов (II, III) и 1,5-дифенил-2,4-дитиобиурета проходит с образованием 1,3,5-дитиазина (V). В среде ледяной АсОН в присутствии эквимольного количества BF3·Et2О при 20°С 1-бензоил- и 1-(2-теноил)-2-фенилацетилены (II, III) взаимодействуют с 1,5-дифенил-2,4-дитиобиуретом (III) с образованием трифторборатов 2-ароилметил-2-фенил-4,6-бис(фенилимино)-5Н-1,3,5-дитиазиния (V) с хорошими выходами [Глотова Т.Е., Процук Н.И., Албанов А.И. и др., Синтез новых производных 1,3,5-дитиазинана, ЖОХ, 2003, Т.73, Вып.5, с 834-838]. В литературе описана реакция тиометилирования бифункционального этилендиамина (VI) с селективным образованием преимущественно 5-(1,3,5-дитиазин-5-ил)-этил-1,3,5-дитиазина (VII), содержание которого в реакционной смеси при 80°С составляет 90%, наряду с тиазетидином (VIII) при смешении диамина с формальдегидом и последующим барботированием реакционной смеси сероводородом [С.Р.Хафизова, В.Р.Ахметова, Т.В.Тюмкина и др., Известия АН, сер. хим., 2005, №2, с 423-427]. Из литературных данных известно, что алифатические амиды (IX, Х) вступают в реакцию тиометилирования в присутствии раствора бутилата натрия в бутаноле с образованием N-ацил-1,3,5-дитиазинанов (XI, XII) [В.Р.Ахметова, P.P.Хайруллина, С.Р.Хафизова и др., Патент РФ 2291150 (20.01.2007), Б.И. №1]. Перечисленными выше способами не может быть получен N-[1 Задачей изобретения является получение N-[1 Синтез осуществляют взаимодействием водного или спиртового раствора карбамилмочевины со смесью сероводород-формалин (37%) при мольном соотношении карбамилмочевина:формальдегид:сероводород = 1:6:4, температуре 40-80°С и постоянном перемешивании в течение 6 часов. Образуется N-[1 Преимущества предлагаемого способа: На основании предложенного способа можно селективно получать N-[1 : ПРИМЕР 1. В стеклянный реактор, снабженный магнитной мешалкой, обратным холодильником, газопроводящей трубкой и капельной воронкой, при температуре 40°С помещают 6 молей формальдегида (4.31 мл. 37%-ного водного раствора), барботированием насыщают раствор формальдегида сероводородом в течение 30 минут. Параллельно растворяют карбамилмочевину (1 моль (1 г)) в н-бутиловом спирте при соотношении биурет:н-бутиловый спирт 1:10, прикалывают в реактор с насыщенным сероводородом формалином и перемешивают 6 часов, поддерживая температуру 40°С. Образовавшийся продукт выпадает в виде порошка белого цвета. После фильтрования выделяют кристаллический N-[1 ПРИМЕР 2. Аналогично примеру 1, но в качестве растворителя используют этиловый спирт, температура 40°С. Выделяют кристаллический N-[1 ПРИМЕР 3. Аналогично примеру 1, но в качестве растворителя используют воду, температура 80°С. Выделяют кристаллический N-[1 Спектральные характеристики N-[1
Выход 82%, т.пл. 85-87°С. ИК-спектр, Спектры ЯМР 1H зарегистрированы на спектрометре “Tesla BS-487” (100 МГц), ЯМР 13С – на спектрометре “Jeol FX 90Q” (89.55 и 22.50 МГц), внутренний стандарт ТМС, растворитель ДМСО-d6. ИК-спектры снимали на спектрометре “Specord 75 IR” в суспензии в вазелиновом масле. Элементный анализ образцов определяли на элементном анализаторе фирмы Karlo Erba, модель №1106. Максимальная погрешность определения 2.0% отн. Для полученного соединения приведена температура плавления, определенная на приборе РНМК 80/2617.
Формула изобретения
Способ получения N-[1
заключающийся в том, что насыщенный сероводородом водный раствор формальдегида подвергают взаимодействию с водным или спиртовым раствором карбамилмочевины в мольном соотношении карбамилмочевина:формальдегид:сероводород, равном 1:6:4, при температуре 40-80°С и постоянном перемешивании в течение 6 ч.
|
||||||||||||||||||||||||||

 ,3
,3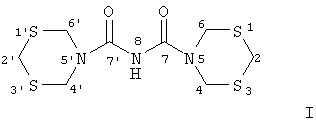

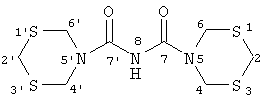
 /см-1: 690-750, 995, 1160, 1350-1440, 1580, 1690, 2900, 3300. Спектр ЯМР 1Н (
/см-1: 690-750, 995, 1160, 1350-1440, 1580, 1690, 2900, 3300. Спектр ЯМР 1Н ( , м.д, ДМСО-d6): 3.92 с (4Н, Н2,2′); 4.71 с (8Н, Н4,4′,6,6′); 6.82 уш.с (1Н, Н8). Спектр ЯМР 13С (
, м.д, ДМСО-d6): 3.92 с (4Н, Н2,2′); 4.71 с (8Н, Н4,4′,6,6′); 6.82 уш.с (1Н, Н8). Спектр ЯМР 13С (