Патент на изобретение №2341459
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ДИОКСИДА ЦЕРИЯ
(57) Реферат:
Изобретение относится к технологии получения соединений редкоземельных элементов, в частности к получению порошков диоксида церия, используемых в производстве катализаторов, присадок к дизельному топливу и других областях техники. В способе получения диоксида церия вводят раствор нитрата церия (III) в качестве католита в катодную камеру электролизера, отделенную мембраной от анодной камеры, заполненной анолитом, и пропускают электрический ток плотностью 2,5-7,5 А/дм2 через католит и анолит. Осуществляют гидролиз нитрата церия (III) с образованием на катоде осадка оксида церия (IV), выделением нитрат-ионов, мигрирующих в анодную камеру, и концентрированием азотной кислоты в анодной камере до содержания 100-250 г/л HNO3. При этом в качестве мембраны берут анионообменную мембрану, а в качестве анолита используют раствор азотной кислоты. После отмывки катодного осадка и его сушки получают оксид церия (IV). Изобретение позволяет получить порошок диоксида церия CeO2 с размером частиц 8-22 нм, выходом по току церия 70-90% и извлечением его в конечный продукт до 97,6% с одновременной утилизацией азотной кислоты, ограничением числа используемых реагентов и снижением энергоемкости. 4 з.п. ф-лы.
Изобретение относится к технологии получения соединений редкоземельных элементов, в частности к получению наноразмерных порошков оксидов церия, используемых в производстве катализаторов, присадок к дизельному топливу, люминофоров, косметических композиций, оптического стекловарения, антикоррозийных сплавов, магнитных материалов и т.д. Для получения наноразмерных порошков диоксида церия в настоящее время используют методы гидролиза из растворов сложного состава с привлечением комплекса органических и неорганических реагентов для повышения дисперсности осадков при сохранении их фильтрующих свойств. Используемые химические методы являются многостадийными, реагентоемкими, продолжительными и характеризуются значительным объемом сбросных растворов сложного состава, что ограничивает их широкое применение. Электрохимические методы получения наноразмерных порошков диоксида церия позволяют сократить объем реагентов и число стадий с получением мелкокристаллических осадков. Вместе с тем они характеризуются недостаточной эффективностью, поскольку не обеспечивают высокого извлечения церия в конечный продукт при минимальных энергозатратах. Известен способ получения диоксида церия (см. Авт. свид. СССР 1288159, МПК4 С01F 17/00, 1987), включающий гидролитическое осаждение гидроксида церия (III) карбамидом из раствора нитрата церия Се(NO3)3 с последующим введением полиакриламида и доведением рН до полного осаждения аммиачным раствором, сушкой на воздухе и окислительным прокаливанием отделенного осадка при 400-700°С с получением оксида церия (IV). Осаждение ведут в две стадии: сначала в присутствии 3-5 мас.% избыточного количества карбамида по отношению к массе СеО2 при рН=7,4-7,6, а затем последовательно вводят 2% раствор полиакриламида в количестве 0,8-1,0 мас.% к конечному продукту и 5% раствор аммиака до полного осаждения. Получают порошки диоксида церия с удельной поверхностью 53-96 м2/г, определенной методом БЭТ по адсорбции бензола. К недостаткам данного способа относится значительное количество продолжительных операций и большое число используемых реагентов, которые требуют утилизации, что усложняет и удорожает способ. Кроме того, способ включает энергоемкую операцию прокаливания осадка гидроксида церия. 3)3 и 0,5 моль/л NH4NO3 для стабилизации рН в катодную камеру электролизера, отделенную диффузионной мембраной, выполненной в виде стеклянной пористой перегородки, от анодной камеры, заполненной анолитом, содержащим 0,5 моль/л NH4NO3 для повышения электропроводности, пропускание постоянного электрического тока через раствор при плотности тока 1 А/см2, температуре электролита 29-80°С и рН=4,5-7,8, гидролиз нитрата церия (III) с образованием на катоде из платиновой проволоки осадка оксида церия (IV) и выделением нитрат-ионов, миграцию нитрат-ионов в анодную камеру, а катионов водорода, выделившихся на сетчатом платиновом аноде, – в катодную камеру с образованием азотной кислоты, отделение катодного осадка, его отмывку, сушку и измельчение с получением порошка СеО2 с дисперсностью 10-14 нм. Прокаливание полученного порошка при 300°С стабилизирует его кристаллическую структуру, обеспечивая размер кристаллитов 60 нм. Выход CeO2 по току составляет около 28%, извлечение в осадок не превышает 34%. Недостатками известного способа являются низкий выход по току церия (IV) вследствие образования в процессе гидролиза нитрата церия, наряду с диоксидом церия, азотной кислоты. Непрерывное повышение концентрации азотной кислоты по мере гидролиза приводит к снижению рН католита, в результате чего прекращается наращивание катодного осадка и начинается его растворение с переводом церия (IV) в раствор, из которого, будучи сильным окислителем, он восстанавливается на катоде до церия (III). В результате ограничивается и извлечение церия в осадок. Используемая диффузионная мембрана не обеспечивает локализации образующейся азотной кислоты в анолите, вследствие чего затруднена ее утилизация в отдельный продукт по причине ее распределения между анолитом и католитом. Недостатком способа является также использование в составе католита дополнительного реагента – нитрата аммония и получение сложных конечных полупродуктов, утилизация которых затруднена: отработанного католита, содержащего нитраты церия (III) и аммония и свободную азотную кислоту, и анолита – раствора нитрата аммония и свободной азотной кислоты. Способ является весьма энергоемким, вследствие низкого выхода по току и высокой температуры прокаливания порошка СеО2. Настоящее изобретение направлено на достижение технического результата, заключающегося в повышении выхода церия по току, увеличении степени извлечения церия в конечный продукт, в утилизации азотной кислоты, содержащейся в нитрате церия, и ограничении числа используемых реагентов. Изобретение направлено также на снижение энергоемкости способа. Технический результат достигается тем, что в способе получения диоксида церия, включающем введение раствора нитрата церия (III) в качестве католита в катодную камеру электролизера, отделенную мембраной от анодной камеры, заполненной анолитом, пропускание электрического тока через католит и анолит, гидролиз нитрата церия (III) с образованием на катоде осадка оксида церия (IV) и выделением нитрат-ионов, миграцию нитрат-ионов в анодную камеру с концентрированием азотной кислоты, отмывку катодного осадка и его сушку, согласно изобретению в качестве мембраны берут анионообменную мембрану, в качестве анолита используют раствор азотной кислоты, а электрический ток имеет плотность 2,5-7,5 А/дм2. Технический результат достигается тем, что используют раствор нитрата церия (III) с концентрацией 0,2-1,0 моль/л Се(NO3)3. Технический результат достигается также тем, что раствор азотной кислоты, используемый в качестве анолита, имеет исходное содержание не менее 5 г/л HNO3. Технический результат достигается также и тем, что в качестве катода и анода используют пластинчатые электроды, выполненные соответственно из стали или титана и платины. Технический результат достигается и тем, что азотная кислота, концентрирующаяся в анодной камере, имеет конечное содержание 100-250 г/л HNO3. Сущность изобретения заключается в том, что при электролизе в катодной камере мембранного электролизера в результате разложения воды на катоде выделяется водород, генерируются гидроксил-ионы и происходит гидролиз нитрата церия (III) согласно реакции:
Выделившиеся нитрат-ионы под действием электрического тока мигрируют через анионообменную мембрану в анодное пространство к положительному электроду – аноду. Вследствие неустойчивости соединения Се(ОН)3 под влиянием электрического тока оно разлагается с образованием на катоде осадка СеО2 согласно реакции: В анодном пространстве разложение воды на аноде сопровождается выделением кислорода и катионов водорода: Освобождающиеся катионы водорода образуют в анолите азотную кислоту, объединяясь с нитрат-ионами, мигрирующими из катодного пространства через анионообменную мембрану, согласно реакции:
Электрохимический процесс, протекающий в катодной и анодной камерах электролизера, описывается итоговым уравнением реакций: Из этого уравнения следует, что продуктами электрогидролиза нитрата церия (III), протекающего в мембранном электролизере, являются: нанокристаллический диоксид церия и водород в катодной камере, а в анодной – кислород и раствор азотной кислоты. Существенные признаки заявленного изобретения, определяющие объем правовой охраны и достаточные для получения вышеуказанного технического результата, выполняют функции и соотносятся с результатом следующим образом. Использование анионообменной мембраны для разделения катодной и анодной камер препятствует миграции катионов водорода, образующихся в результате анодной электрохимической реакции (4), в катодную камеру, где в результате катодной реакции (1) генерируются гидроксил-ионы, что исключает их взаимную нейтрализацию, а также подкисление католита в результате реакции (5). Локализация гидроксил-ионов способствует достижению и стабилизации рН католита на уровне не менее 7,4 на протяжении всего гидролиза, что способствует повышению извлечения церия в осадок. Кроме того, анионообменная мембрана обеспечивает непрерывное удаление из катодной камеры выделяющихся в результате реакции (2) нитрат-ионов в анолит, где они с катионами водорода образуют азотную кислоту по реакции (5). Это значительно понижает возможность растворения осадка CeO2 с образованием в католите ионов церия (IV) и их обратного восстановления до церия (III) на катоде, приводящего к снижению выхода по току. Таким образом, использование анионообменной мембраны способствует повышению извлечения церия в конечный продукт, повышению выхода по току, получению азотной кислоты в виде индивидуального продукта и исключает использование дополнительного реагента – нитрата аммония. Использование в качестве анолита раствора азотной кислоты необходимо для повышения электропроводности водного раствора, что позволяет уменьшить расход электроэнергии на начальной стадии процесса. Поддержание плотности электрического тока в интервале 2,5-7,5 А/дм2 обеспечивает высокие технические показатели электрохимического процесса и необходимую дисперсность осадка. Понижение плотности тока способствует повышению выхода по току гидроксил-ионов, однако снижение плотности тока ниже 2,5 А/дм2 приводит к уменьшению скорости образования гидроксил-ионов и соответственно увеличению времени электролиза, а также к укрупнению кристаллитов осадка. Повышение плотности тока способствует получению осадков повышенной дисперсности и снижает возможность обратного восстановления церия (IV), однако превышение 7,5 А/дм2 в условиях возрастающего на катоде слоя осадка СеО2 с низкой электропроводностью приводит к повышенной катодной поляризации и соответственно перерасходу электроэнергии. Совокупность вышеуказанных признаков необходима и достаточна для достижения технического результата изобретения, заключающегося в повышении выхода церия по току, увеличении степени извлечения церия в конечный продукт, в утилизации азотной кислоты, содержащейся в нитрате церия, и ограничении числа используемых реагентов. Изобретение направлено также на снижение энергоемкости способа. В частных случаях осуществления изобретения предпочтительны следующие конкретные операции и режимные параметры. Использование раствора нитрата церия (III) с концентрацией 0,2-1,0 моль/л Се(NO3)3 обеспечивает образование нанокристаллического CeO2. Снижение концентрации менее 0,2 моль/л Се(NO3)3 приводит к образованию гелеобразных осадков, склонных к пептизации, и плохо фильтрующихся коллоидных суспензий, что снижает извлечение церия в конечный продукт. Концентрация более 1,0 моль/л Се(NO3)3 ограничена пределом растворимости соли и ведет к образованию более крупных частиц СеО2. Использование в качестве анолита раствора азотной кислоты с исходным содержанием не менее 5 г/л HNO3 обеспечивает минимально необходимую электропроводность водного раствора на начальной стадии процесса, что снижает расход электроэнергии. Для поддержания электропроводности католита на конечной стадии процесса также целесообразно сохранять в нем остаточную концентрацию соли не менее 5 г/л Се(NO3)3. Использование в качестве катода и анода пластинчатых электродов продиктовано конструкцией мембранного электролизера, в качестве которого предпочтительно использовать электролизер фильтр-прессного типа. Выполнение анода из платины, а катода из стали или титана обеспечивает их коррозионную устойчивость в условиях электролиза, высокий выход по току и пониженную энергоемкость. Конечное содержание азотной кислоты, концентрирующейся в анодной камере, в интервале значений 100-250 г/л HNO3 обусловлено соотношением объемов католита и анолита и способствует утилизации азотной кислоты. Снижение содержания менее 100 г/л HNO3 приводит к получению разбавленных растворов кислоты, что нежелательно по причине ее ограниченного использования, а повышение содержания более 250 г/л HNO3 сопровождается уменьшением скорости концентрирования из-за возрастающего градиента концентраций нитрат-ионов между анодной и катодной камерами. Вышеуказанные частные признаки изобретения позволяют осуществить способ в оптимальном режиме с точки зрения повышения выхода церия по току, увеличения степени извлечения церия в конечный продукт – нанокристаллический СеО2, утилизации азотной кислоты, содержащейся в нитрате церия, ограничения числа используемых реагентов, а также снижения энергоемкости процесса и исключения необходимости в переработке сбросных растворов сложного состава. Сущность и преимущества заявляемого изобретения могут быть проиллюстрированы следующими примерами. Пример 1. В катодную камеру электролизера вводят 200 мл раствора, содержащего 0,2 моль/л Се(NO3)3, а в анодную, отделенную анионообменной мембраной, – 50 мл раствора азотной кислоты, содержащего 5 г/л HNO3. В качестве катода в электролизере используют титановую пластину, а в качестве анода – платиновую пластину. Через католит и анолит пропускают электрический ток плотностью 2,5 А/дм2. Гидролиз нитрата церия (III) ведут до его остаточного содержания в катодной камере – 5,5 г/л Се(NO3)3 и конечной концентрации азотной кислоты в анолите – 100 г/л HNO3. Образовавшийся осадок снимают с катода, промывают 10% раствором этилового спирта и сушат при температуре 60°С в течение 1 часа. По данным рентгенофазового анализа (РФА) полученный продукт представляет собой оксид церия (IV) – CeO2 с рефлексами 2 Пример 2. В катодную камеру электролизера вводят 200 мл раствора, содержащего 1,0 моль/л Се(NO3)3, а в анодную, отделенную анионообменной мембраной, – 150 мл раствора азотной кислоты, содержащего 6 г/л HNO3. В качестве катода в электролизере используют титановую пластину, а в качестве анода – платиновую пластину. Через католит и анолит пропускают электрический ток плотностью 2,5 А/дм2. Гидролиз нитрата церия (III) ведут до его остаточного содержания в катодной камере – 7,8 г/л Се(NO3)3 и конечной концентрации азотной кислоты в анолите – 242 г/л HNO3. Образовавшийся осадок снимают с катода, промывают 10% раствором этилового спирта и сушат при температуре 60°С в течение 1 часа. По данным РФА полученный продукт представляет собой оксид церия (IV) – CeO2 с рефлексами Пример 3. В катодную камеру электролизера вводят 200 мл раствора, содержащего 0,3 моль/л Се(NO3)3, а в анодную, отделенную анионообменной мембраной, – 150 мл раствора азотной кислоты, содержащего 5 г/л HNO3. В качестве катода в электролизере используют стальную пластину, а в качестве анода – платиновую пластину. Через католит и анолит пропускают электрический ток плотностью 5 А/дм2. Гидролиз нитрата церия (III) ведут до его остаточного содержания в катодной камере – 7,2 г/л Се(NO3)3 и конечной концентрации азотной кислоты в анолите – 162 г/л HNO3. Образовавшийся осадок снимают с катода, промывают 10% раствором этилового спирта и сушат при температуре 60°С в течение 1 часа. По данным РФА полученный продукт представляет собой оксид церия (IV) – СеО2 с рефлексами 2 Пример 4. В катодную камеру электролизера вводят 200 мл раствора, содержащего 0,8 моль/л Се(NO3)3, а в анодную, отделенную анионообменной мембраной, – 150 мл раствора азотной кислоты, содержащего 7 г/л HNO3. В качестве катода в электролизере используют титановую пластину, а в качестве анода – платиновую пластину. Через католит и анолит пропускают электрический ток плотностью 5 А/дм2. Гидролиз нитрата церия (III) ведут до его остаточного содержания в катодной камере – 12,3 г/л Се(NO3)3 и конечной концентрации азотной кислоты в анолите – 198 г/л HNO3. Образовавшийся осадок снимают с катода, промывают 10% раствором этилового спирта и сушат при температуре 60°С в течение 1 часа. По данным рентгенофазового анализа (РФА) полученный продукт представляет собой оксид церия (IV) – СеО2 с рефлексами 2 Пример 5. В катодную камеру электролизера вводят 200 мл раствора, содержащего 0,5 моль/л Се(NO3)3, а в анодную, отделенную анионообменной мембраной, – 100 мл раствора азотной кислоты, содержащего 7 г/л HNO3. В качестве катода в электролизере используют стальную пластину, а в качестве анода – платиновую пластину. Через католит и анолит пропускают электрический ток плотностью 7,5 А/дм2. Гидролиз нитрата церия (III) ведут до его остаточного содержания в катодной камере – 12,5 г/л Се(NO3)3 и конечной концентрации азотной кислоты в анолите – 160 г/л HNO3. Образовавшийся осадок снимают с катода, промывают 10% раствором этилового спирта и сушат при температуре 60°С в течение 1 часа. По данным рентгенофазового анализа (РФА) полученный продукт представляет собой оксид церия (IV) – CeO2 с рефлексами Пример 6. В катодную камеру электролизера вводят 200 мл раствора, содержащего 1,0 моль/л Се(NO3)3, а в анодную, отделенную анионообменной мембраной, – 140 мл раствора азотной кислоты, содержащего 8 г/л HNO3. В качестве катода в электролизере используют стальную пластину, а в качестве анода – платиновую пластину. Через католит и анолит пропускают электрический ток плотностью 7,5 А/дм2. Гидролиз нитрата церия (III) ведут до его остаточного содержания в катодной камере – 19,6 г/л Се(NO3)3 и конечной концентрации азотной кислоты в анолите – 250 г/л HNO3. Образовавшийся осадок снимают с катода, промывают 10% раствором этилового спирта и сушат при температуре 60°С в течение 1 часа. По данным рентгенофазового анализа (РФА) полученный продукт представляет собой оксид церия (IV) – CeO2 с рефлексами 2 Из анализа вышеприведенных примеров видно, что предлагаемый способ позволяет получать наноразмерные порошки оксида церия CeO2 с дисперсностью 8-22 нм, выходом церия по току 70-90% и извлечением его в конечный продукт до 97,6% с одновременной утилизацией азотной кислоты в виде раствора с содержанием 100-250 г/л HNO3. Предлагаемый способ характеризуется ограниченным числом реагентов и пониженной энергоемкостью. Способ относительно прост и может быть реализован с использованием стандартного оборудования.
Формула изобретения
1. Способ получения диоксида церия, включающий введение раствора нитрата церия (III) в качестве католита в катодную камеру электролизера, отделенную мембраной от анодной камеры, заполненной анолитом, пропускание электрического тока через католит и анолит, гидролиз нитрата церия (III) с образованием на катоде осадка оксида церия (IV) и выделением нитрат-ионов, миграцию нитрат-ионов в анодную камеру с концентрированием азотной кислоты, отмывку катодного осадка и его сушку, отличающийся тем, что в качестве мембраны берут анионообменную мембрану, в качестве анолита используют раствор азотной кислоты, а электрический ток имеет плотность 2,5-7,5 А/дм2. 2. Способ по п.1, отличающийся тем, что используют раствор нитрата церия (III) с концентрацией 0,2-1,0 моль/л Се(NO3)3. 3. Способ по п.1 или 2, отличающийся тем, что раствор азотной кислоты, используемый в качестве анолита, имеет исходное содержание не менее 5 г/л HNO3. 4. Способ по п.1, отличающийся тем, что в качестве катода и анода используют пластинчатые электроды, выполненные соответственно из стали или титана и платины. 5. Способ по п.1, отличающийся тем, что азотная кислота, концентрирующаяся в анодной камере, имеет конечное содержание 100-250 г/л HNO3.
|
||||||||||||||||||||||||||

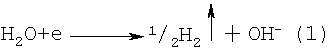


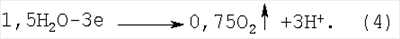
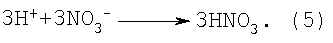
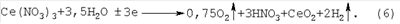
 =3,12Å, 1,91Å и 1,63Å. Средний размер кристаллитов, рассчитанный по свободной удельной поверхности, определенной методом БЭТ по низкотемпературной адсорбции азота, составил 8 нм. Извлечение церия в конечный продукт – 84% при выходе по току 74%.
=3,12Å, 1,91Å и 1,63Å. Средний размер кристаллитов, рассчитанный по свободной удельной поверхности, определенной методом БЭТ по низкотемпературной адсорбции азота, составил 8 нм. Извлечение церия в конечный продукт – 84% при выходе по току 74%.