Патент на изобретение №2341267
|
||||||||||||||||||||||||||
(54) ЖИДКИЙ ПРЕПАРАТ, СОДЕРЖАЩИЙ ТОБРАМИЦИН
(57) Реферат:
Описан стерильный водный раствор для ингаляции, содержащий активное вещество тобрамицин. Препарат по изобретению предложен с высоким содержанием активного вещества (приблизительно от 80 до 120 мг/мл тобрамицина). Препарат также содержит кислотное вспомогательное вещество и имеет низкое содержание хлорида натрия (максимум приблизительно 2 мг/мл). Препарат может быть введен путем инъекции или введен в виде аэрозоля с использованием, например, общепринятых распылителей. Препарат особенно подходит для применения в комбинации с современными распылителями с вибрирующей мембраной и дает возможность для применения индивидуальной терапевтической дозы в течение периода времени, составляющего значительно меньше, чем 10 минут. 4 н. и 20 з.п. ф-лы, 1 табл.
Область техники, к которой относится изобретение Изобретение относится к жидким препаратам, которые содержат антибиотик тобрамицин и которые могут быть введены в виде фармацевтических препаратов путем инъекции или в виде аэрозоля, а именно в легкие или назально. Кроме того, изобретение относится к фармацевтическим наборам, включающим два компонента, из которых могут быть приготовлены жидкие препараты для введения тобрамицина. Кроме того, изобретение относится к применению препаратов в фармацевтических продуктах, которые могут быть введены в легкие или назально посредством распылителя и которые могут быть использованы для лечения муковисцидоза или других инфекционных заболеваний дыхательных путей. Предшествующий уровень техники Тобрамицин представляет собой аминогликозидный антибиотик, имеющий химическое название O-3-амино-3-дезокси- В случае тяжелых инфекций дыхательных путей тобрамицин может быть введен путем ингаляции. Так, например, в Германии имеется лекарственное средство TOBI (поставляемое на рынок Chiron), которое содержит тобрамицин в форме водного раствора без антиоксидантов и которое может быть введено путем ингаляции в виде аэрозоля. В этой форме активный агент может быть использован для лечения инфекций нижних отделов дыхательных путей, вызываемых Pseudomonas aeruginosa. у пациентов, страдающих муковисцидозом, или кистозным фиброзом. Дополнительные области применения, для которых осуществляют клинические тесты, включают лечение бактериальных инфекций в случаях бронхоэктаза и у пациентов с искусственной вентиляцией легких, а также в случаях туберкулеза. Муковисцидоз (или кистозный фиброз) представляет собой одно из наиболее часто встречающихся врожденных метаболических расстройств. Оно представляет собой аутосомально-рецессивный наследственный мультиорганный синдром, вызываемый утратой трансмембранного регуляторного белка муковисцидоза (cystic fibrosis transmembrane regutator, CFTR), представляющего собой регуляторный белок транспорта хлоридов через клеточные мембраны, увеличивающий в результате вязкость секретов организма. Дефект фермента локализован на 7 хромосоме. Генетический дефект оказывает влияние, в частности, на железы внешней секреции, вследствие чего многие органы образуют вязкую слизь, которая блокирует легкие, поджелудочную железу и желчные пути. Приблизительно 90 процентов проблем связано с органами дыхания. Хроническая пневмония часто возникает в том случае, когда вязкая слизь препятствует удалению бактерий. В особенности Pseudomonas aeruginosa имеет тенденцию поражать легкие пациентов, страдающих муковисцидозом. Это вызывает нечто вроде порочного круга: рост и размножение бактерий увеличивают секрецию слизи и приводят в результате к инфекции и воспалению дыхательных путей, и становится все сложнее обеспечивать доступ кислорода в дыхательные пути. У многих пациентов, страдающих муковисцидозом, хроническое воспаление легких приводит в результате к прогрессирующему разрушению тканей легких и к тяжелым расстройствам дыхания, в результате которых в конечном итоге свыше 90% пациентов умирают. Состояние уровня техники Лечение пациентов, страдающих муковисцидозом, путем введения в легкие активного агента тобрамицина в настоящее время осуществляют главным образом с использованием лекарственного средства TOBI. В противоположность инъецируемым препаратам тобрамицина TOBI не содержит стабилизирующую добавку антиоксидантов, которые при ингаляции могут инициировать приступы кашля или астмы. TOBI впрыскивают в виде аэрозоля и ингалируют посредством распылителя. В зависимости от конструкции и типа распылителя достигают сильно отличающихся результатов. Эффективность легочного введения зависит, в частности, от размера частиц получаемого аэрозоля, который значительно варьирует в зависимости от используемого устройства. Производитель фармацевтической продукции Chiron в особенности рекомендует для лечения с использованием TOBI струйный распылитель PARI LC PLUSTM в комбинации с компрессором Pari MasterTM (оба поставляются на рынок PARI). В литературе описаны другие препараты тобрамицина для ингаляции. В патенте США 5508269 описан препарат, содержащий приблизительно от 200 мг до 400 мг тобрамицина в объеме приблизительно 5 мл. В качестве вспомогательного вещества, придающего изотоничность, он содержит хлорид натрия в количестве приблизительно 0,225%, и рН препарата доведен приблизительно до 5,5-6,5. Для введения препарат следует распылять посредством струйного или ультразвукового распылителя с получением аэрозоля, имеющего размер частиц от 1 до 5 мкм. В патенте США 6083922 описаны в некоторой степени подобные препараты активного агента тобрамицина, которые, однако, используют для лечения инфекций, вызываемых Mycobacterium tuberculosis. Приблизительно от 80 до 300 мг активного агента добавляют в виде однократной дозы к объему, составляющему приблизительно от 3 до 5 мл. Значение рН доводят до 5,5-7,0 и для придания изотоничности вновь используют хлорид натрия. Препарат тобрамицина, описанный в патенте США 6387886, также имеет очень похожий состав. Он содержит приблизительно от 250 до 350 мг активного агента в 5 мл раствора хлорида натрия, рН которого вновь доводят до 5,5-6,5. Предполагаемое применение представляет собой лечение хронического бронхита, вызываемого чувствительными к тобрамицину патогенами. В WO 03/004005 описан препарат, имеющий содержание тобрамицина 75 мг/мл и концентрацию хлорида натрия 0,45%. В отличие от цитированных выше документов, согласно этой публикации требуется рН от 4,0 до 5,5. В качестве еще одного признака указано осмотическое давление в диапазоне от 250 до 450 мОсмоль/л. В предпочтительном воплощении препарат имеет рН 5,2 и осмотическое давление от 280 до 350 мОсмоль/л. При практическом применении все эти препараты тобрамицина проявляют различные недостатки. Во-первых, их переносимость не особенно удовлетворительна. Это вероятно вызвано самим активным агентом и усугубляется аффективным состоянием дыхательных путей пациентов, страдающих муковисцидозом. Во-вторых, пациентам требуется длительная ингаляция одной дозы активного агента (в настоящее время наиболее общепринятой является ингаляция 300 мг тобрамицина в 5 мл жидкости), а именно, в течение приблизительно 15-20 минут при использовании обычного струйного распылителя (в зависимости от устройства). В особенности это трудно выполнимо для тяжелобольных пациентов. Еще одним недостатком общепринятых препаратов является их вкус, который многие пациенты воспринимают как плохой; безусловно, это преимущественно вызвано активным агентом, то есть каплями аэрозоля, которые попадают в полость рта и гортань и затем смешиваются со слюной и достигают вкусовых сосочков языка. Это происходит со значительной долей ингалируемых капель аэрозоля. Для решения по меньшей мере проблемы длительного времени ингаляции и возникающей в результате этого нагрузки для пациентов в WO 02/094217 предложено применение более концентрированного раствора тобрамицина, с использованием которого разовая доза может быть ингалирована быстрее вследствие меньшего объема. Применяемый объем должен быть уменьшен до не более чем 4, предпочтительно до не более чем 3,5 мл. Концентрация активного агента, в свою очередь, должна быть уменьшена приблизительно до 200 мг/мл, так что достигается время ингаляции менее чем 10 минут. Особенно предпочтительна концентрация активного агента от 90 до 120 мг/мл и время ингаляции менее чем приблизительно 6 минут. Однако последнее также должно быть достигнуто путем использования вместо обычных распылителей современных устройств с особенно высоким выбросом аэрозоля. Например, рекомендуются более сильные компрессоры, которые могут быть соединены с обычными струйными распылителями или пьезоэлектрическими распылителями, которые благодаря принципу своего действия демонстрируют большую производительность. Тем не менее, в более подробном обсуждении примеров в этом документе описан только один препарат, который имеет концентрацию активного агента более чем 60 мг/мл, а именно препарат, содержащий 420 мг тобрамицина в 3,5 мл, который соответствует концентрации активного агента 120 мг/мл. В то же время этот препарат содержит неспецифичное вспомогательное вещество для доведения рН до 6,0±0,5, а также 0,225% хлорида натрия. Однако оказалось, что этот препарат не может быть эффективно использован с выбранными средствами, которые были оптимизированы для короткого времени ингаляции. В клиническом исследовании количество активного агента, обнаруженное в плазме крови и слюне, было не больше, чем после ингаляции 300 мг тобрамицина в форме лекарственного средства TOBI. Таким образом, время ингаляции может быть уменьшено по сравнению с TOBI (300 мг) с 18,1 до 9,7 минут, но только за счет биодоступности. Одним из недостатков известных препаратов тобрамицина для ингаляции является неоптимальная переносимость в дыхательных путях. По сравнению с применением распыляемого раствора плацебо реакции, такие как кашель и раздражение дыхательных путей, более часто наблюдаются при ингаляции TOBI или известных экспериментальных препаратов тобрамицина. До сих пор не было полностью выяснено, является ли это эффектом только активного агента, на который вряд ли можно влиять, или же комбинация с некоторыми обычными вспомогательными веществами вносит вклад в несовместимость или может вносить вклад в ее уменьшение. Описание изобретения Таким образом, существует потребность в препаратах тобрамицина для действенной, приемлемой для пациента, эффективной и переносимой ингаляции. В частности, существует потребность в препаратах этого активного агента, которые могут быть введены быстро и эффективно с использованием высокоэффективных ингаляторов и хорошо переносятся и которые не обладают недостатками известных препаратов. Задача изобретения заключается в том, чтобы предложить такие улучшенные препараты. Эта задача решена посредством предложения препаратов по п.1 формулы изобретения. Дополнительные решения проблемы станут понятны из других пунктов формулы изобретения и из следующего описания. Препараты могут улучшать легочную антибиотикотерапию пациентов, страдающих муковисцидозом; тем не менее, они также могут быть использованы в качестве растворов для инъекции или для местного лечения инфекций, поражающих верхние отделы дыхательных путей. Заявлен стерильный жидкий препарат в форме водного раствора для инъекции или ингаляции, который содержит приблизительно от 80 до 120 мг тобрамицина на мл и дополнительно кислотное вспомогательное вещество и концентрацию хлорида натрия максимум приблизительно 2 мг/мл. В этом контексте водный раствор означает раствор или коллоидный раствор, в котором растворитель состоит полностью или преимущественно из воды. Стерильный означает, что препарат удовлетворяет, в отношении его стерильности, соответствующим требованиям Европейской фармакопеи (Pharm. Eur.). Тобрамицин представляет собой вещество О-3-амино-3-дезокси- Кислотное вспомогательное вещество представляет собой физиологически приемлемую кислоту или кислую соль, которой доводят рН препарата. В соответствии с изобретением хлорид натрия или не присутствует вообще или присутствует лишь в концентрации максимум 2 мг/мл, где применяются те же самые переносимости, как и в отношении активного агента. Было обнаружено, что препараты, приготовленные в соответствии с п.1, превосходно подходят для распыления в обычных распылителях. Аэрозоли могут быть ингалированы быстро и эффективно. В частности, в комбинации с возможными признаками, которые описаны ниже, может быть достигнуто значительно улучшенное, приемлемое для пациента лечение легочных инфекций в случаях муковисцидоза. Для того чтобы достигнуть цели удобной, безопасной и действенной ингаляции терапевтической дозы тобрамицина, следует принимать во внимание различные параметры, некоторые из которых связаны с препаратом. Одним из решающих параметров является концентрация активного агента в ингалируемом растворе. Поставляемый на рынок продукт TOBI в концентрации 300 мг/5 мл имеет явно меньшую концентрацию активного агента, чем та, которая требуется в соответствии с настоящим изобретением. Вследствие низкой концентрации вряд ли возможно вводить ингалируемый раствор TOBI в течение короткого времени ингаляции. Хотя, по-видимому, желательно время ингаляции, составляющее максимум приблизительно 6-8 минут, и особенно желательно время ингаляции, составляющее максимум 4-5 минут, для достижения высокой степени соблюдения пациентом режима и схемы лечения для ингаляции 5 мл раствора TOBI в комбинации с распылителем, рекомендуемым в инструкциях по применению, требуется по меньшей мере приблизительно 15-20 минут. Даже если игнорировать эту рекомендацию и использовать более мощный распылитель, вряд ли может быть достигнуто желаемое время ингаляции, поскольку из-за низкой концентрации активного агента следует распылять относительно большое количество жидкости. Неожиданно было обнаружено, что концентрацию активного агента не следует выбирать произвольно высокой в пределах растворимости активного агента и что не должно быть превышено значение приблизительно 120 мг/мл. Таким образом, было обнаружено, что при увеличивающейся концентрации тобрамицина поверхностное натяжение раствора может поддерживаться в пределах желаемого диапазона, составляющего приблизительно 70-76 мН/м, но динамическая вязкость, которая в равной степени важна для распыления, значительно увеличивается и оказывает отрицательное действие на распыление. Так, водные растворы тобрамицина, имеющие рН от 6,0 до 6,5, имеют на 50% большую вязкость (приблизительно 2,9 мПа·с) при концентрации активного агента 180 мг/мл по сравнению с раствором, имеющим концентрацию 100 мг/мл (приблизительно 1,8 мПа·с). Сравнимые растворы, имеющие концентрацию тобрамицина 120 мг/мл, обладают вязкостью приблизительно 2,1 мПа·с, и их все еще можно распылять почти с той же эффективностью, что и растворы, имеющие концентрацию 100 мг/мл. В стандартных условиях препараты по настоящему изобретению имеют вязкость приблизительно от 1,4 до 2,3 мПа·с и предпочтительно вязкость, находящуюся в диапазоне приблизительно от 1,6 до 2,0 мПа·c. Наиболее предпочтительна вязкость, составляющая приблизительно 1,8 мПа·с. Выбор и количество агента, придающего изотоничность, оказывает особое влияние на местную переносимость препарата. Хлорид натрия, содержащийся в поставляемом на рынок продукте TOBI, также применяют или рекомендуют для применения почти во всех препаратах, описанных в литературе, например в WO 03/004005, где используют 0,45% (мас./об.) хлорида натрия, и в WO 02/094217, где предпочтительно используют 0,225% (мас./об.). Однако эксперименты по ингаляции, осуществленные авторами изобретения, продемонстрировали, что низкая концентрация хлорида натрия от 0,0 до 0,2% (мас./об.) является менее раздражающей и оптимально совместима с другими обязательными и возможными ингредиентами. В одном из предпочтительных воплощений изобретения хлорид натрия присутствует в концентрации менее чем 0,2% (мас./об.), предпочтительно в концентрации 0,17% (мас./об.). В еще одном воплощении хлорид натрия не присутствует, за исключением убиквитарных количеств хлорида натрия, которые также могут содержаться в воде фармацевтического качества. В еще одном воплощении в препарате в качестве агента, придающего изотоничность, содержится по существу нейтральная соль, которая не является хлоридом натрия, например сульфат натрия или фосфат натрия. Однако в данном случае соли, отличные от солей натрия, еще более предпочтительны. Так, для некоторых солей кальция и магния известно, что они могут обладать положительным или вспомогательным эффектом при ингаляции растворов активных агентов, возможно потому что они сами противодействуют местному раздражению, вызываемому введением, и обладают бронхолитическим действием, которое в настоящее время постулируется в клинической литературе (например, смотри R. Hughes et al., Lancet. 2003; 361 (9375):2114-7), и/или поскольку они ингибируют адгезию микроорганизмов к протеогликанам слизистой оболочки дыхательных путей, так что опосредованно поддерживается мукоцилиарный клиренс в качестве природного защитного механизма организма против микробов (К.W.Tsang et al., Eur. Resp. 2003, 21, 932-938). Особенно предпочтителен сульфат магния, который обладает превосходной легочной переносимостью и может быть ингалирован без риска возникновения проблем, а также хлорид кальция (1-10 мМоль). Если последнее действие должно быть усилено, может быть рассмотрено применение гепарина или фитогемагглютинина, хотя эти вещества могут, безусловно, не обеспечить вклад в осмоляльность, которая была описана для минеральных солей. Как альтернатива нейтральным минеральным солям, в качестве агентов, придающих изотоничность, могут быть использованы физиологически приемлемые органические вспомогательные вещества. Особенно полезны водорастворимые вещества с относительно низкой молекулярной массой, например молекулярной массой менее чем 300 или, еще лучше, менее чем 200, и с соответственно высокой осмотической активностью. Примеры таких вспомогательных веществ представляют собой сахара и сахарные спирты, в частности маннит и сорбит. Количество используемого выбранного агента, придающего изотоничность, должно быть определено так, чтобы в результате получить осмоляльность приблизительно от 150 до 350 мОсмоль/л, принимая во внимание содержание тобрамицина и кислотного вспомогательного вещества и содержание других возможных вспомогательных веществ, находящихся в препарате. Более того, предпочтительна осмоляльность в диапазоне приблизительно от 200 до 300 мОсмоль/л. В еще одном воплощении препарат имеет осмоляльность приблизительно от 230 до 280 мОсмоль/л. Кислотное вспомогательное вещество в препарате одновременно служит нескольким задачам. Во-первых, оно доводит рН до диапазона, который физиологически хорошо переносится (водный раствор основания тобрамицина дает основную реакцию, которая неблагоприятна для ингаляции). Для переносимости рН препарата, тем не менее, должно быть доведено до значения приблизительно от 5,0 до 7,0, предпочтительно до рН от 5,5 до 6,5. Во-вторых, в отношении физико-химических и химических свойств препарата, в частности в отношении химической стабильности содержащегося в нем активного агента, особенно благоприятно значение рН, находящееся в вышеупомянутом диапазоне от 5,0 до 7,0, или от 5,5 до 6,5. Если желателен компромисс между особенно высокой стабильностью и приемлемой переносимостью, также может быть выбрано значение рН, находящееся в кислой области приблизительно до рН 4,0. Применение кислотного вспомогательного вещества обеспечивает то, чтобы активный агент тобраминицин присутствовал в препарате по меньшей мере частично в виде соли. Особенно полезные вспомогательные вещества для понижения значения рН представляют собой сильные неорганические кислоты, в частности серную кислоту и соляную кислоту. Кроме того, могут быть использованы неорганические или органические кислоты, обладающие промежуточной силой, а также кислые соли, например, фосфорная кислота, лимонная кислота, винная кислота, янтарная кислота, фумаровая кислота, лизин, метионин, кислые гидрофосфаты натрия или калия, молочная кислота и так далее. Однако наиболее предпочтительны серная кислота и соляная кислота. Препарат, возможно, может содержать поверхностно-активное вещество в качестве вспомогательного вещества. Для стабилизации диспергированных твердых или жидких частиц или для того, чтобы коллоидно солюбилизировать обычно плохо растворимый активный агент, например, в форме мицелл или в виде так называемой микроэмульсии, в жидких фармацевтических препаратах используют поверхностно-активные вещества. Для достижения специфического поверхностного натяжения могут быть использованы поверхностно-активные вещества, которые особенно важны для оптимального и воспроизводимого распыления. В предпочтительном воплощении препарат по изобретению имеет поверхностное натяжение в стандартных условиях, то есть при комнатной температуре и при нормальном давлении, составляющее приблизительно от 70 до 76 мН/м. В еще одном воплощении препарат имеет поверхностное натяжение, составляющее приблизительно 72 мН/м. Эти поверхностные натяжения облегчают эффективное распыление посредством обычных распылителей с высоким соотношением вдыхаемых капель, имеющих диаметр максимум 5 мкм. Это также может быть достигнуто без добавления поверхностно-активного вещества. Тем не менее, если препарат должен быть приспособлен для применения в конкретном типе распылителя, поверхностное натяжение может быть уменьшено до значений ниже приблизительно 70 мН/м, возможно даже до значений ниже приблизительно 55 мН/м при комнатной температуре. Даже когда добавляют поверхностно-активные вещества, поверхностное натяжение должно быть не менее чем приблизительно 30-35 мН/м. Поверхностное натяжение, сниженное посредством поверхностно-активных веществ, может быть полезно в улучшении способности к распылению аэрозолей в легких, которая в свою очередь может оказывать положительное влияние на эффективность применения. Как неожиданно было обнаружено авторами изобретения, добавление поверхностно-активных веществ может оказывать дополнительный благоприятный эффект: сенсорное качество, то есть, в частности, вкус препарата при ингаляции может быть улучшен путем добавления подходящих поверхностно-активных веществ. Однако поверхностно-активные вещества должны быть фармацевтически приемлемыми и подходящими для применения путем введения в легкие. Примеры таких поверхностно-активных веществ представляют собой Tween® (в частности, Tween® 80), тилоксапол, витамин E D-альфатокоферилполиэтиленгликоля 1000 сукцинат (витамин Е TPGS) и фосфолипиды, такие как гидрированные лецитины. Используемое количество зависит от предполагаемого эффекта: если в первую очередь предполагается улучшенная способность к распылению в легких, особенно полезно применение Tween® 80 и фосфолипидов в относительно высоких концентрациях, составляющих приблизительно от 0,01 до 0,1% (мас./об.). Если в дополнение к этому должен быть замаскирован вкус активного агента, должно быть предпочтительно применение несколько более высоких концентраций, составляющих, например, приблизительно от 0,2 до 2% (мас./об.). Особенно предпочтительна комбинация тилоксапола и фосфолипида, такого как димиристоилфосфатидилхолин (DMPC), и концентрация тилоксапола должна составлять приблизительно от 0,5 до 1,5% (мас./об.), наиболее предпочтительно приблизительно 1,0% (мас./об.), и концентрация DMPC или сопоставимого фосфолипида должна составлять приблизительно от 0,2 до 1,0% (мас./об.), особенно предпочтительно приблизительно 0,5% (мас./об.). Неожиданно оказалось, что такая комбинация поверхностно-активных веществ не приводит в результате к увеличению, а скорее к уменьшению местных раздражений в дыхательных путях или бронхостенозов. Комбинация тилоксапола и фосфолипида, в частности DMPC, вместе с активным агентом тобрамицином особенно полезна также с точки зрения галеновых препаратов. Сам тилоксапол обладает лишь ограниченной совместимостью с активным агентом, то есть в пределах желаемых диапазонов концентрации тилоксапола и тобрамицина в результате происходит осаждение. Однако эту несовместимость можно уменьшить или полностью устранить путем комбинации с DMPC. В зависимости от типа и конфигурации распылителя плотность препарата также может оказывать влияние на эффективность распыления. Она должна находиться в диапазоне приблизительно от 1,0 до 1,2 г/мл, предпочтительно приблизительно от 1,05 до 1,1 г/мл, например 1,07 г/мл. Приготовление препарата по изобретению может быть осуществлено, например, путем растворения одного за другим кислотного вспомогательного вещества, активного агента и агента, придающего изотоничность, в асептических условиях в отмеренном количестве воды для инъекции. В зависимости от того, используются ли поверхностно-активные вещества и какие поверхностно-активные вещества используются, после их добавления может быть осуществлена стадия гомогенизации. В предпочтительном воплощении способ приготовления включает охлаждение раствора во время растворения активного агента в водной фазе или в тесной временной взаимосвязи с растворением активного агента в водной фазе. Посредством этого активный агент может быть дополнительно стабилизирован и защищен от разрушения. Для стабильности также может быть благоприятно проводить обработку в защитной атмосфере. Заполнение предпочтительно осуществляют в асептических условиях в однодозовые или многодозовые контейнеры. Подходящие первичные упаковки представляют собой, например, полипропиленовые или полиэтиленовые флаконы (РР/РЕ флаконы) и циклоолефиновые сополимерные блистерные упаковки (СОС блистеры). Запаянные пластиковые контейнеры, такие как РР или РЕ флаконы, могут быть произведены, заполнены и запаяны, например, предпочтительно по технологии выдувания-заполнения-запаивания (blow fill seal method) в едином процессе. Произведенный таким образом контейнер особенно подходит для жидких продуктов, имеющих объем от приблизительно 0,2 мл. В особенно благоприятном для пациента воплощении они могут быть произведены с крышкой, которая может быть удалена путем поворачивания или отгибания. Получаемое таким образом отверстие, через которое может быть извлечено жидкое содержимое, может быть сконструировано так, чтобы к нему можно было подсоединить коннектор Люэра или коннектор с наконечником Люэра. Отверстие может быть круглым и иметь диаметр, который по существу соответствует внешнему диаметру вставляемого коннектора Люэра. Таким образом, обычный шприц с коннектором Люэра может быть плотно присоединен к контейнеру, например, для того, чтобы отбирать содержимое контейнера и переносить его в распылитель или для того, чтобы смешивать содержимое контейнера с содержимым шприца и затем переносить их в распылитель. В качестве еще одной альтернативы, пластиковый контейнер может быть сконструирован так, чтобы после удаления закрывающего элемента его можно было присоединить достаточно плотно к соединительному элементу для ввода жидкости в соответствующим образом приспособленный распылитель, посредством чего резервуар ингалятора может быть непосредственно заполнен препаратом. Пластиковые контейнеры этого типа также имеют преимущества, поскольку на них легко может быть нанесено рельефное тиснение. Это делает излишним наличие бумажных этикеток, что является желательным для того, чтобы избежать переноса компонентов клея, бумаги или печатной краски через стенку контейнера в препарат. Кроме того, при помощи такого рельефного тиснения важная информация может стать доступной для пациентов с нарушением зрения. Рельефное тиснение может содержать различную информацию, например обозначение партии, срок годности, обозначение продукта, указания по применению или одну или более чем одну разметку доз. Особенно в случае пациентов-детей, когда часто желательно гибкое дозирование в зависимости от возраста и роста, множество маркировок объема может облегчить извлечение желаемой дозы без дополнительных средств, посредством чего может быть уменьшен риск ошибок дозирования. В еще одном воплощении изобретения предложены фармацевтические наборы, которые содержат два жидких компонента или, альтернативно, твердый и жидкий компонент в раздельных первичных упаковках с общей вторичной упаковкой, в которой содержание компонентов отрегулировано так, что путем их комбинирования и смешивания может быть приготовлен препарат тобрамицина по изобретению, как описано выше, который готов для применения. Жидкий компонент или один из жидких компонентов содержит растворитель и возможно дополнительные содержащиеся в нем вспомогательные вещества, тогда как твердый компонент (или другой жидкий компонент) содержит активный агент (тобрамицин) в концентрированной и стабилизированной форме. Такие наборы могут обладать преимуществом, заключающимся в их особенно высокой фармацевтической стабильности и способности к хранению, но при этом легкости обращения с ними, и таким образом способствовать удобству в обращении для пациента. Альтернативно, наборы могут быть сконструированы так, чтобы медицинскому или фармацевтическому обученному персоналу (например, в больничной аптеке) можно было приготовить из них препараты, готовые к применению. В соответствии с еще одним вариантом изобретения предложены многодозовые контейнеры, которые содержат описанный выше препарат и которые сконструированы с возможностью асептического извлечения одной дозы. Таким образом, многодозовый контейнер может представлять собой стеклянный или пластиковый контейнер, такой как флакон или бутылочка для инфузии с эластомерной крышкой, которую можно проткнуть шприцем, или он может представлять собой комплексный контейнер, снабженный устройствами для дозирования и извлечения. Одно из конкретных преимуществ многодозовых контейнеров в отношении препаратов тобрамицина для ингаляции заключается в гибкости, которая делает возможной легкую корректировку дозы в соответствии с индивидуальными потребностями без потери значительных количеств препарата, как может быть в случае однодозовых контейнеров после их открывания. В больницах и медицинских учреждениях пациенты тем самым могут лечиться особенно эффективно и потенциально рентабельно путем подбора индивидуальной дозы. Также легко могут быть приняты во внимание специальные терапевтические требования индивидуальных пациентов. В принципе, любой распылитель, применяемый при лечении, может быть использован для распыления препарата. Испытанные струйные распылители в принципе так же полезны, как и более современные ультразвуковые или пьезоэлектрические распылители, но они обладают недостатком в отношении времени ингаляции. Преимущество струйных распылителей заключается в том, что они уже повсеместно доступны и могут быть рентабельно произведены. Многие пациенты уже привыкли использовать обычные струйные распылители. В некоторых современных струйных распылителях (например PARI LC PLUS® и PARI LC STAR®) используются механизмы, при помощи которых распыление регулируется в соответствии с типом дыхания пациента, так что для ингаляции доступна максимально возможная доля создаваемого аэрозоля. Особенно предпочтительна аэрозолизация препарата посредством современного пьезоэлектрического распылителя, в частности посредством распылителей типа eFlowTM PARI. Особое преимущество для пациентов при использовании этого устройства (или подобного устройства) заключается в относительно более коротком времени по сравнению с альтернативными способами. Это устройство не только распыляет большее количество жидкости в единицу времени, но также создает аэрозоль особенно высокого качества с высокой долей небольших вдыхаемых капель аэрозоля. Терапевтически благоприятный результат чрезвычайно зависит от достоверной и адекватной доступности активного агента в легких. Достижение этого в течение приемлемого периода времени способствует соблюдению пациентом режима и схемы лечения. Пациенты предпочитают короткие периоды времени ингаляции и время ингаляции, составляющее более чем приблизительно 6-8 минут, уже может негативно влиять на соблюдение пациентом режима и схемы лечения. Особенно нежелательно время ингаляции, составляющее более чем приблизительно 10 минут. В противоположность этому, с точки зрения пациента, особенно желательно время ингаляции менее чем приблизительно 5-6 минут. При традиционном лечении тобрамицином лекарственное средство TOBI, которое содержит 300 мг тобрамицина в 5 мл водного раствора, распыляют посредством струйного распылителя, рекомендуемого в инструкциях по применению, представляющего собой устройство PARI LC PLUS®, которое при практическом применении требует достаточно длительного времени, составляющего примерно 15-20 минут. Фракция вдыхаемых капель аэрозоля, имеющих диаметр менее чем 5 мкм, при этом лечении составляет приблизительно 60% от создаваемого аэрозоля (измеренная посредством лазерной дифракции с использованием MasterSizer X, Malvern). Принимая во внимание все потери активного агента, происходящие в распылителе, при выдыхании пациентом и при оседании аэрозоля в верхних отделах дыхательных путей, можно предположить, что только приблизительно 60-80 мг тобрамицина достигают легких пациента (вдыхаемая доза, RD). В противоположность этому, препараты по настоящему изобретению в комбинации с пьезоэлектрическим распылителем достигают значительно более высоких скоростей выброса. Это относится, в частности, к распылению с использованием распылителя с вибрационной мембраной типа eFlowTM, который в то же время продуцирует большие фракции вдыхаемых капель аэрозоля, а именно приблизительно 75%. Кроме того, связанные с дизайном потери внутри устройства меньше, чем в случае струйного распылителя. Таким образом, меньшее количество активного агента достаточно для приготовления той же самой дозы активного агента, доставляемой в легкие. Таким образом, можно предположить, например, на основе данных in vitro, что препарат по настоящему изобретению, содержащий только 200 мг тобрамицина в 2 мл раствора для ингаляции, при распылении с использованием устройства eFlowTM приводит в результате к доступности приблизительно 70-80 мг активного агента в легких (вдыхаемая доза, RD), то есть должен быть биологически эквивалентен обычному лечению с использованием 5 мл TOBI 300 мг. Особое преимущество для пациентов заключается в более коротком периоде времени, необходимом для ингаляции 2 мл препарата по настоящему изобретению с использованием устройства eFlowTM: в экспериментальной установке in vitro это занимает приблизительно 3-4 минуты, тогда как при практическом применении требуется приблизительно 4-5 минут, но в любом случае менее чем 6 минут, что представляет собой существенное отличие по сравнению с обычным лечением. Таким образом, в соответствии с настоящим изобретением предпочтительно готовить препарат в отношении его фармацевтических и, в частности, физико-химических параметров для оптимапьного распыления с использованием пьезоэлектрического распылителя или распылителя с вибрационной мембраной, такого как устройство eFlowTM, так чтобы обеспечить особенно значительную пользу для пациентов с точки зрения значительно уменьшенного времени ингаляции. В еще одном воплощении препарат приспособлен для применения в виде аэрозоля для лечения верхних отделов дыхательных путей. В этом случае также возможно местное лечение инфекций, вызываемых чувствительными к тобрамицину патогенами. В частности, слизистая оболочка носовой и ротовой полости, а также слизистая оболочка придаточных пазух носа, гайморовых и лобных пазух в принципе поддаются аэрозольному лечению. Наиболее легко аэрозоль достигает слизистых оболочек ротовой и носовой полости. В этом случае могут быть использованы механические распылители, такие как распылители, часто используемые для назальных и оральных спреев. Особенно приспособленные струйные, ультразвуковые или пьезоэлектрические распылители, тем не менее могут быть использованы для значительно улучшенного увлажнения слизистой оболочки ротовой или носовой полости распыляемым препаратом. Эффективное применение аэрозоля в отношении менее хорошо вентилируемых полостей верхних отделов дыхательных путей является более сложным. Тем не менее, лобные и придаточные пазухи носа часто являются местом инфекции. Обычно такие инфекции пытаются лечить отхаркивающими и противоотечными средствами, что не всегда приносит пользу. Тяжелые случаи дополнительно лечат при помощи системной антибиотикотерапии, которая, однако, не переносится всеми пациентами хорошо. Простая назальная ингаляция препаратом распыляемого активного агента подводит его к области пазух; однако, преимущественная доля аэрозоля проходит отверстия пазух (устья) без проникновения какой-либо значительной их доли в пазухи. Тем не менее, недавно стали доступны особенно приспособленные струйные распылители, при помощи которых пазух можно достичь гораздо лучше, чем ранее. Эти распылители имеют назальный наконечник для направления потока аэрозоля в нос. Если для ингаляции аэрозоля используется только одна ноздря, другая ноздря должна быть закрыта при помощи подходящего устройства. Кроме того, эти распылители характеризуются тем, что они создают аэрозоль с пульсирующим давлением. Пульсирующее давление приводит в результате к увеличенной вентиляции пазух, так что одновременно ингалируемый аэрозоль может распыляться более эффективно в эти полости. Примеры таких распылителей описаны в DE 10239321 В3. В предпочтительном воплощении препарат по настоящему изобретению используют для приготовления лекарства для применения посредством одного из описанных здесь устройств для лечения инфекций верхних отделов дыхательных путей, в частности, при помощи устройства типа PARI Sinus. Примеры Следующие примеры служат для иллюстрации изобретения посредством множества выбранных воплощений. Пример 1: Приготовление раствора для ингаляции, содержащего 100 мг/мл тобрамицина 11,08 г тобрамицина, 5,41 г серной кислоты (96%), 0,2 г хлорида натрия и 90,95 г воды для инъекции используют в качестве исходных веществ. Все стадии осуществляют в асептических условиях и в атмосфере газообразного азота. Сначала берут воду, к которой добавляют серную кислоту. Затем последовательно добавляют хлорид натрия и активный агент. Смесь перемешивают до полного растворения всех твердых компонентов, что определяют визуально. Это дает приблизительно 100 мл раствора, который имеет рН приблизительно 6,0, осмоляльность приблизительно 0,22 Осмоль/л, динамическую вязкость приблизительно 1,9 мПа·с и поверхностное натяжение приблизительно 71 мН/м. Этот раствор стерильно фильтруют и заполняют в бутылочку для инфузии объемом 100 мл. Эту бутылочку плотно закрывают поддающейся прокалыванию эластомерной пробкой и закрывают алюминиевой крышкой. Пример 2: Распыление раствора для ингаляции, содержащего 100 мг/мл тобрамицина, пьезоэлектрическим распылителем 2 мл раствора, приготовленного в соответствие с Примером 1, асептически отбирают при помощи стерильной канюли и шприца и добавляют в резервуар пьезоэлектрического распылителя типа eFlowTM (PARI). Это устройство действует в соответствии с указаниями по применению для создания аэрозоля. Аэрозоль проверяют в отношении пригодности для вдыхания посредством лазерной дифракции (Malvern MasterSizer X) и в каскадном импакторе Андерсена. На распыление требуется 3,2 минуты. Фракция частиц вплоть до 5 мкм, определяемая посредством лазерной дифракции, составила 75%, фракция вплоть до 5 мкм, определяемая при помощи каскадного импактора, составила 77%. Пример 3: Приготовление раствора тобрамицина для ингаляции, содержащего поверхностно-активное вещество 10,88 г тобрамицина, 5,41 г серной кислоты (96%), 0,2 г хлорида натрия, 0,1 г Tween® 80 и 90,95 г воды для инъекции используют в качестве исходных веществ. Все стадии осуществляют в асептических условиях и в атмосфере газообразного азота. Сначала берут воду, к которой добавляют серную кислоту. Затем добавляют тобрамицин и растворяют при комнатной температуре. К этому раствору добавляют хлорид натрия и Tween®. Смесь перемешивают до образования прозрачного раствора. Это дает приблизительно 100 мл раствора, который имеет значение рН приблизительно 6,2, осмоляльность приблизительно 0,22 Осмоль/л, динамическую вязкость приблизительно 1,9 мПа·с и поверхностное натяжение приблизительно 43 мН/м. Раствор стерильно фильтруют и асептически заполняют в однодозовые полипропиленовые контейнеры по 2 мл в каждый. Пример 4: Приготовление раствора тобрамицина для ингаляции с двумя поверхностно-активными веществами 10,88 г тобрамицина, 5,41 г серной кислоты (96%), 0,2 г хлорида натрия, 0,45 г димиристоилфосфатидилхолина (DMPC), 0,91 г тилоксапола и 89,59 г воды для инъекции используют в качестве исходных веществ. Сначала в воде диспергируют DMPC и тилоксапол. Затем эту смесь гомогенизируют при высоком давлении 150 МПа (1500 бар) до получения опалесцирующего раствора. Затем добавляют серную кислоту и активный агент, который сначала приводит к образованию осадка, который тем не менее не наблюдается после перемешивания в течение 24 ч при комнатной температуре, когда смесь станет в крайнем случае опалесцирующей. Наконец, добавляют хлорид натрия, раствор стерильно фильтруют и заполняют в однодозовые контейнеры. Раствор имеет значение рН приблизительно 6,2, поверхностное натяжение приблизительно 36,5 мН/м, динамическую вязкость приблизительно 2,07 мПа·с и осмоляльность приблизительно 0,23 Осмоль/л. Пример 5: Приготовление раствора тобрамицина для ингаляции с добавлением CaCl2 10,88 г тобрамицина, 5,41 г серной кислоты (96%), 0,2 г хлорида натрия, 0,07 г хлорида кальция и 90,95 г воды для инъекции используют в качестве исходных веществ. Сначала берут воду, в которую добавляют серную кислоту. Затем последовательно добавляют активный агент и затем хлорид натрия вместе с хлоридом кальция. Смесь перемешивают до полного растворения всех твердых компонентов, определяемого визуально. Добавление солей может приводить в результате к временному осаждению, которое не наблюдают после перемешивания в течение 12 часов. Раствор стерильно фильтруют и заполняют в однодозовые контейнеры. Препарат имеет значение рН приблизительно 6,0, поверхностное натяжение приблизительно 70,2 мН/м, вязкость приблизительно 1,87 мПа·с и осмоляльность приблизительно 0,24 Осмоль/кг. Пример 6: Приготовление раствора тобрамицина для ингаляции с добавлением MgSO4 10,88 г тобрамицина, 5,41 г серной кислоты (96%), 0,2 г хлорида натрия, 0,12 г гептагидрата сульфата магния и 90,95 г воды для инъекции используют в качестве исходных веществ. Приготовление раствора осуществляют, как в Примере 5. Раствор стерильно фильтруют и заполняют в однодозовые контейнеры. Препарат имеет значение рН приблизительно 6,1, поверхностное натяжение приблизительно 69,8 мН/м, вязкость приблизительно 1,86 мПа·с и осмоляльность приблизительно 0,24 Осмоль/кг. Пример 7: Распыление раствора тобрамицина для ингаляции с испопьзованием распылителя с вибрационной мембраной и характеристика аэрозоля в каскадном импакторе и имитаторе дыхания 1,4 мл раствора тобрамицина по изобретению, приготовленного как в Примере 1, отбирают и распыляют с использованием пьезоэлектрического распылителя (распылителя с вибрационной мембраной) типа eFlowTM (PARI GmbH), и аэрозоль характеризуют с использованием каскадного импактора Андерсена (ACI) и имитатора дыхания типа PARI COMPASTM (15 вдохов/мин, 500 мл дыхательных объемов, отношение ингаляция:выдох 1:1) и сравнивают с распылением имеющегося в продаже раствора тобрамицина (TOBITM 300, 5 мл) в струйном распылителе типа PARI LC PLUS®. Кроме того, геометрическое распределение размера капель аэрозоля определяли путем фотонно-корреляционной спектроскопии (PCS) с использованием Malvern MasterSizer X. Результаты приведены в Таблице. Сокращения:
Формула изобретения
1. Стерильный жидкий препарат в форме водного раствора для применения в виде раствора для инъекций или в виде аэрозоля, содержащий приблизительно от 80 до 120 мг/мл тобрамицина и кислотное вспомогательное вещество, отличающийся тем, что препарат содержит не более чем 2 мг/мл хлорида натрия. 2. Препарат по п.1, по существу, свободный от хлорида натрия. 3. Препарат по п.2, содержащий по меньшей мере один, по существу, нейтральный агент, придающий изотоничность. 4. Препарат по п.3, где агент, придающий изотоничность, представляет собой соль магния, соль кальция, сахар или сахарный спирт. 5. Препарат по одному из пп.1-4, имеющий рН от приблизительно 5,5 до приблизительно 6,5. 6. Препарат по п.1, где кислотное вспомогательное вещество представляет собой серную кислоту или соляную кислоту. 7. Препарат по п.1, содержащий по меньшей мере одно поверхностно-активное вспомогательное вещество. 8. Препарат по п.7, где поверхностно-активное вспомогательное вещество представляет собой фосфолипид. 9. Препарат по п.8, содержащий тилоксапол в качестве дополнительного поверхностно-активного вспомогательного вещества. 10. Препарат по п.1, обладающий динамической вязкостью при комнатной температуре приблизительно от 1,6 до 2,0 мПа·с и осмоляльностью приблизительно от 200 до 300 мОсмоль/л. 11. Препарат по п.1, обладающий осмоляльностью приблизительно от 230 до 280 мОсмоль/л. 12. Препарат по п.1, где препарат находится в форме с отмеренной однократной дозой в первичной упаковке. 13. Препарат по п.12, где первичная упаковка имеет форму пластикового контейнера, включающего съемный закрывающий элемент. 14. Препарат по п.13, где удаление закрывающего элемента приводит к образованию круглого отверстия в пластиковом контейнере, диаметр которого соответствует приблизительно внутреннему диаметру адаптера с вставляемым наконечником Люэра. 15. Препарат по п.13 или 14, где пластиковый контейнер после удаления закрывающего элемента может быть присоединен очень плотно к соединительному устройству распылителя, предназначенного для введения жидкости. 16. Препарат по п.13, где пластиковый контейнер снабжен по меньшей мере одним рельефным тиснением, которое представляет собой обозначение продукта, код партии, срок годности и/или маркировку объема или дозы. 17. Набор для приготовления препарата по одному из пп.1-16, включающий (а) жидкий или твердый компонент, содержащий активный агент, и (б) жидкий компонент, свободный от активного агента. 18. Применение препарата по одному из пп.1-16 или набора по п.17 для приготовления лекарства для внутривенной, внутриартериальной, подкожной или внутримышечной инъекции. 19. Применение препарата по одному из пп.1-16 или набора по п.17 для приготовления лекарства для применения в форме аэрозоля. 20. Применение по п.19 для введения в легкие посредством струйного, ультразвукового или пьезоэлектрического распылителя. 21. Применение по п.20, где пьезоэлектрический распылитель представляет собой устройство типа eFlow 22. Применение по п.21 для назального введения посредством механического пульверизатора или струйного, ультразвукового или пьезоэлектрического распылителя. 23. Применение по п.22 для введения в слизистые оболочки придаточных пазух носа и/или лобных пазух. 24. Применение по п.22 для введения посредством струйного распылителя, включающего назальный наконечник для ввода аэрозоля в одну или обе ноздри пациента, и выход аэрозоля из которого осуществляется под пульсирующим давлением.
|
||||||||||||||||||||||||||

 -D-глюкопиранозил(1
-D-глюкопиранозил(1 4)-O-[2,6-диамино-2,3,6-тридезокси-
4)-O-[2,6-диамино-2,3,6-тридезокси-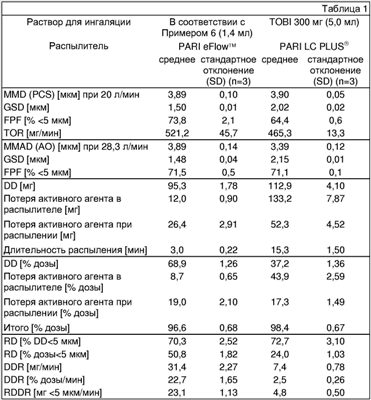
 PARI.
PARI.