Патент на изобретение №2161982
|
||||||||||||||||||||||||||
(54) ТЕТРАПЕПТИД, СТИМУЛИРУЮЩИЙ ФУНКЦИЮ СЕТЧАТОЙ ОБОЛОЧКИ ГЛАЗА, ФАРМАКОЛОГИЧЕСКОЕ СРЕДСТВО НА ЕГО ОСНОВЕ И СПОСОБ ЕГО ПРИМЕНЕНИЯ
(57) Реферат: Изобретение относится к медицине и касается создания препаратов для лечения глазных болезней. Предложены: тетрапептид аланил-глутамил-аспарагил-глицин общей формулы Ala-Glu-Asp-Gly в качестве средства, обладающего способностью стимулировать функцию сетчатой оболочки глаза; фармакологическое средство, содержащее в качестве активного начала эффективное количество тетрапептида Ala-Glu-Asp-Gly или его солей по аминогруппе (ацетат, гидрохлорид, оксалат) и по карбоксильным группам (соли металлов – натрия, калия, кальция, лития, цинка, магния, а также органических и неорганических катионов – аммония, триэтиламмония); способ лечения заболеваний и патологических состояний, сопровождающихся нарушением функции сетчатой оболочки глаза, включающий профилактическое и/или лечебное введение пациенту фармакологического средства в дозах 0,01-1000 мкг/кг массы тела по крайней мере один раз в день в течение периода, необходимого для достижения терапевтического эффекта. Технический результат: новое биологически активное соединение при низких дозах обеспечивает терапевтический эффект. 3 с. и 9 з.п.ф-лы, 9 табл. Изобретение относится к медицине и касается использования в офтальмологии синтезированного тетрапептида для лечения глазных болезней путем стимуляции функции сетчатой оболочки глаза. Известны следующие группы фармакологических препаратов, применяемых при заболеваниях, сопровождающихся нарушением функции сетчатой оболочки глаза: сосудорасширяющие средства (никотиновая кислота, нигексин, но-шпа, никошпан, теофиллин, эуфиллин, компламин, нитрат натрия); средства, улучшающие состояние сосудистой стенки и микроциркуляцию (продектин, трентал); антикоагулянты (гепарин); биогенные стимуляторы (алоэ, торфот, плацентарная кровь, ФиБС, стекловидное тело, пелоидодистиллят, антиретикулярная цитотоксическая сыворотка); АТФ; витаминные препараты (витамины A, E, B1, B6, C); дезинтоксикационные препараты (унитиол); препараты нуклеиновых кислот (дронуклид, энкад, нуклеинат натрия) [1,2]. Однако вследствие неспецифичности терапии указанными препаратами их терапевтический эффект, как правило, оказывается кратковременным и нестойким, кроме того, эти препараты обладают выраженными побочными эффектами [3]. Известно использование пептидных препаратов для лечения глазных болезней. В частности известно средство, используемое в офтальмологии и восстанавливающее функцию сетчатой оболочки глаза [4]. Этот препарат представляет собой комплекс низкомолекулярных полипептидов, полученный из сетчатки животных путем экстракции 3%-ным раствором уксусной кислоты с добавлением хлористого цинка и обработкой надосадочной жидкости ацетоном. Следует отметить, что указанный способ производства лекарственного вещества имеет некоторые недостатки, к которым относятся ограниченные запасы исходного органического сырья, трудоемкость и энергоемкость производства. Заявляемое изобретение направлено на получение нового биологически активного соединения пептидной природы, обладающего свойством стимулировать функцию сетчатой оболочки глаза, получение которого возможно в крупномасштабном производстве с минимальными затратами. Сущность изобретения состоит в использовании тетрапептида Ala-Glu-Asp-Gly, или его солей (далее – тетрапептид), в качестве средства, обладающего способностью стимулировать функцию сетчатой оболочки глаза, с целью длительного и стойкого улучшения зрительных функций. Тетрапептид получают классическим методом пептидного синтеза в растворе [5]. Согласно изобретению тетрапептид аланил-глутамил-аспарагил-глицин со следующей аминокислотной последовательностью: Ala-Glu-Asp-Gly, проявляет новую биологическую активность, заключающуюся в способности стимулировать функцию сетчатой оболочки глаза. Согласно изобретению фармакологическое средство, обладающее способностью стимулировать функцию сетчатой оболочки глаза, содержит в качестве активного начала эффективное количество тетрапептида формулы аланил-глутамил-аспарагил-глицин (Ala-Glu-Asp-Gly) или его солей. Согласно изобретению фармакологическое средство, обладающее способностью стимулировать функцию сетчатой оболочки глаза, может содержать соли по аминогруппе (ацетат, гидрохлорид, оксалат), или по карбоксильным группам (соли металлов – натрия, калия, кальция, лития, цинка, магния, а также органических и неорганических катионов – аммония, триэтиламмония). Согласно изобретению фармакологическое средство предназначено для парентерального, парабульбарного, ретробульбарного, субконъюнктивального, локального применения, а также в виде глазных инстилляций, накожной аппликации и при физиотерапевтических воздействиях в составе любой лекарственной формы или композиции, в качестве единственного средства медикации или в комбинации с другими лекарственными препаратами. Понятие “фармакологическое средство”, используемое в данной заявке, подразумевает использование лекарственной формы, приемлемой для способа введения и содержащей тетрапептид или его соли, которые могут найти профилактическое и/или лечебное применение в медицине в качестве средства, стимулирующего функцию сетчатой оболочки глаза. Понятие “эффективное количество”, используемое в данной заявке, подразумевает использование того количества активного начала, которое в соответствии с его количественными показателями активности и токсичности, а также на основании знаний специалиста должно быть эффективным в данной лекарственной форме. Согласно изобретению способ лечения заболеваний и патологических состояний включает профилактическое или лечебное введение пациенту заявляемого фармакологического средства в дозах от 0,01 до 1000 мкг/кг массы тела не менее одного раза в день в течение периода, необходимого для достижения терапевтического эффекта в зависимости от характера течения патологического процесса. Согласно изобретению тетрапептид активен при введении его в дозах от 0,01 мкг/кг массы тела, хотя могут быть использованы и более низкие дозы в зависимости от характера течения патологического процесса. Изобретение иллюстрируется примером синтеза тетрапептида формулы аланил-глутамил-аспарагил-глицин (Ala-Glu-Asp-Gly) (пример 1), примерами, наглядно демонстрирующими выявленные новые свойства исследуемого препарата в экспериментальных моделях (примеры 2, 3, 4, 5), а также примерами результатов клинического применения фармакологического средства у ограниченного контингента больных, демонстрирующими его фармакологические свойства и подтверждающими возможность достижения профилактического и/или лечебного эффекта (примеры 6, 7, 8, 9, 10). ПРИМЕР 1 Синтез тетрапептида формулы аланил-глутамил-аспарагил-глицин (Ala-Glu-Asp-Gly) 1) BOC-Glu(OBzl)-Asp(OBzl)-OH (I), N-трет.бутилоксикарбонил- (  – бензил)глутамил- – бензил)глутамил-  бензил)аспартат.
N-оксисукцинимидный эфир N-трет.бутилоксикарбонил- ( бензил)аспартат.
N-оксисукцинимидный эфир N-трет.бутилоксикарбонил- ( – бензил)глутаминовой кислоты BOC-Glu(OBzl)-OSu 4,34 г (0,0100 моль) растворяют в 20 мл диметилформамида, добавляют триэтиламин 1,72 мл (0,0125 моль) и – бензил)глутаминовой кислоты BOC-Glu(OBzl)-OSu 4,34 г (0,0100 моль) растворяют в 20 мл диметилформамида, добавляют триэтиламин 1,72 мл (0,0125 моль) и  -бензиласпартат 2,80 г (0,0125 моль). Перемешивают при комнатной температуре 24 час. Продукт высаживают 0,5 н. раствором серной кислоты (150 мл), экстрагируют в этилацетат (3х30 мл), промывают 0,5 н. раствором серной кислоты (2х20 мл), водой, 5% раствором бикарбоната натрия (1х20 мл), водой, 0,5 н. раствором серной кислоты (2х20 мл), водой и сушат над безводным сульфатом натрия. Этилацетат фильтруют, упаривают в вакууме при 40oC, остаток сушат в вакууме над P2O5. Получают масло 5,68 г ( -бензиласпартат 2,80 г (0,0125 моль). Перемешивают при комнатной температуре 24 час. Продукт высаживают 0,5 н. раствором серной кислоты (150 мл), экстрагируют в этилацетат (3х30 мл), промывают 0,5 н. раствором серной кислоты (2х20 мл), водой, 5% раствором бикарбоната натрия (1х20 мл), водой, 0,5 н. раствором серной кислоты (2х20 мл), водой и сушат над безводным сульфатом натрия. Этилацетат фильтруют, упаривают в вакууме при 40oC, остаток сушат в вакууме над P2O5. Получают масло 5,68 г (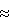 100%). Rf = 0,42 (бензол-ацетон 2: 1, пластинки ПТСХ-П-В-УФ Sorbfil, силикагель СТХ-1ВЭ 8-12 мкм, проявление УФ и хлор/бензидин).
2) TFA 100%). Rf = 0,42 (бензол-ацетон 2: 1, пластинки ПТСХ-П-В-УФ Sorbfil, силикагель СТХ-1ВЭ 8-12 мкм, проявление УФ и хлор/бензидин).
2) TFA H-Glu(OBzl)-Asp(OBzl)-OH (II), трифторацетат ( H-Glu(OBzl)-Asp(OBzl)-OH (II), трифторацетат ( – бензил)-глутамил- ( – бензил)-глутамил- ( -бензил)аспартата.
N-трет. бутилоксикарбонил- ( -бензил)аспартата.
N-трет. бутилоксикарбонил- ( – бензил)глутамил- ( – бензил)глутамил- ( – бензил)аспартат (I) 5,68 г ( – бензил)аспартат (I) 5,68 г (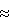 0,01 моль) растворяют в 20 мл смеси дихлорметан-трифторуксусная кислота (3:1). Через 2 часа растворитель упаривают в вакууме при 40oC, упаривание повторяют с новой порцией дихлорметана (2х10 мл), остаток сушат в вакууме над NaOH. Получают масло 5,80 г ( 0,01 моль) растворяют в 20 мл смеси дихлорметан-трифторуксусная кислота (3:1). Через 2 часа растворитель упаривают в вакууме при 40oC, упаривание повторяют с новой порцией дихлорметана (2х10 мл), остаток сушат в вакууме над NaOH. Получают масло 5,80 г (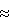 100%). Rf= 0,63 (н-бутанол-пиридин-уксусная кислота-вода, 15:10:3:12).
3) Z-Ala-Glu(OBzl)-Asp(OBzl)-OH (III), N-карбобензоксиаланил- ( 100%). Rf= 0,63 (н-бутанол-пиридин-уксусная кислота-вода, 15:10:3:12).
3) Z-Ala-Glu(OBzl)-Asp(OBzl)-OH (III), N-карбобензоксиаланил- ( – бензил)-глутамил- ( – бензил)-глутамил- ( – бензил)аспартат.
Трифторацетат ( – бензил)аспартат.
Трифторацетат ( – бензил)глутамил- ( – бензил)глутамил- ( – бензил)аспартата (II) 5,65 г (0,01 моль) растворяют в 10 мл диметилформамида, добавляют триэтиламин 2,80 мл (0,02 моль) и N-оксисукцинимидный эфир N-карбобензоксиаланина 4,14 г (0,013 моль). Смесь перемешивают 24 часа при комнатной температуре. Продукт высаживают 0,5 н. раствором серной кислоты (150 мл), экстрагируют в этилацетат (3х30 мл), промывают 0,5 н. раствором серной кислоты (2х20 мл), водой, 5% раствором бикарбоната натрия (1х20 мл), водой, 0,5 н. раствором серной кислоты (2х20 мл), водой и сушат над безводным сульфатом натрия. Этилацетат фильтруют, упаривают в вакууме при 40oC, остаток закристаллизовывают в системе этилацетат/гексан. Продукт отфильтровывают и сушат в вакууме над P2O5. Выход 4,10 г (66 %). Тпл.= 154oC. Rf= 0,48 (бензол-ацетон, 1:1), Rf = 0,72 (н-бутанол-пиридин-уксусная кислота-вода, 15:10:3:12).
4) Z-Ala-Glu(OBzl)-Asp(OBzl)-Gly-OBzl (III), бензиловый эфир N-карбобензоксиаланил-( – бензил)аспартата (II) 5,65 г (0,01 моль) растворяют в 10 мл диметилформамида, добавляют триэтиламин 2,80 мл (0,02 моль) и N-оксисукцинимидный эфир N-карбобензоксиаланина 4,14 г (0,013 моль). Смесь перемешивают 24 часа при комнатной температуре. Продукт высаживают 0,5 н. раствором серной кислоты (150 мл), экстрагируют в этилацетат (3х30 мл), промывают 0,5 н. раствором серной кислоты (2х20 мл), водой, 5% раствором бикарбоната натрия (1х20 мл), водой, 0,5 н. раствором серной кислоты (2х20 мл), водой и сушат над безводным сульфатом натрия. Этилацетат фильтруют, упаривают в вакууме при 40oC, остаток закристаллизовывают в системе этилацетат/гексан. Продукт отфильтровывают и сушат в вакууме над P2O5. Выход 4,10 г (66 %). Тпл.= 154oC. Rf= 0,48 (бензол-ацетон, 1:1), Rf = 0,72 (н-бутанол-пиридин-уксусная кислота-вода, 15:10:3:12).
4) Z-Ala-Glu(OBzl)-Asp(OBzl)-Gly-OBzl (III), бензиловый эфир N-карбобензоксиаланил-( – бензил)глутамил- ( – бензил)глутамил- ( -бензил)аспартилглицина.
TosOH -бензил)аспартилглицина.
TosOH H-Gly-OBzl, тозилат бензилового эфира глицина 1,01 г (3 ммоль) суспендируют в 15 мл тетрагидрофурана и при перемешивании добавляют триэтиламин 0,4 мл (3 ммоль), далее через 5 мин. N-карбобензоксиаланил- ( H-Gly-OBzl, тозилат бензилового эфира глицина 1,01 г (3 ммоль) суспендируют в 15 мл тетрагидрофурана и при перемешивании добавляют триэтиламин 0,4 мл (3 ммоль), далее через 5 мин. N-карбобензоксиаланил- ( – -бензил)глутамил- ( – -бензил)глутамил- ( -бензил)аспартат (III) 1,28 г (2 ммоль), N-оксибензотриазол 0,27 г (2 ммоль) и охлаждают смесь до 0oC. Затем добавляют охлажденный до 0oC раствор N, N’-дициклогексилкарбодиимида 0,42 г (2 ммоль) в 5 мл тетрагидрофурана, перемешивают смесь при этой температуре 2 часа и оставляют на ночь перемешиваться при комнатной температуре. Осадок дициклогексилмочевины отфильтровывают, растворитель упаривают в вакууме, остаток растворяют в 30 мл этилацетата и промывают раствор 1 н. раствором соляной кислоты, водой, 5%-ным раствором бикарбоната натрия, водой, 1 н. раствором соляной кислоты, водой и сушат над безводным сульфатом натрия. Растворитель упаривают в вакууме и продукт закристаллизовывают в системе этилацетат/гексан. Выход 1,30 г (82%). Тпл. = 146-148oC. Rf= 0,75 (бензол-ацетон, 2:1).
5) H-Ala-Glu-Asp-Gly-OH (IV), аланил-глутамил-аспартил-глицин.
Бензиловый эфир N- карбобензоксиаланил- ( -бензил)аспартат (III) 1,28 г (2 ммоль), N-оксибензотриазол 0,27 г (2 ммоль) и охлаждают смесь до 0oC. Затем добавляют охлажденный до 0oC раствор N, N’-дициклогексилкарбодиимида 0,42 г (2 ммоль) в 5 мл тетрагидрофурана, перемешивают смесь при этой температуре 2 часа и оставляют на ночь перемешиваться при комнатной температуре. Осадок дициклогексилмочевины отфильтровывают, растворитель упаривают в вакууме, остаток растворяют в 30 мл этилацетата и промывают раствор 1 н. раствором соляной кислоты, водой, 5%-ным раствором бикарбоната натрия, водой, 1 н. раствором соляной кислоты, водой и сушат над безводным сульфатом натрия. Растворитель упаривают в вакууме и продукт закристаллизовывают в системе этилацетат/гексан. Выход 1,30 г (82%). Тпл. = 146-148oC. Rf= 0,75 (бензол-ацетон, 2:1).
5) H-Ala-Glu-Asp-Gly-OH (IV), аланил-глутамил-аспартил-глицин.
Бензиловый эфир N- карбобензоксиаланил- ( – бензил)глутамил- ( – бензил)глутамил- ( -бензил)аспартилглицина (III) 1,25 г гидрировали в системе метанол-вода-уксусная кислота (3:1:1) над катализатором Pd/C. Контроль за полнотой деблокирования в ТСХ системах бензол-ацетон (2:1) и ацетонитрил- уксусная кислота-вода (5: 1:3). По окончании реакции катализатор отфильтровывают, фильтрат упаривают в вакууме и остаток закристаллизовывают в системе вода/метанол. Продукт сушат в вакууме над КОН. Выход 520 мг (95%). Rf = 0,73 (ацетонитрил- уксусная кислота-вода, 5: 1:3). Для очистки 390 мг препарата растворяли в 4 мл 0,01% трифторуксусной кислоты и подвергали высокоэффективной жидкостной хроматографии на колонке с обращенной фазой 50х250 мм Diasorb-130-C16T, 7 mkm. Хроматограф Beckman System Gold, 126 Solvent Module, 168 Diode Array Detector Module. Условия хроматографирования A: 0,1% TFA; B: 50% MeCN/0,1% TFA, градиент B 0 —> 5% за 80 мин. Объем пробы 5 мл, детекция при 215 нм, сканирование 190-600 нм, скорость потока 10 мл/мин. Отбирали фракцию 54,0-66,0 мин. Растворитель упаривали в вакууме при температуре не выше 40oC, упаривание многократно (5 раз) повторяли с 10 мл 10% раствора уксусной кислоты. Окончательно остаток растворяли в 20 мл деионизованной воды и лиофилизовывали. Получено 290 мг очищенного препарата в виде аморфного белого порошка без запаха.
Полученный пептид в виде ацетата переводят в свободную форму обработкой анионитом IRA или аналогичным в (OH–) – форме. Далее получают соли по аминогруппе, прибавляя эквивалент соответствующей кислоты (соляной или щавелевой). Полученный водный раствор лиофилизуют и анализируют как готовый продукт.
Для получения соответствующих солей по карбоксильным группам к свободному тетрапептиду добавляют рассчитанное количество водного раствора гидроокиси соответствующего металла (NaOH, KOH, Zn(OH)2, LiOH, Ca(OH)2, Mg(OH)2, NH4OH). Для получения триэтиламмониевой соли обработку проводят аналогичным образом, используя в качестве основания триэтиламин.
Содержание основного вещества определяют методом ВЭЖХ на колонке Supelco LC-18-DB 4,6х250 mm, gard. LC-18-DB. A:0,1% TFA; B: 50% MeCN/0,1% TFA; grad B 0 —> 20% за 20 минут. Скорость потока 1 мл/мин. Детекция при 220 нм, сканирование 190-600 нм, проба 20 мк. Содержание основного вещества 98,45%.
Определение аминокислотного состава проводят на анализаторе после 6 часового гидролиза в 6 н. HCl при 125oC 24 часа. Содержание аминокислот: Glu: Asp:Ala:Gly составляет 1,02:1,00:1,01:1,00 соответственно.
Фармакологическое средство в инъекционной форме, содержащее в качестве активного начала тетрапептид, получают следующим образом. Пептид, полученный описанным выше способом, растворяют в изотоническом растворе натрия хлорида 0,9%. Содержимое одного флакона составляет 1 мл раствора с концентрацией тетрапептида 10 мкг/мл.
При экспериментальном исследовании тетрапептида выявлены такие его не известные ранее фармакологические эффекты, как стимулирование зрительных функций и уменьшение деструктивных процессов в сетчатке при ее токсической дистрофии, предотвращение развития токсической дистрофии сетчатки, предотвращение развития абиотрофических изменений и улучшение зрительной функции при наследственной абиотрофии сетчатки, ускорение восстановления световой чувствительности сетчатки после зрительной дезадаптации.
ПРИМЕР 2 -бензил)аспартилглицина (III) 1,25 г гидрировали в системе метанол-вода-уксусная кислота (3:1:1) над катализатором Pd/C. Контроль за полнотой деблокирования в ТСХ системах бензол-ацетон (2:1) и ацетонитрил- уксусная кислота-вода (5: 1:3). По окончании реакции катализатор отфильтровывают, фильтрат упаривают в вакууме и остаток закристаллизовывают в системе вода/метанол. Продукт сушат в вакууме над КОН. Выход 520 мг (95%). Rf = 0,73 (ацетонитрил- уксусная кислота-вода, 5: 1:3). Для очистки 390 мг препарата растворяли в 4 мл 0,01% трифторуксусной кислоты и подвергали высокоэффективной жидкостной хроматографии на колонке с обращенной фазой 50х250 мм Diasorb-130-C16T, 7 mkm. Хроматограф Beckman System Gold, 126 Solvent Module, 168 Diode Array Detector Module. Условия хроматографирования A: 0,1% TFA; B: 50% MeCN/0,1% TFA, градиент B 0 —> 5% за 80 мин. Объем пробы 5 мл, детекция при 215 нм, сканирование 190-600 нм, скорость потока 10 мл/мин. Отбирали фракцию 54,0-66,0 мин. Растворитель упаривали в вакууме при температуре не выше 40oC, упаривание многократно (5 раз) повторяли с 10 мл 10% раствора уксусной кислоты. Окончательно остаток растворяли в 20 мл деионизованной воды и лиофилизовывали. Получено 290 мг очищенного препарата в виде аморфного белого порошка без запаха.
Полученный пептид в виде ацетата переводят в свободную форму обработкой анионитом IRA или аналогичным в (OH–) – форме. Далее получают соли по аминогруппе, прибавляя эквивалент соответствующей кислоты (соляной или щавелевой). Полученный водный раствор лиофилизуют и анализируют как готовый продукт.
Для получения соответствующих солей по карбоксильным группам к свободному тетрапептиду добавляют рассчитанное количество водного раствора гидроокиси соответствующего металла (NaOH, KOH, Zn(OH)2, LiOH, Ca(OH)2, Mg(OH)2, NH4OH). Для получения триэтиламмониевой соли обработку проводят аналогичным образом, используя в качестве основания триэтиламин.
Содержание основного вещества определяют методом ВЭЖХ на колонке Supelco LC-18-DB 4,6х250 mm, gard. LC-18-DB. A:0,1% TFA; B: 50% MeCN/0,1% TFA; grad B 0 —> 20% за 20 минут. Скорость потока 1 мл/мин. Детекция при 220 нм, сканирование 190-600 нм, проба 20 мк. Содержание основного вещества 98,45%.
Определение аминокислотного состава проводят на анализаторе после 6 часового гидролиза в 6 н. HCl при 125oC 24 часа. Содержание аминокислот: Glu: Asp:Ala:Gly составляет 1,02:1,00:1,01:1,00 соответственно.
Фармакологическое средство в инъекционной форме, содержащее в качестве активного начала тетрапептид, получают следующим образом. Пептид, полученный описанным выше способом, растворяют в изотоническом растворе натрия хлорида 0,9%. Содержимое одного флакона составляет 1 мл раствора с концентрацией тетрапептида 10 мкг/мл.
При экспериментальном исследовании тетрапептида выявлены такие его не известные ранее фармакологические эффекты, как стимулирование зрительных функций и уменьшение деструктивных процессов в сетчатке при ее токсической дистрофии, предотвращение развития токсической дистрофии сетчатки, предотвращение развития абиотрофических изменений и улучшение зрительной функции при наследственной абиотрофии сетчатки, ускорение восстановления световой чувствительности сетчатки после зрительной дезадаптации.
ПРИМЕР 2Влияние лечебного курса тетрапептида на функцию и морфологию сетчатки при токсической дистрофии. 2.1. Влияние лечебного курса тетрапептида на параметры электроретинограммы при токсической дистрофии сетчатки кроликов. Исследовано возможное лечебное действие тетрапептида на сетчатку в условиях ее экспериментальной дистрофии на глазах 15 половозрелых кроликов породы “шиншилла” массой 2,5-3,5 кг. Экспериментальную токсическую дисторофию сетчатки создавали путем внутривенного введения 4%-ного раствора монойодуксусной кислоты (далее – МЙУК) в дозах 15 мг/кг (тяжелая степень повреждения сетчатки) и 5 мг/кг (средняя степень повреждения сетчатки). Степень поражения сетчатки оценивали по уровню ее биоэлектрической активности, определяемой методом электроретинографии (ЭРГ). ЭРГ регистрировали в условиях адаптации к темноте до введения монойодуксусной кислоты (исходные значения), а также через 20 мин, 5, 10, 15 и 35 суток после ее введения. Животные опытной группы на протяжении всего эксперимента получали ежедневные однократные внутримышечные инъекции тетрапептида в дозе 1 мкг/кг, начиная с 3-х суток после введения монойодуксусной кислоты. Животные контрольной группы получали соответствующие инъекции стерильного физиологического раствора. Результаты исследования биоэлектрической активности сетчатки глаз кроликов опытной и контрольной группы представлены ниже в таблице 1. Как видно, амплитуда волны “в” ЭРГ уже через 20 минут после введения монойодуксусной кислоты составила 4% от исходных значений при тяжелом поражении и 40% от исходных значений при средней степени поражения сетчатки. Применение тетрапептида приводит к достоверному повышению волны “в” ЭРГ по сравнению с контролем. Так, при средней степени тяжести повреждения сетчатки лечебный эффект тетрапептида обнаруживается уже на 15-е сутки наблюдения, достигая своего максимума к 35 суткам. Амплитуда волны “в” ЭРГ у опытных животных за этот период достигает 85% от фонового уровня и почти в 2 раза превышает таковую в контрольной группе. Положительный эффект тетрапептида наблюдается и в случае тяжелых повреждений сетчатки. Если в контрольной группе после введения монойодуксусной кислоты (15 мг/кг) ЭРГ практически не регистрировалась в течение всего периода наблюдения у всех животных, то в опытной группе на фоне применения тетрапептида у 50% животных регистрировалась волна “в”, а к 35 суткам исследования амплитуда волны “в” ЭРГ составила 18% от исходного уровня. Как показывают данные таблицы, еще одним подтверждением положительного влияния тетрапептида на функцию поврежденной сетчатки является стабилизация амплитуды волны “в” ЭРГ на начальном этапе развития дистрофии в опытной группе, в то время как в контрольной группе наблюдалось стойкое снижение амплитуды волны “в” ЭРГ в последующие 5-10 суток после инъекции монойодуксусной кислоты. Таким образом, полученные результаты свидетельствуют о том, что заявляемый тетрапептид стимулирует функции поврежденной сетчатки при токсической дистрофических заболеваниях сетчатки, вызванных токсическим агентом. 2.2. Влияние лечебного курса тетрапептида на морфологию сетчатки при токсической дистрофии сетчатки кроликов. Действие, стимулирующее функции сетчатки, исследовано при действии тетрапептида на сетчатку в условиях ее экспериментальной дистрофии на глазах 15 половозрелых кроликов породы “шиншилла” массой 2-3 кг. Экспериментальную токсическую дистрофию сетчатки создавали путем внутривенного введения 3%-ного раствора йодистого калия в дозе 30 мг/кг. Животные опытной группы (10 кроликов) в течение 7 суток получали ежедневные однократные внутримышечные инъекции тетрапептида в дозе 0,3 мкг/кг, начиная с 10-х суток после введения токсического агента. Животные контрольной группы получали соответствующие инъекции стерильного физиологического раствора. Проводили ежедневное офтальмоскопическое исследование, а также гистологическое исследование глаз в различные сроки после введения йодистого калия. Через 1 час после введения токсического агента наблюдался отек диска зрительного нерва и сетчатки, более выраженный по периферии. Гистологически на 2-е сутки после введения йодистого калия выявлено, что сетчатка резко отечна, слои разрыхлены, в области I и III нейронов значительное накопление жидкости, кровеносные сосуды радужной оболочки переполнены. На 7-е сутки офтальмоскопически отмечалось появление аморфных очагов серовато-черного цвета по периферии глазного дна. В дальнейшем сохранялся отек сетчатой оболочки глаза, а по периферии сетчатки наблюдалось скопление пигментных клеток, расположенных ближе к углу глаза. В цилиарном теле обнаруживали сращение между собой отростоков с образованием “пещеристых лакун”. Гистологически через 5 суток после окончания курса лечения у контрольных (нелеченых) животных сохранялся умеренный отек сетчатки и наблюдались аморфные очаги по периферии сетчатки. При офтальмоскопии у кроликов, получавших тетрапептид, выявлено снижение отека сетчатки, уменьшение размеров аморфных очагов. Это подтверждали данные гистологического исследования, проведенного через 5 суток после окончания курса лечения тетрапептидом: у опытных животных отека сетчатки не обнаруживалось, сохранившиеся очаги отличались меньшими по сравнению с контролем размерами. Таким образом, результаты исследования свидетельствуют, что тетрапептид, введенный на фоне развивающихся дистрофических изменений сетчатки, вызванных токсическим агентом, уменьшает степень выраженности деструктивных изменений, предотвращает дальнейшее развитие патологического процесса и способствует нормализации структур сетчатки. Такое свойство тетрапептида позволяет предположить его высокую терапевтическую ценность при заболеваниях, сопровождающихся нарушением функции сетчатки, в частности при вторичных хориоретинальных дистрофиях, ретинопатиях различного генеза, сосудисто-ретинальных нарушениях, макулярных дегенерациях и периферических дегенерациях сетчатки, отслойке и дефектах сетчатки, поражениях сетчатки химическими и физическими факторами, других хориоретинальных расстройствах. ПРИМЕР 3 Влияние профилактического курса тетрапептида на морфологию сетчатки при токсической дистрофии. Исследовано возможное профилактическое действие тетрапептида на развитие экспериментальной дистрофии сетчатки на глазах 12 половозрелых кроликов породы “шиншилла” массой 2-3 кг. Животные опытной группы в течение 30 суток получали ежедневные однократные внутримышечные инъекции тетрапептида в дозе 0,3 мкг/кг. Животные контрольной группы получали соответствующие инъекции стерильного физиологического раствора. После окончания инъекций у животных моделировали экспериментальную токсическую дистрофию сетчатки путем внутривенного введения 3%-ного раствора йодистого калия в дозе 30 мг/кг. В дальнейшем в течение 2-х недель проводили ежедневное офтальмоскопическое исследование, а также гистологическое исследование глаз на различные сроки после введения йодистого калия. У контрольных животных после введения йодистого калия офтальмоскопически и гистологически определяли выраженный отек сетчатки и диска зрительного нерва, формирование аморфных очагов по периферии сетчатой оболочки. В отличие от контроля у животных, получавших профилактические инъекции тетрапептида, офтальмоскопически отека диска зрительного нерва и появления аморфных очагов на сетчатке не выявлено. При гистологическом исследовании сетчатки животных опытной группы патологических изменений не обнаружено. Таким образом, результаты исследования свидетельствуют, что тетрапептид, введенный в течение 1 месяца до начала действия токсического агента, обладает выраженным защитным действием и предотвращает развитие токсической дистрофии сетчатки. Такое свойство тетрапептида позволяет предположить его высокую профилактическую ценность при заболеваниях, сопровождающихся нарушением функции сетчатки, в частности при вторичных хориоретинальных дистрофиях, ретинопатиях различного генеза, сосудисто-ретинальных нарушениях, макулярных дегенерациях и периферических дегенерациях сетчатки, отслойке и дефектах сетчатки, поражениях сетчатки химическими и физическими факторами, других хориоретинальных расстройствах. ПРИМЕР 4 Применение тетрапептида при наследственной дегенерации сетчатки у крыс линии CAMBELL. Исследовали влияние тетрапептида на функцию сетчатки глаза 19 крыс линии Campbell, характеризующейся развитием наследственной дегенерации сетчатки. Пигментная атрофия сетчатки у крыс линии Campbell начинает развиваться спустя 17-20 суток после рождения и приводит к полной слепоте животных к концу 2-го месяща после рождения. Животные опытной группы (10 крыс) в течение всего срока исследования получали ежедневные однократные внутримышечные инъекции тетрапептида в дозе 1 мкг/кг, начиная с 17-х суток после рождения. Животные контрольной группы (9 крыс) получали соответствующие инъекции стерильного физиологического раствора. Функцию сетчатки у животных обеих групп оценивали по электроретинограмме (ЭРГ), регистрировавшейся на 30-е и 47-е сутки после рождения. Всех животных содержали при естественном освещении. Перед регистрацией ЭРГ крыс адаптировали к темное в течение 2-х часов. ЭРГ отводили под нембуталовым наркозом при помощи фитилькового электрода, касающегося увлажненной роговицы. Зрачок расширяли 1% раствором атропина, роговицу анестезировали 0,25%-ным раствором дикаина. В качестве фотостимула использовали белый рассеиватель. Применяли световые вспышки длительностью 100 мс, максимальная яркость стимула составляла 5  104 нт. Частоту стимуляции изменяли от одиночных до 34 импульсов в секунду. Критерием оценки эффективности тетрапептида было изменение амплитуды волны “в” ЭРГ при различных частотах воспроизведения ритма фотостимуляции.
Показатели ЭРГ у животных обеих групп на 30-е сутки после рождения представлены ниже в таблице 2.
Как видно, у крыс, получавших тетрапептид, амплитуда волны “в” ЭРГ на 30-е сутки достоверно более высокая по сравнению с контролем, причем эта разница наблюдается во всем диапазоне частоты стимулов. Кроме того, у контрольных крыс при частоте 34 имп/с не представлялось возможным вызвать соответствующие волны ЭРГ, что свидетельствует о снижении функциональных возможностей рецепторных элементов сетчатки к воспроизведению ритма стимуляции. Напротив, у животных, леченных тетрапептидом, такая способность к воспроизведению ритма стимуляции сохранялось. Следует отметить, что существенных различий в картине глазного дна у животных изученных групп выявить не представлялось возможным, однако поведенческая реакция крыс контрольной группы свидетельствовала о снижении зрительной функции.
Показатели ЭРГ у животных обеих групп на 47-е сутки после рождения представлены ниже в таблице 3.
Как и на 30-е сутки, амплитуда волны “в” ЭРГ у крыс, получавших тетрапептид, достоверно более высокая по сравнению с контролем во всем диапазоне частоты стимулов. При анализе динамики ЭРГ у контрольных животных отмечается снижение амплитуды волны “в” на 50-80% по сравнению с 30-м днем, в то время как у животных, леченных тетрапептидом, это снижение по сравнению с 30-м днем составило лишь 15-20%. Кроме того, у контрольных животных при частоте импульсов 24 в минуту и более рецепторные элементы сетчатки не воспроизводили ритм стимуляции, а у крыс, получавших тетрапептид, способность к воспроизведению ритма сохранялась при всех уровнях частоты фотостимуляции.
На глазном дне у крыс контрольной группы в эти сроки отмечались признаки абиотрофических изменений сетчатки; выраженность этих изменений в опытной группе оказалась значительно меньшей. Резкие отличия обнаруживались и в поведенческой реакции. Так, у крыс контрольной группы в отличие от опытных животных наблюдались признаки резкого падения зрительной функции.
Таким образом, проведенное исследование показывает высокую эффективность тетрапептида в предотвращении развития и лечении абиотрофии сетчатки наследственного генеза. Такое свойство ретилина позволяет предположить его высокую терапевтическую и профилактическую ценность при таких заболеваниях, как наследственные дистрофии сетчатки и врожденные аномалии глаза, сопровождающиеся нарушением функции сетчатки.
ПРИМЕР 5 104 нт. Частоту стимуляции изменяли от одиночных до 34 импульсов в секунду. Критерием оценки эффективности тетрапептида было изменение амплитуды волны “в” ЭРГ при различных частотах воспроизведения ритма фотостимуляции.
Показатели ЭРГ у животных обеих групп на 30-е сутки после рождения представлены ниже в таблице 2.
Как видно, у крыс, получавших тетрапептид, амплитуда волны “в” ЭРГ на 30-е сутки достоверно более высокая по сравнению с контролем, причем эта разница наблюдается во всем диапазоне частоты стимулов. Кроме того, у контрольных крыс при частоте 34 имп/с не представлялось возможным вызвать соответствующие волны ЭРГ, что свидетельствует о снижении функциональных возможностей рецепторных элементов сетчатки к воспроизведению ритма стимуляции. Напротив, у животных, леченных тетрапептидом, такая способность к воспроизведению ритма стимуляции сохранялось. Следует отметить, что существенных различий в картине глазного дна у животных изученных групп выявить не представлялось возможным, однако поведенческая реакция крыс контрольной группы свидетельствовала о снижении зрительной функции.
Показатели ЭРГ у животных обеих групп на 47-е сутки после рождения представлены ниже в таблице 3.
Как и на 30-е сутки, амплитуда волны “в” ЭРГ у крыс, получавших тетрапептид, достоверно более высокая по сравнению с контролем во всем диапазоне частоты стимулов. При анализе динамики ЭРГ у контрольных животных отмечается снижение амплитуды волны “в” на 50-80% по сравнению с 30-м днем, в то время как у животных, леченных тетрапептидом, это снижение по сравнению с 30-м днем составило лишь 15-20%. Кроме того, у контрольных животных при частоте импульсов 24 в минуту и более рецепторные элементы сетчатки не воспроизводили ритм стимуляции, а у крыс, получавших тетрапептид, способность к воспроизведению ритма сохранялась при всех уровнях частоты фотостимуляции.
На глазном дне у крыс контрольной группы в эти сроки отмечались признаки абиотрофических изменений сетчатки; выраженность этих изменений в опытной группе оказалась значительно меньшей. Резкие отличия обнаруживались и в поведенческой реакции. Так, у крыс контрольной группы в отличие от опытных животных наблюдались признаки резкого падения зрительной функции.
Таким образом, проведенное исследование показывает высокую эффективность тетрапептида в предотвращении развития и лечении абиотрофии сетчатки наследственного генеза. Такое свойство ретилина позволяет предположить его высокую терапевтическую и профилактическую ценность при таких заболеваниях, как наследственные дистрофии сетчатки и врожденные аномалии глаза, сопровождающиеся нарушением функции сетчатки.
ПРИМЕР 5Влияние тетрапептида на скорость восстановления световой чувствительности сетчатки после дезадаптирующего фотостимула. Проведено исследование влияния тетрапептида на скорость восстановления световой чувствительности сетчатки по восстановлению волны “в” электроретинограммы (ЭРГ) после дезадаптирующих вспышек света. У 18 кроликов массой 3-4 кг после предъявления дезадаптирующего фотостимула регистрировали ЭРГ (контроль), затем однократно внутримышечно вводили исследуемый тетрапептид в дозе 1 мкг/кг. После темновой адаптации и последующего повторного воздействия дезадаптирующего фотостимула снова регистрировали ЭРГ. Результаты исследования представлены в таблице 4. Как видно, тетрапептид существенно ускоряет восстановление световой чувствительности сетчатки на начальном этапе зрительной дезадаптации, что проявляется в достоверно более высоких значениях амплитуды волны “в” ЭРГ по сравнению с контролем. Таким образом, полученные данные свидетельствуют, что тетрапептид ускоряет восстановление световой чувствительности сетчатки после зрительной дезадаптации. В связи с этим можно сделать вывод об эффективности заявляемого средства при лечении и профилактике заболеваний сетчатки, а также иных заболеваний и патологических состояний, которые сами по себе либо посредством своих осложнений приводят к снижению функции сетчатки и могут сопровождаться такими расстройствами зрения, как нарушение полей зрения, нарушение цветоощущения, гемералопия и др. Выявленные в результате экспериментального изучения новые свойства препарата тетрапептида позволяют считать показанным его лечебное и профилактическое применение для стимулирования функций сетчатки при ряде заболеваний и патологических состояний, сопровождающихся нарушением функции сетчатой оболочки глаза. Перечень заболеваний и патологических состояний приводится в соответствии с международной классификацией заболеваний (ICD-9-CM, Вашингтон, 1989). 360 Поражения глазного яблока 360.0 Гнойный эндофтальмит 360.00 Гнойный эндофтальмит (неклассифицированный иным образом) 360.01 Острый эндофтальмит 360.02 Панофтальмит 360.03 Хронический эндофтальмит 360.04 Витреальный абсцесс 360.1 Другие эндофтальмиты 360.11 Симпатический уевит 360.12 Пануевит 360.13 Паразитарный эндофтальмит (неклассифицированный иным образом) 360.19 Другие Факоанафилактический эндофтальмин 360.2 Дегенеративные поражения глазного яблока 360.20 Дегенеративное поражение глазного яблока (неклассифицированное иным образом) 360.21 Прогрессирующая высокая (дегенеративная) миопия Злокачественная миопия 360.23 Сидероз 360.24 Другие металлозы Халькоз 360.29 Другие 361 Отслойки и дефекты сетчатки 361.0 Отслойка сетчатки с ретинальным дефектом Регматогенная отслойка сетчатки 361.00 Отслойка сетчатки с ретинальным дефектом (неклассифицированная иным образом) 361.01 Свежая отслойка, частичная, с одиночным дефектом 361.02 Свежая отслойка, частичная, с множественными дефектами 361.03 Свежая отслойка, частичная, с гигантским разрывом 361.04 Свежая отслойка, частичная, с ретинальным диализом Диализ (юношеский) сетчатки (с отслойкой) 361.05 Свежая отслойка, тотальная или субтотальная 361.06 Старая отслойка, частичная Ограниченная старая отслойка сетчатки 361.07 Старая отслойка, тотальная или субтотальная 361.1 Ретиношизис и кисты сетчатки 361.10 Ретиношизис (неклассифицированный иным образом) 361.11 Плоский ретиношизис 361.12 Буллезный ретиношизис 361.13 Первичные кисты сетчатки 361.14 Вторичные кисты сетчатки 361.19 Другие Псевдокиста сетчатки 361.2 Серозная отслойка сетчатки Отслойка сетчатки без ретинального дефекта 361.3 Дефекты сетчатки без отслойки 361.30 Дефект сетчатки (неклассифицированный иным образом) Разрыв(ы) сетчатки (неклассифицированные иным образом) 361.31 Округлое отверстие сетчатки без отслойки 361.32 Подковообразный разрыв сетчатки без отслойки Разрыв сетчатки с “крышечкой” 361.33 Множественные дефекты сетчатки без отслойки 361.8 Другие формы отслойки сетчатки 361.81 Тракционная отслойка сетчатки Тракционная отслойка с витреоретинальной организацией 361.89 Другие 361.9 Неклассифицированная отслойка сетчатки 362 Другие поражения сетчатки 362.0 Диабетическая ретинопатия Также: Диабет с офтальмологическими проявлениями (250,5) 362.01 Фоновая диабетическая ретинопатия Диабетические ретинальные микроаневризмы Диабетическая ретинопатия (неклассифицированная иным образом) 362.02 Пролиферативная диабетическая ретинопатия 362.1 Другие вторичные ретинопатии и сосудисто-ретинальные нарушения 362.10 Вторичная ретинопатия, неспецифическая 362.11 Гипертоническая ретинопатия 362.12 Экссудативная ретинопатия Синдром Коутса 362.13 Изменение внешнего вида сосудов Утолщение стенки сосудов сетчатки Атеросклероз сосудов сетчатки (440.8) 362.14 Ретинальные микроаневризмы (неклассифицированные иным образом) 362.15 Ретинальная телеангиэктазия 362.16 Ретинальная неоваскуляризация (неклассифицированная иным образом) Неоваскуляризация: хлоридальная субретинальная 362.17 Другие интраретинальные микрососудистые нарушения Ретинальные варикозы 362.18 Ретинальные васкулиты Болезнь Илза Ретинальный: артериит эндартериит Ретинальный: периваскулит флебит 362.2 Другие пролиферативные ретинопатии 362.21 Ретролентальная фиброплазия 362.29 Другие недиабетические пролиферативные ретинопатии 362.3 Окклюзия сосудов сетчатки 362.30 Окклюзия сосудов сетчатки (неклассифицированная иным образом) 362.31 Окклюзия центральной ретинальной артерии 362.32 Окклюзия ветви артерии 362.33 Частичная артериальная окклюзия Бляшка Холленхроста Ретинальная микроэмболия 362.34 Транзиторная артериальная окклюзия Преходящая слепота (ammaurosis fugax) 362.35 Окклюзия центральной ретинальной вены 362.36 Окклюзия венозной ветви 362.37 Венозный застой Окклюзия ретинальной вены: начальная частичная 362.4 Отслойка слоев сетчатки 362.40 Отслойка ретинального слоя (неклассифицированная иным образом) 362.41 Центральная серозная ретинопатия 362.42 Серозная отслойка пигментного эпителия сетчатки Экссудативная отслойка пигментного эпителия сетчатки 362.43 Геморрагическая отслойка пигментного эпителия сетчатки 362.5 Дегенерация макулы и заднего полюса 362.50 Сенильная макулярная дегенерация (неклассифицированная иным образом) 362.51 Неэкссудативная сенильная макулярная дегенерация Сенильная макулярная дегенерация: атрофическая сухая 362.52 Экссудативная сенильная макулярная дегенерация Дегенерация Кунта-Юниуса Сенильная макулярная дегенерация: дисциформная влажная 362.53 Кистевидная макулярная дегенерация 362.54 Макулярная киста, углубление или псевдоуглубление 362.55 Токсическая макулопатия 362.56 Макулярная складчатость Преретинальный фиброз 362.57 Друзы (дегенеративные) 362.6 Периферические дегенерации сетчатки 362.60 Периферическая дегенерация сетчатки (неклассифицированная иным образом) 362.61 Дегенерация типа “булыжной мостовой” 362.62 Микрокистовидная дегенерация Кисты Блессига Кисты Иванова 362.63 Решетчатая дегенерация Частокольная дегенерация сетчатки 362.64 Вторичная пигментная дегенерация Пигментный псевдоретинит 362.65 Вторичные витреоретинальные дегенерации 362.7 Наследственные дистрофии сетчатки 362.70 Наследственная дистрофия сетчатки (неклассифицированная иным образом) 362.71 Дистрофия сетчатки при системных или цереброретинальных липидозах C указанием основного заболевания, например: Цереброретинальные липидозы (330.1) Системные липидозы (272.7) 362.72 Дистрофия сетчатки при других системных расстройствах и синдромах C указанием основного заболевания, например: синдром Бессена-Корнцвейга (272.5) болезнь Рефсума (356.3) 362.73 Витреоретинальные дистрофии Юношеский ретиношизис 362.74 Пигментная дистрофия сетчатки Бело-точечная ретинальная дистрофия Пигментный ретинит 362.75 Другие дистрофии с первичным поражением сенсорного слоя сетчатки Прогрессирующая дистрофия колбочек (палочек) Болезнь Штаргардта 362.76 Дистрофии с первичным поражением пигментного эпителия сетчатки Желто-пятнистое глазное дно Вителлиформная дистрофия 362.77 Дистрофия с первичным поражением мембраны Бруха Дистрофии: гиалиновая псевдовоспалительная фовеальная Наследственные друзы 362.8 Другие расстройства сетчатки 362.81 Кровоизлияние в сетчатку Кровоизлияние: преретинальное ретинальное (глубокое, поверхностное) субретинальное 362.82 Экссудаты и отложения в сетчатку 362.83 Отек сетчатки ватообразные пятна ретинальный отек (очаговый) (макулярный) (периферический) 362.84 Ишемия сетчатки 362.85 Дефекты нервных волокнистых пучков сетчатки 362.89 Неклассифицированное расстройство сетчатки 363 Хориоретинальное воспаление, рубцы и другие расстройства сосудистой оболочки глаза 363.0 Фокальный хориоретинит и фокальный ретинохориоидит 363.00 Фокальный хориоретинит (неклассифицированный иным образом) Фокальный: хориоидит или хориоретинит ретинит или ретинохориоидит 363.01 Фокальный хориоидит и хориоретинит, юкстапапиллярный 363.03 Фокальный хориоидит и хориоретинит заднего полюса глаза другой локализации 363.04 Фокальный хориоидит и хориоретинит, периферический 363.05 Фокальный ретинит и ретинохориоидит, юкстапапиллярный Нейроретинит 363.06 Фокальный ретинит и ретинохориоидит, макулярный или парамакулярный 363.07 Фокальный ретинит и ретинохориоидит заднего полюса глаза другой локализации 363.08 Фокальный ретинит и ретинохориоидит, периферический 363.1 Диссеминированный хориоретинит и диссеминированный ретинохориоидит 363.10 Диссеминированный хориоретинит (неклассифицированный иным образом) Диссеминированный: хориоидит или хориоретинит ретинит или ретинохориоидит 363.11 Диссеминированный хориоидит и хориоретинит, заднего полюса 363.12 Диссеминированный хориоидит и хориоретинит, периферический 363.13 Диссеминированный хориоидит и хориоретинит, генерализованный C указанием основного заболевания, например: туберкулез (017.3) 363.14 Диссеминированный ретинит и ретинохориоидит, метастатический 363.15 Диссеминированный ретинит и ретинохориоидит, пигментная эпителиопатия Острая задняя мультифокальная плакоидная пигментная эпителиопатия 363.2 Другие формы и неклассифицированные формы хориоретинитов и ретинохориоидитов 363.20 Хориоретинит, неклассифицированный Хориоидит (неклассифицированный иным образом) Ретинит (неклассифицированный иным образом) Увеит, задний (неклассифицированный иным образом) 363.21 Парспланит Задний циклит 363.22 Болезнь Харады 363.3 Хориоретинальные рубцы Рубец (противовоспалительный) (постхирургический) (посттравматический): хориоидеи сетчатки 363.30 Хориоретинальный рубец, неклассифицированный 363.31 Лучевая ретинопатия 363.32 Другие рубцы макулы 363.33 Другие рубцы заднего полюса 363.34 Периферические рубцы 363.35 Диссеминированные рубцы 363.4 Дегенерация хориоидеи 363.40 Дегенерация хориоидеи, неклассифицированная Хориоидальный склероз 363.41 Сенильная атрофия хориоидеи 363.42 Диффузная вторичная атрофия хориоидеи 363.43 Ангиоидные полосы хориоидеи 363.5 Наследственные хориоидальные дистрофии Наследственная хориоидальная атрофия: частичная (капилляры) тотальная (все сосуды) 363.50 Наследственная хориоидальная дистрофия или атрофия, неклассифицированная 363.51 Околопапиллярная дистрофия хориоидеи, частичная 363.52 Околопапиллярная дистрофия хориоидеи, тотальная Геликоидная дистрофия хориоидеи 363.53 Центральная дистрофия хориоидеи, частичная Хориоидальная дистрофия: центральная ареолярная кольцевидная 363.54 Центральная дистрофия хориоидеи, тотальная Хориоидальная дистрофия: центральная спиральная ползучая 363.55 Хориоидермия 363.56 Другие диффузные или генерализованные дистрофии, частичные Диффузный хориоидальный склероз 363.57 Другие диффузные или генерализованные дистрофии, тотальные Генерализованная спиральная атрофия хориоидеи 363.6 Хориоидальные геморрагии и разрывы 363.61 Хориоидальное кровоизлияние, неклассифицированное 363.62 Экспульсивное хориоидальное кровоизлияние 363.63 Хориоидальный разрыв 363.7 Отслойка хориоидеи 363.70 Отслойка хориоидеи, неклассифицированная 363.71 Серозная отслойка хориоидеи 363.72 Геморрагическая отслойка хориоидеи 363.8 Другие расстройства хориоидеи 363.9 Неклассифицированное расстройство хориоидеи 366 Катаракта 366.3 Вторичная катаракта при заболеваниях глаз 366.34 Катаракта при дегенеративных расстройствах Подсолнечная катаракта С указанием основного заболевания, например: пигментная дистрофия сетчатки 368 Зрительные нарушения 368.4 Дефекты полей зрения 368.40 Дефект полей зрения, неклассифицированный 368.41 Скотома с вовлечением центральной области Скотома: центральная центроцекальная парацентральная 368.42 Скотома с вовлечением области слепого пятна Парацекальная скотома Расширенная: ангиоскотома слепое пятно 368.43 Секторные и дугообразные дефекты Скотома: дугообразная Бьеррума Зейделя 368.44 Другие ограниченные дефекты полей зрения Скотома: кольцевидная неклассифицированная иным образом Дефект полей зрения периферический назальная ступенька 368.5 Дефициты цветного зрения Цветовая слепота 368.51 Протановый дефект Протаномалия Протанопия 368.52 Дейтановый дефект Дейтераномалия Дейтеранопия 368.53 Тритановый дефект Тританомалия Тританопия 368.54 Ахроматопсия монохроматизм (палочковый) (колбочковый) 368.55 Приобретенные дефициты цветного зрения 368.59 Другие дефициты цветного зрения 368.6 Ночная слепота Гемералопия Никталопия 368.60 Ночная слепота, неклассифицированная 368.61 Врожденная ночная слепота Наследственная ночная слепота Болезнь Огучи 368.62 Приобретенная ночная слепота 368.63 Нарушенная кривая темновой адаптации Нарушенный порог палочек или колбочек Замедленная адаптация палочек или колбочек 368.69 Другие виды ночной слепоты 377 Поражения зрительного нерва и зрительных путей 377.0 Отек соска зрительного нерва, неклассифицированный 377.01 Отек соска зрительного нерва, связанный с повышенным внутричерепным давлением 377.02 Отек соска зрительного нерва, связанный с пониженным внутриглазным давлением 377.03 Отек соска зрительного нерва, связанный с расстройством сетчатки 377.04 Синдром Кеннеди 377.1 Атрофия зрительного нерва 377.10 Атрофия зрительного нерва, неклассифицированная 377.11 Первичная атрофия зрительного нерва 377.12 Поствостпалительная атрофия зрительного нерва 377.13 Атрофия зрительного нерва, связанная с ретинальными дистрофиями 377.14 Глаукоматозная атрофия диска зрительного нерва 377.15 Частичная атрофия зрительного нерва Временная бледность диска зрительного нерва 377.16 Наследственная атрофия зрительного нерва Атрофия зрительного нерва: доминантная наследственная Лебера 377.2 Другие поражения диска зрительного нерва 377.21 Друзы диска зрительного нерва 377.22 Кратероподобные углубления диска зрительного нерва 377.23 Колобома диска зрительного нерва 377.24 Псевдоотек соска зрительного нерва 377.3 Неврит зрительного нерва 377.30 Неврит зрительного нерва, неклассифицированный 377.31 Папиллит 377.32 Ретробульбарный неврит (острый) 377.33 Трофическая нейропатия зрительного нерва 377.34 Токсическая нейропатия зрительного нерва Токсическая амблиопия 377.39 Другие 377.4 Другие расстройства зрительного нерва 377.41 Ишемическая нейропатия зрительного нерва 377.42 Кровоизлияние в оболочки зрительного нерва 377.49 Другие Компрессия зрительного нерва 743 Врожденные аномалии глаза 743.5 Врожденные аномалии заднего сегмента 743.53 Хориоретинальная дегенерация, врожденная 743.54 Врожденные складки и кисты заднего сегмента 743.55 Врожденные изменения макулы 743.56 Другие врожденные изменения сетчатки 743.57 Классифицированные аномалии диска зрительного нерва Колобома диска зрительного нерва (врожденная) 743.58 Сосудистые аномалии Врожденная аневризма сетчатки 743.59 Другие 794 Неспецифические результаты функциональных исследований, не соответствующие норме 794.1 Периферическая нервная система и органы чувств 794.11 Нарушения, выявленные при функциональных исследованиях сетчатки Нарушения на электроретинограмме (ЭРГ) 794.12 Нарушения на электроокулограмме (ЭОГ) 794.13 Нарушения визуально индуцируемого потенциала Ниже приведены примеры клинических испытаний заявляемого средства на ограниченном контингенте больных. Проведенные исследования лечебной эффективности заявляемого средства при заболеваниях сетчатки убедительно продемонстрировали высокую клиническую эффективность данного препарата. Приведенные примеры результатов клинического изучения заявляемого препарата свидетельствуют о его высокой терапевтической ценности и подтверждают возможность его использования в качестве средства, стимулирующего функцию сетчатой оболочки глаза. ПРИМЕР 6. Применение тетрапептида при других поражениях сетчатки [362] на примере дегенерации макулы и заднего полюса [362.5]. 6.1. Тетрапептид применяли у 56 больных (112 глаз) с центральной инволюционной хориоретинальной дистрофией (неэкссудативная сенильная макулярная дегенерация [362.51] и дисциформная сенильная макулярная дегенерация [362.52]. Возраст больных составлял от 48 до 79 лет. Препарат вводился парабульбарно или внутримышечно по 10,0 мкг однократно ежедневно в течение 10 дней. Контрольную группу составили 24 больных (48 глаз) с аналогичным заболеванием, получавших традиционное в таких случаях лечение (тканевую, витаминную, сосудорасширяющую терапию) по отработанной схеме. Клиническая картина у пациентов (предисциформная стадия, неэкссудативная форма, преимущественные изменения в пигментном эпителии сетчатки) характеризовалась исчезновением макулярных рефлексов, наличием крапчатости, друз, дистрофических очагов в макулярной области. В ряде случаев наблюдалась деструкция пигментного эпителия и крапчатость в заднем полюсе глаза. У пациентов с дисциформной стадией дистрофии выявлялись выраженные изменения пигментного эпителия в макуле, рубцовые изменения, суб- и преретинальный фиброз. В 90% случаев регистрировался склероз ретинальных сосудов. Зрительные функции были снижены у всех пациентов. При флюоресцентной ангиографии выявлялись типичные признаки данной патологии (свечение друз; яркие флюоресцирующие пятна – участки просачивания элементов плазмы крови через мембрану Бруха и дефекты пигментного эпителия; ярко светящиеся полусерпа на темном фоне, свидетельствующие о наличие субретинальной неоваскуляризации). При электрофизиологическом исследовании сетчатки наблюдалось снижение активности и увеличение времени латентности I и II нейронов в макуле. Применение тетрапептида способствовало повышению зрительных функций. Острота зрения в 82,1% случаев возросла, в 17,9% – осталась без динамики и ни в одном случае не было зарегистрировано ее снижение. Количество регистрируемых положительных или относительных скотом снизилось на 68%, произошло расширение периферических границ поля зрения по различным меридианам от 5 до 10 градусов. Результаты флюоресцентной ангиографии свидетельствовали об уменьшении пропотевания красителя во всех случаях. В таблице 5 представлены данные, полученные при локальной ЭРГ электроретинографическом исследовании сетчатки до и после лечения. Как видно, инъекции тетрапептда приводили к повышению активности и снижению времени латентности I и II нейронов в макуле по результатам локальной ЭРГ. Стойкость клинического улучшения у пациентов, получивших курс препарата тетрапептида, сохранялась в 79,4% случаев полгода и в 20,6% – год и более. В контрольной группе положительный клинический результат был получен только в 39,6% случаев, кроме того, в 28,5% случаев было зарегистрировано прогрессирование патологического процесса (снижение остроты зрения, появление новых скотом в центральном поле зрения, ухудшение результатов флюоресцентной ангиографии, электрофизиологического исследования сетчатки, появление кровоизлияний на глазном дне). 6.2. Больная И., 70 лет. Амблиопия на левый глаз с детства. Диагноз: сухая склеротическая макулодистрофия (неэкссудативная сенильная макулярная дегенерация [362.51] ) на оба глаза поставлен пять лет назад. Два раза в год получала курс консервативной терапии в ведущих медицинских учреждениях города, однако зрительные функции продолжали снижаться. При осмотре: острота зрения правого глаза 0,25 не корригируется, острота зрения левого глаза 0,06 со сферой + 6,0 дптр = 0,25 не корригируется. Периферические границы поля зрения на оба глаза концентрически сужены. В поле зрения правого глаза определяются 3 относительные центральные скотомы, для левого глаза – 2. При биомикроскопии хрусталика обоих глаз в кортикальных слоях – начинающиеся помутнения. При офтальмоскопии глазного дна обоих глаз выявлены дистрофические очажки в макуле. Умеренно выраженный ангиосклероз сетчатки. Диск зрительного нерва и видимая периферия без патологических изменений. При электрофизиологическом исследовании сетчатки было выявлено снижение активности I нейрона на обоих глазах и увеличение времени латентности на правом глазу в макуле. Проведен курс парабульбарных инъекций тетрапептида в оба глаза по 10 мкг ежедневно однократно в течение 10 дней. После 4-й инъекции препарата пациентка стала отмечать субъективное улучшение (более четкое изображение, повышение зрительной работоспособности). К концу курса острота зрения повысилась на 0,3 на правом глазу и на 0,15 с коррекцией на левом. Произошло расширение периферических границ поля зрения по различным меридианам на 5 – 13 градусов. В поле зрения правого глаза скотомы исчезли полностью, а левого – осталась одна. По данным электрофизиологического исследования сетчатки было зарегистрировано значительное повышение активности I нейрона в макуле на обоих глазах. Динамическое наблюдение в течение 6 месяцев показало стабилизацию патологического процесса. 6.3. Больной Л., 49 лет, обратился к офтальмологу в связи с ухудшением зрения на оба глаза и появлением пятен перед правым глазом. Снижение остроты зрения и появление скотом в поле зрения отметил год назад. Диагноз: макулопатия обоих глаз (дегенерация макулы и заднего полюса [362.5]) При осмотре: острота зрения правого глаза 0,4, левого – 0,85. В поле зрения правого глаза определяются две абсолютные центральные скотомы. При биомикроскопии оптические среды прозрачные. При офтальмоскопии глазного дна правого глаза в макуле определяется небольшой дефект с перифокальным отеком и мелкими дистрофическими очажками парамакулярно. Ход и калибр сосудов не изменен. Диск зрительного нерва и видимая периферия без патологических изменений. При офтальмоскопии левого глаза определяется нечеткость макулярного рефлекса. Ход и калибр сосудов не изменен. ДЗН и видимая периферия без патологических изменений. По данным электрофизиологического исследования сетчатки отмечается изменение активности I нейрона в макуле справа, остальные показатели – на верхней границе нормы. Проведен курс парабульбарных инъекций тетрапептида в оба глаза по 10 мкг ежедневно однократно в течение 10 дней. После второй инъекции пациент стал отмечать, что скотомы уменьшились в размерах и посветлели. Ежедневно пациент фиксировал динамику размеров скотом по сетке Амслера. С первых дней лечения больной отмечал субъективные положительные зрительные ощущения, которые шли параллельно с повышением остроты зрения. К концу курса препаратом тетрапептида острота зрения на оба глаза достигла 1,0. В поле зрения правого глаза осталась только одна скотома, которая значительно уменьшилась в размерах и посветлела. При офтальмоскопии глазного дна правого глаза макулярный отек полностью исчез, макулярный рефлекс на левом глазу стал более четким. При электрофизиологическом исследовании сетчатки все показатели оказались в пределах нормы. Таким образом, применение препарата заявляемого тетрапептида является эффективным методом лечения центральных дистрофических процессов (дегенерация макулы и заднего полюса [362.5]). ПРИМЕР 7. Применение тетрапептида при прогрессирующей высокой (дегенеративной) миопии [360.20]. 7.1. Тетрапептид применяли у пациентов с миопией высокой степени и изменениями на глазном дне. Основную группу составили 39 больных (78 глаз), страдающих миопической болезнью. Возраст больных колебался от 19 до 43 лет. Препарат тетрапептида вводился парабульбарно или внутримышечно по 10,0 мкг однократно ежедневно в течение 10 дней. Контрольную группу составили 16 больных (32 глаза) со сходной клинической картиной и получающих принятую в этих случаях трофическую терапию. Клиническая картина у всех больных характеризовалась дистрофическими изменениями во всех оболочках глаза и средах, но в первую очередь в сетчатке. При офтальмоскопии было выявлено: миопический конус у диска зрительного нерва, истинные стафиломы склеры, дистрофически измененные участки сетчатки, разрывы сетчатки, участки отслойки сетчатки. Результаты электроретинографии (ЭРГ) сетчатки свидетельствовали о снижении активности и увеличении времени латентности I и II нейронов в общей ЭРГ. Все пациенты, получившие тетрапептид, отмечали субъективное повышение зрительных функций – изображение становилось более четким, ярким, пропадали “мушки” в поле зрения, повышалась зрительная работоспособность. Кроме того, отмечалось улучшение временных показателей зрительного последовательного образа, вызванного цветострессом. В таблице 6 представлены данные, полученные при общей ЭРГ сетчатки до и после лечения. Результаты исследований показывают, что после проведения курса лечения препаратом тетрапептида происходит увеличение активности и снижение времени латентности I и II нейронов в общей ЭРГ. Полученные данные также свидетельствуют об улучшении процессов метаболизма в сетчатке и увеличении проводимости импульсов между нейронами зрительного анализатора. Необходимо отметить, что регулярное применение заявляемого препарата предотвращало появление дистрофически измененных участков сетчатки, разрывов или ее отслойки. У пациентов контрольной группы курс трофической терапии в большинстве случаев не давал никакой положительной динамики в клинической картине. 7.2. Больной П., 28 лет. Близорукость с детства. В 1983 была произведена склероукрепляющая операция на оба глаза, однако миопия продолжала прогрессировать. В феврале 1997 была произведена лазеркоагуляция (ЛК) клапанных разрывов сетчатки на оба глаза. Диагноз: прогрессирующая высокая (дегенеративная) миопии обоих глаз [360.20]. При осмотре: жалобы на быструю утомляемость, снижение зрительной работоспособности и метаморфопсии в поле зрения обоих глаз. Острота зрения правого глаза – 0,03 со сферой – 15,0 дптр = 0,3; левого глаза – 0,03 со сферой – 15,0 дптр = 0,2. При биомикроскопии определяется деструкция стекловидного тела обоих глаз. На глазном дне правого глаза: диск зрительного нерва с сероватым оттенком, стафилома. Сосуды умеренно сужены. Перераспределение пигмента по всему глазному дну. На 11-й часах клапанный разрыв отграничен ЛК. На глазном дне левого глаза изменения аналогичны правому, однако клапанный разрыв сетчатки, отграниченный ЛК, располагается на 2-х часах. Результаты ЭРГ свидетельствовали о снижении активности I нейрона, увеличении времени латентности II нейрона с обоих сторон и резком снижении амплитудной активности II нейрона слева. Проведен курс парабульбарных инъекций тетрапептида в оба глаза по 10 мкг ежедневно однократно в течение 10 дней. Субъективные положительные зрительные ощущения пациент стал отмечать после 4 инъекции препарата. К концу курса полностью пропали жалобы на метаморфопсии в поле зрения обоих глаз, существенно повысилась зрительная работоспособность. Острота зрения осталась прежней, однако повысилась яркость и контрастность изображения. Данные ЭРГ свидетельствовали о повышении амплитудной активности и о снижении времени латентности I и II нейронов с обеих сторон. ПРИМЕР 8. Применение тетрапептида при других поражениях сетчатки [362] на примере наследственных центральных тапеторетниальных абиотрофий сетчатки типа Штаргардта, Беста и Франческитти. 8.1. Тетрапептид применяли у 36 больных (72 глаза) в возрасте 18-49 лет с наследственными центральными тапеторетинальными абиотрофиями типа Штаргардта [362.75] , Беста (вителлиформная дистрофия [362.76] и Франческетти (желто-пятнистое глазное дно [362.76]), Препарат тетрапептида вводили парабульбарно по 10,0 мкг однократно ежедневно в течение 10 дней. Контрольную группу составили 20 больных (40 глаз) с тапеторетинальными абиотрофиями, получивших традиционную терапию. На 32 глазах с наследственными центральными тапеторетинальными абиотрофиями типа Штаргардта, Беста и Франческетти в начальной и развитой стадии при парабульбарном введении тетрапептида наблюдали выраженный положительный эффект. Было отмечено повышение остроты зрения на 0,1-0,35, расширение периферических границ поля зрения по различным меридианам на 10o и более, исчезновение в центральном поле зрения скотом. Также наблюдали положительную динамику в цветоощущении (различение синего цвета), значительное уменьшении деструктивных изменений пигментного эпителия на флюоресцентных ангиограммах и положительную динамику показателей ЭРГ. В далеко зашедшей стадии наследственных центральных тапеторетинальных абиотрофий (40 глаз) также был зарегистрирован положительный клинический эффект при лечении препаратом тетрапептида: повышение остроты зрения до 0,1, расширение периферических границ поля зрения по различным меридианам от 5o и выше, уменьшение размеров центральных скотом в поле зрения, положительная динамика в цветоощущении и показателей ЭРГ. У контрольных больных, получавших традиционные методы лечения, выраженный положительный результат был отмечен только в 20% случаев. Таким образом, применение заявляемого тетрапептида является эффективным методом лечения наследственных центральных тапеторетинальных абиотрофий типа Штаргардта, Беста и Франческетти. ПРИМЕР 9. Применение тетрапептида у больных с пигментным ретинитом [362.74]. Препарат тетрапептида применяли у 32 больных (64 глаза) в возрасте 18-69 лет с пигментной периферической абиотрофией сетчатки (пигментный ретинит [362.74] ). Тетрапептид применяли в виде парабульбарных инъекций по 10,0 мкг однократно ежедневно в течение 10 дней. Контрольную группу составили 25 больных (50 глаз) пигментным ретинитом, пролеченных традиционными методами (сосудорасширяющие средства, ангиопротекторы, противосклеротические препараты, витаминная и тканевая терапия). У больных контрольной и опытной групп до проведения лечения наблюдались характерные для пигментной периферической абиотрофии изменения: снижение остроты зрения, нарушения границ поля зрения (сужение периферических границ поля зрения, наличие парацентральных скотом в поле зрения), нарушения цветоощущения, нарушение темновой адаптации, изменение офтальмоскопической картины глазного дна (пигментация глазного дна, характерное “восковидное” окрашивание зрительного нерва), нарушение электрофизиологических показателей (снижение амплитуды волны “в” электроретинограммы, а также светотемнового коэффициента Ардена). Уже на первой неделе лечения препаратом заявляемого тетрапептида наблюдали улучшение зрительных функций у 75,0% больных в основной группе. К концу курса лечения 90,6% больных отмечали субъективные положительные зрительные ощущения, которые имели подтверждения данными офтальмологического осмотра. В первую очередь повышалась острота зрения, происходило расширение периферических границ полей зрения, а также уменьшение или исчезновение парацентральных скотом. В таблице 7 представлены результаты исследований электрофизиологических показателей. Как видно, у всех пациентов основной группы наблюдалось повышение амплитуды волны “в” электроретинограммы и светового коэффициента Ардена, что свидетельствует о положительном влиянии тетрапептида на сетчатую оболочку глаза больных пигментным ретинитом. В контрольной группе положительный клинический эффект был получен только в 24% случаев. Таким образом, проведенное исследование показало, что заявляемый тетрапептид оказывает стимулирующее влияние на зрительные функции глаза у больных с пигментным ретинитом и, следовательно, является высоко эффективным средством лечения. ПРИМЕР 10. Применение тетрапептида при диабетической ретинопатии [361.0]. 10.1. Тетрапептид применяли у 52 больных (104 глаз) в возрасте 21-69 лет с диабетической ретинопатией [362.0]. Препарат вводили парабульбарно по 10,0 мкг однократно ежедневно в течение 10 дней. Контрольную группу составили 21 человек, которые получали стандартную в таких случаях терапию (сосудорасширяющие препараты, ангиопротекторы). У всех пациентов была диагностирована диабетическая ретинопатия (ДР) на разных стадиях. В таблице 8 представлено изменение показателей остроты зрения у больных с диабетической ретинопатией до и после проведения курса лечения препаратом. Как правило, под влиянием тетрапептида первой менялась острота зрения. Уже после нескольких инъекций пациенты отмечали субъективные положительные зрительные ощущения, которые шли параллельно с улучшением зрительных функций. Повышение остроты зрения имело тенденцию к нарастанию по мере прохождения курса лечения. Из таблицы 8 видно, что в 49,1% случаев острота зрения по окончанию лечения достигла максимальных величин – 0,9-1,0. Это на 21,2% больше, чем до лечения. В 21,1% случаев показатели остроты зрения находились в пределах от 0,0 до 0,1 и в 29,8% случаев от 0,2 до 0,8. В контрольной группе под влиянием традиционной терапии увеличение остроты зрения до максимальных величин – 0,9 – 1,0 произошло только в 9,6% случаев, что в два раза меньше, чем в основной группе. Изменения остроты зрения под влиянием препарата оказались неравномерными при различных стадиях диабетической ретинопатии (ДР). Лица, имеющие ранние стадии заболевания, оказались более восприимчивыми к лечению и давали более быстрое и стойкое повышение остроты зрения в среднем на 0,2-0,4. Так, при непролиферативной стадией ДР острота зрения достигала максимальной величины -1,0 в 68,7% случаев. C переходом заболевания на более тяжелые стадии (препролиферативную, пролиферативную) острота зрения уже в меньшем проценте случаев (28,9%) достигала 1,0, что было связано с наличием тяжелых осложнений (осложненной или вторичной катарактой, грубыми пролиферативными изменениями, гемофтальмом). В связи с этим острота зрения в данных группах увеличилась только на сотые или 0,1-0,2. У всех пациентов, имевших до лечения тетрапептидом сужение поля зрения вследствие сочетания ДР с ангиосклерозом, удалось расширить периферические границы поля зрения по различным меридианам на 5-15o. Улучшение офтальмоскопической картины глазного дна наблюдалось у преобладающего большинства больных. Так, в 81,3% случаев наблюдалось частичное или полное рассасывание гемо- и плазморрагий. В остальных 18,7% случаев не произошло значительных изменений в офтальмоскопической картине за счет наличия тяжелых осложнений. Тем не менее у всех пациентов, получивших тетрапептид, наблюдалась явная тенденция к рассасыванию кровоизлияний и экссудатов. По данным флюоресцентной ангиографии глазного дна (ФАГД) после курса лечения препаратом тетрапептида было выявлено уменьшение пропотевания красителя из сосудов, уменьшение количества микроаневризм в центральных и парацентральных областях глазного дна. В таблице 9 приведены некоторые показатели углеводного обмена у пациентов с диабетической ретинопатией до и после лечения заявляемым средством. Видно, что в результате проведенного лечения у всех пациентов достоверно снизился уровень сахара, гликолизировнный гемоглобин. Произошла нормализация иммунного статуса. Нами отмечено достоверное увеличение количества T – клеток с фенотипом CD 3 (T-клетки) с 51,3  0,5% до 65,3 0,5% до 65,3 0,1%, иммунорегуляторного индекса 0,1%, иммунорегуляторного индексаCD4/CD8 до 1,86  0,04 за счет увеличения CD8 с 16,9 0,04 за счет увеличения CD8 с 16,9 0,8 до 21,3 0,8 до 21,3 0,5%. Кроме того, у 90% больных, страдающих ГБ, было достигнуто стойкое снижение артериального давления.
В контрольной группе только в 22,5% случаев произошло повышение зрительных функций, причем повышение остроты зрения не превышало 0,15. В остальных случаях (77,5%) острота зрения либо не изменилась, либо снизилась. Не было зарегистрировано достоверного расширения периферических границ поля зрения после проведенного традиционного лечения. В офтальмоскопической картине глазного дна также не произошло существенной динамики. Только в 21,4% случаев была отмечена тенденция к рассасыванию мелких кровоизлияний. В 69,1% случаев офтальмоскопическая картина осталась без изменений, а в 9,5% – ухудшилась (появились новые кровоизлияния и плазморрагии). По данным ФАГД не было зарегистрировано существенных изменений после проводимого лечения. У пациентов контрольной группы отмечалась некоторая тенденция в снижении уровня сахара в крови и нормализации иммунологических показателей, однако достоверных данных нами получено не было. Каких-либо существенных изменений показателей артериального давления также не было зафиксировано.
10.2. Больной С. , 20 лет. Диабет I типа с 10 лет (с 1987). Наследственность отягощена – диабет у отца. Глазные проявления диабета выявлены с января 1996. Каждые полгода на фоне общей терапии пациент получал курс тауфона парабульбарно – улучшений не отмечалось. Был поставлен вопрос о лазеркоагуляции сетчатки.
Диагноз: пролиферативная стадия диабетической ретинопатии обоих глаз.
Макулопатия обоих глаз.
При осмотре: острота зрения правого глаза = 0,5, острота зрения левого глаза 0,2 сфера + 1,5 дптр = 0,2 Оптические среды прозрачные. Внутриглазное давление в норме. На глазном дне: диск зрительного нерва – розового цвета с сероватым оттенком, неоваскуляризация с височной стороны (больше на левом глазу). Вены расширены, извиты. По ходу сосудов множество мелких геморрагий. В макуле офтальмоскопируются несколько “твердых” эксудатов, геморрагий. На левом глазу количество ретинальных кровоизлияний значительно больше.
Результаты определения уровня сахара и ацетона в суточной мочи: 0,5%. Кроме того, у 90% больных, страдающих ГБ, было достигнуто стойкое снижение артериального давления.
В контрольной группе только в 22,5% случаев произошло повышение зрительных функций, причем повышение остроты зрения не превышало 0,15. В остальных случаях (77,5%) острота зрения либо не изменилась, либо снизилась. Не было зарегистрировано достоверного расширения периферических границ поля зрения после проведенного традиционного лечения. В офтальмоскопической картине глазного дна также не произошло существенной динамики. Только в 21,4% случаев была отмечена тенденция к рассасыванию мелких кровоизлияний. В 69,1% случаев офтальмоскопическая картина осталась без изменений, а в 9,5% – ухудшилась (появились новые кровоизлияния и плазморрагии). По данным ФАГД не было зарегистрировано существенных изменений после проводимого лечения. У пациентов контрольной группы отмечалась некоторая тенденция в снижении уровня сахара в крови и нормализации иммунологических показателей, однако достоверных данных нами получено не было. Каких-либо существенных изменений показателей артериального давления также не было зафиксировано.
10.2. Больной С. , 20 лет. Диабет I типа с 10 лет (с 1987). Наследственность отягощена – диабет у отца. Глазные проявления диабета выявлены с января 1996. Каждые полгода на фоне общей терапии пациент получал курс тауфона парабульбарно – улучшений не отмечалось. Был поставлен вопрос о лазеркоагуляции сетчатки.
Диагноз: пролиферативная стадия диабетической ретинопатии обоих глаз.
Макулопатия обоих глаз.
При осмотре: острота зрения правого глаза = 0,5, острота зрения левого глаза 0,2 сфера + 1,5 дптр = 0,2 Оптические среды прозрачные. Внутриглазное давление в норме. На глазном дне: диск зрительного нерва – розового цвета с сероватым оттенком, неоваскуляризация с височной стороны (больше на левом глазу). Вены расширены, извиты. По ходу сосудов множество мелких геморрагий. В макуле офтальмоскопируются несколько “твердых” эксудатов, геморрагий. На левом глазу количество ретинальных кровоизлияний значительно больше.
Результаты определения уровня сахара и ацетона в суточной мочи:I порция 750 мл, удельный вес 1020, ацетон ” – “, сахар – 2,4% II порция 600 мл, удельный вес 1022, ацетон ” – “, сахар – 5,6% III порция 500 мл, удельный вес 1025, ацетон ” – “, сахар – 5,4%. Результаты определения уровня сахара в крови: 9.00-17,7 ммоль/л 11.00-12,9 ммоль/л 13.00 -13,8 ммоль/л Проведен курс парабульбарных инъекций препарата тетрапептида в оба глаза по 10 мкг ежедневно однократно в течение 10 дней. При осмотре: острота зрения правого глаза = 1,0, острота зрения левого глаза = 0,2 сфера + 1,5 дптр = 0,6 На глазном дне: правый глаз – диск зрительного нерва розового цвета, с четкими контурами. Ретинальные геморрагии по ходу сосудов полностью рассосались, в макуле значительно уменьшилось количество “твердых” экссудатов. На левом глазу – остались единичные геморрагии. Результаты определения уровня сахара и ацетона в суточной мочи: I порция 100 мл, удельный вес 1022, ацетон ” – “, сахар – 2,0% II порция 150 мл, удельный вес 1011, ацетон ” – “, сахар – 0,4% III порция 250 мл, удельный вес 1014, ацетон ” – “, сахар – 0,2% Результаты определение уровня сахара в крови. 9.00-15,7 ммоль/л 11.00-12,3 ммоль/л 13.00-7,4 ммоль/л Под действием заявляемого тетрапептида значительно повысилась острота зрения (особенно на правом глазу), значительно уменьшилось количество гемо- и плазморрагий (на правом глазу – полностью рассосались). По клинико-лабораторным данным видно, что имеется тенденция к снижению уровня сахара в крови, хотя они и не достигли уровня нормы. Сам пациент стал отмечать после курса лечения улучшение самочувствия, повышение работоспособности. К сожалению, флюоресцентная ангиография (ФАГД) сетчатки не была произведена в связи с неблагоприятным аллергическим анамнезом. Однако ни аллергических, ни побочных реакций после применения тетрапептида у пациента не было выявлено. 10.3 Больная Ж., 59 лет. Диабет II типа с 1992 года. Глазные проявления диабета выявлены с конца августа 1997 года. Диагноз: Препролиферативная стадия диабетической ретинопатии обоих глаз. При осмотре: острота зрения правого глаза = 0,5, острота зрения левого глаз = 0,9. Оптические среды прозрачные. Внутриглазное давление в норме. На глазном дне: диск зрительного нерва удовлетворительного питания, с четкими границами. Артерии умеренно сужены. Вены расширены, извиты. По ходу сосудов множестве ретинальных кровоизлияний и плазморрагий (больше на левом глазу). На правою глазу – преретинальное кровоизлияние 2/3 диаметра диска зрительного нерва (DD). Данные ФАГД: обильное пропотевание красителя из сосудов, множество микроаневризм в центральных и парацентральных областях глазного дна. Уровень сахара в крови – 8,9 ммоль/л Гликолизированный гемоглобин – 8,25% Проведен курс парабульбарных инъекций препарата тетрапептида в оба глаза по 10 мкг ежедневно однократно в течение 10 дней. При осмотре: острота зрения правого глаза = 0,8, острота зрения левого глаза = 1,0. Оптические среды прозрачные. Внутриглазное давление в норме. На глазном дне: диск зрительного нерва удовлетворительного питания, с четкими границами. Сосуды – без изменений. Количество геморрагий и плазморрагий значительно уменьшилось. Преретинальное кровоизлияние на правом глазу полностью рассосалось. Данные ФАГД: по сравнению с результатами ФАГД от 10/XII – 97 выявлено значительное уменьшение пропотевания красителя из ретинальных сосудов, уменьшение количества микроаневризм. Уровень сахара в крови – 5,47 ммоль/л Гликолизированный гемоглобин – 6,1% (через 2 месяца после курса пептидных биорегуляторов). Под действием тетрапептида значительно повысилась острота зрения (особенно на правом глазу). Уменьшилось количество геморрагий и плазморрагий, полностью рассосалось преретинальное кровоизлияние на правом глазу. Значительно улучшились результаты ФАГД. Снизился уровень сахара и гликолизированного гемоглобина в крови. Больная отмечает улучшение самочувствия. Таким образом, в результате проведенной терапии с применением тетрапептида у 96,5% больных достигнуто клиническое улучшение в различной степени. Кроме повышения зрительных функций (повышение остроты зрения, расширение полей зрения, улучшение результатов флюоресциентной ангиографии и офтальмоскопической картины глазного дна) заявляемый тетрапептид способствует улучшению соматического статуса пациентов с ДР (нормализация иммунного статуса, гликолизированного гемоглобина, сахара в крови, снижение артериального давления у гипертоников, улучшение самочувствия). Источники информации 1. Терапевтическая офтальмология. Под ред. М.Л. Краснова, Н.Б. Шульпиной.- М.: Медицина, 1985, с.33, 340, 358. 2. Кацнельсон Л.А., Форофонова Т.И., Бунин А.Я. Сосудистые заболевания глаз.- М.: Медицина, 1990, с. 249-256. 3. Машковский М.Д. Лекарственные средства. – М.: Медицина, 1988, т. 1, стр. 450, 456-457, 461; т. 2, стр. 6,181. 4. Патент РФ N 2073518, МКИ A 61 K 35/44, 1993. 5. Якубке Х.-Д. и Ешкайт X. Аминокислоты, пептиды, белки: Пер. с нем. – М.: Мир, 1985. – 456 с. Формула изобретения
РИСУНКИ
|
||||||||||||||||||||||||||
