Патент на изобретение №2339635
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) ПИРИДИЛМЕТИЛАНИЛИДЫ ГЕТЕРОЦИКЛИЧЕСКИХ КИСЛОТ, ОБЛАДАЮЩИЕ ФУНГИЦИДНОЙ АКТИВНОСТЬЮ
(57) Реферат:
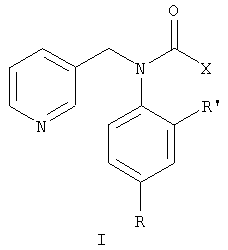
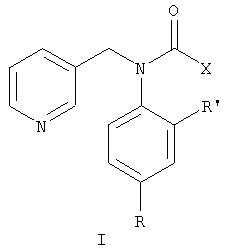
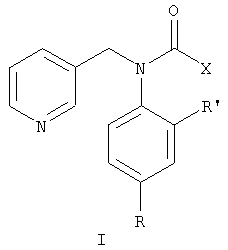
Изобретение относится к пиридилметиланилидам гетероциклических кислот общей формулы I, где R означает атом водорода, галогена или бензилокси-группу, R’ означает атом водорода или галогена, Х означает 2-фурил или 2-пиридил. Технический результат заключается в получении соединений, эффективных против вредоносных грибов. 3 табл.
Изобретение относится к химии гетероциклических соединений, а именно пиридилметиланилидам гетероциклических кислот общей формулы I, где R означает атом водорода, галогена или бензилокси-группу, R’ означает атом водорода или галогена, Х означает 2-фурил или 2-пиридил, обладающим фунгицидной активностью.
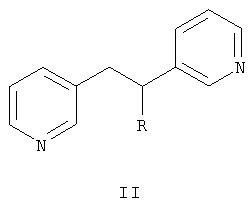
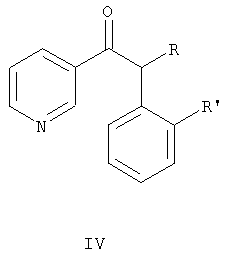
Пиридилметиланилиды гетероциклических кислот общей формулы I могут найти применение для борьбы с вредоносными грибами в медицине, ветеринарии, сельском хозяйстве, строительстве. Известны соединения общей формулы II, где R означает алкил, циклоалкил, PhCH2, Ph, пиридил, тиенил [Патент US 3397273, 1968], обладающие фунгицидной активностью.
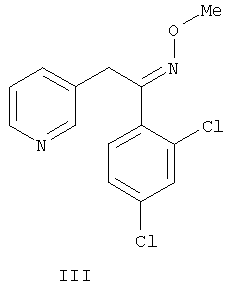
Известен пирифенокс (III), обладающий фунгицидной активностью. [Пестициды и регуляторы роста растений / Н.Н.Мельников, К.В.Новожилов, С.Р.Белан. – М.: Химия, 1995. – 576 с.].
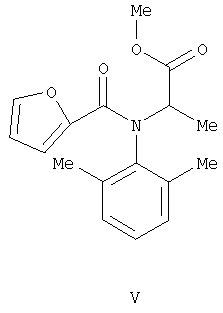
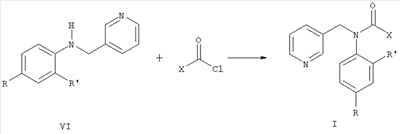
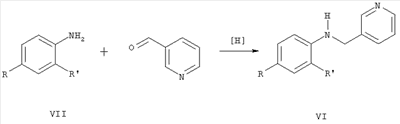
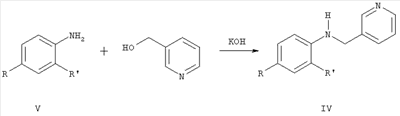
Среди анилидов гетероциклических кислот известны соединения общей формулы IV, где R означает алкил или циклоалкил, R’ означает циано-, нитро- или карбометокси-группу, обладающие фунгицидной активностью [Пат. WO 95/25723, 1994]. Наиболее близок по структуре к соединениям общей формулы I фуралаксил (V) [Пат. GB 1448810, 1976], обладающий фунгицидной активностью. Однако соединения структур II-V имеют узкий спектр действия и проявляют фунгицидную активность только в отношении отдельных видов грибов. Кроме того, к фунгицидам у грибов часто развивается устойчивость. Техническая задача, решаемая настоящим изобретением, состоит в расширении ассортимента фунгицидов для более эффективной борьбы с вредоносными грибами. Поставленная задача решается получением пиридилметиланилидов гетероциклических кислот общей формулы I, обладающих фунгицидной активностью. Пиридилметиланилиды гетероциклических кислот общей формулы I могут быть получены взаимодействием пиридилметиланилинов общей формулы VI, где R и R’ имеют те же значения, что и в формуле I, с хлорангидридами пирослизевой или пиколиновой кислот (X=2-фурил или 2-пиридил): Аналогичные реакции описаны в литературе [Вейганд-Хильгетаг. Методы эксперимента в органической химии. – М.: «Химия», 1968. – 944 с.]. Соединения общей формулы VI могут быть получены из анилинов общей формулы VII, где R и R’ имеют те же значения, что и в формуле I, и 3-пиридинкарбальдегида конденсацией в присутствии боргидрида натрия или муравьиной кислоты с последующим гидролизом полученного формамида (реакция Лейкарта-Валлаха) или восстановлением оснований Шиффа, полученных из тех же соединений, боргидридом натрия, алюмогидридом лития или водородом с использованием катализаторов: Также они могут быть получены алкилированием анилинов общей формулы V 3-пиридилкарбинолом: Аналогичные реакции описаны в литературе [Органикум: в 2-х т., пер. с нем. – М.: Мир, 1979; S. Miyano, A. Uno, N. Abe. Chem. Farm. Bull., 1958, 15(4), p.515-517]. Изобретение может быть проиллюстрировано следующими примерами: Пример 1. Раствор 4,28 г (0,04 моль) 3-пиридинкарбальдегида, 3,72 г (0,04 моль) свежеперегнанного анилина и каталитического количества n-толуолсульфокислоты в 36 мл толуола кипятили 6 ч с насадкой Дина-Старка, после чего растворитель отогнали в вакууме. К остатку прибавили 5,25 мл (0,13 моль) 93%-ной муравьиной кислоты и кипятили с обратным холодильником 15 ч, затем прибавили 50 мл 6N соляной кислоты, продолжали кипячение в течение 1,5 ч. Реакционную массу охладили, прибавили 50%-ный водный раствор гидроксида натрия до рН 12, Продукт экстрагировали хлороформом (3×20 мл), экстракт сушили над безводным сульфатом магния, растворитель отогнали в вакууме. Остаток перегоняли в вакууме, собирая фракцию с т.кип. 120-130°С (0,1 мм рт.ст.). После перекристаллизации из смеси гексан – толуол (4:1) получили 3 г (40%) N-(пирид-3-илметил)анилина в виде светло-коричневых кристаллов с т.пл. 95-96°С. ЯМР 1Н-спектр ( Пример 2. Смесь 7,2 г (0,0417 моль) n-броманилина, 5 г (0,0417 моль) пирид-3-илкарбинола и 0,374 г (0,007 моль) гидроксида калия нагревали до 245°С и выдерживали при этой температуре 1 ч. Выделявшуюся воду отгоняли. Реакционную массу охлаждали, выливали в 50 мл воды и нейтрализовали 5%-ной соляной кислотой. Раствор экстрагировали хлороформом (3×20 мл), экстракт сушили над безводным сульфатом магния. Растворитель отгоняли в вакууме, а остаток перегоняли, собирая фракцию с т.кип. 150-160°С (0,1 мм рт.ст.). После перекристаллизации из смеси гексан-толуол (4:1) получили 4,7 г (43%) N-(пирид-3-илметил)-4-броманилина в виде светло-желтых кристаллов, с т.пл. 89-90°С. ЯМР 1Н-спектр ( Пример 3. К 0,68 г (3,8 ммоль) гидрохлорида хлорангидрида пиколиновой кислоты в 15 мл хлористого метилена добавляли 1,06 мл (7,6 ммоль) сухого триэтиламина и 0,64 г (3,2 ммоль) N-(пирид-3-илметил)-4-фторанилина. Смесь перемешивали в течение 4 ч. Растворитель отгоняли в вакууме, к остатку прибавляли 15 мл воды и экстрагировали хлороформом (3×10 мл). Экстракт промывали 15 мл 10%-ного раствора карбоната калия, водой, сушили над безводным сульфатом магния. Растворитель отгоняли в вакууме, а остаток очищали методом колоночной хроматографии (элюент – хлороформ). Получили 0,72 г (74%) N-(пирид-3-илметил)-4′-фторпиколинанилида (4) в виде белых кристаллов с т.пл. 105-106°С. ЯМР 1Н-спектр ( Пример 4. К 0,65 г (5 ммоль) хлорангидрида пирослизевой кислоты в 20 мл хлористого метилена добавляли 0,7 мл (5 ммоль) сухого триэтиламина и 0,9 г (4,5 ммоль) N-(пирид-3-илметил)-4-(бензилокси)анилина Смесь перемешивали в течение 4 ч. Растворитель отгоняли в вакууме, к остатку прибавляли 20 мл воды, экстрагировали хлороформом (3×0 мл). Экстракт промывали 15 мл 10%-ного раствора карбоната калия, водой, сушили над безводным сульфатом магния. Растворитель отгоняли в вакууме, а остаток очищали методом колоночной хроматографии (элюент – хлороформ). Получили 1,5 г (78%) N-(пирид-3-илметил)-4′-(бензилокси)фуран-2-карбоксанилида (11) в виде желтого масла. ЯМР 1Н-спектр ( ЯМР 1Н-спектры зарегистрированы на приборе Bruker AM300 в DMSO-d6. Выходы и температуры плавления пиридилметиланилидов гетероциклических кислот общей формулы I представлены в табл.1, ЯМР 1Н-спектры – в табл.2.
Пример 5. Испытания на фунгицидную активность соединений проводили in vitro на грибах Ventwia inaequalis (V.i.), Rhizocionia solani (R.s,), Fuzarium oxysporum (F.o.), Sclerotinia sclerotiorum (S.s.), Helminthosporium sativum (H.s.), Fuzarium moniliforme (F.m.) при концентрации активного компонента 30 мг/л. В качестве питательной среды использовали сахарозно-картофельный агар. Инокулированные среды выдерживали в термостате при 25 С в течение 3 суток. Активность соединений определяли как процент подавления роста мицелия гриба по отношению к контролю. В качестве эталона использовали коммерческий фунгицид триадимефон. Фунгицидная активность замещенных анилидов никотиновой кислоты общей формулы I приведена в табл.3.
Формула изобретения
Пиридилметиланилиды гетероциклических кислот общей формулы I, где R означает атом водорода, галогена или бензилокси-группу, R’ означает атом водорода или галогена, Х означает 2-фурил или 2-пиридил.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 , м.д., J, Гц): 4.28 с (2Н, СН2), 6.10 с (1Н, NH), 6.50-6.65 м (3Н, СН фен.), 7.06 т (2Н, СН фен., J=7.8), 7.30-7 40 м (1Н, СН пирид.), 7 75 д (1Н, СН пирид., J=8.9), 8.45 д (1Н, СН пирид., J=4.4), 8.60 с (1Н, СН пирид.).
, м.д., J, Гц): 4.28 с (2Н, СН2), 6.10 с (1Н, NH), 6.50-6.65 м (3Н, СН фен.), 7.06 т (2Н, СН фен., J=7.8), 7.30-7 40 м (1Н, СН пирид.), 7 75 д (1Н, СН пирид., J=8.9), 8.45 д (1Н, СН пирид., J=4.4), 8.60 с (1Н, СН пирид.).