Патент на изобретение №2238106
|
||||||||||||||||||||||||||
(54) ПРЕПАРАТ ВНУТРИВЕННОГО ПРОТИВОАЛЛЕРГИЧЕСКОГО ИММУНОГЛОБУЛИНА И СПОСОБ ЕГО ПОЛУЧЕНИЯ
(57) Реферат:
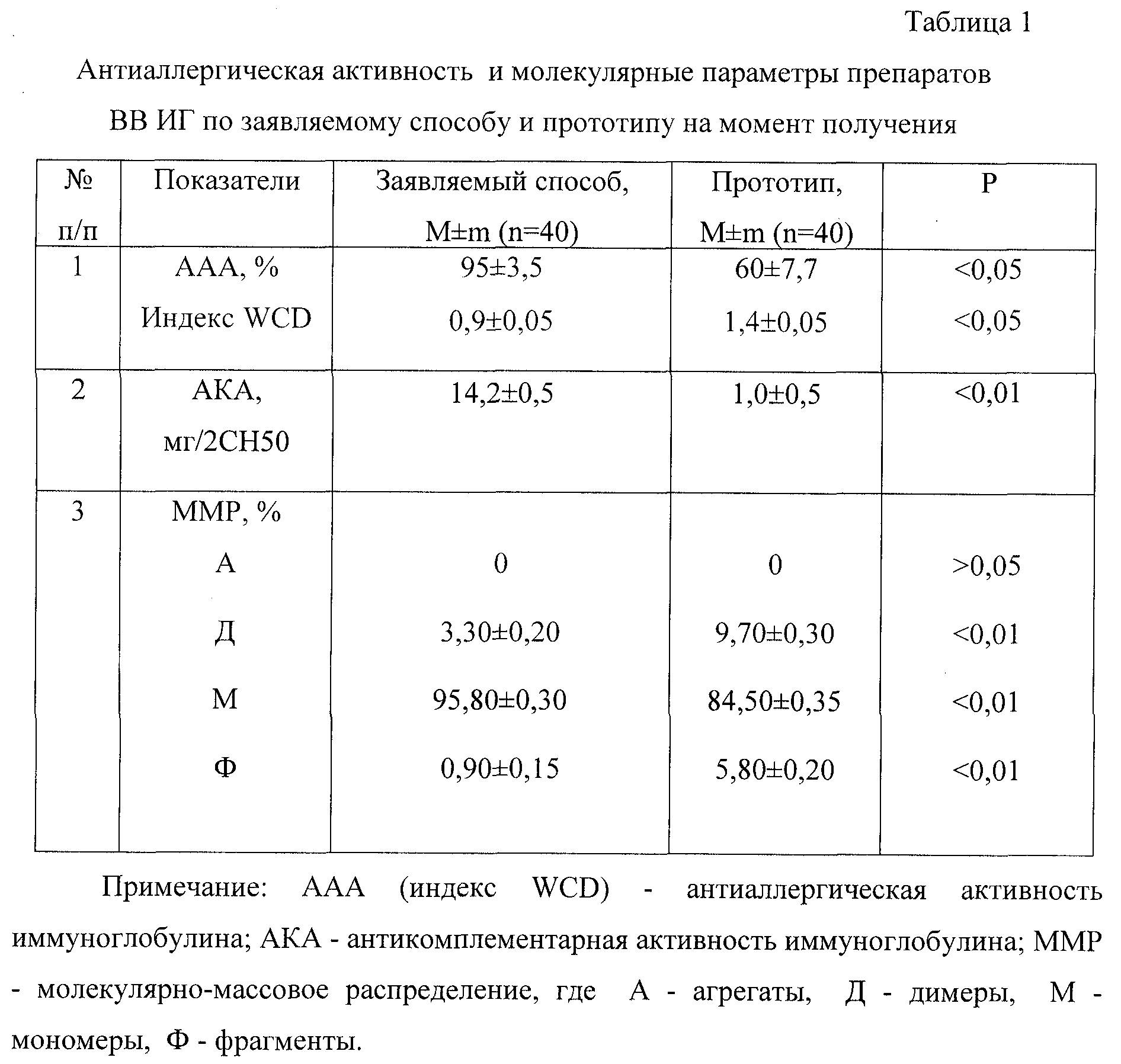
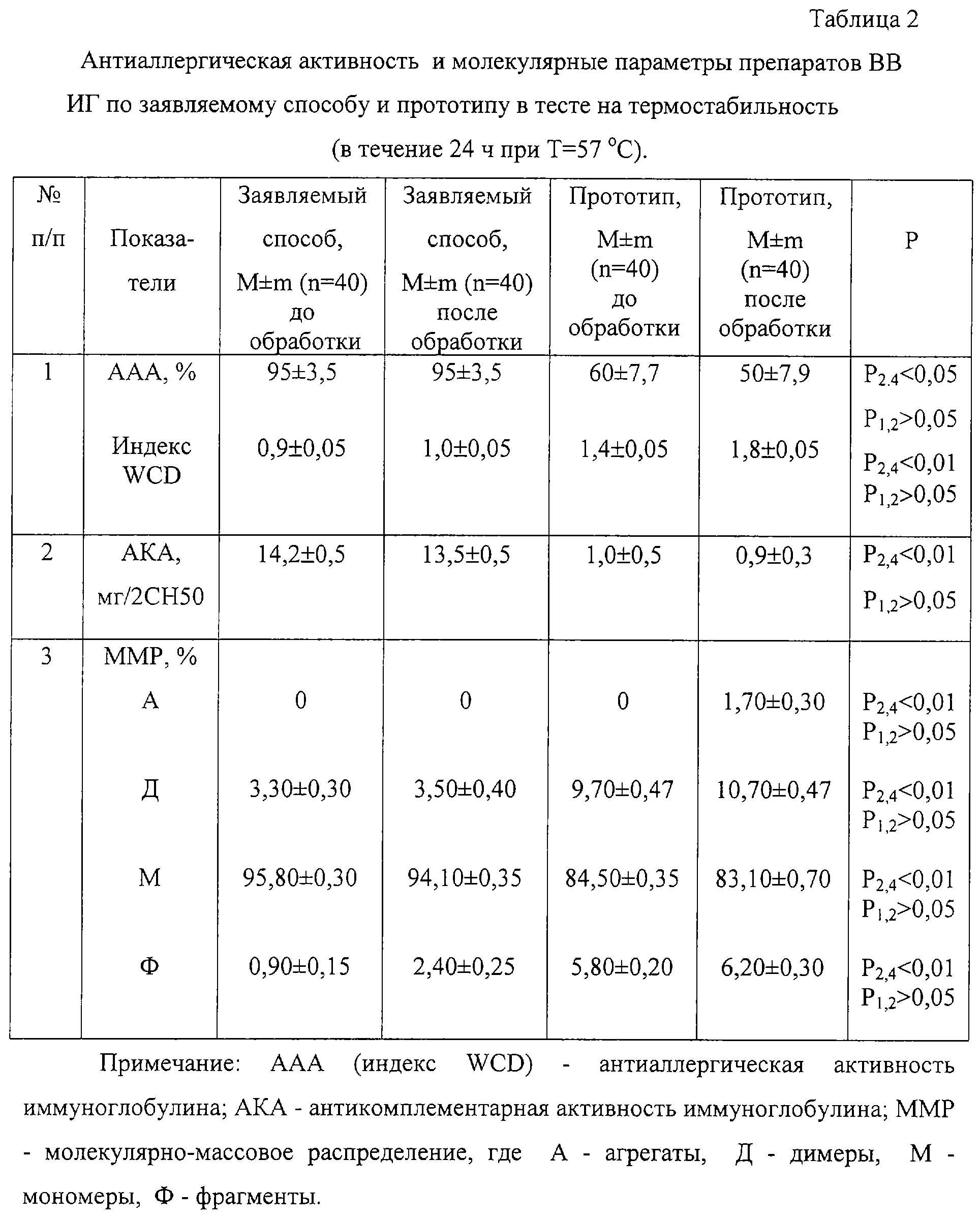
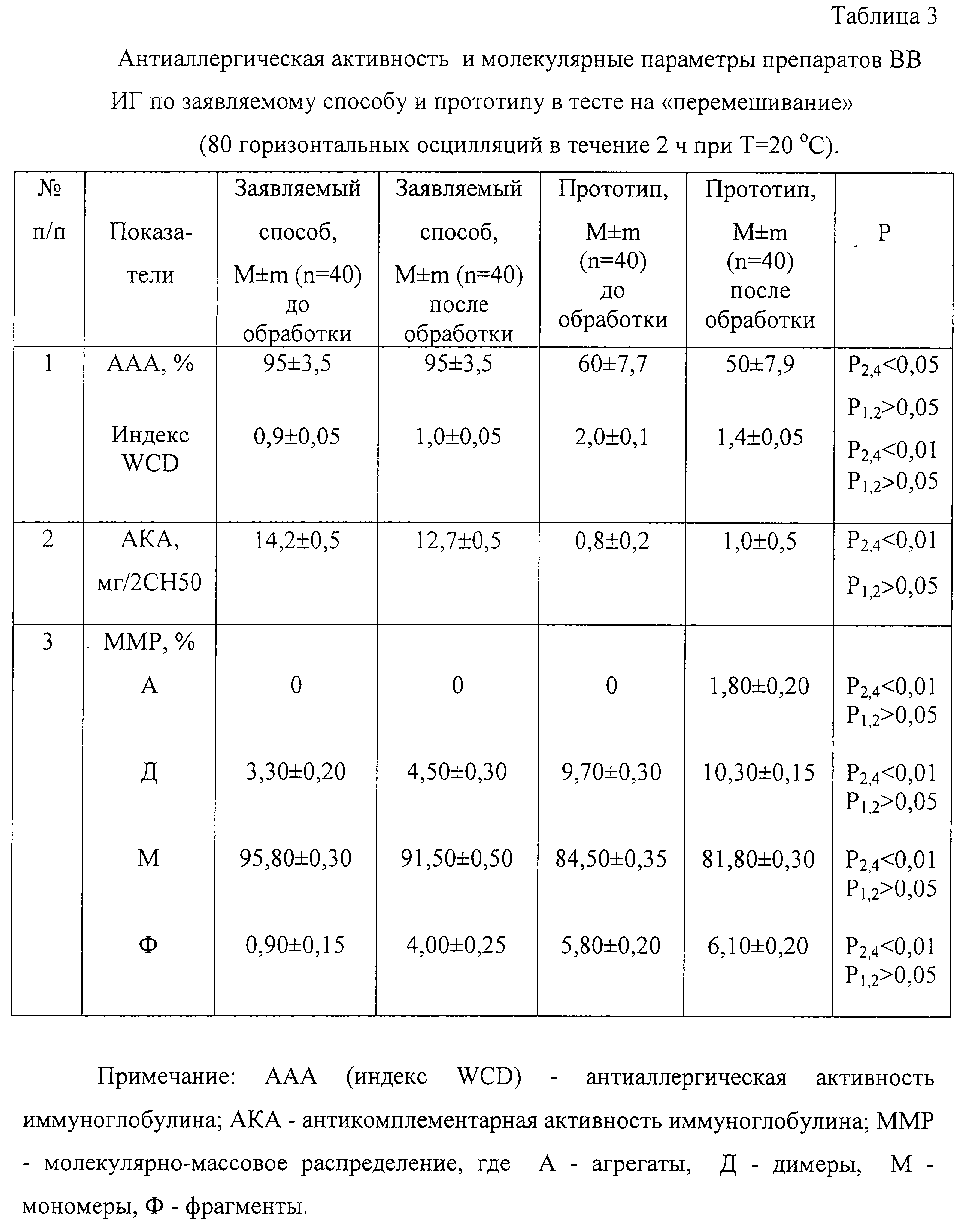
Изобретение относится к биотехнологии, а именно к производству медицинских биологических препаратов, и может быть использовано при получении противоаллергических иммуноглобулинов, предназначенных для внутривенного введения. Сущность изобретения заключается в следующем: получают методом фракционирования по Кону VI фильтрат III, устанавливают рН 4,65-5,35, вводят полиэтиленгликоль с молекулярной массой 4000-6000 Да до концентрации 0,05-0,20% полиэтиленгликоля в растворе центрифугата Б, осуществляют ультрафильтрацию и диафильтрацию на полисульфоновых мембранах с порогом задержания 30-100 кДа при рН 4,65-5,35 и ионной силе не более 0,015 М, в качестве стабилизатора готового препарата применяют мальтозу в концентрации 9-11% и получают препарат мономерного противоаллергического иммуноглобулина для внутривенного введения, представляющий собой иммуноглобулин G с электрофоретической чистотой не менее 99%, концентрацией белка в растворе не менее 2,5%, антикомплементарной активностью более 10 мг/2СН50, имеющий молекулярно-массовое распределение: агрегаты не более 0,5%, мономеры не менее 90%, фрагменты не более 5%, с антиаллергической активностью (ААА) 95±3,5%. Изобретение позволяет получить мономерный противоаллергический иммуноглобулин с низкой антикомплементарной активностью и стабильный при хранении. 2 н.п. ф-лы, 3 табл. Изобретение относится к биотехнологии, а именно к производству медицинских биологических препаратов, и может быть использовано при получении противоаллергических иммуноглобулинов, предназначенных для внутривенного введения. Во всех странах мира отмечается четко выраженная тенденция к стабильному увеличению аллергических заболеваний, что требует продолжения исследований с целью совершенствования существующих и разработки новых средств для лечения этой патологии (1, 2). В связи со значительными трудностями в осуществлении специфической иммунотерапии – применением аллергенов, ее небезопасностью, в аллергологии все чаще применяются неспецифические средства, среди которых весьма перспективны антиаллергические иммуноглобулиновые препараты, поскольку они отличаются гомологичностью, безопасностью, широтой спектра действия независимо от типа аллергена и высокой эффективностью. На протяжении нескольких десятилетий для лечения аллергических заболеваний в нашей стране и за рубежом выпускаются и широко применяются комбинированные антиаллергические иммуноглобулиновые препараты, представляющие собой сочетание иммуноглобулина (ИГ) человека с различными биологически активными веществами. Фирма “Biobasal” (Швейцария) производит два таких препарата – “Histaglobin” и “Histaglobin Triplex”, которые выпускаются в сухом виде и представляют собой комбинацию иммуноглобулина человека и гистамина (3, 4). В России разработаны аналоги данных препаратов, соответственно “Гистаглобулин” и “Тригистаглобулин”. Однако клиническая эффективность комбинированных иммуноглобулиновых антиаллергических препаратов часто ниже желаемой, что неоднократно отмечалось в отечественной и зарубежной научной литературе (1, 2). Наиболее известными в мире являются зарубежные внутримышечные препараты противоаллергического иммуноглобулина – “Allerglobulin” фирмы “Merieux MSD” и “Allergam” фирмы “Ass. Nat. Pour la Distrib. des Fractions Plasmatiques HU”, которые выпускаются во Франции (2). Препарат “Allerglobulin” изготовляется из плацентарного сырья, которое значительно уступает по качеству и безопасности донорскому сырью и часто является причиной нежелательных реакций на введение иммуноглобулинов, поскольку содержит фето-плацентарные антигены, гормоны и токсичный консервант мертиолят. Препарат “Allergam” хотя и производится из донорской плазмы, однако в технологии его получения предусмотрено использование небезопасной каприловой кислоты. Кроме того, вышеуказанные препараты противоаллергического иммуноглобулина в нашей стране являются мало доступными из-за дефицитности и высокой стоимости. Следует отметить, что при лечении аллергических заболеваний наиболее желательным признается внутривенный путь введения препаратов ИГ, что требует применения мономерных препаратов высокой степени очистки. В связи с этим в настоящее время при терапии некоторых аллергических заболеваний используют препараты внутривенного иммуноглобулина (ВВИГ) – препараты нормального полиспецифического иммуноглобулина G (IgG), полученные по различным технологиям (5), такие как “Gammonativ” (фирма “Kabi”, Швеция) и “Sandoglobulin” (фирма “Sandoz”, Швейцария). Однако данные препараты по своему назначению не являются специальными противоаллергическими лечебными средствами и характеризуются невысокой антиаллергической активностью. В этом плане несомненный интерес представляет разработка технологии получения иммуноглобулина с целью создания высокоэффективного препарата противоаллергического ВВИГ, который соответствует всем требованиям, предъявляемым к препаратам ВВИГ, и отвечает потребностям практического здравоохранения (1). К основным показателям качества и безопасности применения препаратов ВВИГ относятся низкая антикомплементарная активность (АКА), отсутствие агрегатов, более высокое содержание мономеров, низкое содержание димеров и фрагментов и стабильность указанных свойств во время хранения и транспортировки (6). Таким образом, технология получения противоаллергического ВВИГ должна гарантировать получение мономерного препарата с наиболее выраженной антиаллергической активностью (ААА) и стабильными физико-химическими свойствами. В Уфимском НИИВС им. И.И. Мечникова ГУП “Иммунопрепарат” разработан и выпускается препарат “Иммуноглобулин человека противоаллергический”, предназначенный для внутримышечного введения и характеризующийся высокой ААА, отсутствием токсичного консерванта мертиолята (оказывает на организм человека токсическое и сенсибилизирующее воздействие), извлечением из более качественного (донорского) сырья и меньшей стоимостью (1). Данный препарат является наиболее близким к заявляемому. Метод его получения включает следующие технологические этапы (7, 8): у доноров без предварительной вакцинации берут кровь, выделяют нативную плазму или сыворотку крови, методом фракционирования по Кону VI получают центрифугат Б, который обрабатывают бикарбонатом натрия и центрифугируют; затем полученный раствор ИГ разбавляют в три раза 0,9% раствором хлорида натрия и осуществляют при рН 5,4-5,6 диафильтрацию против 0,9% раствора хлорида натрия и ультрафильтрацию до 9,5-10,5% белка с использованием полиамидных мембран на подложке УПМ-100. В полученный раствор ИГ вводят в качестве стабилизатора глицин, устанавливают рН 6,6-7,4 и подвергают стерилизующей фильтрации. В готовом препарате отсутствуют агрегаты, содержание мономеров составляет около 85%, димеров – около 10%, фрагментов – около 5%. Однако получаемый препарат противоаллергического иммуноглобулина предназначен только для внутримышечного введения. Задачей, на решение которой направлено изобретение, является разработка препарата мономерного противоаллергического иммуноглобулина для внутривенного введения. Технический результат заключается в получении препарата мономерного противоаллергического иммуноглобулина для внутривенного введения, обладающего низкой АКА и стабильного при хранении и транспортировке. Сущность изобретения заключается в следующем: получают методом фракционирования по Кону VI центрифугат Б, устанавливают рН 4,65-5,35, вводят полиэтиленгликоль с молекулярной массой 4000-6000 Да (ПЭГ с м. м. 4000-6000 Да) до концентрации 0,05-0,20% ПЭГ в растворе центрифугата Б, осуществляют ультрафильтрацию и диафильтрацию на полисульфоновых мембранах с порогом задержания 30-100 кДа при рН 4,65-5,35 и ионной силе не более 0,015 М, в качестве стабилизатора готового препарата применяют мальтозу в концентрации 9-11% и получают препарат мономерного противоаллергического иммуноглобулина для внутривенного введения, представляющий собой IgG с электрофоретической чистотой не менее 99%, концентрацией белка в растворе не менее 2,5%, АКА более 10 мг/2СН50. В отличие от прототипа в заявляемом способе перед стадией ультрафильтрации проводят обработку центрифугата Б ПЭГ с м. м. 4000-6000 Да до концентрации 0,05-0,20% ПЭГ в растворе при кислом рН 4,65-5,35, ультрафильтрацию и диафильтрацию осуществляют на полисульфоновых мембранах с порогом задержания 30-100 кДа при кислом рН 4,65-5,35 и низкой ионной силе не более 0,015 М, готовый препарат иммуноглобулина стабилизируют мальтозой в концентрации 9-11%, получают препарат противоаллергического иммуноглобулина, представляющий собой IgG с электрофоретической чистотой не менее 99%, концентрацией белка в растворе не менее 2,5%, АКА более 10 мг/2СН50 и имеющий молекулярно-массовое распределение: агрегаты не более 0,5%, мономеры не менее 90%, фрагменты не более 5%. Совокупность отличительных признаков заявляемого способа позволила получить следующие преимущества: предварительная обработка центрифугата Б ПЭГ с м. м. 4000-6000 Да до концентрации 0,05-0,20% ПЭГ в растворе при кислом рН 4,65-5,35, ультрафильтрация и диафильтрация при кислом рН 4,65-5,35 и низкой ионной силе не более 0,015 М позволяет получить мономерный раствор противоаллергического иммуноглобулина для внутривенного введения, содержащий не менее 2,5% белка и обладающий низкой АКА (табл. 1), а применение полисульфоновых мембран с порогом задержания 30-100 кДа и введение в качестве стабилизатора мальтозы в концентрации 9-11% способствует сохранению нативности иммуноглобулина, обеспечивает стабильность качественных свойств (АКА, молекулярные параметры, ААА) препарата и препятствует его агрегации и фрагментации во время хранения и транспортировки (табл.2, 3). Препараты ВВИГ контролировались по следующим методикам. Проявление ААА (в дозе 100 мг белка) воспроизводили в тесте пассивной системной анафилаксии (1, 8) на морских свинках массой 230-270 г, которых иммунизировали, вводя внутривенно по 2 мл испытуемого препарата в смеси с иммунной сывороткой, и спустя 1 сутки разрешали внутривенной инъекцией яичного альбумина (в качестве контроля брали 0,9% раствор NaCl). ААА препаратов оценивали по степени выживаемости животных в течение 2-5 ч после разрешения антигеном и вычисляли индекс WCD (9). Содержание молекулярных параметров определялось методом колоночной гель-хроматографии на сефадексе G-200 (10). Также контролировали содержание и распределение классов и субклассов ИГ методами иммуноэлектрофореза и иммуноферментного анализа и оценивали АКА препаратов пробирочным методом (11). Тест на термостабильность, который является аналогом условий хранения, осуществлялся путем прогрева стерильного раствора иммуноглобулина в течение 24 ч при t=57 Полученные результаты приведены в табл.1-3. Как видно из представленных данных (табл.1), использование предлагаемого способа позволяет получить препарат противоаллергического иммуноглобулина для внутривенного введения, характеризующегося низкой АКА, отсутствием агрегатов, минимальным содержанием димеров и фрагментов и большим содержанием мономеров. Стабильность указанных показателей представлена в тесте на термостабильность (табл.2) и в тесте на “перемешивание” (табл.3), которые являются соответственно аналогами условий хранения и транспортировки. Результаты иммуноэлектрофореза показали, что электрофоретическая чистота препаратов составляла не менее 99%. Содержание и распределение классов и субклассов иммуноглобулинов в препаратах также несколько отличается, но является близким к естественному содержанию и распределению их в нормальной донорской плазме. Способ осуществляется следующим образом. В качестве сырья используется центрифугат Б с электрофоретической чистотой не менее 98% и содержанием белка не менее 0,25-0,35%, полученный методом фракционирования по Кону VI. Центрифугат Б разбавляют дистиллированной водой до содержания белка 0,15-0,20% в растворе ИГ, устанавливают рН 4,65-5,35 и ионную силу не более 0,015 М, добавляют ПЭГ с м.м. 4000-6000 Да до содержания 0,05-0,20% ПЭГ в растворе центрифугата Б. Проводят концентрирование ультрафильтрацией до 2-3% белка и диафильтрацию против 5-8 объемов дистиллированной воды при t=0-4 Примеры конкретного выполнения Пример 1. Сырье – центрифугат Б, полученный по методу Кона VI (содержание белка 0,3%; электрофоретическая чистота не менее 98%). 2 л раствора ИГ. 4 л центрифугата Б донорской загрузки разбавляют дистиллированной водой до 8 л, устанавливают рН 4,8 и ионную силу Пример 2. Сырье – центрифугат Б, полученный по методу Кона VI (содержание белка 0,6%; электрофоретическая чистота не менее 98%). 2 л центрифугата Б донорской загрузки разбавляют дистиллированной водой до 8 л, устанавливают рН 5,3, добавляют 35 мл 30% раствора ПЭГ с м. м. 4000 Да. Проводят концентрирование ультрафильтрацией до 2% белка и диафильтрацию против 8 объемов воды при t=0-4 Источники информации 1. Стригин В.А., Трофимов В.А., Магазов Р.Ш. Антиаллергические иммуноглобулиновые препараты. – Уфа: Гилем, 1997. – 140 с. 4. Патент ЕР 0758656. Активация иммуноглобулина с помощью добавления гистамина. А 61 К 39/395. Опубл. 19.02.1997. 6. Анастасиев В.В. Иммуноглобулин для внутривенного введения. – Н.Новгород, 2000. – 168 с. 7. Регламент производства иммуноглобулина человека нормального донорского ОКП 93 8153 0397 от 17.04.2000. 8. Изменения №3 к Регламенту производства иммуноглобулина человека нормального донорского ОКП 93 8153 0397 для производства иммуноглобулина противоаллергического человека от 17.04.2000. 10. ФС 42-3874-99. Физико-химические, химические, физические и иммунохимические методы контроля медицинских иммунологических препаратов. 12. Патент РФ 2140289. Способ получения внутривенного иммуноглобулина. А 61 К 39/395. Опубл. 27.10.1999. Формула изобретения
1. Препарат противоаллергического внутривенного иммуноглобулина, представляющий собой иммуноглобулин G с электрофоретической чистотой не менее 99%, концентрацией белка в растворе не менее 2,5%, антиаллергической активностью (95,0±3,5)%, антикомплементарной активностью более 10 мг/2СН50, имеющий молекулярно-массовое распределение: агрегаты не более 0,5%, мономеры не менее 90%, фрагменты не более 5% и рН 6,5-7,5. 2. Способ получения противоаллергического иммуноглобулина для внутривенного введения, включающий ультрафильтрацию и диафильтрацию полученного по методу Кона 6 фильтрата III, введение стабилизатора и заключительную стерилизацию, отличающийся тем, что полученный по методу Кона 6 фильтрат III при рН 4,65-5,35 обрабатывают полиэтиленгликолем с молекулярной массой 4000-6000 Да до содержания 0,05-0,20% полиэтиленгликоля в растворе фильтрата III, осуществляют ультрафильтрацию и диафильтрацию на полисульфоновых мембранах с порогом задержания 30-100 кДа при рН 4,65-5,35 и ионной силе не более 0,015 М, стабилизируют готовый препарат мальтозой в концентрации 9-11%. |
||||||||||||||||||||||||||

 C (12). Тест на “перемешивание”, который является аналогом условий транспортировки готового препарата до потребителя, осуществлялся путем перемешивания флакона с 20 мл стерильного раствора иммуноглобулина в течение 2 ч при t=20
C (12). Тест на “перемешивание”, который является аналогом условий транспортировки готового препарата до потребителя, осуществлялся путем перемешивания флакона с 20 мл стерильного раствора иммуноглобулина в течение 2 ч при t=20 =0 М, добавляют 18 мл 50% раствора ПЭГ с м. м. 6000 Да. Проводят концентрирование ультрафильтрацией до 2% белка и диафильтрацию против 5 объемов воды при t=0-4
=0 М, добавляют 18 мл 50% раствора ПЭГ с м. м. 6000 Да. Проводят концентрирование ультрафильтрацией до 2% белка и диафильтрацию против 5 объемов воды при t=0-4