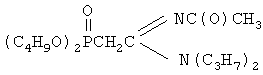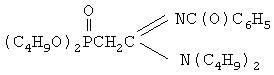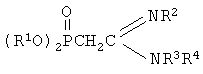Патент на изобретение №2334753
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) С-ФОСФОРИЛИРОВАННЫЕ АЦЕТАМИДИНЫ, СОДЕРЖАЩИЕ РЕАКЦИОННОСПОСОБНУЮ СН-КИСЛОТНУЮ МЕТИЛЕНОВУЮ ГРУППУ, В КАЧЕСТВЕ ИСХОДНЫХ СОЕДИНЕНИЙ ДЛЯ ПОЛУЧЕНИЯ БРОМПРОИЗВОДНЫХ С-ФОСФОРИЛИРОВАННЫХ АЦЕТАМИДИНОВ
(57) Реферат:
Настоящее изобретение относится к С-фосфорилированным ацетамидинам, содержащим реакционноспособную СН-кислотную метиленовую группу, которые могут быть использованы в качестве исходного продукта для получения бромпроизводных С-фосфорилированных ацетамидинов, представляющих интерес в качестве биологически активных веществ для нужд медицины и сельского хозяйства. С-фосфорилированные ацетамидины в настоящем изобретении охарактеризованы общей формулой:
где R1 выбран из групп i-C3H7, i-C4H9, C4H9; R2 выбран из групп C(O)CH3, C(O)C3H7, C(O)C6H5, P(O)(OC4H9-i)2; R3 представляет собой С1-С4-алкил; R4 выбран из группы С1-С4-алкил или фенил, при условии, что R4 представляет собой фенил, если R2 представляет собой группу P(O)(OC4H9-i)2. Техническим результатом является расширение арсенала химических соединений, пригодных для получения биологически активных веществ. 1 табл.
С-фосфорилированные ацетамидины, содержащие реакционноспособную СН-кислотную метиленовую группу в качестве исходного продукта для получения бромпроизводных С-фосфорилированных ацетамидинов. Изобретение относится к химии элементоорганических соединений, а именно к новым С-фосфорилированным ацетамидинам промежуточным соединениям в синтезах широкого спектра веществ, обладающих биологической активностью для нужд медицины и сельского хозяйства, общей формулы
где R1 выбран из групп i-C3H7, i-C4H9, C4H9; R2 выбран из групп С(O)СН3, C(O)C3H7, C(O)C6H5, P(O)(OC4H9-i)2; R3 представляет собой С1-С4-алкил; R4 выбран из группы С1-С4-алкил или фенил при условии, что R4 представляет собой фенил, если R2 представляет собой группу P(O)(OC4H9-i)2. Известен этил(диэтоксифосфорил)ацетат с подвижным атомом водорода в метиленовой группе, способным замещаться на натрий в среде диэтилового эфира. [А.Е.Арбузов. ЖРФХО, 1927,59,239.] Также нитрилы диалкоксифосфорилуксусной кислоты имеют подвижный водородный атом в метиленовой группе, способный к замещению на натрий. [А.Н.Пудовик, Г.Е.Ястребова. Успехи химии, 1970, Т.39, Вып.5, с.1190-1219.] Перечисленные выше СН-кислотные фосфорорганические соединения имеют совершенно иную структуру, чем предлагаемые в изобретении фосфорилированные ацетамидины. Задача заключается в синтезе новых фосфорилированных СН-кислотных соединений, являющихся исходными для получения новых бромпроизводных С-фосфорилированных ацетамидинов. Техническим результатом является расширение арсенала химических соединений, обладающих биологической активностью. Поставленный технический результат достигается тем, что предлагаются С-фосфорилированные ацетамидины, содержащие реакционноспособную СН-кислотную метиленовую группу, общей формулы
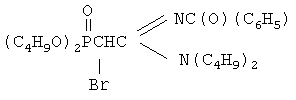
где R1 выбран из групп i-C3H7, i-C4H9, C4H9; R2 выбран из групп С(O)СН3, C(O)C3H7, C(O)C6H5, P(O)(OC4H9-i)2; R3 представляет собой С1-С4-алкил; R4 выбран из группы С1-С4-алкил или фенил при условии, что R4 представляет собой фенил, если R представляет собой группу P(O)(OC4H9-i)2; в качестве исходных соединений для получения бромпроизводных С-фосфорилированных ацетамидинов. Для получения С-фосфорилированных ацетамидинов осуществляют химическое взаимодействие N-замещенных С-фосфорилированных имидатов с диалкиламинами по схеме 1. Реакция протекает без участия растворителей при температуре 50-60°С в течение 1,5-2 часов. Выход амидинов до 96%. Идентификация синтезированных соединений проводилась по данным элементного анализа, ИК- и ЯМР 1Н-спектроскопии. Синтезированные ацетамидины проявляют СН-кислотные свойства вследствие подвижности водородных атомов метиленовой группы, активированной электроноакцепторной фосфонатной и амидиновой группами. Подвижность водородных атомов в метиленовой группе С-фосфорилированных ацетамидинов столь высока, что позволяет действием металлического натрия на них получать соответствующие натриевые производные с последующим замещением натрия на различные функциональные группы и атомы галогенов. Возможность использования С-фосфорилированных ацетамидинов в качестве исходных реагентов в синтезах новых соединений показана на примере взаимодействие N-замещенных С-фосфорилированных ацетамидинов с натрием с последующим бромированием по схеме: Бромирование С-фосфорилированных ацетамидинов проходит гладко и с высокими выходами бромпроизводных. Ацетамидин под действием металлического натрия образует металлоорганическое соединение, в котором связь металл-углерод имеет ионную природу, как и во всех соединениях, которые образуют карбанионы с очень электроположительными щелочными металлами. Образовавшийся карбанион ацетамидина обладает высокой реакционной способностью и быстро реагирует с молекулой брома. В реакцию с бромом вступают натриевые производные всех представленных в изобретении С-фосфорилированных ацетамидинов. Общая методика бромирования К диоксановому раствору С-фосфорилированного ацетамидина при перемешивании и температуре 20÷30°С прибавляли эквимольное количество мелкодиспергированного натрия. Процесс проводили до полного превращения натрия, для ускорения завершения процесса проводили нагревание реакционной смеси до температуры 50÷60°С. Так как выход натриевого производного является количественным, то дальнейшие превращения проводили без выделения последнего. Для этого в полученную реакционную массу при перемешивании и температуре 20-30°С добавляли по каплям эквимольное количество брома. Соль бромида натрия отделяли фильтрацией, растворитель удаляли отгонкой в вакууме (при 15-30 гПа), остаток вакуумировали в течение 1 часа при 50-60°С и 2-4 гПа. Выход С-фосфорилированных бромацетамидинов составил 88%. Изобретение иллюстрируется примерами получения исходных С-фосфорилированных ацетамидинов. Константы и выходы полученных соединений приведены в таблице. Пример 1. Получение N,N-диэтил-N’-ацетил-(дибутоксифосфорил)ацетамидина.
В колбе, снабженной обратным холодильником и термометром, нагревают смесь 7.9 г (0.0239 моль) этил-N-ацетил-(дибутоксифосфорил)ацетимидата с 1.74 г (0.0239 моль) диэтиламина в течение 1.5 часов при температуре 50-60°С. Полноту протекания реакции контролируют методом ТСХ (элюент хлороформ:гексан:изопропиловый спирт 2:2:1 об. Rf 0.68). После чего отгоняют образовавшийся спирт. Получают 7.9 г N,N-диэтил-N’-ацетил-(дибутоксифосфорил)ацетамидина. Выход 96%. По nD 20 1.4546 d4 20 1.0063. MRD 93.80, выч. 93.45. Найдено, %: N 7.91, Р 11.16. C16Н33O4PN2. Вычислено, %: N 8.08, Р 11.44. Спектр ЯМР 1Н (CCl4), м.д.: 0.95 т (12Н, СН3); 1.32 м (8Н СН2); 1.96 с (3Н, СН3С(О)), 2.77 д (2Н, СН2Р); 3.44 к (4Н, NCH2); 3.94 м (4Н, СН2ОР). ИК-спектр, Пример 2. Получение N,N-дипропил-N’-ацетил-(дибутоксифосфорил)ацетамидина
В колбе, снабженной обратным холодильником и термометром, нагревают смесь 6.3 г (0.0177 моль) этил-N-ацетил-(дибутоксифосфорил)ацетимидата с 1.8 г (0.0177 моль) дипропиламина в течение 2 часов при температуре 50-60°С. Полноту протекания реакции контролируют методом ТСХ (элюент хлороформ:диэтиловый эфир:ацетон 1:2:1 об. Rf 0.60). После чего отгоняют образовавшийся спирт. Получают 6.3 г N,N-дипропил-N’-ацетил-(дибутоксифосфорил)ацетамидина. Выход 95%. nD 20 1.4678 d4 20 1.0146. MRD 102.97, выч. 102.75. Найдено, %: N 7.70, Р 10.82. C18H37O4PN2. Вычислено, %: N 7.48, Р 10.59. Спектр ЯМР 1Н (CCl4), м.д.: 0.89 т (12Н, СН3); 1.32 м (12Н, CH2); 1.95 с (3Н, СН3С(О)), 2.76 д (2Н, СН2Р); 3.31 т (4Н, NCH2); 3.92 м (4Н, СН2ОР). ИК-спектр, Пример 3. Получение N,N-дибутил-N’-бензоил-(дибутоксифосфорил)ацетамидина
В колбе, снабженной обратным холодильником и термометром, нагревают смесь 5 г (0.0131 моль) этил-N-бензоил-(дибутоксифосфорил)ацетимидата с 1.68 г (0.0131 моль) дибутиламина в течение 2 часов при температуре 50-60°С. Полноту протекания реакции контролируют методом ТСХ (элюент хлороформ:диэтиловый эфир:ацетон 1:2:1 об. Rf 0.75). После чего отгоняют образовавшийся спирт. Получают 5.7 г N,N-дибутил-N’-бензоил-(дибутоксифосфорил)ацетамидина. Выход 93%. nD 20 1.4980 d4 20 1.0445. MRD 130.85, выч. 131.53. Найдено, %: N 5.82, Р 5.96. С25Н43O4PN2. Вычислено, %: N 6.03, Р 6.23. Спектр ЯМР 1Н (CCl4), м.д.: 0.75 т (12Н, СН3); 1.34 м (16Н, СН2); 2.75 д (2Н, СН2Р); 3.45 к (4Н, NCH2); 3.75 м (4Н, СН2ОР); 7.30 м (5Н, С6Н5). ИК-спектр, По аналогичной методике получают остальные С-фосфорилированные ацетамидины. Пример 4. Получение N,N-диэтил-N’-диизобутоксифосфорил-(дибутоксифосфорил)ацетамидина
В четырехгорлый реактор, снабженный мешалкой, термометром, обратным холодильником и капельной воронкой, к раствору 1.6 г (0.0034 моль) N,N-дибутил-N’-бензоил-(дибутоксифосфорил)ацетамидина в 3 мл диоксана при перемешивании и температуре 20÷30°С прибавляют небольшими порциями 0.078 г (0.0034 моль) натрия. К раствору полученного натриевого производного ацетамидина при перемешивании и температуре 20-30°С добавляют по каплям 0.54 г (0.0034 моль) брома. Соль бромида натрия отделяют фильтрацией, растворитель удаляют отгонкой в вакууме (при 15-30 гПа), остаток вакуумируют в течение 1 часа при 50-60°С и 2-4 гПа. Получают 1.58 г N,N-дибутил-К’-бензоил-(дибутоксифосфорил)бром-ацетамидина. Выход 88%. nD 20 1.5192 d4 20 1.1924. MRD 138.90, выч. 139.24. Спектр ЯМР 1Н (CCl4), м.д.: 0.75 т (12Н, СН3); 1.34 м (16Н, СН2); 2.74 д (1Н, СНР); 3.45 к (4Н, NCH2); 3.74 м (4Н, СН2ОР); 7.30 м (5Н, С6Н5). ИК-спектр,
Предложенные С-фосфорилированные ацетамидины являются исходными соединениями в синтезах С-фосфорилированных бром-ацетамидинов вследствие высоких СН-кислотных свойств активированной метиленовой группы.
Формула изобретения
С-фосфорилированные ацетамидины, содержащие реакционноспособную СН-кислотную метиленовую группу, общей формулы
где R1 выбран из групп i-С3Н7, i-C4H9, C4H9; R2 выбран из групп C(O)CH3, C(O)C3H7, C(O)C6H5, P(O)(OC4H9-i)2; R3 представляет собой С1-С4-алкил; R4 выбран из группы С1-С4-алкил или фенил при условии, что R4 представляет собой фенил, если R2 представляет собой группу P(O)(OC4H9-i)2; в качестве исходных соединений для получения бромпроизводных С-фосфорилированных ацетамидинов.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

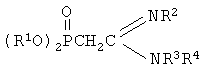
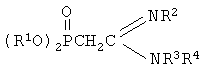

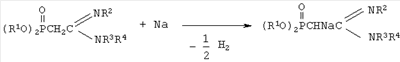
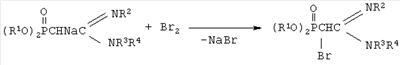
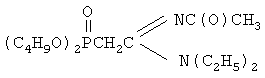
 , см-1: 928-1030 (РОС); 1270 (Р=O); 1660 (C=N); 1680 (С=O).
, см-1: 928-1030 (РОС); 1270 (Р=O); 1660 (C=N); 1680 (С=O).