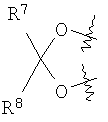Патент на изобретение №2333216
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ТОПИРАМАТА-АНТИКОНВУЛЬСАНТОВ
(57) Реферат:
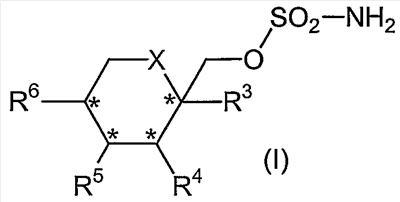
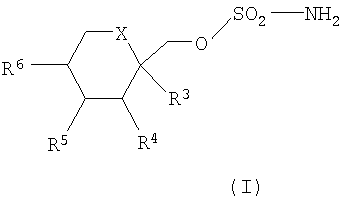
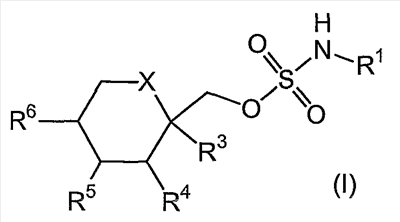
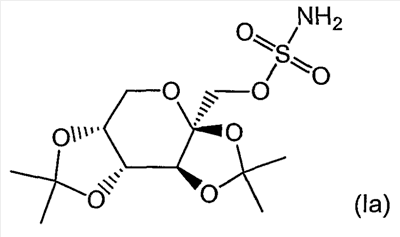
Настоящее изобретение относится к одностадийному способу получения производных сульфамата фруктопиранозы общей формулы (I)
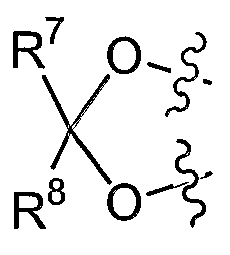
где Х выбирается из СН2 или О; R3, R4, R5 и R6, каждый независимо, выбирается из водорода или низшего алкила, и когда Х представляет собой СН2, R5 и R6 могут представлять собой алкеновые группы, соединенные с образованием бензольного кольца, и когда Х представляет собой О, R3 и R4 и/или R5 и R6 вместе могут представлять собой метилендиоксигруппу формулы
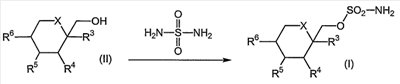
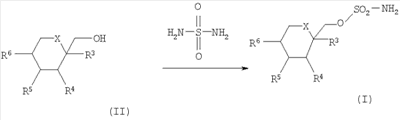
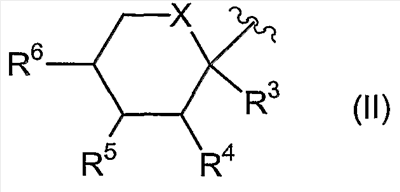
где R7 и R8 являются одинаковыми или различными и представляют собой водород, низший алкил, или представляют собой алкил и соединяются вместе с образованием циклопентильного или циклогексильного кольца; включающий взаимодействие соединения формулы (II) с сульфурилдиамидом при повышенной температуре, в присутствии от 0 до примерно 10% воды, с получением соответствующего соединения формулы (I), и способу получения соединения формулы (1а). 2 н. и 27 з.п. ф-лы, 10 табл.
Область техники, к которой относится изобретение Настоящее изобретение относится к одностадийному способу получения соединений формулы (I) где X, R1, R3, R4, R5 и R6 являются такими, как определено далее. Соединения формулы (I) являются пригодными для лечения эпилепсии. Предшествующий уровень техники Соединения формулы (I) где R1 выбирается из группы, состоящей из водорода и C1-4алкила, и где X, R3, R4, R5 и R6 являются такими, как определено далее, представляют собой известные соединения, которые, как обнаружено, демонстрируют противосудорожную активность и по этой причине являются пригодными для лечения таких состояний, как эпилепсия. Эти соединения описываются в патенте США №4582916 и патенте США №4513006, которые также раскрывают способы получения указанных соединений и которые включаются сюда посредством ссылок. Один из способов, описанных в указанных выше патентах, представляет собой способ получения соединений формулы (I), включающий взаимодействие спирта формулы RCH2OH с хлорсульфаматом формулы ClSO2NH2 или ClSO2NHR1 в присутствии основания, такого как трет-бутоксид калия или гидрид натрия, при температуре примерно от -20°C до 25°C и в растворителе, таком как толуол, тетрагидрофуран или диметилформамид, где R представляет собой остаток формулы (II) Этот способ имеет два основных недостатка. Одним недостатком является то, что способ требует сочетания NaH и ДМФ, которое имеет неконтролируемое выделение тепла и по этой причине является потенциально взрывоопасным. Смотри J. Buckley et al., Chemical & Engineering News, July 12, 1982, page 5; и G. DeWail, Chemical & Engineering News, Sept. 13, 1982. Другим недостатком является то, что способ также использует очень токсичный и коррозионно-активный хлорсульфонилизоцианат (CSI) для получения коммерчески недоступного сульфамилхлорида (ClSO2NH2). С CSI не только сложно работать из-за его токсичности и коррозионной активности, но он также является малодоступным в связи с ограниченным числом поставщиков. Другой способ получения соединения формулы (I), описываемый в указанном выше патенте США № 4513006, включает взаимодействие спирта формулы RCH2OH с сульфурилхлоридом формулы SO2Cl2 в присутствии основания, такого как триэтиламин или пиридин, при температуре примерно от -40°C до 25°C, в простом диэтиловом эфире или метиленхлориде, с получением хлорсульфата формулы RCH2OSO2Cl2. Затем хлорсульфат формулы RCH2OSO2Cl2 может взаимодействовать с амином формулы R1NH2 при температуре примерно от -40°C до 25°C, в метиленхлориде или ацетонитриле с получением соединения формулы (I). Этот способ, использующий растворители: простой диэтиловый эфир, метиленхлорид и ацетонитрил, дает относительно низкие выходы желаемого конечного продукта формулы (I). Третий способ, описываемый в двух патентах, рассмотренных выше, включает взаимодействие хлорсульфата формулы RCH2OSO2Cl2, полученного, как описано ранее, с азидом металла, таким как азид натрия, в растворителе, таком как метиленхлорид или ацетонитрил, с получением азидосульфата формулы RCH2OSO3N3. Затем азидосульфат восстанавливается до соединения формулы I, где R1 представляет собой водород, путем каталитического гидрирования. Недостатком этого способа является то, что при манипуляциях с азидными соединениями может произойти взрыв. Также способ включает дополнительное химическое преобразование, включающее восстановление азида до остатка NH2. Maryanoff et al., в патенте США № 5387700, описывает способ получения соединений формулы (I), который включает взаимодействие спирта формулы RCH2OH с сульфурилхлоридом в присутствии основания, в растворителе, выбранном из группы, состоящей из толуола, простого трет-бутилметилового эфира и тетрагидрофурана, с получением хлорсульфатного промежуточного соединения формулы RCH2OSO2Cl2. Хлорсульфат формулы RCH2OSO2Cl2 взаимодействует с амином формулы R1NH2 в растворителе, выбранном из группы, состоящей из тетрагидрофурана, простого трет-бутилметилового эфира и низшего алканола (например, метанола или этанола), с получением соединения формулы (I). Одним из недостатков этого способа является то, что соединение формулы (I) получают в периодическом процессе, где осуществляется первая реакция, растворитель удаляется, продукт выделяется, выделенный продукт повторно растворяется во втором растворителе, а затем взаимодействует с получением конечного продукта. Это приводит к способу, который требует выделения полустабильного, термически лабильного промежуточного соединения ROSO2Cl. В дополнение к этому этот способ требует манипуляций с множеством растворителей и множества процессов извлечения растворителей для рециркуляции или сброса, что приводит к способу, который требует как больших средств, так и большого объема работы. Целью настоящего изобретения является создание одностадийного способа получения соединений формулы (I), способа, который использует легкодоступные материалы, может осуществляться без выделения промежуточных соединений и/или дает относительно высокие выходы, тем самым делая возможным промышленное производство соединений формулы (I). Сущность изобретения Настоящее изобретение направлено на одностадийный способ получения соединений формулы (I) где X выбирается из CH2 или O; R1 выбирается из группы, состоящей из водорода и C1-4алкила; R3, R4, R5 и R6, каждый независимо, выбирается из водорода или низшего алкила, и когда X представляет собой CH2, R5 и R6 могут представлять собой алкеновые группы, соединенные с образованием бензольного кольца, и когда X представляет собой O, R3 и R4 и/или R5 и R6 вместе могут представлять собой метилендиоксигруппу формулы
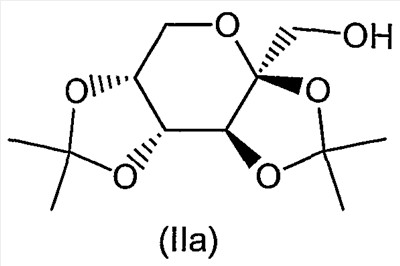
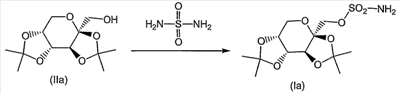
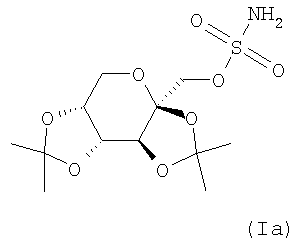
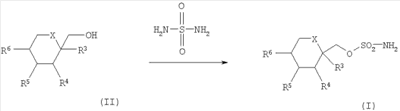
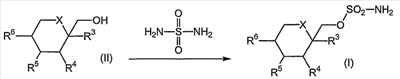
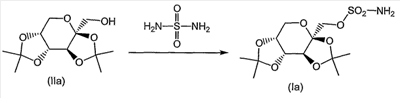
где R7 и R8 являются одинаковыми или различными и представляют собой водород, низший алкил, или представляют собой алкил и соединяются вместе с образованием циклопентильного или циклогексильного кольца; включающий взаимодействие соединения формулы (II) с сульфурилдиамидом (также известен как сульфамид), при повышенной температуре, в присутствии от 0 до примерно 10% воды, с получением соответствующего соединения формулы (I). Настоящее изобретение, кроме того, направлено на способ получения соединения формулы (Ia) также известного как топирамат, включающий взаимодействие соединения формулы (IIa) (также известное как диацетонфруктоза или DAF) с сульфурилдиамидом (также известен как сульфамид), при повышенной температуре, в присутствии от 0 до примерно 10% воды, с получением соответствующего соединения формулы (Ia). Настоящее изобретение, кроме того, направлено на соединение, полученное в соответствии с любым из способов, описанных здесь. Иллюстрацией настоящего изобретения является фармацевтическая композиция, содержащая фармацевтически приемлемый носитель и соединение, полученное в соответствии с любым из способов, описанных выше. Иллюстрацией настоящего изобретения является фармацевтическая композиция, полученная путем смешивания фармацевтически приемлемого носителя и соединения, полученного в соответствии с любым из способов, описанных выше. Иллюстрацией настоящего изобретения является способ получения фармацевтической композиции, включающий смешивание фармацевтически приемлемого носителя и соединения, полученного в соответствии с любым из способов, описанных выше. Другим примером настоящего изобретения является применение соединения, полученного в соответствии с любым из способов, описанных здесь, при получении лекарственного средства для лечения эпилепсии. Подробное описание изобретения В одном из вариантов осуществления настоящего изобретения соединение формулы (I) представляет собой топирамат, соединение формулы (Ia) Как они здесь используются, термины “диацетонфруктоза” и “DAF” должны обозначать диацетон- Как он здесь используется, термин “алкил”, используется ли он отдельно или как часть группы заместителя, должен включать прямые и разветвленные углеродные цепи. Например, алкильные группы включают метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил и тому подобное. Если не отмечается иного, термин “низший”, когда он используется вместе с алкилом, должен обозначать углеродные цепи из одного – четырех атомов углерода. Как оно здесь используется, обозначение “*” должно обозначать присутствие стереогенного центра. Как он здесь используется, термин “повышенная температура” должен обозначать температуру, большую примерно чем 90°C, предпочтительно температуру, превышающую или равную температуре кипения растворителя реакционной смеси, более предпочтительно температуру в пределах от примерно 90°C до примерно 170°C, еще более предпочтительно температуру в пределах от примерно 110°C до примерно 160°C и еще более предпочтительно температуру в пределах от примерно 120°C до примерно 140°C. Как он здесь используется, если не отмечается иного, термин “в присутствии от 0 до примерно 10% воды” должен обозначать, что общее молярное количество воды по отношению к молярному количеству DAF находится в пределах от 0 до примерно 10%. Как он здесь используется, термин “апротонный органический растворитель” должен обозначать любой органический растворитель, который не дает протона при условиях реакции. Соответствующие примеры включают, но не ограничиваются этим, ксилол (например, o-ксилол, п-ксилол, м-ксилол или их смесь), этилбензол, мезитилен, тетрагидронафталин, пиридин, 1-метил-2-пирролидинон, толуол, 4-метил-2-пентанон, бензонитрил, диметилформамид, сульфолан, простой дифениловый эфир и тому подобное. Термин “субъект”, как он здесь используется, относится к животному, предпочтительно млекопитающему, более предпочтительно человеку, который является или являлся объектом лечения, наблюдения или эксперимента. Термин “терапевтически эффективное количество”, как он здесь используется, обозначает то количество активного соединения или фармацевтического агента, которое вызывает биологическую или медицинскую реакцию в системе тканей, животном или человеке, которые изучаются исследователем, ветеринаром, врачом или другим клиницистом, которая включает ослабление симптомов заболевания или расстройства, которое лечится. Как он здесь используется, термин “композиция” предназначается для охвата продукта, содержащего указанные ингредиенты в указанных количествах, а также любой продукт, который возникает, прямо или косвенно, от объединения указанных ингредиентов в указанных количествах. Специалист в данной области заметит, что соединения формулы (I) имеют несколько стереогенных центров, как отмечено ниже звездочками: Специалист в данной области, кроме того, заметит, что способы по настоящему изобретению могут использоваться для получения рацемических смесей соединения формулы (I) или любого из стереоизомеров соединения формулы (I) посредством выбора и замены соответствующих рацемических смесей или стереоизомеров реагентов. Настоящее изобретение направлено на одностадийный способ получения соединения формулы (I), как показано на схеме 1: Схема 1 Соответственно, соответствующим образом замещенное соединение формулы (II), известное соединение или соединение, полученное посредством известных способов, взаимодействует с сульфурилдиамидом (также известным как сульфамид), где сульфурилдиамид предпочтительно присутствует в количестве, большем или равном примерно 0,9 эквивалента; более предпочтительно в количестве, находящемся в пределах от примерно 1,5 до примерно 3 эквивалентов; еще более предпочтительно в количестве, примерно равном 2 эквивалентам; предпочтительно, в присутствии неводного органического основания, такого как органический третичный амин, такой как пиридин, 4-пиколин, изохинолин, диметилбутиламин, 4-диметиламинопиридин, 4-трет-бутилпиридин, имидазол, трибутиламин, диметилбензиламин, и тому подобное; или неводного неорганического основания, такого как K2CO3, KHCO3, Na2CO3, NaHCO3, и тому подобное; более предпочтительно в присутствии неводного органического третичного амина; еще более предпочтительно в присутствии пиридина; где неводное органическое или неорганическое основание предпочтительно присутствует в количестве, большем примерно чем 1 эквивалент; более предпочтительно в количестве, находящемся в пределах от примерно 3 до примерно 6 эквивалентов; еще более предпочтительно в количестве, равном примерно 4 эквивалентам; в присутствии от 0% до примерно 10% воды, предпочтительно от 0% до примерно 5% воды, более предпочтительно от 0% до примерно 3% воды; предпочтительно в апротонном органическом растворителе, таком как ксилол (например, o-ксилол, п-ксилол, м-ксилол или их смесь), этилбензол, мезитилен, тетрагидронафталин, пиридин, 1-метил-2-пирролидинон, толуол, 4-метил-2-пентанон, бензонитрил, диметилформамид, сульфолан, простой дифениловый эфир и тому подобное; или в смесях апротонных органических растворителей, таких как простой дифениловый эфир:бифенил, ксилол:толуол, смешанные ксилолы технического качества, и тому подобное; более предпочтительно в o-ксилоле, п-ксилоле, м-ксилоле, их смеси или в смешанных ксилолах технического качества; альтернативно, растворитель может выбираться из неводного органического основания, такого как органический третичный амин, например пиридин, 4-пиколин, изохинолин, диметилбутиламин, 4-диметиламинопиридин, 4-трет-бутилпиридин, имидазол, трибутиламин, диметилбензиламин, и тому подобное; предпочтительно неводного органического третичного амина; более предпочтительно пиридина; альтернативно, еще, когда соединение формулы (II) взаимодействует в присутствии неводного органического основания, неводное органическое основание может действовать как растворитель; при повышенной температуре, предпочтительно при температуре в пределах от примерно 90°C до примерно 170°C; более предпочтительно при температуре в пределах от примерно 110°C до примерно 160°C; еще более предпочтительно при температуре в пределах от примерно 120°C до примерно 140°C; с получением соответствующего соединения формулы (I). Предпочтительно соединение формулы (II) взаимодействует с сульфурилдиамидом в соответствии со способом, приведенным выше на схеме 1, в отсутствие какого-либо иного спирта (то есть спирта, иного, чем соединение формулы (II). Соединение формулы (Ia) может быть получено в соответствии со способом, приведенным на схеме 2 Схема 2 Соответственно, соединение формулы (IIa), известное соединение, также известное как диацетонфруктоза (DAF), взаимодействует с сульфурилдиамидом (также известен как сульфамид), где сульфурилдиамид предпочтительно присутствует в количестве, равном или большем примерно чем 0,9 эквивалента; более предпочтительно в количестве, находящемся в пределах от примерно 1,5 до примерно 3 эквивалентов; еще более предпочтительно в количестве, равном примерно 2 эквивалентам; предпочтительно в присутствии неводного органического основания, такого как органический третичный амин, такой как пиридин, 4-пиколин, изохинолин, диметилбутиламин, 4-диметиламинопиридин, 4-трет-бутилпиридин, имидазол, трибутиламин, диметилбензиламин, и тому подобное; или неводного неорганического основания, такого как K2CO3, KHCO3, Na2CO3, NaHCO3, и тому подобное; более предпочтительно в присутствии неводного органического третичного амина; еще более предпочтительно в присутствии пиридина; где неводное органическое или неорганическое основание предпочтительно присутствует в количестве, большем примерно чем 1 эквивалент; более предпочтительно в количестве, находящемся в пределах от примерно 3 до примерно 6 эквивалентов; еще более предпочтительно в количестве, равном примерно 4 эквивалентам; в присутствии от 0% до примерно 10% воды, предпочтительно от 0% до примерно 5% воды, более предпочтительно от 0% до примерно 3% воды; предпочтительно в апротонном органическом растворителе, таком как ксилол (например, o-ксилол, п-ксилол, м-ксилол или их смесь), этилбензол, мезитилен, тетрагидронафталин, пиридин, 1-метил-2-пирролидинон, толуол, 4-метил-2-пентанон, бензонитрил, диметилформамид, сульфолан, простой дифениловый эфир, и тому подобное; или в смесях апротонных органических растворителей, таких как простой дифениловый эфир:бифенил, ксилол:толуол, смешанные ксилолы технического качества, и тому подобное; более предпочтительно в o-ксилоле, п-ксилоле, м-ксилоле, их смеси или смешанных ксилолах технического качества; альтернативно, растворитель может выбираться из неводного органического основания, такого как органический третичный амин, например из пиридина, 4-пиколина, изохинолина, диметилбутиламина, 4-диметиламинопиридина, 4-трет-бутилпиридина, имидазола, трибутиламина, диметилбензиламина, и тому подобное; предпочтительно неводного органического третичного амина; более предпочтительно пиридина; альтернативно, еще, когда соединение формулы (II) взаимодействует в присутствии неводного органического основания, неводное органическое основание может действовать как растворитель; при повышенной температуре, предпочтительно при температуре в пределах от примерно 90°C до примерно 170°C; более предпочтительно при температуре в пределах от примерно 110°C до примерно 160°C; еще более предпочтительно при температуре в пределах от примерно 120°C до примерно 140°C; с получением соответствующего соединения формулы (Ia). Предпочтительно соединение формулы (IIa) взаимодействует с сульфурилдиамидом в соответствии со способом, приведенным выше на схеме 2, в отсутствие любого другого спирта (то есть спирта иного, чем соединение формулы (IIa)). Когда соединения по настоящему изобретению имеет, по меньшей мере, один хиральный (или стереогенный) центр, они могут, соответственно, существовать в виде энантиомеров. Когда соединения имеют два или более хиральных (или стереогенных) центра, они могут, в дополнение к этому, существовать в виде диастереомеров. Необходимо понять, что все такие изомеры и их смеси входят в объем настоящего изобретения. Кроме того, некоторые кристаллические формы соединения могут существовать в виде полиморфов, и, как таковые, как имеется в виду, включаются в настоящее изобретение. В дополнение к этому, некоторые соединения могут образовывать сольваты с водой (то есть гидраты) или с обычными органическими растворителями, и такие сольваты также, как имеется в виду, должны включаться в объем настоящего изобретения. Когда способы получения соединений в соответствии с настоящим изобретением дают смеси стереоизомеров, эти изомеры могут разделяться посредством обычных методик, таких как препаративная хроматография. Соединения могут быть получены в рацемической форме, или же индивидуальные энантиомеры могут быть получены посредством либо энантиоселективного синтеза, либо посредством разделения. Соединения могут, например, разделяться на составляющие их энантиомеры с помощью стандартных методик, таких как образование диастереомерных пар посредством образования соли с оптически активной кислотой, такой как (-)-ди-п-толуоил-D-винная кислота и/или (+)-ди-п-толуоил-L-винная кислота, с последующей фракционированной кристаллизацией и регенерацией свободного основания. Соединения могут также разделяться путем образования сложных диастереомерных эфиров или амидов с последующим хроматографическим разделением и удалением хирального вспомогательного вещества. Альтернативно, соединения могут разделяться с использованием хиральной колонки для ВЭЖХ. В ходе протекания любого из способов получения соединений по настоящему изобретению может быть необходимой и/или желательной защита чувствительных или реакционно-способных групп на любой из рассматриваемых молекул. Это может достигаться посредством обычных защитных групп, таких как те, которые описываются в Protective Groups in Organic Chemistry, ed. J.F.W. McOmie, Plenum Press, 1973; и T.W. Greene & P.G.M. Wuts, Protective Groups in Organic Synthesis, John Wiley & Sons, 1991. Защитные группы могут удаляться на удобной следующей далее стадии с использованием способов, известных в данной области. Следующие далее примеры описывают настоящее изобретение более подробно и предназначены для иллюстрации настоящего изобретения, но не для его ограничения. Пример A1 Экспериментальные испытания #101-116: Реактор загружают DAF, сульфамидом, основанием и растворителем, как описано в табл. 1. При перемешивании реакционную смесь нагревают и поддерживают при желаемой температуре и в течение выбранного периода времени (как указано в табл. 2). Для экспериментальных испытаний 101, 102, 103 смесь дистиллируют при 41°C в вакууме в течение 30, 35 и 20 минут соответственно. Реакционную смесь охлаждают до комнатной температуры, затем экстрагируют дважды примерно 50 мл 1M водного раствора NaOH (0,3M водный раствор NaOH используют для экспериментальных испытаний #101-108). Полученный щелочной раствор продукта нейтрализуют с использованием 6M водного раствора HCl. После кристаллизации раствор продукта фильтруют и влажную лепешку сушат в течение 16-20 час (примерно 22 час для экспериментальных испытаний #106 и 107) примерно при 50°C в вакууме с получением продукта-топирамат. Сухой продукт анализируют с помощью ВЭЖХ. Экспериментальные испытания # 117-139: Реактор загружают DAF, сульфамидом, основанием и растворителем, как описано в табл. 1. При перемешивании реакционную смесь нагревают и поддерживают в течение периода примерно 60 минут при желаемой температуре (как указано в табл. 2). После охлаждения до комнатной температуры реакционную смесь экстрагируют дважды примерно 75 мл 1M водного раствора NaOH. Полученный щелочной раствор продукта нейтрализуют с использованием 6M водного раствора HCl. После кристаллизации раствор продукта фильтруют и влажную лепешку сушат в течение 16-20 час (24 час для экспериментальных испытаний 129, 134, 137 и 48 час для экспериментальных испытаний #126, 128, 130, 131, 136) примерно при 50°C в вакууме с получением продукта – топирамат. Экспериментальные испытания #123, 125 и 135, как ожидается, должны давать продукт, но были прекращены из-за трудностей во время экстракции или кристаллизации. Сухой продукт анализируют с помощью ВЭЖХ. Указанные выше процедуры завершаются в соответствии с условиями испытаний, как перечислено ниже в табл. 1 и 2. Продукт – топирамат – получают во всех экспериментальных испытаниях, за исключением случаев, отмеченных выше.
Пример A2 Экспериментальные испытания #140-147; пиридиновое основание: Осуществляют восемь экспериментов для оценки объединенного воздействия объема растворителя, времени реакции и температуры реакции на одностадийный синтез топирамата, исходя из диацетонфруктозы (DAF). DAF объединяют с сульфамидом, пиридином и выбранным объемом растворителя на основе o-ксилола (в таких количествах, как перечислено в табл. 3) в 1-литровой круглодонной колбе. Затем загруженную колбу погружают в предварительно нагретую масляную баню при выбранной внешней температуре, реакционную смесь перемешивают и нагревают до выбранной температуры реакции, где она выдерживается в течение выбранного времени, до того как колбу удаляют из масляной бани и охлаждают до комнатной температуры. Затем реакционную смесь дважды экстрагируют 1M NaOH (75 мл порциями). Водные экстракты объединяют и нейтрализуют 6M HCl, чтобы вызвать кристаллизацию продукта. Во всех случаях продукт осаждается в виде масла. Масло перемешивают в течение ночи, чтобы оно стало фильтруемыми кристаллами. Полученные твердые продукты сушат в вакууме в течение 16-18 час при 50°C. Высушенный продукт анализируют с помощью ВЭЖХ. Следуя указанной выше процедуре, осуществляют восемь экспериментов при экспериментальных условиях, как указано ниже в табл. 3 и 4. Все экспериментальные испытания дают продукт – топирамат.
Пример A3 Экспериментальные испытания #148-156: трет-бутилпиридиновое основание: Осуществляют девять экспериментов для оценки объединенного воздействия количества эквивалентов основания, температуры реакции и времени реакции на одностадийный синтез топирамата с использованием 4-трет-бутилпиридина, исходя из диацетонфруктозы (DAF). DAF объединяют с сульфамидом, 4-трет-бутилпиридином (в таких количествах, как перечислено в табл. 4) и 40 мл o-ксилола в 500 мл круглодонной колбе. Реакционную смесь перемешивают и нагревают до выбранной температуры реакции на масляной бане в течение примерно 19-23 мин. Реакционную смесь поддерживают при выбранной температуре реакции в течение выбранного времени, а затем быстро охлаждают до 25°C. Реакционную смесь экстрагируют дважды 1M NaOH (75 мл порциями). Водные экстракты объединяют и нейтрализуют с использованием 6M HCl, чтобы вызвать кристаллизацию продукта. Во всех случаях продукт осаждается в виде масла, которое перемешивают в течение ночи, чтобы оно стало фильтруемыми кристаллами. Кристаллы сушат в вакууме в течение 16-18 час при 50°C. Высушенный продукт анализируют с помощью ВЭЖХ. Следуя указанной выше процедуре, осуществляют девять экспериментов при экспериментальных условиях, как перечислено ниже в табл. 5 и 6. Все экспериментальные испытания дают продукт – топирамат.
Пример A4 Осуществляют ряд экспериментов для оценки воздействия растворителя и основания на одностадийный способ получения топирамата. Экспериментальные условия являются такими, как перечислено в табл. 7 и 8, с экспериментальными процедурами для индивидуальных испытаний, как описано ниже. Испытание #157, 158, 160, 164-166: DAF и сульфамид (в таких количествах, как в табл. 8) переносят в пробирку. Затем добавляют выбранный растворитель и выбранное основание (в таких количествах, как указано в табл. 7) в смесь DAF/сульфамид. Затем реакционную смесь перемешивают и нагревают, при этом реакционную смесь поддерживают при выбранной температуре (смотри табл. 8) в течение выбранного времени (смотри табл. 8), по прохождении этого времени образец верхнего слоя отбирают и анализируют с помощью ВЭЖХ. Испытание #159, 188-198: DAF, сульфамид, o-ксилол и указанное количество выбранного основания (смотри табл. 7 и 8) переносят в 500 мл круглодонную колбу. Затем реакционную смесь перемешивают и нагревают, при этом смесь поддерживают при выбранной температуре в течение выбранного времени (смотри табл. 8), используя масляную баню. Реакционную смесь удаляют из горячего масла, охлаждают до примерно комнатной температуры, а затем экстрагируют дважды 1M NaOH (75 мл порциями). Водные экстракты объединяют и нейтрализуют с использованием 6M HCl, чтобы вызвать кристаллизацию продукта. Полученные твердые продукты сушат в вакууме в течение 16-18 час при 50°C. Высушенный продукт анализируют с помощью ВЭЖХ. Испытание #161-163: DAF, сульфамид, 4-пиколин и выбранный растворитель (в таких количествах, как в табл. 7 и 8) переносят в 250 мл круглодонную колбу. Колбу опускают в нагреваемую масляную баню и смесь перемешивают при выбранной поддерживаемой температуре в течение выбранного времени реакции (смотри табл. 8). Затем реакционную смесь охлаждают до комнатной температуры и дважды экстрагируют 1M NaOH (75 мл порциями). Водные экстракты нейтрализуют 6M HCl, а затем поддерживают при комнатной температуре в течение ночи, чтобы дать возможность для кристаллизации продукта. Полученные кристаллические твердые продукты фильтруют и сушат в течение 16-18 час, в вакуумной печи, при 50°C. Затем продукт анализируют с помощью ВЭЖХ. Примечание: Хотя в испытании #162 ожидалось получение продукта, продукт не кристаллизовался и по этой причине не анализировался; продукт из испытания #163 представляет собой липкий твердый продукт. Испытание #167-172: Выбранный растворитель в выбранном количестве (смотри табл. 7) переносят в 125 мл пробирку вместе с пиридином (в таких количествах, как в табл. 7) и полученный раствор нагревают до выбранной температуры. Затем предварительно взвешенную смесь DAF и сульфамида (в таких количествах, как в табл. 8) добавляют вместе с переносом промывочной жидкости растворителя (примерно 2 мл). Реакционную смесь перемешивают при выбранной температуре в течение выбранного времени (смотри табл. 8), в это время отбирают образец верхнего слоя (некоторые смеси образуют второй небольшой, темный слой) и анализируют с помощью ВЭЖХ. Испытание #173: DAF, сульфамид, пиридин и смешанные ксилолы (в таких количествах, как перечислено в табл. 7 и 8) переносят в 1000 мл круглодонную колбу в предварительно нагретой (140°C) масляной бане. Реакционную смесь перемешивают при выбранной температуре реакции в течение 90 мин. Колбу удаляют из масляной бани, и остаточное тепло используется для дистилляции примерно 22 г жидкости из реакционной смеси. Реакционную смесь экстрагируют тремя порциями (90 мл, 30 мл и 10 мл) 0,35M NaOH. В водные экстракты добавляют 1 н. HCl (50 мл), что приводит к образованию масла. Смесь перемешивают для преобразования масла в фильтруемые кристаллы. Кристаллы собирают путем фильтрования, промывают водой и сушат в вакуумной печи в течение 16 час при 50°C. Затем продукт анализируют с помощью ВЭЖХ. Испытание #174-180: DAF, сульфамид пиридин и выбранный растворитель (в таких количествах, как перечислено в табл. 7 и 8) переносят в 500 мл круглодонную колбу. Затем реакционную смесь перемешивают и нагревают на масляной бане до заданной температуры. Реакционную смесь поддерживают примерно при заданной температуре (указано в табл. 8) в течение выбранного времени (смотри табл. 8), удаляют из горячего масла и охлаждают до примерно комнатной температуры. Затем в реакционную смесь добавляют воду (100 мл) и/или другие растворители (MeOH, 0,5M NaOH или реакционный растворитель), по потребности, с получением гетерогенной смеси, состоящей из двух прозрачных слоев жидкости. Затем оба слоя анализируют с помощью ГХ. Испытание #181-183: DAF, сульфамид, 4-трет-бутилпиридин и выбранный растворитель (в таких количествах, как перечислено в табл. 7 и 8) переносят в 500 мл круглодонную колбу. Затем реакционную смесь помещают на масляную баню и перемешивают, при этом нагревая при выбранной температуре реакции в течение выбранного времени (смотри табл. 8). Затем реакционной смеси дают охладиться до комнатной температуры. Затем реакционную смесь экстрагируют соответствующими растворителями с получением двух прозрачных слоев жидкости (для испытания 181 растворители для экстракции представляют собой воду (125 мл) и смешанные ксилолы (25 мл); для испытания 182 растворители для экстракции представляют собой воду (150 мл) и метанол (25 мл); для испытания 183 растворитель для экстракции представляет собой 0,3M NaOH (100 мл). Осуществляют ГХ анализ образцов жидкости из обоих слоев. Испытание #184: DAF, сульфамид, диметилбутиламин и 1,2,3,4-тетрагидронафталин (в таких количествах, как перечислено в табл. 7 и 8) переносят в 250 мл круглодонную колбу. Колбу помещают на нагреваемую масляную баню (136°C) и смесь перемешивают, при этом, нагревая при выбранной температуре в течение выбранного времени (смотри табл. 8). Реакционную смесь охлаждают до примерно комнатной температуры, а затем экстрагируют дважды 1M NaOH (75 мл порциями). Водные экстракты нейтрализуют с использованием 6M HCl и перемешивают в течение 2 час, чтобы дать возможность для кристаллизации. Кристаллы собирают путем фильтрования, а затем сушат примерно в течение 17 час 45 мин, в вакуумной печи, при 52°C. Затем продукт анализируют посредством ВЭЖХ. Испытание #185-187: DAF, сульфамид, изохинолин и выбранный растворитель (в таких количествах, как перечислено в табл. 7 и 8) переносят в 250 мл круглодонную колбу. Затем реакционную смесь помещают на масляную баню и перемешивают, при этом нагревая при выбранной температуре реакции в течение выбранного времени (смотри табл. 8). Реакционную смесь охлаждают до примерно комнатной температуры, а затем экстрагируют дважды 1M NaOH (75 мл порциями). Водные экстракты нейтрализуют 6M HCl и дают им постоять при комнатной температуре в течение нескольких дней для облегчения кристаллизации. Кристаллы собирают путем фильтрования, а затем сушат в течение примерно 16-18 часов в вакуумной печи при 50°C. Высушенный продукт анализируют с помощью ВЭЖХ. Примечание: Все экспериментальные испытания дают продукт – топирамат, за исключением тех случаев, которые отмечены. Во время экстракции экспериментального испытания #187 наблюдается образование эмульсии, и хотя ожидалось получение продукта – топирамат, продукт не был собран. Продукт, собранный в экспериментальных испытаниях #187, 191, 194 и 197, как ожидается, должен представлять собой топирамат, но не анализировался. Табл. 7 и 8, ниже, перечисляют условия испытаний для экспериментальных процедур, описанных выше. За исключением случаев, отмеченных выше, все экспериментальные испытания дают продукт – топирамат.
Пример A5 Топирамат получают в соответствии со способом по настоящему изобретению. Ниже перечислены экспериментальные процедуры для экспериментов. Табл. 9 и 10, которые следуют далее, подробно перечисляют экспериментальные условия. Эксперимент 2: DAF, сульфамид, пиридин и o-ксилол в таких количествах, как перечислено ниже в табл. 9, загружают в 1-литровый реактор. Реактор нагревают до температуры кожуха примерно 155°C и поддерживают при этой температуре в течение 30 минут. Реактор охлаждают до 60°C и начинают дистилляцию в вакууме, при этом дистилляция продолжается до тех пор, пока жидкости для дистилляции не останется. Для разделения реакционной смеси на слои добавляют 1M NaOH. Нижний, водный, слой отбирают и переносят в разделительную воронку. Для дополнительного разделения слоев добавляют 1M NaOH. Опять же низший, водный, слой отбирают и переносят в чистый реактор. Для нейтрализации раствора до pH 7 добавляют 6M HCl. Продукт кристаллизуют, фильтруют, а затем сушат с получением топирамата. Эксперименты 3-8, 19-21: DAF, сульфамид, пиридин и o-ксилол в таких количествах, как перечислено в табл. 9, ниже, загружают в 1-литровый реактор. Реактор нагревают и поддерживают при выбранной температуре в течение выбранного времени (смотри табл. 10), затем быстро охлаждают до 65°C. После охлаждения устанавливают вакуум, что приводит к дистилляции некоторого количества органических жидкостей. Температуру во время дистилляции поддерживают в пределах между 55°C и 75°C. После дистилляции добавляют некоторое количество (от 0 до 200 миллилитров) NaOH (крепостью от 1M до 3,5M) для разделения реакционной смеси на две отдельные фазы, верхнюю органическую и нижнюю водную. Нижний, водный, слой отбирают и переносят в чистый реактор. Добавляют кислоту (6M HCl) для нейтрализации реакционной смеси до pH 7. Продукт, кристаллизуемый при нейтрализации, фильтруют, а затем сушат с получением топирамата. Эксперимент 9: DAF, сульфамид, пиридин и o-ксилол в таких количествах, как перечислено в табл. 9, ниже, загружают в 1-литровый реактор. Реактор нагревают до выбранной температуры. Реактор поддерживают при максимальной температуре в течение выбранного количества времени (смотри табл. 9 и 10), а затем быстро охлаждают до 65°C. После охлаждения устанавливают вакуум, что приводит к дистилляции некоторого количества органических жидкостей. Температуру во время дистилляции поддерживают в пределах между 55°C и 75°C. После дистилляции добавляют 3,5M NaOH для разделения реакционной смеси на две отдельные фазы, верхнюю органическую и нижнюю водную. Нижний, водный, слой отбирают и переносят в чистый реактор. Затем в реактор быстро вводят пиридин (40 мл). Добавляют кислоту (6M HCl) для нейтрализации реакционной смеси до примерно pH 7. Продукт кристаллизуют при нейтрализации, а затем фильтруют и сушат с получением топирамата. Эксперименты 10, 15-17: DAF, сульфамид, пиридин и o-ксилол в таких количествах, как перечислено в табл. 9, ниже, загружают в 1-литровый реактор. Реактор нагревают до выбранной температуры. Реактор поддерживают при выбранной температуре в течение выбранного времени (смотри табл. 9 и 10), а затем быстро охлаждают до 65°C. После охлаждения добавляют 3,5M NaOH для разделения реакционной смеси на две отдельные фазы, верхнюю органическую и нижнюю водную. Нижний, водный, слой отбирают и переносят в чистый реактор. Вакуум и тепло применяют для отгонки водной жидкости. Для нейтрализации реакционной смеси до примерно pH 7 добавляют кислоту (6M HCl). Если продукт не кристаллизуется после нейтрализации, добавляют дополнительную воду: для эксперимента #15 добавляют 350 мл воды; для эксперимента #16 добавляют 390 мл воды; для эксперимента #17 добавляют 120 мл воды. Когда продукт кристаллизуется, его фильтруют и сушат с получением топирамата. Эксперимент 11: DAF, сульфамид, пиридин и o-ксилол в таких количествах, как перечислено в табл. 9, ниже, загружают в 1-литровый реактор. Реактор нагревают до выбранной температуры, поддерживают при этой температуре в течение выбранного времени (смотри табл. 9 и 10), а затем быстро охлаждают до 65°C. После охлаждения добавляют 3,5M NaOH для разделения реакционной смеси на две отдельные фазы, верхнюю органическую и нижнюю водную. Нижний, водный, слой отбирают и переносят в чистый реактор. Устанавливают вакуум и прикладывают тепло, что приводит к дистилляции некоторой части водной жидкости. Реактор нагревают до 60°C и добавляют кислоту (6M HCl) для нейтрализации реакционной смеси до pH 7. Реактор охлаждают до 1,5°C, а затем добавляют воду до тех пор, пока не образуются кристаллы. Продукт кристаллизуют, а затем фильтруют и сушат с получением топирамата. Эксперименты 12-14: DAF и сульфамид в таких количествах, как перечислено в табл. 9, ниже, загружают в 1-литровый реактор. Реактор нагревают до выбранной температуры. Реактор поддерживают при выбранной температуре в течение выбранного времени (смотри табл. 9 и 10), а затем быстро охлаждают до примерно комнатной температуры. После охлаждения добавляют 3,5M NaOH для разделения реакционной смеси на две отдельные фазы, верхнюю органическую и нижнюю водную. Нижний, водный, слой отбирают и переносят в чистый реактор. Для нейтрализации реакционной смеси до примерно pH 7 добавляют кислоту (6M HCl). Продукт кристаллизуют при нейтрализации, а затем фильтруют и сушат с получением топирамата. Эксперимент 18: DAF, сульфамид, пиридин и o-ксилол в таких количествах, как перечислено в табл. 9, ниже, загружают в 1-литровый реактор. Реактор нагревают до выбранной температуры. Реактор поддерживают при выбранной температуре в течение выбранного времени (смотри табл. 9 и 10), а затем быстро охлаждают до 65°C. После охлаждения добавляют 3,5M NaOH для разделения реакционной смеси на две отдельные фазы, верхнюю органическую и нижнюю водную. Нижний, водный, слой отбирают и переносят в чистый реактор. Устанавливают вакуум и прикладывают тепло для отгонки примерно половины водной жидкости. Оставшийся водный раствор отбирают и переносят в химический стакан. В очищенный реактор добавляют 6M HCl (60 мл). Реакционную смесь и дополнительную 6M HCl дозируют в реактор для поддержания pH примерно 7. Добавляют воду, чтобы вызвать кристаллизацию. Продукт кристаллизуют, а затем фильтруют и сушат с получением топирамата. Эксперимент 19: DAF, сульфамид и пиридин в таких количествах, как перечислено в табл. 9, ниже, загружают в 1-литровый реактор. Реактор нагревают до выбранной температуры. Реактор поддерживают при выбранной температуре в течение выбранного времени (смотри табл. 9 и 10), а затем быстро охлаждают. После охлаждения до 22°C добавляют 3,5M NaOH для разделения реакционной смеси на отдельные фазы. Три пятых водного слоя отбирают и переносят в чистый реактор. Затем добавляют кислоту (6M HCl) для нейтрализации реакционной смеси до pH примерно 7. В реакционную смесь добавляют 100 мл воды. Продукт кристаллизуют, а затем фильтруют и сушат с получением топирамата.
Пример A6 Диацетонфруктоза (DAF) (780 кг; 780 кг, загрузки 1 и 2), пиридин (950,6 кг; 950,0 кг) и ксилолы (1950 л; 1950 л) смешивают в резервуаре, и раствор переносят в реактор с сульфамидом (575 кг; 575 кг). Смесь нагревают до 128-133°C посредством ступенчатого нагрева. Более конкретно, смесь нагревают от 30 до 65°C в течение 80 минут, затем от 65 до 95°C в течение 60 минут, с последующим нагревом от 95 до 113°C в течение 60 минут и от 113 до 125°C в течение 85 минут. Температуру кожуха реактора увеличивают с приростом по 5°C для нагрева загрузки до 128-133°C в течение 30 минут, а затем выдерживают при этой температуре в течение 30 минут. Затем реакционную смесь охлаждают до 40°C со скоростью 30°C в час. Затем к смеси добавляют очищенную воду (1243 л; 1240 л). Смесь охлаждают до 20°C перед добавлением 50% раствора NaOH (436 кг; 437 кг). Органический и водный слои (слои продукта) разделяют, водный слой фильтруют и переносят в другой реактор. Органический слой отбрасывают. К водной смеси добавляют очищенную воду (1400 л; 1400 л), а оставшиеся органические соединения (пиридин и ксилол) и вода отгоняются в вакууме. Отгонку прекращают после отгонки известного объема (784 л; 784 л). Для нейтрализации раствора до pH 7 добавляют ледяную уксусную кислоту (214,5 кг; 224,4 кг). В смесь вводят затравку топирамата (1,0 кг; 1,0 кг) и охлаждают до 0-5°C для кристаллизации сырого топирамата. Сырой, влажный топирамат (730 кг; выход сырого продукта 803,8 кг) центрифугируют и собирают. Хотя приведенное выше описание говорит о принципах настоящего изобретения с примерами, приводимыми для целей иллюстрации, будет понятно, что осуществление настоящего изобретения охватывает все обычные варианты, адаптации и/или модификации, которые входят в объем следующей далее формулы изобретения и ее эквивалентов.
Формула изобретения
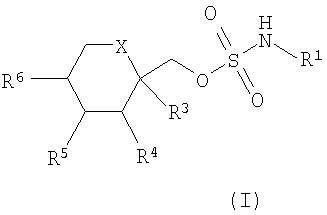
1. Способ получения соединения формулы (I)
где Х выбирается из СН2 или О; R3, R4, R5 и R6, каждый, независимо, выбирается из водорода или низшего алкила, и когда Х представляет собой СН2, R5 и R6 могут представлять собой алкеновые группы, соединенные с образованием бензольного кольца, и когда Х представляет собой О, R3 и R4 и/или R5 и R6 вместе могут представлять собой метилендиоксигруппу формулы:
где R7 и R8 являются одинаковыми или различными, и представляют собой водород, низший алкил, или представляют собой алкил и соединяются вместе с образованием циклопентильного или циклогексильного кольца, включающий взаимодействие соединения формулы (II) с сульфурилдиамидом при повышенной температуре, в присутствии от 0 до примерно 10% воды, с получением соответствующего соединения формулы (I). 2. Способ по п.1, в котором соединение формулы (II) представляет собой диацетонфруктозу. 3. Способ по п.2, в котором сульфурилдиамид присутствует в количестве большем, чем 0,9 эквивалента. 4. Способ по п.3, в котором сульфурилдиамид присутствует в количестве, равном от 1,5 до 3 эквивалентов. 5. Способ по п.2, в котором соединение формулы (II) взаимодействует с сульфурилдиамидом в присутствии неводного органического или неорганического основания. 6. Способ по п.5, в котором неводное органическое основание представляет собой основание третичного амина. 7. Способ по п.6, в котором основание третичного амина представляет собой пиридин. 8. Способ по п.5, в котором неводное органическое или неорганическое основание присутствует в количестве большем, чем 1 эквивалент. 9. Способ по п.8, в котором неводное органическое или неорганическое основание присутствует в количестве, равном от 3 до 5 эквивалентов. 10. Способ по п.2, в котором соединение формулы (II) взаимодействует с сульфурилдиамидом в апротонном органическом растворителе. 11. Способ по п.10, в котором апротонный органический растворитель представляет собой неводное органическое основание. 12. Способ по п.11, в котором неводное органическое основание представляет собой пиридин. 13. Способ по п.2, в котором повышенная температура находится в пределах от 90 до 170°С. 14. Способ по п.13, в котором повышенная температура находится в пределах от 120 до 140°С. 15. Способ по п.2, в котором соединение формулы (II) взаимодействует с сульфурилдиамидом в присутствии от 0 до 3% воды. 16. Способ получения соединения формулы (Ia) включающий взаимодействие соединения формулы (IIa) с сульфурилдиамидом при повышенной температуре, в присутствии от 0 до примерно 10% воды, с получением соответствующего соединения формулы (Ia). 17. Способ по п.16, в котором сульфурилдиамид присутствует в количестве, большем, чем 0,9 эквивалента. 18. Способ по п.17, в котором сульфурилдиамид присутствует в количестве, равном от 1,5 до 3 эквивалентов. 19. Способ по п.16, в котором соединение формулы (IIa) взаимодействует с сульфурилдиамидом в присутствии неводного органического или неорганического основания. 20. Способ по п.19, в котором неводное органическое основание представляет собой основание третичного амина. 21. Способ по п.20, в котором основание третичного амина представляет собой пиридин. 22. Способ по п.19, в котором неводное органическое или неорганическое основание присутствует в количестве, большем, чем 1 эквивалент. 23. Способ по п.22, в котором неводное органическое или неорганическое основание присутствует в количестве, равном от 3 до 5 эквивалентов. 24. Способ по п.16, в котором соединение формулы (IIa) взаимодействует с сульфурилдиамидом в апротонном органическом растворителе. 25. Способ по п.24, в котором апротонный органический растворитель представляет собой неводное органическое основание. 26. Способ по п.25, в котором неводное органическое основание представляет собой пиридин. 27. Способ по п.16, в котором повышенная температура находится в пределах от 90 до 170°С. 28. Способ по п.27, в котором повышенная температура находится в пределах от 120 до 140°С. 29. Способ по п.16, в котором соединение формулы (IIa) взаимодействует с сульфурилдиамидом в присутствии от 0 до 3% воды.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

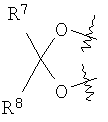
 -D-фруктозу, соединение формулы (IIa)
-D-фруктозу, соединение формулы (IIa)