Патент на изобретение №2333214
|
||||||||||||||||||||||||||
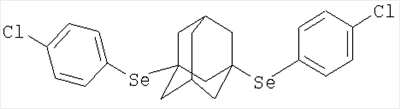
(54) СПОСОБ ПОЛУЧЕНИЯ 1,3-ДИ (4-R-ФЕНИЛСЕЛЕНО)АДАМАНТАНОВ
(57) Реферат:
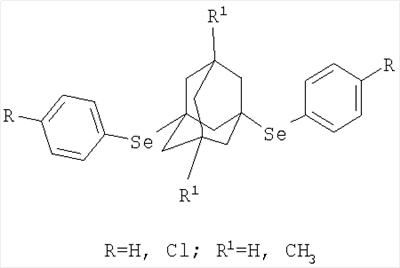
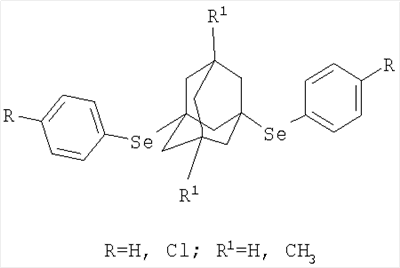
Изобретение относится к химии производных адамантана, а именно к новому способу получения 1,3-ди(4-11-фенилселено)адамантанов общей формулы которые могут представлять интерес в качестве полупродуктов в синтезе некоторых биологически активных веществ. Сущностью метода является реакция получения 1,3-ди(4-R-фенилселено)адамантанов по реакции присоединения к 1,3-дегидроадамантану или 5,7-диметил-1,3-дегидроадамантану соответствующих ди-(4-R)-фенилдиселенидов: бис-фенилдиселенида, бис-4-хлорфенилдиселенида при эквимолярных соотношениях реагентов, в среде абсолютного диэтилового эфира при температуре 34-40°С, в течение 0.5-1 часа. Техническим результатом является расширение ассортимента химических соединений, в частности получение новых 1,3-ди(4-R-фенилселено)адамантанов с высоким выходом.
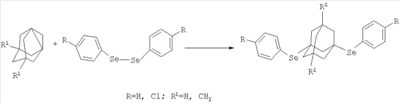
Изобретение относится к химии производных адамантана, а именно к новому способу получения 1,3-ди(4-R-фенилселено)адамантанов общей формулы которые могут представлять интерес в качестве полупродуктов в синтезе некоторых биологически активных веществ. В частности, некоторые органические производные селена нашли применение в ветеринарии, животноводстве, птицеводстве [Патент РФ №2051681, А61К 33/04, опубл. 10.01.96]. Известно также применение ди(3-метилпиразолил-4)селенида, обладающего противоопухолевым действием [Патент РФ №2185819, А61К 9/08, А61К 31/415, А61К 31/095 А61К 33/04 А61Р 35/00, опубл. 27.07.02]. Известен способ получения 9R-симм.-октагидроселеноксантенов на основе взаимодействия 4-R-2,3-тетраметилен[3.3.1]бициклононан-3-ол-9-онов с селеноводородом в условиях кислотного катализа [Патент РФ №2221793, С07D 345/00, опубл. 20.01.04]. Недостатком этого метода является невозможность получения соединений заявляемой структурной формулы. Известен способ получения солей селенопирилия путем взаимодействия 1,5-дикетонов с селеноводородом, получающимся при растворении селенида цинка в реакционной среде [Патент РФ №2276150, С07D 345/00, опубл. 10.05.06]. Однако этим способом невозможно получить соединения заявляемой структурной формулы. Известен способ получения диорганилселенидов или диорганилтеллуридов, в которых органил выбран из ряда: C1-C4-алкил, изо-пропил, аллил, бензил, причем используют следующие условия восстановления: нагревание при 50-80°С в среде гидразин-гидрата с помощью 2-4-кратного избытка КОН. Дальнейшее алкилирование полученных селенидов и теллуридов, прогретых при 60-90°С, ведут обработкой соответствующим органилгалогенидом при нагревании 35-120°С. [Патент РФ №1387365, С07С 395/00, опубл. 30.09.94]. Недостатком этого метода является невозможность получения соединений заявляемой структурной формулы. Известен способ получения 6-(адамант-1-ил-3-бензилоксифенилселенил)-никотиновой кислоты, протекающий через несколько стадий, причем в качестве производного адамантана используют 2-(адамант-1-ил)-5-бромофенол, в качестве производного селена – элементарный селен и процесс протекает при -78°С в присутствии бутиллития [Патент США №6992094, C07D 409/12. Опубл 31.01.06]. Недостатками этого метода являются сложные условия проведения реакций, многостадийность. Кроме этого, данный способ не позволят получать соединения заявляемой структурной формулы. Наиболее близким к предлагаемому изобретению является реакция 2,21 Задачей предлагаемого изобретения является разработка технологичного малостадийного метода синтеза 1,3-ди(4-R-фенилселено)адамантанов, протекающего с высоким выходом по исходному адамантану. Техническим результатом является расширение ассортимента химических соединений, в частности получение новых 1,3-ди(4-R-фенилселено)адамантанов с высоким выходом. Поставленный технический результат достигается в новом способе получения 1,3-ди(4-R-фенилселено)адамантанов общей формулы путем взаимодействия 1,3-дегидроадамантана или 5,7-диметил-1,3-дегидроадамантана с ди-(4-R)-фенилдиселенидами: бис-фенилдиселенидом, бис-4-хлорфенилдиселенидом при эквимолярных соотношениях реагентов, в среде абсолютного диэтилового эфира при температуре 34-40°С, в течение 0.5-1 часа. Сущностью метода является реакция получения 1,3-ди(4-R-фенилселено)адамантанов по реакции присоединения к 1,3-дегидроадамантану (1,3-ДГА) или 5,7-диметил-1,3-дегидроадамантану (5,7-ДМ-1,3-ДГА) соответствующих ди-(4-R)-фенилдиселенидов. Реакция основана на ранее неизвестных свойствах 1,3-дегидроадамантана или 5,7-диметил-1,3-дегидроадамантана расщеплять ди-(4-R)-фенилдиселениды по связи селен-селен. Реакция является неизвестной, так как в литературе отсутствуют сведения о взаимодействии 1,3-дегидроадамантана или 5,7-диметил-1,3-дегидроадамантана с ди-(4-R)-фенилдиселенидами или родственным им соединениями, равно как и отсутствуют сведения о получении и свойствах соединений заявляемой структурной формулы. Взаимодействие является возможным благодаря высокой реакционной способности 1,3-дегидроадамантана или 5,7-диметил-1,3-дегидроадамантана в радикальных реакциях, а также высокой лабильностью связи селен-селен. Данная реакция является первым примером внедрения углеводорода по связи Se-Se в диселенидах с образованием бисселенидов заявляемой формулы в мягких условиях, так как в литературе известны реакции расщепления связи Se-Se хлором, бромом, тионилхлоридами и сульфурилга-логенидами, водными растворами щелочей, дегидробензолом и диазометаном [Общая органическая химия / Под ред. Д.Бартона и У.Д.Оллиса. Т.6. Соединения селена, теллура, кремния и бора. М.: Химия, 1984. – c.35]. Способ осуществляется следующим образом. К раствору соответствующего ди-(4-R)-фенилдиселенида из ряда: бис-фенилдиселенид, бис-4-хлорфенилдиселенид в осушенном диэтиловом эфире приливают раствор эквимолярного количества 1,3-дегидроадамантана или 5,7-диметил-1,3-дегидроадамантана в диэтиловом эфире, при этом наблюдается незначительный экзотермический эффект. Реакционную смесь нагревают в течение 0.5-1 часа при температуре кипения реакционной смеси (34-40°С), после чего растворитель отгоняют, остаток выдерживают в вакууме водоструйного насоса при 60-80°С в течение 2 часов. Выходы 1,3-ди(4-R-фенилселено)адамантанов составляют 81-86%. Как показали проведенные исследования, обязательным условием чистоты образующихся 1,3-ди(4-R-фенилселено)адамантанов является использование стехиометрического соотношения 1,3-дегидроадамантана или 5,7-диметил-1,3-дегидроадамантана и соответствующего ди-(4-R)-фенилдиселенида. Избыток 1,3-дегидроадамантана или 5,7-диметил-1,3-дегидроадамантана приводит к значительному содержанию побочных продуктов их димеризации. Избыток ди-(4-R)-фенилдиселенидов приводит загрязнению им целевых продуктов. Исследования показали, что повышение температуры нецелесообразно в связи с достаточно высокой скоростью реакции. Оптимальной продолжительностью процесса является 0.5-1 час. При этом наблюдалась полная конверсия 1,3-дегидроадамантана или 5,7-диметил-1,3-дегидроадамантана. Строение синтезированных соединений подтверждено хромато-масс, ЯМР 1Н-спектроскопией. Изобретение иллюстрируется следующими примерами. Пример 1. 13-Ди(фенилселено)адамантан.
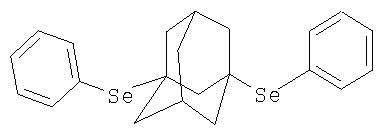
К раствору 1 г (0.0032 моль) бис-фенилдиселенида в 10 мл абсолютного диэтилового эфира в атмосфере сухого азота при комнатной температуре прикапывают раствор 0.43 г (0.0032 моль) свежевозогнанного 1,3-дегидроадамантана (соотношение 1,3-ДГА: бис-фенилдиселенид = 1:1) в 10 мл абсолютного диэтилового эфира, после чего реакционную смесь кипятят при температуре 34-40°С в течение 1 часа, после чего диэтиловый эфир удаляют перегонкой, остаток выдерживают в вакууме водоструйного насоса и получают 1.23 г (0.00275 моль, 86%) 1,3-ди(фенилселено)адамантана. Спектр ЯМР 1Н, Пример 2. 1,3-Ди(4-хлорфенилселено)адамантан. К раствору 1 г (0.00262 моль) бис-(4-хлорфенил)диселенида в 5 мл диэтилового эфира в атмосфере сухого азота при комнатной температуре прикапывают раствор 0.35 г (0.00262 моль) свежевозогнанного 1,3-дегидроадамантана (соотношение 1,3-ДГА:бис-(4-хлорфенил)диселенид = 1:1) в 10 мл абсолютного диэтилового эфира. Реакционную смесь кипятят при температуре 34-40°С в течение 40 мин, после чего диэтиловый эфир удаляют перегонкой, остаток выдерживают в вакууме водоструйного насоса и получают 1.122 г (0.00218 моль, 83%) 1,3-ди(4-хлорфенилселено)адамантана. Тпл=117-118°С. Спектр ЯМР 1Н, Пример 3. 5,7-Диметил-1,3-ди(фенилселено)адамантан.
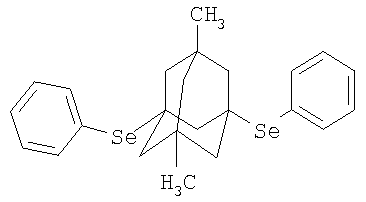
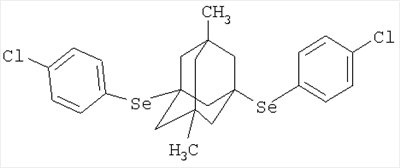
К раствору 1 г (0.0032 моль) бис-фенилдиселенида в 5 мл абсолютного диэтилового эфира в атмосфере сухого азота при комнатной температуре прикапывают раствор 0.525 г (0.0032 моль) свежевозогнанного 5,7-диметил-1,3-дегидроадамантана (соотношение 5,7-ДМ-1,3-ДГА:бис-фенилдиселенид = 1:1) в 10 мл абсолютного диэтилового эфира, после чего реакционную смесь кипятят при температуре 34-40°С в течение 45 минут, после чего диэтиловый эфир удаляют перегонкой, остаток выдерживают в вакууме водоструйного насоса и получают 1.304 г (0,00275 моль, 86%) 5,7-диметил-1,3-ди(фенилселено)адамантана, белые кристаллы, Tпл.=102-103°С. Спектр ЯМР 1Н, Пример 4. 5,7-Диметил-1,3-ди(4-хлорфеннлселено)адамантан. К раствору 1 г (0.00262 моль) бис-(4-хлорфенил)диселенида в 10 мл абсолютного диэтилового эфира в атмосфере сухого азота при комнатной температуре прикапывают раствор 0.43 г (0.00262 моль) свежевозогнанного 5,7-диметил-1,3-дегидроадамантана (соотношение 5,7-ДМ-1,3-ДГА:бис-(4-хлорфенил)диселенид = 1:1) в10 мл абсолютного диэтилового эфира, после чего реакционную смесь кипятят при температуре 34-40°С в течение 0.5 часа, после чего диэтиловый эфир удаляют перегонкой, остаток выдерживают в вакууме водоструйного насоса и получают 1.152 г (0.0021 моль, 81%) 5,7-диметил-1,3-ди(4-хлорфенилселено)адамантана, белые кристаллы, Тпл.=145-147°С. Спектр ЯМР 1Н, Выводы Разработан одностадийный способ получения 1,3-ди(4-R-фенилселено)адамантанов, позволяющий получать соединения заявляемой структурной формулы с высокими выходами. Структура полученных соединений подтверждена хромато-масс- и ЯМР’Н-спектроскопией.
Формула изобретения
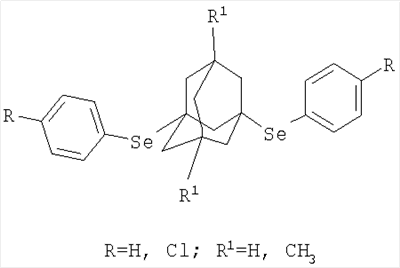
Способ получения 1,3-ди(4-R-фенилселено)адамантанов общей формулы заключающийся во взаимодействии 1,3-дегидроадамантана или 5,7-диметил-1,3-дегидроадамантана с ди-(4-R)-фенилдиселенидами: бис-фенилдиселенидом, бис-4-хлорфенилдиселенидом при эквимолярных соотношениях реагентов в среде абсолютного диэтилового эфира при температуре 34-40°С в течение 0,5-1 ч.
|
||||||||||||||||||||||||||

 , м.д.: 1.42 с, 1.74 д, 1.83 с, 2.10 с (12Н, 6 CH2 (адамантил); 7.14-7.27 м (2+1Н, Ph); 7.39-7.43 м (2Н, Ph). Масс-спектр, m/e, (I, %): 448 (М+, 7%), 291 (100), 235 (6), 157 (50), 133 (78).
, м.д.: 1.42 с, 1.74 д, 1.83 с, 2.10 с (12Н, 6 CH2 (адамантил); 7.14-7.27 м (2+1Н, Ph); 7.39-7.43 м (2Н, Ph). Масс-спектр, m/e, (I, %): 448 (М+, 7%), 291 (100), 235 (6), 157 (50), 133 (78).