Патент на изобретение №2333212
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) ПРОИЗВОДНЫЕ 1-И 7-[
(57) Реферат:
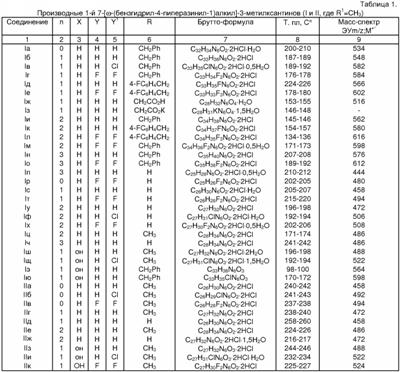
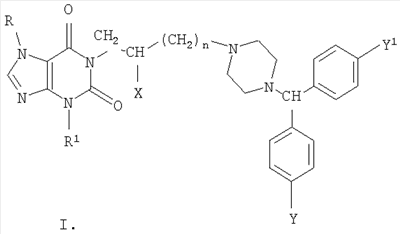
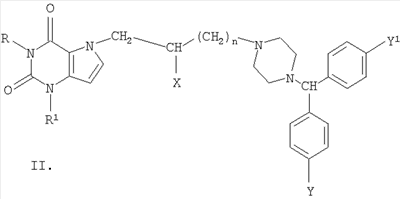
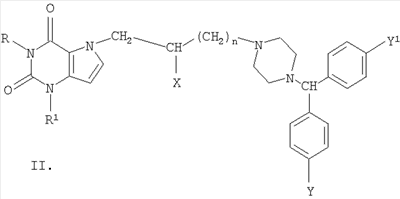
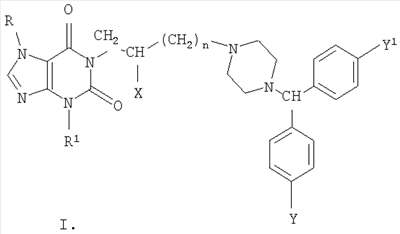
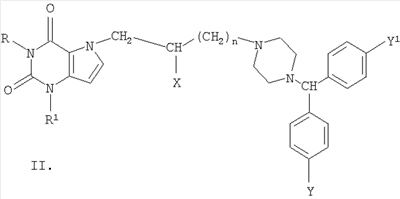
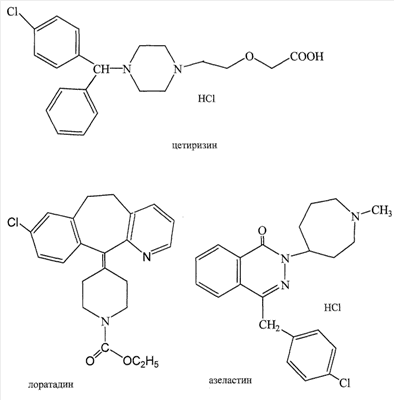
Изобретение относится к новым производным 1- и 7-[ R=Н, Me, CH2Ph; R1=Me, н – С4Н9; n=0-3; Х=Н, ОН, OCOCH2CH2СООН; Y=Y1=Н, Cl, F; при условии, что R и R1 одновременно не означают метил. Соединения настоящего изобретения обладают высокой противогистаминной и антиаллергической активностью. Например, 7-[4-(бензгидрил-4-пиперазинил-1)бутил]-3-метилксантина дигидрохлорид по активности, включая длительность действия, превосходит наиболее эффективные современные противогистаминные и антиаллергические препараты: цетиризин, лоратадин и азеластин. 1 з.п. ф-лы, 3 табл.
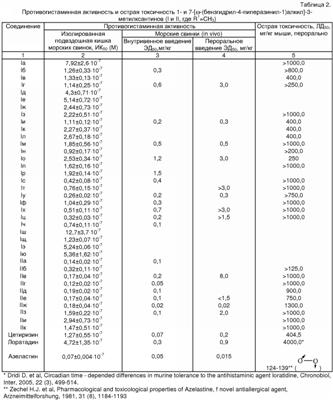
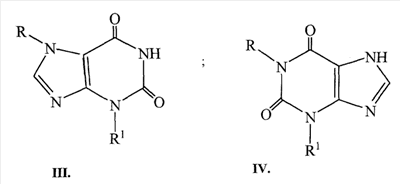
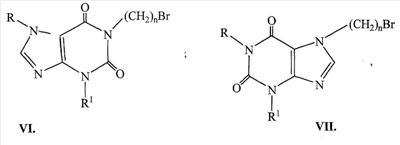
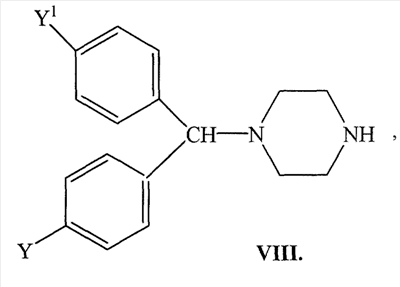
Несмотря на довольно большую номенклатуру противогистаминных препаратов, применяющихся в медицинской практике в качестве антиаллергических средств, поиск новых блокаторов Н-1 гистаминовых рецепторов остается актуальной задачей в связи с тем, что большинство существующих препаратов этого класса не лишены недостатков, таких как: кратковременность действия, наличие побочных эффектов со стороны центральной нервной системы и др. (М.Д.Машковский, Лекарственные средства, Москва, «Новая волна», 2005 г., 15 издание, с.285-297). В этой связи особый интерес представляет поиск оригинальных противогистаминных (антиаллергических) лекарственных средств с новой химической структурой и, в частности, в ряду производных ксантина, среди которых имеется ряд высокоактивных природных соединений (теофиллин, теобромин, кофеин), обладающие ценными фармакотерапевтическими свойствами. Целью изобретения является расширение номенклатуры противогистаминных (антиаллергических) лекарственных средств. Указанная цель достигается синтезом и оценкой биологической активности оригинальных химических соединений, в основе которых лежит структура ксантина, в частности производных 1- и 7-[ где R=Н, Me, CH2Ph; R1=Me, н – С4Н9; n=0-3 X=Н, ОН, ОСОСН2СН2СООН; Y=Y1=Н, Cl, F; при условии, что R и R1 одновременно не означают Me которые обладают противогистаминной и антиаллергической активностью и могут быть использованы в медицине для изготовления на их основе новых высокоактивных и малотоксичных антиаллергических лекарственных средств. Заявляемые соединения синтезируют следующими методами: Метод А. Производные ксантина общих формул III и IV, где R=H, Me, CH2Ph; R1=Me, н -С4Н9; которые получают по классическому методу Траубе (К.В.Вацуро, Г.Л.Мищенко, Именные реакции в органической химии, Москва, Из-во «Химия», 1976, с.400; П.М.Кочергин и сотр., ХГС, 1995 г., №9, с.388), алкилируют в виде соли со щелочным металлом (Na, К) Br(CH2)nBr (V, где n=2-5). Образующиеся обрабатывают в присутствии иодистого калия замещенными бензгидрилпиперазинами общей формулы VIII: при этом получают заявляемые соединения I и II, где Х=Н (таблица 1). Метод Б. Согласно этому методу производные ксантина III и IV, где R=H, Me, CH2Ph; R1=Me, н-С4Н9; обрабатывают эпихлоргидрином. При этом в зависимости от условий реакции (безводная или водная среда) образуются замещенные 1- или 7-(2,3-эпоксипропил)ксантины (IX и X, где (H.J.Roth, Reaction of theophylline and theobromine with 1,2-epoxides, Arch. Pharm., 1959, 292, 234-238; J.Med. Chem., 1985, 28, №5, 652). При взаимодействии IX и Х с бензгидрилпиперазином и его производными получают заявляемые соединения I и II, где Х=ОН; n=1 (Таблица 1). Биологическая активность производных 1- и 7-[ Исследование антигистаминной активности заявляемых соединений проводили по известным методикам (Руководство по экспериментальному изучению новых фармакологических веществ, Москва, 2005 г., с.489) на изолированной подвздошной кишке морских свинок (подавление спазмогенного эффекта гистамина) и на наркотизированных морских свинках (антагонизм в отношении бронхоконстрикторного эффекта гистамина). В опытах на целых животных вещества вводили внутривенно (за 5 минут до введения гистамина) и внутрь (за 2 часа до начала исследования). При оценке длительности противогистаминного действия соединения вводили внутрь за 24-72 часа до начала исследования. Наиболее активное соединение IIж (где R=H; R1=СН3; n=2; X=H; Y=Y1=H) изучено также на бодрствующих морских свинках с использованием модели зуда, вызываемого инстилляцией в глаз животного раствора гистамина (противогистаминное действие), а также у крыс на модели пассивной кожной анафилаксии (противоаллергический эффект); (Руководство по экспериментальному изучению новых фармакологических веществ, Москва, 2005 г., с.511) Заявляемые соединения I и II изучали в сравнении с близкими по фармакологическому действию и широко использующимися в медицинской практике препаратами: цетиризином, лоратадином и азеластином (Машковский М.Д., Лекарственные средства, «Новая Волна», 2005 г., 15 издание, с.285-297) Результаты исследования противогистаминной активности и токсичности заявляемых соединений I и II представлены в таблице 2. Как следует из представленных данных, большинство заявляемых соединений в условиях in vitro и in vivo по противогистаминной активности (показатели ИК50 и ЭД50 соответственно) не уступают цетиризину и лоратадину, но менее активны в сравнении с азеластином. Исключением является соединение IIж, которое на изолированной кишке морских свинок существенно превосходит по активности цетиризин и лоратадин, хотя несколько уступает азеластину. Вместе с тем, в условиях in vivo при внутривенном введении соединение IIж активнее всех указанных выше препаратов сравнения; при введении внутрь (за 2 часа до начала исследования) соединение IIж по силе действия превосходит цетиризин и лоратадин и сходно с азеластином. Следует подчеркнуть, что по длительности противогистаминного действия соединение IIж превосходит все препараты сравнения, включая азеластин. Так, на модели гистаминового бронхоспазма, соединение IIж, цетиризин, лоратадин и азеластин после введения внутрь в дозе 3 мг/кг обеспечивают эффективную блокаду H1-гистаминовых рецепторов бронхов в течение 72, 48, 18 и 48 часов соответственно. На модели зуда, вызываемого гистамином, защитный эффект соединения IIж в дозе 3 мг/кг внутрь сохраняется на стабильном уровне в течение 2 суток и уменьшается лишь через 72 часа, тогда как аналогичный эффект цетиризина и азеластина в такой же дозе уже через 48 часов существенно уменьшается, а через 72 часа полностью исчезает. На модели пассивной кожной анафилаксии соединение IIж и цетиризин в дозах 1 и 3 мг/кг соответственно оказывают умеренное и сходное антиаллергическое действие. Весьма важным обстоятельством является тот факт, что соединение IIж менее токсично, чем азеластин и цетиризин. Соединение IIж термически устойчиво, легко растворимо в воде и в отличие от лоратадина может быть использовано для приготовления как твердых лекарственных форм, так и глазных капель. Полученные результаты позволяют заключить, что найденный и изученный нами ряд производных 1- и 7-[ Пример 1. Получение 1-(4-бромбутил)-3-метил-7-бензилксантина (VIк, R=CH2Ph; R1=СН3, n=4). К 60 мл абс. СН3ОН, содержащего 2,79 г (0,0517 моль) метилата натрия, прибавляют 10,0 г (0,039 моль) 3-метил-7-бензилксантина (III. R=СН2Ph, R1=СН3). Суспензию кипятят при перемешивании 30 минут; реакционную массу упаривают досуха; в конце процесса остатки метанола удаляют с отгонкой толуола, получают 10,86 г 1-натриевой соли 3-метил-7-бензилксантина. К раствору 42,3 г (24,4 мл; 0,196 моль) 1,4-дибромбутана в 100 мл диметилформамида (ДМФА) прибавляют 10,86 г (0,039 моль) 1-натриевой соли 3-метил-7-бензилксантина и кипятят (-150°) при пермешивании 3,5 часа. Массу упаривают в вакууме, к остатку добавляют воду и бензол, перемешивают, бензольный слой отделяют, промывают водой, сушат над сульфатом натрия и фильтруют через слой окиси алюминия. Фильтрат упаривают до объема 30 мл и прибавляют равное количество гексана. Выпавший осадок отфильтровывают и сушат. Получают 12,16 г (79,6%), 1-(4-бромбутил)-3-метил-7-бензилксантина, т.пл. 90-92° (из метанола), М+. 91. Пример 2. Получение 3-метил-7-(4-бромбутил)ксантина (VIIк, R=H, R1=СН3, n=4). К раствору 42,3 г (0,196 моль; 23,4 мл) 1,4-дибромбутана в 100 мл ацетонитрила прибавляют 10,0 г (0,049 моль) 7-калиевой соли 3-метилксантина. Суспензию кипятят при перемешивании 28 часов, охлаждают, выпавший осадок отфильтровывают, промывают до нейтральной реакции водой, затем метанолом и сушат. Получают 9,0 (61%) технического 3-метил-7-(4-бромбутил)ксантина (VII, R=H, R1=СН3, n=4), после двукратной очистки технического образца кристаллизацией из смеси бензола и метанола, а затем диметисульфоксида, т.пл. 218-220°, М+. 301. Аналогично синтезируют другие VI и VII (см. таблицу 3). Пример 3. Получение 1-(2,3-эпоксипропил)-3,7-диметилксантина (IX, где Аналогично из Na-соли 3-метил-7-бензилксантина (III, 1-Na-соль, R=CH2Ph; R1=СН3) синтезируют 1-(2,3-эпоксипропил)-3-метил-7-бензилксантин (IX, где Пример 4. Получение 3-метил-7-[4-(бензгидрил-4-пиперазинил-1)бутил]ксантина дигидрохлорида (II, где R=H, R1=СН3, Х=Н, n=2, Y=Y1=H). Смесь 2,0 г (0,006 моль) 90%-ного 3-метил-7-(4-бромбутил)ксантина (VII, где R=H, R1=Me, n=4), 1,5 г (0,006 моль) бензгидрилпиперазина VIII (где Y=Y1=H) и 0,05 г йодистого калия в 40 мл ацетонитрила кипятят при перемешивании 30 часов. Реакционную массу упаривают, к остатку добавляют 25 мл 5%-ной соляной кислоты; нерастворившийся осадок отфильтровывают, а раствор экстрагируют хлороформом. Полученный после экстракции солянокислый раствор подщелачивают до рН 8 твердым бикарбонатом натрия и экстрагируют хлороформом. Экстракт промывают насыщенным раствором хлористого натрия и сушат сульфатом магния. К высушенному хлороформному раствору прибавляют до рН2 насыщенный раствор хлористого водорода в метаноле, массу упаривают и остаток кристаллизуют из этанола с добавлением воды, получают 1,95 г (56,7%) 3-метил-7-[4-(бензгидрил-4-пиперазинил-1)бутил]ксантина дигидрохлорида (II, где R=H, R1=СН3, Х=Н, n=2, Y=Y1=H), т.пл. 216-217°. Найдено %: С56,47; Н6,75; N 14,63; Н20 4,70. C27H32N6O2·2 HCl·1,5Н20 Вычислено %: С56,47; Н 6,50; N 14,63; Н2O 4,93. Сукцинат 3-метил-7-[4-бензгидрил-4-пиперазинил-1)бутил]ксантина, т.пл. 187,5-189°. Найдено%: С 62,95; Н 7,06; N 14,28; C31H38N6O6; Вычислено %: 63,04; Н 6,48; N 14,23. В аналогичных условиях из 3-бутал-7-(4-бромбутил)ксантина (VII, где R=Н R1=н-Bu; n=4) и бензгидрилпиперазина (VIII, где Y=Y1=H) синтезируют 3-бутил-7-[4-(бензгидрил-4-пиперазинил-1)бутил]ксантина дигидрохлорид (II, где R=H, R1=н-C4H9, Х=Н, n=2, Y=Y1=H), выход 49,4%, т.пл. 240-242°; M+. 514. Найдено %: С61,07; Н 6,98; N14,21. C30H38N6O2·2 HCl Вычислено %: 61,32; Н 6,86; N14,30. Пример 5. Получение 1-[4-(бензгидрил-4-пиперазинил-1)бутил]-3-метилксантина дигидрохлорида (I, где R=H, R1=СН3, Х=Н, n=2, Y=Y1=H) из 7-бензил-1-(4-бромбутил)-3-метилксантина (VI, где R=бензил, R1=Me). Раствор 2,1 г (0,005 моль) 95%-ного 7-бензил-1-(4-бромбутил)-3-метилксантина в 50 мл метанола и 0,21 г 20%-ной гидроокиси палладия на угле гидрируют при 40° до прекращения поглощения водорода (1,5 часа). Катализатор отфильтровывают, промывают горячим метанолом, фильтрат упаривают, получают 1,35 г 1-(4-бромбутил)-3-метилксантина (VI, где R=H, R1=Me, n=4). Смесь 1,35 г последнего, 1,13 г (0,045 моль) бензгидрилпиперазина (VIII, где Y=Y1=H), 0,036 (0,00022 моль) иодистого калия и 30 мл ацетонитрила кипятят при перемешивании 15 час. Реакционную массу упаривают, остаток растворяют в 25 мл 5%-ной соляной кислоты, раствор промывают хлороформом и солянокислый раствор подщелачивают твердым бикарбонатом натрия до рН8. Полученную массу экстрагируют хлороформом, экстракт промывают насыщенным водным раствором хлористого натрия и сушат сульфатом магния. Хлороформный раствор упаривают, остаток растворяют в 5 мл изопропанола, к раствору добавляют насыщенный раствор хлористого водорода в изопропаноле до рН 2. После охлаждения (5-7°, 16 час) осадок отфильтровывают и кристаллизуют из смеси метанол-изопропанол, получают 1, 38 г (50,7%) 1-[4-(бензгидрил-4-пиперазинил-1)бутил]-3-метилксантина дигидрохлорида, т.пл. 198-198°. Найдено %: С59,41; Н6,54; N15,06. C27H32N6O2·2 HCl Вычислено %: C59,45; H6,28; N15,40. Аналогично из 1-(4-бромбутил)-3-бутил-7-бензилксантина (VI, где R=СН2Ph; R1=н-Bu; n=4) и бензгидрилпиперазина (VIII, где Y=Y1=H) получают 1-[4-(бензгидрил-4-пиперазинил-1)бутил]-3-бутилксантин дигидрохлорид (I, где R=H, R1=н-Bu, X=H, n=2, Y=Y1=H), выход 42,2%, т.пл. 215-217°; М+. 514. Найдено %: С60,29; Н7,44; N13,93; Н2O 2,55. C30H38N6O2·2HCl·0,75 H2O Вычислено %: С59,94; Н7,04; N13,98; Н2O 2,25. Пример 6. Получение 1,3-диметил-7-[2-окси-3-(бензгидрил-4-пиперазинил-1)пропил]ксантина дигидрохлорида (II, где R=R1=СН3, n=1, Х=ОН, Y=Y1=H). Смесь 2,45 г (0,009 моль) 1,3-диметил-7-(2-окси-3-хлорпропил)ксантина (X, где Z=-CH(OH)-CH2Cl) (см. H.J.Roth, Arch. Pharm., 1959, 292, 234-238), 2,27 г (0,009 моль) бензгидрилпиперазина (VIII, где Y=Y1=H), 1,38 г. поташа, 0,08 г (0,00005 моль) иодистого калия и 50 мл ацетонитрила кипятят при перемешивании 20 часов. Массу упаривают, остаток растворяют в хлороформе, раствор промывают водой, сушат сульфатом магния. После отгонки хлороформа, остаток кристаллизуют из этилацетата, получают 2, 61 г. основания II (где R=R1=СН3; n=1, Х=ОН, Y=Y1=H), которое растворяют в 70 мл изопропанола. К полученному раствору добавляют раствор хлористого водорода в изопропаноле до рН 2, выпавший осадок отфильтровывают и сушат. Получают 3,34 (66%) 1,3-диметил-7-[2-окси-3-(бензгидрил-4-пиперазинил-1)пропил]ксантинадигидрохлорида, т.пл. 224-226°. Найдено %: С57,32; Н6,10; N14,86. С27Н32N6О3·2 HCl Вычислено %: С57,75; Н6,10; N14,97. Пример 7. Получение 1,3-диметил-7-[2-карбоксиэтилкарбонилокси-3-(бензгидрил-4-пиперазинил-1)пропил]ксантина (II, где R=Rl=CH3; n=1; Х=ОСОСН2СН2СООН; Y=Y1=H). Смесь 2,0 г (0,004 моль) 1,3-диметил-7-[2-окси-3(бензгидрил-4-пиперазинил-1)пропил]ксантина (II, где R=R1=СН3; n=1; Х=ОН; Y=Y1=H), 0,5 г (0,005 моль) ангидрида янтарной кислоты и 20 мл дихлорэтана кипятят 4 часа и упаривают досуха. Остаток кристаллизуют из абсолютного этанола, получают 2,04 г (86,7%) 1,3-диметил-7-[2-карбоксиэтилкарбонилокси)-3-(бензгидрил-4-пиперазинил-1)пропил]ксантина, т.пл. 183-185°. Найдено %: С63,28; Н6,53; N14,32. C31H36N6O2. Вычислено %: С63,25; Н6,16; N14,28. Пример 8 Получение 1-[2-окси-3-(бензгидрил-4-пиперазинил-1)пропил]-3,7-диметилксантин дигидрохлорида I (где R=R1=СН3; n=1; X=OH; Y=Y1=H). Смесь 1 г (0,0042 моль) 1-(2,3-эпоксипропил)-3,7-диметилксантина, 1,26 г (0,0044 моль) бензгидрилпиперазина и 30 мл изопропанола кипятят при перемешивании 30 часов. По охлаждении осадок отфильтровывают, промывают эфиром и сушат. Получают 1,96 г (95%) 1-[2-окси-3-(бензгидрил-4-пиперазинил-1)пропил]-3,7-диметилксантина: – основание, т.пл. 120-122°, М+. 488; – дигидрохлорид, т.пл. 196-198°; М+. 488. Аналогично синтезируют: – 1-[2-окси-3-(41-хлорбензгидрил-4-пиперазинил-1)пропил]-3,7-диметилксантин (I, где R=Rl=CH3; n=1; Х=ОН; Y=Cl; Y1=H): – основание, выход 67%, т.пл. 152-155°; – дигидрохлорид, т.пл. 192-194°. 1-[2-окси-3-(бензгидрил-4-пиперазинил-1)-пропил]-3-метил-7-бензилксантин (I, где R=CH2Ph, R1=Me; n=1; X=OH; Y=Y1=H), выход 50%, т.пл. 98-100°. 1-[2-окси-3-(41-хлорбензгидрил-4-пиперазинил-1)пропил]-3-метил-7-бензилксантин (I, где R=СН2Ph, R1=Ме; n=1; X=OH; Y=Cl; Y1=H), выход 50%, т.пл. 170-172°.
Формула изобретения
1. Производные 1- и 7-[ где R=Н, Me, CH2Ph; R1=Me, н – С4Н9; n=0-3; X=Н, ОН, ОСОСН2СН2СООН; Y=Y1=Н, Cl, F, при условии, что R и R1 одновременно не означают метил, включая их фармацевтически приемлемые соли и/или их гидраты. 2. Соединение по п.1, а именно, 7-[4-(бензгидрилпиперазинил-1)бутил]-3-метилксантина дигидрохлорид (IIж, где R=Н; R1=Me; n=2; Х=Н; Y=Y1=Н), обладающее противогистаминным и антиаллергическим действием.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 -(БЕНЗГИДРИЛ-4-ПИПЕРАЗИНИЛ-1)АЛКИЛ]-3-АЛКИЛКСАНТИНОВ, ОБЛАДАЮЩИЕ ПРОТИВОГИСТАМИННОЙ И АНТИАЛЛЕРГИЧЕСКОЙ АКТИВНОСТЬЮ
-(БЕНЗГИДРИЛ-4-ПИПЕРАЗИНИЛ-1)АЛКИЛ]-3-АЛКИЛКСАНТИНОВ, ОБЛАДАЮЩИЕ ПРОТИВОГИСТАМИННОЙ И АНТИАЛЛЕРГИЧЕСКОЙ АКТИВНОСТЬЮ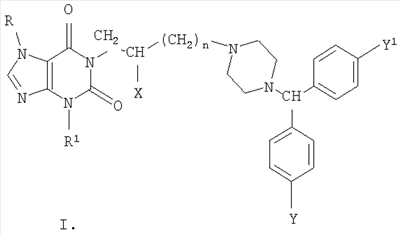
 ,
,
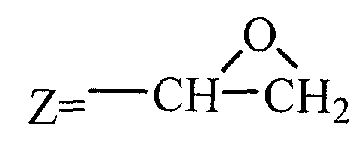 ) или 1- и 7- (3-хлор-2-оксипропил)-ксантины (IX и X, где Z=-СН(ОН)-СН2Cl)
) или 1- и 7- (3-хлор-2-оксипропил)-ксантины (IX и X, где Z=-СН(ОН)-СН2Cl)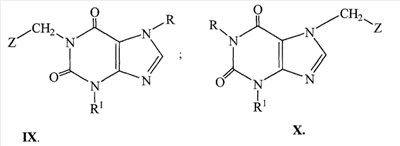
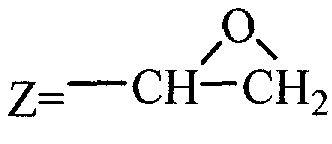 , R=R1=СН3). Суспензию 3 г (0,148 моль) натриевой соли 3,7-диметилксантина (III, 1-Na соль; R=R1=СН3) и 20 мл эпихлоргидрина нагревают при перемешивании при 65-70° в течение 20 часов. По охлаждении осадок отфильтровывают и промывают хлористым метиленом. Полученный раствор IX в хлористом метилене упаривают, маслообразный остаток растирают в абсолютном эфире, получают 2,7 (77%) 1-(2,3-эпоксипропил)-3,7-диметилксантина, т.пл. 115-119°, M+. 236 (J-C. Pascal et al, J. Med. Chem., 1985, №28, №5, 647-652, т.пл. 116-117°).
, R=R1=СН3). Суспензию 3 г (0,148 моль) натриевой соли 3,7-диметилксантина (III, 1-Na соль; R=R1=СН3) и 20 мл эпихлоргидрина нагревают при перемешивании при 65-70° в течение 20 часов. По охлаждении осадок отфильтровывают и промывают хлористым метиленом. Полученный раствор IX в хлористом метилене упаривают, маслообразный остаток растирают в абсолютном эфире, получают 2,7 (77%) 1-(2,3-эпоксипропил)-3,7-диметилксантина, т.пл. 115-119°, M+. 236 (J-C. Pascal et al, J. Med. Chem., 1985, №28, №5, 647-652, т.пл. 116-117°).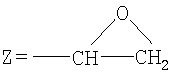 , R=CH2Ph; R1=СН3), выход 80%, т.пл. 90-95°, М+. 312.
, R=CH2Ph; R1=СН3), выход 80%, т.пл. 90-95°, М+. 312.