|
|
(21), (22) Заявка: 2004137708/04, 23.12.2004
(24) Дата начала отсчета срока действия патента:
23.12.2004
(43) Дата публикации заявки: 10.06.2006
(46) Опубликовано: 27.08.2008
(56) Список документов, цитированных в отчете о
поиске:
WO 02/064590 A3, 22.08.2002. WO 94/23720, 27.10.1994. УЭЛИ В.М., ГОВИНДАЧАРИ Т.Р. Синтез тетрагидроизохинолинов и подобных им соединений по методу Пиктэ-Шпенглера. Органические реакции. Сборник 6. / Под общей редакцией Р.Адамса. – М.: Изд-во иностранной литературы, 1953, c.177-217. HORIGUCHI Y. et al «A synthesis of chiral 1,1,3-trisubstituted
Адрес для переписки:
125047, Москва, Миусская пл., 9, РХТУ им. Д.И. Менделеева, патентный отдел
|
(72) Автор(ы):
Семенов Борис Борисович (RU),
Новиков Кирилл Александрович (RU),
Качала Вадим Вадимович (RU)
(73) Патентообладатель(и):
Российский Химико-Технологический Университет им. Д.И. Менделеева (РХТУ им. Д.И. Менделеева) (RU)
|
(54) СПОСОБ ПОЛУЧЕНИЯ 1- И 1,1-ДИЗАМЕЩЕННЫХ-4-ФЕНИЛ-2,3,4,9-ТЕТРАГИДРО-1H-БЕТТА-КАРБОЛИНОВ
(57) Реферат:
Настоящее изобретение относится к способу получения аналогов природных алкалоидов гарманового ряда (елеагнина), обладающих потенциальной биологической активностью, в частности к способу получения 1-замещенных-4-фенил-2,3,4,9-тетрагидро-1Н-бетта-карболинов общей формулы
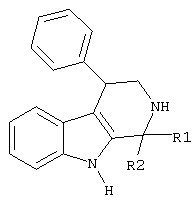
в которой один из R1 и R2 означает атом водорода, а другой представляет собой алкил с числом атомов углерода от одного до двух либо арил, гетарил, либо R1 и R2 вместе с атомом углерода, к которому они присоединены, образуют необязательно замещенный индол-3-он. Способ заключается в циклизации альдегидов с замещенным триптамином в присутствии кислот, при этом в качестве замещенного триптамина используют бета-фенилтриптамин, в качестве альдегидов используют алифатические или ароматические альдегиды или необязательно замещенные изатины, в качестве кислот используют минеральные кислоты или катализаторы Льюиса. 4 табл.
(56) (продолжение):
CLASS=”b560m”1,2,3,4-tetrahydro-beta-carbolines by the Pictet-Spengler reaction of tryptophan and ketones: conversion of (1R,3S)-diastereomers into their (1S,3S)-counterparts by scission of the C(1)-N(2) bond.» Chem. Pharm. Bull. (Tokyo). 2003 Dec, 51(12): 1368-73.
Настоящее изобретение относится к области химии гетероциклических соединений, обладающих потенциальной биологической активностью, аналогов природных алкалоидов гарманового ряда (елеагнина), в частности к способу получения 1-замещенных-4-фенил-2,3,4,9-тетрагидро-1 Н-бетта-карболинов. Гармановые алкалоиды – важные элементы лекарственных растений: Passiflora fluidum, Passiflora edulis, Passiflora incarnata, Bansteriopsis caapi и Perganum harmala, в традиционной медицине они применяются для лечения астмы, желтухи, радикулита и других человеческих болезней. Гармалин – известный ингибитор МАО, мощный серотониновый антагонист. Гармановые алкалоиды были обнаружены в растительной пище: сое, ржи, пшенице, рисе, ячмене, грибах, в напитках: хорошо приготовленном виноградном соке, вине, пиве, виски, бренди, обугленных насекомых, сигаретном дыме и дыме марихуаны. Имеются данные, что алкоголь повышает содержание гармана в мозге и моче. Был исследован метаболизм гармалина. на крысах было показано, что он легко проникает с кровью в мозг животного и действует непосредственно на центральную нервную систему. Основным продуктом метаболизма гармалина является дезметилированный  -карболиновый алкалоид – гармалол. Также было показано цитотоксическое действие гармановых алкалоидов. Сообщается также о действии гармановых алкалоидов на сердечно-сосудистую систему, гипотензивном и цитотоксическом эффектах. [Д.А. Муравьева. Фармакогнозия, Москва: Медицина, 1981, 369 с.] -карболиновый алкалоид – гармалол. Также было показано цитотоксическое действие гармановых алкалоидов. Сообщается также о действии гармановых алкалоидов на сердечно-сосудистую систему, гипотензивном и цитотоксическом эффектах. [Д.А. Муравьева. Фармакогнозия, Москва: Медицина, 1981, 369 с.]
К группе гармановых алкалоидов относится также Елеагнин (1R)-1-метил-2,3,4,9-тетрагидро-1H- -карболин). -карболин).
Наиболее близким является способ получения 3,5-диметил-2,3,4,9-тетрагидро-1H-бетта-карболина внутримолекулярной циклизацией индопана с ацетальдегидом в присутствии серной кислоты [Синтезы гетероциклических соединений. Выпуск 6, стр 46, Ереван, 1964].
Недостатком способа, принятого за прототип, является невозможность синтеза 1-замещенных-4-фенил-2,3,4,9-тетрагидро-1H-бетта-карболинов.
Задачей изобретения является обеспечение возможности синтеза 1-замещенных 4-фенил-2,3,4,9-тетрагидро-1Н-бетта-карболинов.
Поставленная задача решается способом получения 1- и 1,1-замещенных-4-фенил-2,3,4,9-тетрагидро-1H-бетта-карболинов 3 путем циклизации алифатических или ароматических альдегидов или изатинов 2 в присутствии кислот или катализаторов Льюиса с бетта-фенилтриптамином 1:
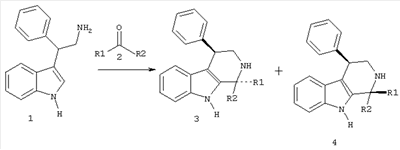
где R1-Н, СН3; R1=Ar, Het
Соединения 3, 4 представляли собой смесь двух диастереомеров с преобладанием R*R* диастереомера (a de 44%, b de 70%, с de 62%, d de63%, e de 62%, f de 56%, h de 66%, i de 88%, j de 72%, k de72%, l de 66%).
Пример по прототипу 1.
1-Метил-1,2,3,4-тетрагидро-2-карболин.
Раствор 5 г триптамина в 100 мл воды и 16 мл 2 н. раствора серной кислоты добавляют к 100 мл 10%-ного раствора ацетальдегида. Смесь постепенно нагревают на масляной бане до 110°, а затем выдерживают при этой температуре в течение 20 мин. По охлаждении к смеси добавляют избыток раствора соды. Выпавший осадок растворяют в разбавленной соляной кислоте; раствор фильтруют и обрабатывают едким натром. В результате снова выделяется осадок, который экстрагируют эфиром. Затем растворитель испаряют и получают 5,0 г (86%) кристаллического карболина. После перекристаллизации вещества из 50%-ного этилового спирта его т.пл. 179-180°. (Органические реакции. Сборник 6. Москва: Иностранная литература, 1953, стр.199.)
Пример 2 по прототипу
Смесь 8,7 г (0,05 моль)  -метилтриптамина, 375 мл 5% водного раствора ацетальдегида и 32 мл 2 н. серной кислоты кипятят с обратным холодильником в течение 2 часов. После охлаждения смесь подщелачивают 10% водным раствором карбоната калия (35 – 40 мл). Выделившиеся кристаллы отсасывают, растворяют в 50 мл 10%-ной соляной кислоты, прибавляют 1 г животного угля и фильтруют. Светло-желтого цвета фильтрат подщелачивают 10% водным раствором карбоната калия. Щелочной раствор с выделившимися кристаллами трижды обрабатывают эфиром (по 80 мл). Эфирный раствор сушат едким кали и после удаления большой части эфира (до 20 мл оставшегося объема) выделившийся диметилтетрагидроноргарман отфильтровывают и высушивают в эксикаторе над едким кали (примечание). Получают 8,2-9,0 г, или 82,5-90,6% теоретического количества белого кристаллического вещества с т.пл. 180-182°С. [Синтезы гетероциклических соединений, Выпуск 6, стр 46, Ереван, 1964.] Соотношение диастереомеров (de) было установлено на основании сравнения интегральных интенсивностей метиленовых протонов полученных соединений в спектрах ЯМР 1Н. Строение полученных соединений было исследовано при помощи одно- и двумерной спектроскопии ЯМР. В одномерных спектрах ЯМР 1Н и 13С наблюдались два набора сигналов с разной интенсивностью, соответствующие двум диастереомерам. Сигналы были отнесены путем анализа двумерных спектров COSY, TOCSY, HSQC и НМВС. Пространственное строение каждого диастереомера было выявлено при помощи двумерной спектроскопии Н-Н NOE (NOESY), которая позволила выявить близко расположенные протоны. Хим. сдвиги соединений 3 и 4, ЯМР 1Н и 13С приведены в таблицах 1-4 -метилтриптамина, 375 мл 5% водного раствора ацетальдегида и 32 мл 2 н. серной кислоты кипятят с обратным холодильником в течение 2 часов. После охлаждения смесь подщелачивают 10% водным раствором карбоната калия (35 – 40 мл). Выделившиеся кристаллы отсасывают, растворяют в 50 мл 10%-ной соляной кислоты, прибавляют 1 г животного угля и фильтруют. Светло-желтого цвета фильтрат подщелачивают 10% водным раствором карбоната калия. Щелочной раствор с выделившимися кристаллами трижды обрабатывают эфиром (по 80 мл). Эфирный раствор сушат едким кали и после удаления большой части эфира (до 20 мл оставшегося объема) выделившийся диметилтетрагидроноргарман отфильтровывают и высушивают в эксикаторе над едким кали (примечание). Получают 8,2-9,0 г, или 82,5-90,6% теоретического количества белого кристаллического вещества с т.пл. 180-182°С. [Синтезы гетероциклических соединений, Выпуск 6, стр 46, Ереван, 1964.] Соотношение диастереомеров (de) было установлено на основании сравнения интегральных интенсивностей метиленовых протонов полученных соединений в спектрах ЯМР 1Н. Строение полученных соединений было исследовано при помощи одно- и двумерной спектроскопии ЯМР. В одномерных спектрах ЯМР 1Н и 13С наблюдались два набора сигналов с разной интенсивностью, соответствующие двум диастереомерам. Сигналы были отнесены путем анализа двумерных спектров COSY, TOCSY, HSQC и НМВС. Пространственное строение каждого диастереомера было выявлено при помощи двумерной спектроскопии Н-Н NOE (NOESY), которая позволила выявить близко расположенные протоны. Хим. сдвиги соединений 3 и 4, ЯМР 1Н и 13С приведены в таблицах 1-4
Способ получения 3 и 4.
Пример 3.
Общая методика получения соединений 3 и 4:
К смеси 1 г (0,005 моль)  -фенилтриптамина в 40 мл воды и 0,72 гр (0,0043 моль) альдегида или изатина добавляют 1 г конц. H2SO4. Кипятят 60 часов, осадок сульфатов 3 и 4 отфильтровывают. Кристаллизуют из водного спирта. Основание получают взмучиванием сульфатов с избытком водного поташа. -фенилтриптамина в 40 мл воды и 0,72 гр (0,0043 моль) альдегида или изатина добавляют 1 г конц. H2SO4. Кипятят 60 часов, осадок сульфатов 3 и 4 отфильтровывают. Кристаллизуют из водного спирта. Основание получают взмучиванием сульфатов с избытком водного поташа.
Пример 4.
По приведенной методике получены:
На основе ацетальдегида и 1-сульфаты 1-метил-4-фенил-2,3,4,9-тетрагидро- -карболина (3а и 4а) -карболина (3а и 4а)
Выход 50%, т.пл. 218°С (сульфата), m/z (IOTH, %): 262 (М+, 10).
Пример 5.
На основе бензальдегида и 1-сульфаты 1,4-дифенил-2,3,4,9-тетрагидро- -карболина (3b и 4b) -карболина (3b и 4b)
Выход 60%, т.пл. 228°С (сульфата), m/z (IOTH, %): 324 (М+, 14).
Пример 6.
На основе p-Cl-бензальдегида и 1-сульфаты 4-фенил-1-(4-хлорфенил)-2,3,4,9-тетрагидро- -карболина (3с и 4с) -карболина (3с и 4с)
Выход 63%, т.пл. 255°С (сульфата) m/z (IOTH, %); 358 (М+, 14).
Пример 7.
На основе р-СН3О-бензальдегида и 1-сульфаты 1-(4-метоксифенил)-4-фенил-2,3,4,9-тетрагидро- -карболина (3d и 4d) -карболина (3d и 4d)
Выход 55%, т.пл. 225°С (сульфата) m/z (IOTH, %): 354 (М+, 20).
Пример 8.
На основе р-NO2-бензальдегида и 1-сульфаты 1-(4-нитрофенил)-4-фенил-2,3,4,9-тетрагидро- -карболина (3е и 4е) -карболина (3е и 4е)
Выход 80%, т.пл. >260°С (сульфата) m/z (IOTH, %): 369 (М+, 30).
Пример 9.
На основе m-NO2-бензальдегида и 1-сульфаты 1-(3-нитрофенил)-4-фенил-2,3,4,9-тетрагидро- -карболина (3f и 4f) -карболина (3f и 4f)
Выход 76%, т.пл. >260°С (сульфата) m/z (IOTH, %): 369 (М+, 27).
Пример 10.
На основе этил 4-формил-1/7-пиразол-3(5)-карбоксилата и 1-сульфаты этил 4-(4-фенил-2,3,4,9-тетрагидро-1H- -карболин-1-ил)-1H-пиразол-3(5)-карбоксилата (3h и 4h) -карболин-1-ил)-1H-пиразол-3(5)-карбоксилата (3h и 4h)
Выход 87%, т.пл. 255°С (сульфата), m/z (IOTH, %): 386 (М+, 10).
Пример 11.
На основе 1H-индол-2,3-диона и 1-сульфаты 4-фенил-2,3,4,9-тетрагидроспиро[ -карболин-1,3′-индол]-2′(1’H)-она (3i и 4i). -карболин-1,3′-индол]-2′(1’H)-она (3i и 4i).
Выход 46%, Т.пл. >300°С. Масс-спектр (ЭУ, 70 эВ), m/z (IOTH (%)): 365 (M+,10).
Пример 12.
На основе 5-бром-1H-индол-2,3-диона и 1-сульфаты 5′-бром-4-фенил-2,3,4,9-тетрагидроспиро[ -карболин-1,3′-индол]-2′(1’H)-она 3j и 4j. -карболин-1,3′-индол]-2′(1’H)-она 3j и 4j.
Выход 60%, Т. пл. 263°С(с разл.). Масс-спектр (ЭУ, 70 эВ), m/z (IOTH (%)): 444 (М+, 15).
5,7-Дибром-1H-индол-2,3-дион.
К смеси 30 г изатина, 80 мл концентрированной серной кислоты добавляют 40 г брома при температуре ниже 0°С и интенсивном перемешивании, выдерживают при 1 час при этой температуре. Оставляют на ночь, дав температуре подняться до комнатной. К полученной смеси добавляют 300 мл ледяной уксусной кислоты и 40 г брома. Кипятят до исчезновения брома. Выливают на лед и затем фильтруют. Суспендируют с водным раствором поташа и промывают водой до нейтральной реакции фильтрата. Получают 59 гр. Выход 95%. Т. пл. – 253°С.
Пример 13.
На основе 5,7-дибром-1H-индол-2,3-диона и 1-сульфаты 5′,7′-дибром-4-фенил-2,3,4,9-тетрагидроспиро[ -карболин-1,3′-индол](1’H)-она (3k и 4k). -карболин-1,3′-индол](1’H)-она (3k и 4k).
Выход 76%, Т. пл. >300°С. Масс-спектр (ЭУ, 70 эВ), m/z (IOTH (%)): 523 (М+, 15).
Пример 14.
На основе 5-нитро-1H-индол-2,3-диона и 1-сульфаты 5′-нитро-4-фенил-2,3,4,9-тетрагидроспиро[ -карболин-1,3′-индол]-2′(1’H)-она (3l и 4l). -карболин-1,3′-индол]-2′(1’H)-она (3l и 4l).
Выход 39%, Т. пл. 246°С. Масс-спектр (ЭУ, 70 эВ), m/z (IOTH (%)): 410 (М+, 15).
| Таблица 1. |
| Химические сдвиги ЯМР 1Н, м.д. соединений 3а-f и 4a-f. |
| Соединение |
3а (1R*, 4R*) |
4а (1S*, 4R*) |
3b (1R*, 4R*) |
4b (1S*, 4R*) |
3с (1R*, 4R*) |
4с (1S*, 4R*) |
3d (1R*, 4R*) |
4d (1S*, 4R*) |
3е (1R*, 4R*) |
4е (1S*, 4R*) |
3f (1R*, 4R*) |
4f (1S*, 4R*) |
| Протоны |
| 1-Н |
4.91 |
4.75 |
5.89 |
5.76 |
5.75 |
5.58 |
5.76 |
5.60 |
5.89 |
5.70 |
5.92 |
5.75 |
| 2-Н |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
| 3-Н |
3.79 |
3.56 |
3.67 |
3.41 |
3.59 |
3.37 |
3.60 |
3.39 |
3.60 |
3.40 |
3.65 |
3.40 |
| |
3.20 |
3.22 |
3.38 |
2.85 |
3.16 |
2.82 |
3.19 |
2.89 |
3.17 |
2.81 |
3.20 |
2.82 |
| 4-Н |
4.55 |
4.41 |
4.60 |
4.46 |
4.51 |
4.36 |
4.61 |
4.42 |
4.51 |
4.37 |
4.56 |
4.39 |
| 7-Н |
6.53 |
6.58 |
6.58 |
6.69 |
6.59 |
6.69 |
6.59 |
6.72 |
6.64 |
а |
6.61 |
а |
| 8-Н |
6.76 |
6.78 |
6.74 |
6.80 |
6.74 |
6.79 |
6.74 |
6.80 |
6.78 |
а |
6.76 |
а |
| 9-Н |
7.04 |
7.08 |
6.99 |
7.03 |
6.98 |
7.01 |
6.97 |
7.00 |
6.99 |
а |
6.99 |
а |
| 10-Н |
7.40 |
7.40 |
7.27 |
7.32 |
7.25 |
7.30 |
7.31 |
7.36 |
7.26 |
а |
7.25 |
а |
| 11-Н |
11.33 |
11.29 |
10.76 |
11.02 |
10.71 |
10.94 |
10.67 |
10.94 |
10.74 |
10.99 |
10.77 |
11.02 |
| 14-Н |
7.28 |
7.31 |
7.29 |
7.35 |
7.30 |
7.32 |
7.30 |
7.30 |
7.31 |
а |
7.29 |
а |
| 15-Н |
7.35 |
7.35 |
7.35 |
а |
7.32 |
7.32 |
7.30 |
7.30 |
7.33 |
а |
7.33 |
а |
| 16-Н |
7.35 |
7.35 |
7.31 |
а |
7.32 |
7.32 |
7.26 |
7.26 |
7.37 |
а |
7.29 |
а |
| 17-Н |
1.61 |
1.64 |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
| 18-Н |
– |
– |
7.43 |
7.44 |
7.45 |
7.45 |
7.38 |
7.30 |
7.68 |
8.06 |
8.30 |
а |
| 19-Н |
– |
– |
7.49 |
а |
7.56 |
7.51 |
7.00 |
7.02 |
8.30 |
8.39 |
– |
– |
| 20-Н |
– |
– |
7.44 |
а |
– |
– |
– |
– |
– |
– |
8.31 |
а |
| 21-Н |
– |
– |
– |
– |
– |
– |
3.78 |
3.76 |
– |
– |
– |
– |
| а – сигнал не отнесен |
| Таблица 2. |
| Химические сдвиги ЯМР 13С, м.д. соединений 3а-f и 4а-f. |
| Соединение |
3а (1R*, 4R*) |
4а (1S*, 4R*) |
3b (1R*, 4R*) |
4b (1S*, 4R*) |
3с (1R*, 4R*) |
4с (1S*, 4R*) |
3d (1R*, 4R*) |
4d (1S*, 4R*) |
3е (1R*, 4R*) |
4е (1S*, 4R*) |
3f (1R*, 4R*) |
4f (1S*, 4R*) |
| Атомы углерода |
| C(1) |
49.0 |
47.3 |
56.9 |
54.6 |
55.9 |
54.0 |
56.5 |
54.6 |
56.0 |
а |
56.0 |
А |
| С(3) |
48.5 |
44.9 |
49.7 |
46.2 |
50.6 |
47.3 |
50.3 |
47.1 |
49.9 |
а |
50.1 |
А |
| С(4) |
37.4 |
36.8 |
38.4 |
38.2 |
39.6 |
39.6 |
38.8 |
38.9 |
38.7 |
а |
39.2 |
А |
| С(5) |
108.2 |
107.3 |
110.4 |
110.3 |
110.6 |
109.2 |
110.5 |
110.4 |
110.6 |
а |
110.7 |
а |
| С(6) |
125.0 |
125.0 |
125.2 |
а |
125.7 |
126.2 |
125.6 |
125.8 |
125.3 |
а |
125.4 |
а |
| С(7) |
118.8 |
118.8 |
118.9 |
118.8 |
118.7 |
118.5 |
118.9 |
118.7 |
118.8 |
а |
118.8 |
а |
| С(8) |
118.8 |
118.8 |
118.7 |
118.7 |
118.3 |
118.4 |
118.7 |
118.8 |
118.6 |
а |
118.6 |
а |
| С(9) |
121.4 |
121.5 |
121.3 |
121.3 |
120.8 |
120.8 |
121.3 |
121.4 |
121.2 |
а |
121.2 |
а |
| C(10) |
111.4 |
111.4 |
111.6 |
111.6 |
111.3 |
111.5 |
111.6 |
111.5 |
111.4 |
а |
111.4 |
а |
| С(11) |
136.4 |
136.3 |
136.6 |
136.5 |
136.3 |
136.4 |
136.7 |
136.6 |
136.5 |
а |
136.5 |
а |
| С(12) |
132.0 |
132.5 |
131.7 |
а |
134.1 |
133.7 |
133.0 |
133.4 |
132.0 |
а |
132.1 |
а |
| С(13) |
140.3 |
140.3 |
141.4 |
а |
142.8 |
141.5 |
142.0 |
142.7 |
141.9 |
а |
141.9 |
а |
| С(14) |
128.2 |
128.2 |
128.4 |
128.4 |
128.2 |
128.2 |
128.4 |
128.4 |
128.3 |
а |
128.3 |
а |
| С(15) |
128.3 |
128.3 |
128.4 |
а |
128.2 |
128.2 |
128.4 |
128.4 |
128.3 |
а |
128.3 |
а |
| С(16) |
127.3 |
127.2 |
127.1 |
а |
126.5 |
126.7 |
127.0 |
126.8 |
126.8 |
а |
126.8 |
а |
| С(17) |
16.7 |
17.9 |
А |
а |
139.1 |
а |
129.7 |
129.7 |
145.6 |
а |
139.9 |
А |
| С(18) |
– |
– |
129.6 |
а |
131.1 |
129.3 |
130.7 |
130.5 |
130.7 |
а |
123.9 |
А |
| С(19) |
– |
– |
129.3 |
а |
128.3 |
128.3 |
114.2 |
114.1 |
123.6 |
а |
147.8 |
А |
| С(20) |
– |
– |
129.3 |
а |
а |
а |
159.8 |
159.5 |
147.7 |
а |
123.6 |
А |
| С(21) |
– |
– |
– |
– |
– |
– |
55.4 |
55.8 |
– |
– |
– |
– |
| а – сигнал не отнесен |
| Таблица 3. |
| Химические сдвиги ЯМР 1Н, м.д. соединений 3h-l и 4h-l |
| Соединение |
3h (1R*, 4R*) |
4h (1S*, 4R*) |
3i (1R*, 4R*) |
4i (1S*, 4R*) |
3j (1R*, 4R*) |
4j (1S*, 4R*) |
3k (1R*, 4R*) |
4k (1S*, 4R*) |
3l (1R*, 4R*) |
4l (1S*, 4R*) |
| Протоны |
| 1 |
5.78 |
5.70 |
– |
– |
– |
– |
– |
– |
– |
– |
| 3 |
3.41
2.80 |
3.22
2.78 |
3.79
4.13 |
3.44
3.98 |
3.97
3.88 |
3.16
3.63 |
3.37
3.63 |
3.03
4.02 |
3.41
3.71 |
3.06
4.03 |
| 4 |
4.24 |
4.19 |
4.80 |
4.68 |
4.57 |
4.40 |
4.37 |
4.29 |
4.45 |
4.34 |
| 7 |
6.70 |
6.61 |
6.58 |
6.70 |
6.59 |
6.83 |
6.62 |
6.93 |
6.60 |
6.95 |
| 8 |
6.75 |
6.79 |
6.77 |
6.82 |
6.76 |
6.83 |
6.73 |
6.82 |
6.75 |
6.85 |
| 9 |
6.94 |
7.01 |
7.03 |
7.08 |
7.01 |
7.04 |
6.97 |
7.03 |
6.98 |
7.03 |
| 10 |
7.28 |
7.35 |
7.25 |
7.28 |
7.23 |
7.23 |
7.20 |
7.21 |
7.18 |
7.20 |
| 11 |
10.51 |
10.78 |
10.97 |
11.08 |
10.88 |
10.91 |
10,76 |
10.81 |
10.76 |
10.81 |
| 14 |
7.28 |
7.28 |
7.41 |
7.40 |
7.38 |
7.38 |
7.33 |
7.33 |
7.35 |
7.35 |
| 15 |
7.28 |
7.28 |
7.40 |
7.40 |
7.38 |
7.38 |
7.32 |
7.32 |
7.35 |
7.35 |
| 16 |
7.21 |
7.20 |
7.33 |
7.34 |
7.31 |
7.31 |
7.25 |
7.25 |
7.28 |
7.26 |
| 17 |
7.51 |
7.47 |
11.31 |
11.28 |
11.14 |
11.02 |
11.08 |
10.99 |
11.41 |
11.25 |
| 19 |
– |
– |
7.45 |
7.43 |
7.47 |
7.36 |
7.33 |
7.28 |
8.06 |
7.91 |
| 20 |
– |
– |
7.13 |
7.15 |
– |
– |
– |
– |
– |
– |
| 21 |
4.34 |
4.28 |
7.52 |
7.46 |
7.62 |
7.54 |
7.75 |
7.73 |
8.33 |
8.29 |
| 22 |
1.30 |
1.32 |
7.16 |
7.20 |
7.04 |
6.98 |
– |
– |
7.21 |
7.18 |
| Таблица 4. |
| Химические сдвиги ЯМР 13С, м.д. соединений 3h-l и 4h-l. |
| Соединение |
3h (1R*, 4R*) |
4h (1S*, 4R*) |
3i (1R*, 4R*) |
4i (1S*, 4R*) |
3j (1R*, 4R*) |
4i (1S*, 4R*) |
3k (1R*, 4R*) |
4k (1S*, 4R*) |
3l (1R*, 4R*) |
4l (1S*, 4R*) |
| Атомы углерода |
| C(1) |
47.8 |
46.1 |
59.7 |
60.3 |
60.2 |
61.3 |
61.9 |
62.2 |
60.4 |
60.9 |
| C(3) |
49.7 |
45.0 |
45.2 |
46.8 |
46.2 |
47.3 |
47.8 |
47.4 |
47.5 |
47.5 |
| С(4) |
38.7 |
38.6 |
37.1 |
37.2 |
38.3 |
38.3 |
39.8 |
38.5 |
39.4 |
38.1 |
| С(5) |
108.9 |
108.5 |
112.0 |
111.9* |
112.5 |
112.0 |
113.9 |
113.8 |
113.3 |
112.4 |
| С(6) |
125.3 |
125.2 |
125.0 |
125.1* |
125.2 |
125.5 |
125.6 |
125.5 |
125.5 |
125.8 |
| С(7) |
118.4 |
118.6 |
119.2 |
119.1 |
119.1 |
118.8 |
119.0 |
118.6 |
119.0 |
118.6 |
| С(8) |
118.0 |
118.3 |
119.0 |
119.0 |
118.9 |
118.8 |
118.5 |
118.5 |
118.5 |
118.5 |
| С(9) |
120.2 |
120.6 |
122.2 |
122.2 |
121.9 |
121.7 |
121.4 |
121.5 |
121.4 |
121.4 |
| C(10) |
111.2 |
111.4 |
111.7 |
111.7 |
111.6 |
111.5 |
111.4 |
111.4 |
111.3 |
111.3 |
| С(10а) |
136.9 |
136.5 |
136.8 |
136.8 |
136.6 |
136.6 |
136.4 |
136.4 |
136.4 |
136.4 |
| С(12) |
131.7 |
131.6 |
127.5 |
127.6* |
128.6 |
128.6 |
131.0 |
131.3 |
132.2 |
130.6 |
| С(13) |
144.4 |
140.9 |
140.7 |
140.3 |
141.9 |
141.7 |
143.1 |
144.3 |
142.8 |
144.2 |
| C(14) |
128.2 |
128.2 |
128.7 |
128.6 |
128.6 |
128.6 |
128.3 |
128.2 |
128.2 |
128.1 |
| С(15) |
128.1 |
128.2 |
128.5 |
128.5 |
128.4 |
128.4 |
128.2 |
128.2 |
128.2 |
128.2 |
| С(16) |
126.1 |
126.3 |
127.5 |
127.2 |
127.1 |
126.5 |
126.8 |
126.5 |
126.5 |
126.1 |
| С(17) |
133.5 |
133.4 |
– |
– |
– |
– |
– |
– |
– |
– |
| С(18) |
130.4 |
130.4 |
172.6 |
170.9* |
174.3 |
173.1* |
177.1 |
175.0 |
177.3 |
178.4 |
| С(18a) |
– |
– |
124.9 |
126.6* |
130.2 |
132.4* |
134.8 |
135.9* |
131.4 |
133.1 |
| С(19) |
111.3 |
111.1 |
126.2 |
125.7 |
128.3 |
128.3 |
126.2 |
126.1 |
120.6 |
119.8 |
| С(20) |
161.8 |
161.8 |
122.8 |
122.7 |
114.0 |
114.0 |
114.0 |
113.9 |
142.3 |
142.2 |
| С(21) |
60.2 |
60.2 |
131.7 |
131.2 |
133.6 |
132.7 |
134.1 |
133.9 |
126.9 |
126.5 |
| С(22) |
14.1 |
14.1 |
111.2 |
111.6 |
112.7 |
112.5 |
103.4 |
103.5 |
110.4 |
110.3 |
| С(23) |
– |
– |
143.1 |
142.7 |
142.3 |
142.0 |
141.8 |
141.8 |
149.3 |
149.3 |
Как видно из приведенных примеров, разработанный способ позволяет получать бетта-карболины самого разнообразного строения, содержащие алкильные, арильные и гетарильные заместители в 1 положении бетта-карболинового цикла при занятом 4 положением.
Характерной особенностью данного класса соединений является: усиление действия снотворных, проявление гипотензивного, антисеротонинового и сосудорасширяющего действия.
Формула изобретения
Способ получения соединений общей формулы
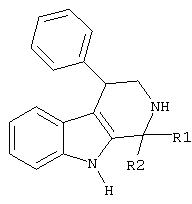
где один из R1 и R2 означает атом водорода, а другой представляет собой алкил с числом атомов углерода от одного до двух либо арил, гетарил, либо R1 и R2 вместе с атомом углерода, к которому они присоединены, образуют необязательно замещенный индол-3-он, путем циклизации альдегидов с замещенным триптамином в присутствии кислот, отличающийся тем, что в качестве замещенного триптамина используют бета-фенилтриптамин, в качестве альдегидов используют алифатические или ароматические альдегиды или необязательно замещенные изатины, в качестве кислот используют минеральные кислоты или катализаторы Льюиса.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Извещение опубликовано: 10.08.2009 БИ: 22/2009
|
|


 -карболиновый алкалоид – гармалол. Также было показано цитотоксическое действие гармановых алкалоидов. Сообщается также о действии гармановых алкалоидов на сердечно-сосудистую систему, гипотензивном и цитотоксическом эффектах. [Д.А. Муравьева. Фармакогнозия, Москва: Медицина, 1981, 369 с.]
-карболиновый алкалоид – гармалол. Также было показано цитотоксическое действие гармановых алкалоидов. Сообщается также о действии гармановых алкалоидов на сердечно-сосудистую систему, гипотензивном и цитотоксическом эффектах. [Д.А. Муравьева. Фармакогнозия, Москва: Медицина, 1981, 369 с.]
 -метилтриптамина, 375 мл 5% водного раствора ацетальдегида и 32 мл 2 н. серной кислоты кипятят с обратным холодильником в течение 2 часов. После охлаждения смесь подщелачивают 10% водным раствором карбоната калия (35 – 40 мл). Выделившиеся кристаллы отсасывают, растворяют в 50 мл 10%-ной соляной кислоты, прибавляют 1 г животного угля и фильтруют. Светло-желтого цвета фильтрат подщелачивают 10% водным раствором карбоната калия. Щелочной раствор с выделившимися кристаллами трижды обрабатывают эфиром (по 80 мл). Эфирный раствор сушат едким кали и после удаления большой части эфира (до 20 мл оставшегося объема) выделившийся диметилтетрагидроноргарман отфильтровывают и высушивают в эксикаторе над едким кали (примечание). Получают 8,2-9,0 г, или 82,5-90,6% теоретического количества белого кристаллического вещества с т.пл. 180-182°С. [Синтезы гетероциклических соединений, Выпуск 6, стр 46, Ереван, 1964.] Соотношение диастереомеров (de) было установлено на основании сравнения интегральных интенсивностей метиленовых протонов полученных соединений в спектрах ЯМР 1Н. Строение полученных соединений было исследовано при помощи одно- и двумерной спектроскопии ЯМР. В одномерных спектрах ЯМР 1Н и 13С наблюдались два набора сигналов с разной интенсивностью, соответствующие двум диастереомерам. Сигналы были отнесены путем анализа двумерных спектров COSY, TOCSY, HSQC и НМВС. Пространственное строение каждого диастереомера было выявлено при помощи двумерной спектроскопии Н-Н NOE (NOESY), которая позволила выявить близко расположенные протоны. Хим. сдвиги соединений 3 и 4, ЯМР 1Н и 13С приведены в таблицах 1-4
-метилтриптамина, 375 мл 5% водного раствора ацетальдегида и 32 мл 2 н. серной кислоты кипятят с обратным холодильником в течение 2 часов. После охлаждения смесь подщелачивают 10% водным раствором карбоната калия (35 – 40 мл). Выделившиеся кристаллы отсасывают, растворяют в 50 мл 10%-ной соляной кислоты, прибавляют 1 г животного угля и фильтруют. Светло-желтого цвета фильтрат подщелачивают 10% водным раствором карбоната калия. Щелочной раствор с выделившимися кристаллами трижды обрабатывают эфиром (по 80 мл). Эфирный раствор сушат едким кали и после удаления большой части эфира (до 20 мл оставшегося объема) выделившийся диметилтетрагидроноргарман отфильтровывают и высушивают в эксикаторе над едким кали (примечание). Получают 8,2-9,0 г, или 82,5-90,6% теоретического количества белого кристаллического вещества с т.пл. 180-182°С. [Синтезы гетероциклических соединений, Выпуск 6, стр 46, Ереван, 1964.] Соотношение диастереомеров (de) было установлено на основании сравнения интегральных интенсивностей метиленовых протонов полученных соединений в спектрах ЯМР 1Н. Строение полученных соединений было исследовано при помощи одно- и двумерной спектроскопии ЯМР. В одномерных спектрах ЯМР 1Н и 13С наблюдались два набора сигналов с разной интенсивностью, соответствующие двум диастереомерам. Сигналы были отнесены путем анализа двумерных спектров COSY, TOCSY, HSQC и НМВС. Пространственное строение каждого диастереомера было выявлено при помощи двумерной спектроскопии Н-Н NOE (NOESY), которая позволила выявить близко расположенные протоны. Хим. сдвиги соединений 3 и 4, ЯМР 1Н и 13С приведены в таблицах 1-4