|
|
(21), (22) Заявка: 2006133787/15, 22.09.2006
(24) Дата начала отсчета срока действия патента:
22.09.2006
(43) Дата публикации заявки: 27.03.2008
(46) Опубликовано: 10.08.2008
(56) Список документов, цитированных в отчете о
поиске:
MADORE D.V. et al. Interlaboratory study evaluating quantitation of antibodies to Haemophilus influenzae type b polysaccharide by enzyme-linked immunosorbent assay, Clin. Diagn. Lab. Immunol, 1996, Jan., 3(1), 84-88. MITCHELL J., HILL S.L. Immune response to Haemophilus parainfluenzae in patients with chronic obstructive lung disease. Clinical and
Адрес для переписки:
105064, Москва, М. Казенный пер., 5а, ГУ НИИВС им. И.И. Мечникова, директору В.В. Звереву
|
(72) Автор(ы):
Ястребова Наталия Евгеньевна (RU),
Ванеева Наталья Павловна (RU),
Маркина Ольга Анатольевна (RU),
Орлова Ольга Евгеньевна (RU),
Елкина Станислава Ивановна (RU),
Костинов Михаил Петрович (RU),
Апарин Петр Геннадьевич (RU),
Львов Вячеслав Леонидович (RU)
(73) Патентообладатель(и):
Научно-исследовательский институт вакцин и сывороток им. И.И. Мечникова (ГУ НИВС им. И.И. Мечникова) (RU)
|
(54) СПОСОБ ОПРЕДЕЛЕНИЯ АНТИТЕЛ К КАПСУЛЬНОМУ ПОЛИСАХАРИДУ Haemophilus influenzae ТИПА b
(57) Реферат:
Изобретение относится к области медицины, а именно к иммунологии, и касается способа определения антител к капсульному полисахариду Haemophilus influenzae типа b. Сущность изобретения заключается в том, что на твердый носитель с сорбированным на нем высокоочищенным капсульным полисахаридом Haemophilus influenzae типа b наносят рабочие разведения исследуемой и контрольной сывороток, а также калибровочные пробы, представляющие собой сыворотки с относительным содержанием IgG антител к капсульному полисахариду – полирибозилрибитолфосфату Haemophilus influenzae, инкубируют, удаляют избыток антител, вносят конъюгат в рабочем разведении, повторно инкубируют при тех же параметрах, отмывают от избытка конъюгата, вносят субстратную смесь, содержащую тетраметилбензидин и перекись водорода в заданных значениях, инкубируют в защищенном от света месте, останавливают реакцию введением реагента, измеряют оптическую плотность исследуемой и контрольной сывороток на содержание антител, строят график зависимости оптической плотности от условного количества антител в калибровочных пробах и по графику зависимости определяют количество антител в условных единицах в исследуемых пробах. Преимущество изобретения заключается в повышении чувствительности способа. 2 табл., 1 ил.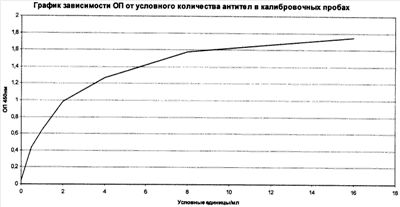
(56) (продолжение):
CLASS=”b560m”Diagnostic Laboratory Immunol., 2000, Jan. 7(1), 25-30. RU 2257412 C1, 27.07.2005. US 6177085 A, 23.01.2001.
Изобретение относится к области медицины, а именно к иммунологии, и может быть использовано для оценки поствакцинального иммунитета при вакцинации существующими (АКТ-ХИБ) и разрабатываемыми форсифицированными вакцинами.
Haemophilus influenzae типа b (Hib) является наиболее частой причиной бактериальных менингитов, поражающих детей до 6-летнего возраста, особенно детей от 3 до 12 месяцев. При инфицировании этим видом бактерий у человека формируется иммунный ответ к трем основным антигенам: капсульному полисахариду, белкам наружной мембраны и липоолигосахаридам. Капсульный полисахарид – полирибозилрибитолфосфат (ПРФ) – является основой современных вакцинных препаратов. Для формирования Т-клеточного иммунитета его конъюгируют с различными бактериальными белками, такими как столбнячный и дифтерийный анатоксины и др. Для профилактики заболеваний, вызываемых Hib, за рубежом созданы вакцинирующие препараты. Одна из таких вакцин «АКТ-ХИБ» (Авентис Пастер, Франция), представляющая собой конъюгат ПРФ со столбнячным анатоксином, сертифицирована и разрешена к применению на территории России. Доказана ее высокая эффективность и безопасность. Разрабатываются подобные вакцины и в нашей стране. Для оценки эффективности разрабатываемых отечественных форсифицированных вакцин необходимы тесты, регистрирующие уровень поствакцинального иммунитета.
Известен способ выявления антител к олигосахариду капсульного полисахарида Hib с помощью ИФА. В качестве иммуносорбента используют 96-луночный полистироловый планшет, на котором сорбирован олигосахарид, конъюгированный с альбумином человека [Clin. And Diagn. Labor. Immunol., 1996, Jan., p.84-88]. Анализируемые образцы сывороток титруют с 1:50 в фосфатно-солевом буфере с добавлением твина и ЭДТА. После инкубации и отмывания вносят моноклональный конъюгат. Полученное соединение антиген-антитело-конъюгат проявляют субстратной смесью с последующей детекцией на спектрофотометре. Для калибровочной кривой используют аффинноочищенные антитела.
Однако при использовании иммуносорбента, содержащего альбумин человека, есть вероятность определения аутоантител к нему в анализируемых пробах.
Технический результат заявленного способа заключается в повышении эффективности определения антител к капсульному полисахариду H.influenzae за счет использования высокоочищенного полисахарида, не требующего конъюгации, а также за счет использования поликлонального конъюгата, представляющего собой кроличьи антитела против иммуноглобулинов G (H+L) человека, меченные пероксидазой, и калибровочных проб, представляющих собой сыворотки с относительным содержанием IgG антител к ПРФ Hib.
Для достижения указанного технического результата способ определения антител к капсульному полисахариду Haemophilus influenzae типа b заключается в том, что на твердый носитель с сорбированным на нем высокоочищенным капсульным полисахаридом Haemophilus influenzae типа b наносят рабочие разведения исследуемой и контрольной сывороток, а также калибровочные пробы, представляющие собой сыворотки с относительным содержанием IgG антител к капсульному полисахариду – полирибозилрибитолфосфату Haemophilus influenzae: 16; 8; 4; 2; 1; 0,5; 0,25 и 0 усл. Ед./мл, инкубируют при температуре 18-22°С в течение 30 минут, удаляют избыток антител, вносят конъюгат в рабочем разведении, повторно инкубируют при тех же параметрах, отмывают от избытка конъюгата, вносят субстратную смесь, содержащую тетраметилбензидин и перекись водорода в заданных значениях, инкубируют при температуре 18-22°С в течение 15-20 минут в защищенном от света месте, останавливают реакцию введением реагента, измеряют оптическую плотность исследуемой и контрольной сывороток на содержание антител, строят график зависимости оптической плотности от условного количества антител в калибровочных пробах и по графику зависимости определяют количество антител в условных единицах в исследуемых пробах.
Наличие гуморального иммунитета может быть оценено с помощью твердофазного иммуноферментного анализа (ИФА). В основе метода лежит иммуносорбент, представляющий собой стрипированный 96-луночный планшет, сорбированный высокоочищенным капсульным полисахаридом Hib, принадлежность которого к ПРФ доказана с помощью ядерно-магнитно-резонансной спектроскопии и химического анализа, а специфическая активность – в различных серологических тестах.
При выполнении анализа образцы сывороток и калибровочные пробы вносят в лунки иммуносорбента в рабочем разведении. После инкубации и отмывки во все лунки иммуносорбента вносят конъюгат в рабочем разведении. Проявка реакции осуществляется субстратной смесью, содержащей тетраметилбензидин (ТМБ) и перекись водорода.
Калибровочные пробы – сыворотки с относительным содержанием IgG антител к ПРФ Hib: 16; 8; 4; 2; 1; 0,5; 0,25 и 0 усл. ед./мл. На их основе строится график зависимости оптической плотности от условного количества антител в калибровочных пробах (см. чертеж).
По калибровочному графику определяют относительное количество IgG антител к ПРФ Hib в анализируемых сыворотках крови человека.
Используемые реагенты:
(1) иммуносорбент – планшет полистирольный разборный, состоящий из 128-луночных стрипов, сорбированных капсульным полисахаридом Hib, – 1 шт.;
(2) калибровочные пробы (8) – сыворотки с относительным содержанием IgG антител к ПРФ Hib: 16; 8; 4; 2; 1; 0,5; 0,25 и 0 усл. ед./мл. Каждая проба содержит 0,2 мл раствора, во флаконе;
(3) отрицательный контроль (К-) – сыворотка крови человека, содержащая <0,5 усл. ед./мл, жидкая – 1 фл., 0,1 мл;
(4) положительный контроль (К+) – сыворотка крови человека, содержащая >2,0 усл. ед./мл, жидкая – 1 фл., 0,1 мл;
(5) конъюгат (КГ) – антитела кроличьи против IgG (H+L) человека, меченные пероксидазой, жидкий, концентрированный – 1 фл., 0,2 мл;
(6) субстратная смесь, содержащая тетраметилбензидин (ТМБ) – 1 фл., 12 мл;
(7) промывающий и разводящий фосфатно-солевой буферный раствор, десятикратный концентрат с детергентом (ФСБ-Д)к – 1 фл., 50 мл;
(8) стоп-реагент – 0,9 М H2SO4.
Приготовление растворов для проведения анализа:
1) (ФСБ-Д)к перед применением разводят дистиллированной водой в 10 раз. Полученный раствор ФСБ-Д хранят не более 3 недель при 4-8°С. Раствор предназначен для отмывки планшета от непрореагировавших компонентов, разведения сывороток и конъюгата;
2) контроли (К+ и К-), а также анализируемые сыворотки перед проведением анализа разводят раствором ФСБ-Д до соотношения 1:100 (10 мкл на 1000 мкл ФСБ-Д.) Рабочее разведение сывороток хранению не подлежит;
3) рабочее разведение конъюгата готовят непосредственно перед использованием, разводя исходный раствор до соотношения 1:200 ФСБ-Д (50 мкл на 10 мл ФСБ-Д).
Последовательность операций
Отмывка иммуносорбента. Во все лунки планшета вносят ФСБ-Д в объеме не менее 0,2 мл. Выдерживают планшет при комнатной температуре в течение 2-3 мин. Содержимое лунок удаляют вытряхиванием. Отмывку повторяют еще 3 раза.
Внесение образцов. В лунки первого ряда планшета последовательно вносят калибровочные пробы №№1-8. Далее последовательно вносят рабочие растворы (1:100) контролей (К+ и К-) в дублях и анализируемые сыворотки. Объем вносимых проб – 100 мкл.
Инкубация. Выдерживают планшет с растворами сывороток в течение 30 мин при 18-22°С.
Отмывка от избытка антител. Жидкость из лунок планшета удаляют вытряхиванием и трехкратно отмывают раствором ФСБ-Д, как указано в п.1.
Внесение рабочего раствора конъюгата. Во все лунки планшета вносят по 100 мкл рабочего раствора КГ.
Инкубация. Как в п.3.
Отмывка от избытка КГ. Как в п.1.
Внесение субстратного раствора ТМБ. Во все лунки вносят по 100 мкл раствора ТМБ.
Инкубация. 15-20 мин в темноте при температуре 18-22°С.
В каждую лунку вносят по 50 мкл стоп-реагента.
Учет результатов
Вывести спектрофотометр на нулевой уровень («blank») по воздуху.
Измерить оптическую плотность в лунках планшета при 450 нм в течение 10 минут после остановки реакции.
Построить график зависимости оптической плотности от условного количества антител в калибровочных пробах.
По калибровочному графику определить относительное количество IgG антител к ПРФ Hib в анализируемых пробах.
Пример исследования сывороток детей в возрасте до 3 лет, подвергшихся иммунизации вакциной «АКТ-ХИБ» (Авентис Пастер, Франция), на наличие антител к капсульному полисахариду Hib
| №№ п/п |
ОП 450 нм |
Усл. ед./мл |
| до иммунизации |
через месяц после иммунизации |
до иммунизации |
через месяц после иммунизации |
| 1 |
0,76 |
0,65 |
1,3 |
1,04° |
| 2 |
0,83 |
0,94 |
1,6 |
1,9* |
| 3 |
1,02 |
0,55 |
2,3 |
0,8° |
| 4 |
0,71 |
1,36 |
1,2 |
5,2** |
| 5 |
0,61 |
0,36 |
0,9 |
0,4° |
| 6 |
0,55 |
0,56 |
0,8 |
0,8– |
| 7 |
0,94 |
0,99 |
1,9 |
2,0* |
| 8 |
0,93 |
1,05 |
1,8 |
2,4* |
| 9 |
0,27 |
0,70 |
0,3 |
1,2** |
| 10 |
0,70 |
1,25 |
1,2 |
3,9* |
| 11 |
0,52 |
0,56 |
0,7 |
0,8* |
| 12 |
0,65 |
0,86 |
1,0 |
1,6* |
| 13 |
0,33 |
0,52 |
0,4 |
0,7* |
| 14 |
0,28 |
1,48 |
0,3 |
6,7** |
| 15 |
0,34 |
0,75 |
0,4 |
1,3* |
| 16 |
1,32 |
1,73 |
4,7 |
14,8** |
| 17 |
0,84 |
1,79 |
1,6 |
17,9** |
Из 17 детей у 13 (*) уровень IgG AT после вакцинации вырос (из них – в 4 и более раз – только у 5 человек (**)). У 3 детей произошло понижение уровня AT после вакцинации (°), а у одного уровень AT не изменился (-).
Пример определения антител капсульному полисахариду в сыворотках вакцинированных детей с помощью набора «Fuller Laboratories» и предложенного способа.
| №№ сыворотки |
Набор «Fuller» |
Предложенный способ |
| до вакцинациим кг/мл |
после вакцинациим кг/мл |
до вакцинации усл.ед./мл |
после вакцинации усл.ед./мл |
| 1 |
0,7 |
21,1 |
1,58 |
1,87 |
| 2 |
0,5 |
22,4 |
1,2 |
5,17 |
| 3 |
0,5 |
21,9 |
0,27 |
1,09 |
| 4 |
0,4 |
21,8 |
1,17 |
3,87 |
| 5 |
0,4 |
22,6 |
0,28 |
6,68 |
| 6 |
0,2 |
11,4 |
0,38 |
1,32 |
| 7 |
1,7 |
22,2 |
4,71 |
14,75 |
| 8 |
1,6 |
22,4 |
1,6 |
17,88 |
Формула изобретения
Способ определения антител к капсульному полисахариду Haemophilus influenzae типа b, заключающийся в том, что на твердый носитель с сорбированным на нем высокоочищенным капсульным полисахаридом Haemophilus influenzae типа b наносят рабочие разведения исследуемой и контрольной сывороток, а также калибровочные пробы, представляющие собой сыворотки с относительным содержанием IgG антител к капсульному полисахариду – полирибозилрибитолфосфату Haemophilus influenzae: 16; 8; 4; 2; 1; 0,5; 0,25 и 0 условных единиц/мл, инкубируют при температуре 18-22°С в течение 30 мин, удаляют избыток антител, вносят конъюгат в рабочем разведении, повторно инкубируют при тех же параметрах, отмывают от избытка конъюгата, вносят субстратную смесь, содержащую тетраметилбензидин и перекись водорода в заданных значениях, инкубируют при температуре 18-22°С в течение 15-20 мин в защищенном от света месте, останавливают реакцию введением реагента, измеряют оптическую плотность исследуемой и контрольной сывороток на содержание антител, строят график зависимости оптической плотности от условного количества антител в калибровочных пробах и по графику зависимости определяют количество антител в условных единицах в исследуемых пробах.
РИСУНКИ
|
|