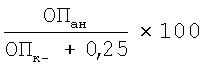Патент на изобретение №2331074
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ОПРЕДЕЛЕНИЯ НАЛИЧИЯ ПОСТВАКЦИНАЛЬНОГО ИММУНИТЕТА К АНТИГЕНАМ ВАКЦИНЫ “ПНЕВМО-23”
(57) Реферат:
Изобретение относится к области медицины, а именно к иммунологии, и может быть использовано для оценки поствакцинального иммунитета при вакцинации вакциной «Пневмо-23». Сущность изобретения заключается в том, что на твердый носитель с сорбированной вакциной «Пневмо-23», содержащей 23 полисахарида пневмококка, наносят рабочие разведения исследуемых и контрольной сывороток, инкубируют при температуре 18-22°С в течение 30 мин, удаляют избыток антител, вносят конъюгат в рабочем разведении, повторно инкубируют при тех же параметрах, отмывают от избытка конъюгата, вносят субстратную смесь, содержащую тетраметилбензидин и перекись водорода в заданных значениях, инкубируют при температуре 18-22°С в течение 15-20 мин в защищенном от света месте, останавливают реакцию введением реагента, измеряют оптическую плотность исследуемой и контрольной сывороток на содержание антител до вакцинации и после вакцинации и по увеличению оптической плотности в исследуемых сыворотках в 4 и более раза судят о наличии поствакцинального иммунитета. Преимущество изобретения заключается в повышении чувствительности способа. 1 табл.
(56) (продолжение): CLASS=”b560m”коллективе военнослужащих с высоким риском развития пневмоний. Сборник научно-практической конференции с международным участием “Вирусные инфекции на пороге XXI века: Эпидемиология и профилактика”. – СПб., 1999, с.223-227. КОСТИНОВ М.П. и др. Клинический и иммунологический эффекты вакцины “Пневмо-23” у детей с бронхиальной астмой. – Вакцинация, 2004, №2, с.25-27. BLACK S. et al. Efficacy and immunogenicity of heptavalent pneumococcal conjugate vaccine in children. – Pediatr. Infect. Dis. J., 2000, v. 19, p.187-195.
Изобретение относится к области медицины, а именно к иммунологии, и может быть использовано для оценки поствакцинального иммунитета при вакцинации вакциной «Пневмо-23» (Авентис Пастер, Франция), зарегистрированной в Российской Федерации. Streptococcus pneumoniae – широко распространенный возбудитель инфекционных заболеваний у человека. Самыми частыми клиническими формами пневмококковой инфекции у детей являются средний отит, пневмония и менингит. У взрослых – пневмония, сепсис, менингит. Пневмококк служит причиной 20% обострений хронического бронхита. Поскольку возбудитель распространяется преимущественно воздушно-капельным путем, основным способом борьбы с болезнями, вызываемыми пневмококком, является вакцинопрофилактика. Иммунитет у заболевших и привитых обеспечивается за счет образования антител к капсульным полисахаридам пневмококка. Отсюда – все вакцины для профилактики пневмококковых заболеваний основным компонентом имеют тот или иной полисахарид. «Пневмо-23» содержит полисахариды 23 серотипов пневмококка, которые составляют примерно 90% всех циркулирующих среди населения. Полисахаридные антигены капсулы вызывают иммунный ответ по Т-независимому механизму. Защитные типоспецифические антитела появляются при колонизации, инфекции и при вакцинации. Уровень антител, необходимый для защиты от пневмококковой инфекции, точно не установлен. Данные литературы свидетельствуют, что после вакцинации в течение 2-3 недель концентрация специфических антител возрастает в 2 и более раз (Musher D.M. et al., 1990). Известен способ выявления антител к капсульным полисахаридам S.pneumoniae с помощью ИФА, рекомендованный Всемирной Организацией Здравоохранения и описанный Wernette C.M. et al. (Clin.Diagn. Lab. Immunol. 2003, July, 10(4), P.514-519) или на сайте www.vaccine.uab.edu. Способ заключается в анализе каждого образца сывороток с каждым из выделенных капсульных полисахаридов для выявления серотиповых специфических IgG антител. Способ, вероятней всего, подходит для серодиагностики и, поскольку он количественный, подразумевает использование референс-сывороток. Для изучения поствакцинального иммунитета описанный способ трудоемок и требует большего времени, чем предложенный нами. Кроме того, в рекомендованном ВОЗ-тесте используют препараты, содержащие С-полисахарид, что требует дополнительной обработки анализируемых сывороток для нейтрализации антител к нему. Из уровня техники не известен способ определения наличия поствакцинального иммунитета к антигенам вакцины «Пневмо-23». Техническим результатом, на решение которого направлено данное изобретение, является ускорение и упрощение способа оценки поствакцинального иммунитета к антигенам вакцины «Пневмо-23», а также он не требует дополнительной обработки анализируемых сывороток для нейтрализации антител к С-полисахаридам. Для достижения указанного технического результата способ определения наличия поствакцинального иммунитета к антигенам вакцины «Пневмо-23» методом ИФА заключается в том, что твердый носитель сорбируют вакциной «Пневмо-23», содержащей 23 полисахарида пневмококка, разведенной в фосфатно-солевом буфере с рН 7,0-7,4 в течение 2-х часов при температуре 37°С и затем при температуре 8-10°С в течение 16-18 часов и наносят рабочие разведения исследуемых и контрольной сывороток, инкубируют при температуре 18-22°С в течение 30 мин, удаляют избыток антител, вносят конъгат, представляющий собой антитела кроличьи против IgG (H+L) человека, меченные пероксидазой, повторно инкубируют при тех же параметрах, отмывают от избытка конъюгата, вносят субстратную смесь, содержащую тетраметилбензидин и перекись водорода в заданных значениях, инкубируют при температуре 18-22°С в течение 15-20 мин. В защищенном от света месте останавливают реакцию введением реагента, измеряют оптическую плотность исследуемой и контрольной сывороток на содержание антител до вакцинации и после вакцинации и по увеличению оптической плотности в исследуемых сыворотках в 4 и более раза судят о наличии поствакцинального иммунитета. Наличие гуморального иммунитета может быть оценено с помощью твердофазного иммуноферментного анализа (ИФА). В основе метода лежит иммуносорбент, представляющий собой стрипированный 96-луночный планшет, сорбированный вакциной «Pneumo-23» (Авентис Пастер, Франция) – 0,5 мл вакцины разводят в 50 мл фосфатно-солевого буферного раствора с рН 7,0-7,4 и этим раствором сорбируют полистирольные планшеты (100 мкл в лунку) в течение 2-х часов при 37°С, а затем 16-18 час при 8-10°С. При выполнении анализа образцы сывороток вносят в лунки иммуносорбента в рабочем разведении 1:200. Для анализа используют парные сыворотки – до и минимум через 14 дней после вакцинации. В качестве контроля используют пул сывороток 100 клинически здоровых людей в том же разведении. После инкубации и отмывки во все лунки иммуносорбента вносят конъюгат в рабочем разведении. Проявка реакции осуществляется субстратной смесью, содержащей тетраметилбензидин (ТМБ) и перекись водорода. Используемые реагенты: (1) иммуносорбент – планшет полистирольный разборный, состоящий из 12 8-луночных стрипов, сорбированных вакциной «Pneumo-23»; (2) отрицательный контроль (К-) – пул сывороток, полученный смешением равных объемов 100 сывороток здоровых доноров; (3) конъюгат (КГ) – антитела кроличьи против IgG (H+L) человека, меченные пероксидазой, жидкий, концентрированный; (4) субстратная смесь, содержащая тетраметилбензидин (ТМБ); (5) промывающий и разводящий фосфатно-солевой буферный раствор, десятикратный концентрат с детергентом (ФСБ-Д)к; (6) стоп-реагент – 0,9 М H2SO4. Приготовление растворов для проведения анализа: 1) (ФСБ-Д)к перед применением разводят дистиллированной водой в 10 раз. Полученный раствор ФСБ-Д хранят не более 3-х недель при 4-8°С. Раствор предназначен для отмывки планшета от непрореагировавших компонентов, разведения сывороток и конъюгата. 2) Контроль (К-), а также анализируемые сыворотки перед проведением анализа разводят раствором ФСБ-Д до соотношения 1:200 (5 мкл на 1000 мкл ФСБ-Д). Рабочее разведение сывороток хранению не подлежит. 3) Рабочее разведение конъюгата готовят непосредственно перед использованием, разводя исходный раствор до соотношения 1:400 ФСБ-Д (25 мкл на 10 мл ФСБ-Д). Последовательность операций Отмывка иммуносорбента. Во все лунки планшета вносят ФСБ-Д в объеме не менее 0,2 мл. Выдерживают планшет при комнатной температуре в течение 2-3 мин. Содержимое лунок удаляют вытряхиванием. Отмывку повторяют еще 3 раза. Внесение образцов. Во все лунки планшета последовательно вносят рабочие растворы (1:200) контроля (К-) в дублях и анализируемые сыворотки. Объем вносимых проб – 100 мкл. Инкубация. Выдерживают планшет с растворами сывороток в течение 30 мин при 18-22°С. Отмывка от избытка антител. Жидкость из лунок планшета удаляют вытряхиванием и 3-кратно отмывают раствором ФСБ-Д, как указано в п.1. Внесение рабочего раствора конъюгата. Во все лунки планшета вносят по 100 мкл рабочего раствора КГ. Инкубация. Как в п.3. Отмывка от избытка КГ. Как в п.1. Внесение субстратного раствора ТМБ. Во все лунки вносят по 100 мкл раствора ТМБ. Инкубация. 15-20 мин в темноте при температуре 18-22°С. В каждую лунку вносят по 50 мкл стоп-реагента. Учет результатов: Вывести спектрофотометр на нулевой уровень («blank») по воздуху. Измерить оптическую плотность в лунках планшета при
N для взрослых клинически здоровых людей – (ОПк-+0,25) или до 100 у.е. Пример исследования сывороток людей, вакцинированных «Пневмо-23» (до и после вакцинации)
Формула изобретения
Способ определения наличия поствакцинального иммунитета к антигенам вакцины “Пневмо-23” методом ИФА, заключающийся в том, что твердый носитель сорбируют вакциной “Пневмо-23”, содержащей 23 полисахарида пневмококка, разведенной в фосфатно-солевом буфере с рН 7,0-7,4 в течение 2 ч при температуре 37°С и затем при температуре 8-10°С в течение 16-18 ч и наносят рабочие разведения исследуемых и контрольной сывороток, инкубируют при температуре 18-22°С в течение 30 мин, удаляют избыток антител, вносят конъюгат, представляющий собой антитела кроличьи против IgG (H+L) человека, меченные пероксидазой, повторно инкубируют при тех же параметрах, отмывают от избытка конъюгата, вносят субстратную смесь, содержащую тетраметилбензидин и перекись водорода в заданных значениях, инкубируют при температуре 18-22°С в течение 15-20 мин в защищенном от света месте, останавливают реакцию введением реагента, измеряют оптическую плотность исследуемой и контрольной сывороток на содержание антител до вакцинации и после вакцинации и по увеличению оптической плотности в исследуемых сыворотках в 4 и более раза судят о наличии поствакцинального иммунитета.
|
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 =450 нм в течение 10 минут после остановки реакции. Результаты могут быть представлены в ОП и у.е. (условные единицы), которые рассчитывают по формуле:
=450 нм в течение 10 минут после остановки реакции. Результаты могут быть представлены в ОП и у.е. (условные единицы), которые рассчитывают по формуле: