Патент на изобретение №2161037
|
||||||||||||||||||||||||||
(54) НИЗКОТОКСИЧНЫЙ, НИЗКОПИРОГЕННЫЙ ЛИПООЛИГОСАХАРИД ИЗ NEISSERIA MENINGITIDIS
(57) Реферат: Изобретение относится к медицине, а именно к иммунологии. Сущность изобретения состоит в следующем. Липоолигосахарид (ЛОС), выделенный из Neisseria meningitidis серогруппы В, штамм N 125, обладает повышенной безопасностью применения при введении в организм лабораторных животных: низкой пирогенностью (пороговая пирогенная доза – 0,0125 мкг/кг) и низкой острой токсичностью (ЛД50 = 200 мг/кг). Улучшенный профиль безопасности препарата ЛОС не влияет на его высокую иммуногенность и позволяет использовать его для индукции системного гуморального иммунного ответа как при парентеральном, так и пероральном введении в расширенном диапазоне доз. Технический результат изобретения состоит в расширении арсенала средств регулирования системного гуморального иммунитета. 2 ил., 4 табл. Изобретение относится к области медицины, в частности инфекционной иммунологии, а именно описывает соматический антиген – липоолигосахарид (ЛОС) менингококка группы B с улучшенными иммунобиологическими характеристиками, а именно пониженной пирогенностью и токсичностью, может быть использован как основа для создания противоменингококковой вакцины. ЛОС является весьма важным поверхностным антигеном менингококка группы B, обладающим выраженными протективными свойствами. Однако серьезным препятствием на пути использования этого антигена в качестве вакцинного компонента является его высокая токсичность и пирогенность. Поэтому если ЛОС и обнаруживается в составе вакцин против менингита группы B, то в весьма незначительных количествах либо в условиях, резко снижающих его токсичность (липосомы, детоксифицирующие пептиды). В доступной нам литературе и материалах не обнаружены описания ЛОС с низкой пирогенностью и токсичностью, выделенного из какого-либо штамма N. meningitidis. Попытки снизить уровень токсичности ЛОС путем его введения в липосомы или с использованием детоксифицирующих пептидов направлены на функциональную детоксификацию ЛОС. Такие модификации не могут рассматриваться в качестве прямых аналогов данного изобретения, так как они предлагают использование специфических приемов (веществ) для “маскировки” пирогенности и токсичности ЛОС N.meningitidis серогруппы B, штамм N125 получают в результате выращивания микробной культуры в условиях управляемого культивирования в жидкой синтетической питательной среде, дополнительно содержащей L-глутамат и L-цистеин при pH 7,6-7,7; полученную культуральную жидкость концентрируют ультрафильтрацией и проводят дополнительную очистку трехкратным ультрацентрифугированием. Технической задачей настоящего изобретения является повышение безопасности использования ЛОС путем разработки препарата, обладающего улучшенными токсикологическими характеристиками. Полученный препарат ЛОС из N.meningitidis группы B обладает в 20 раз более низкой пирогенностью и в 5-6 раз более низкой острой токсичностью по сравнению с препаратом традиционного липополисахарида (ЛПС), полученного по методу Westphal из брюшно-тифозной бактерии. Порог пирогенности препарата 0,0125 мкг/кг веса кролика приближается к таковому, установленному ВОЗ для менингококковых и тифозных вакцин на основе соответствующих капсульных полисахаридов – 0,025 мкг/кг веса кролика. Таким образом, по своей пирогенности ЛОС близок к другому компоненту, широко используемому в менингококковых вакцинах – капсульному полисахариду. Исследования, проведенные в Центре лекарств и биологических препаратов (США), позволяют оценивать порог пирогенности для препаратов ЛОС групп A и C на значительно более низком уровне – 0,025-0,25 нг/кг веса кролика ЛД50 ЛОС – 200 мг/кг веса позволяет его оценить как умеренно токсичный препарат. Проверка предложенного ЛОС на его соответствие критерию “изобретательский уровень” показала, что ни в научной, ни в патентной литературе не выявлено бактериальных источников, которые содержали бы липоолигосахаридный антиген с таким низким уровнем токсичности. Ниже приводятся примеры, характеризующие химические и иммунобиологические характеристики ЛОС N.meningitidis серогруппы B. Пример 1 Химическая идентификация ЛОС. В полученных образцах B-ЛОС определяли содержание примесей: -белок – по методу Lowry -капсульный полисахарид группы B – с помощью резорцинового реагента (на сиаловые кислоты), -нуклеиновые кислоты – по методу Спирина. Полученные образцы ЛОС N.meningitidis серогруппы B содержали менее 3% примесей. Структурные характеристики ЛОС (моносахаридный состав и фосфорсодержащие заместители липида A) изучали методами газожидкостной хроматографии (ГЖХ) и спектроскопии ядерного магнитного резонанса на ядрах 31P(31P-ЯМР). ГЖХ ацетатов полиолов моносахаридов проводили на хроматографе Hewlett-Packard 5890 с капиллярной колонкой Ultra U (25 м) в градиенте температуры от 150oC до 290 C со скоростью изменения 10oC/мин. Спектры 31P-ЯМР записывали на приборе Bruker Physics AM-250. В качестве внешнего стандарта использовали 85% фосфорную кислоту ( 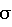 0 ppm).
Анализ моносахаридного состава ЛОС показал, что все изучаемые образцы препарата содержат гептозу, галактозу, глюкозу и глюкозамин, что соответствует данным, описанным в литературе.
Анализ 31P-спектров ЯМР подтверждает содержание в препарате ЛОС N.meningitidis серогруппы B, штамм 125 полностью достроенного липида A, несущего 0 ppm).
Анализ моносахаридного состава ЛОС показал, что все изучаемые образцы препарата содержат гептозу, галактозу, глюкозу и глюкозамин, что соответствует данным, описанным в литературе.
Анализ 31P-спектров ЯМР подтверждает содержание в препарате ЛОС N.meningitidis серогруппы B, штамм 125 полностью достроенного липида A, несущего  – (2-аминоэтил) пирофосфатные заместители при C-1 и C-4′.
Из данных SDS-гель-электрофореза в полиакриламидном геле последующим окрашиванием аммиачным раствором азотнокислого серебра следовало, ЛОС представляет собой довольно гомогенное соединение с молекулярной массой 3,5- 4.0 КД, что типично для менингококковых ЛОС (фиг 1.) – (2-аминоэтил) пирофосфатные заместители при C-1 и C-4′.
Из данных SDS-гель-электрофореза в полиакриламидном геле последующим окрашиванием аммиачным раствором азотнокислого серебра следовало, ЛОС представляет собой довольно гомогенное соединение с молекулярной массой 3,5- 4.0 КД, что типично для менингококковых ЛОС (фиг 1.)Таким образом, данные определения моносахаридного состава, анализа спектров 31P-ЯМР и картины гель-электрофореза полученного препарата позволили однозначно идентифицировать препарат как высокоочищенный ЛОС N.meningitidis группы B. Пример 2 Пирогенность Пирогенность препарата ЛОС N.meningitidis серогруппы B, штамм 125 определяли в сравнении с образцами традиционного ЛПС Salmonella typhi, а также коммерческими полисахаридными вакцинами ВИАНВАК и Тифим-Ви. Пирогенный тест ставился на кроликах в соответствии с требованиями Государственной Фармакопеи XII изд. и Европейской Фармакопеи, результаты представлены в табл 1. Данные, представленные в табл. 1, подтверждают низкую пирогенность препарата ЛОС – пороговая апирогенная доза – 0,0125  g/кг веса кролика.
Такой ЛОС по своей пирогенности близок к коммерческим полисахаридным вакцинам ВИАНВАК и Тифим-Ви и существенно отличается по этой характеристике от классического ЛПС из брюшно-тифозной бактерии.
Пример 3 Острая токсичность g/кг веса кролика.
Такой ЛОС по своей пирогенности близок к коммерческим полисахаридным вакцинам ВИАНВАК и Тифим-Ви и существенно отличается по этой характеристике от классического ЛПС из брюшно-тифозной бактерии.
Пример 3 Острая токсичностьОпределение острой токсичности препаратов проводили на мышах (СВА х C57BL/6)F1, самках весом 18-20 г. Препараты вводили внутривенно или внутрибрюшинно. Учет гибели животных вели в течение одной недели. Расчет ЛД50 проводили традиционным методом по формуле Korber (8). ЛД50 для препарата ЛОС N. meningitidis группы B существенно выше, чем для ЛПС S.typhi (см. табл. 2). Пример 4 Иммуногенность Мышей (СВА х C57/BL/6)F1 самок весом 18-20 г иммунизировали препаратом ЛОС внутрибрюшинно в дозах 0,1; 1; 5; 25; 125; 250  g. Ни одно из иммунизированных животных не погибло при иммунизации ЛОС в диапазоне доз 25-250 мкг, то есть в зоне пирогенности ЛОС.
Титр ЛОС- специфических IgG антител определяли на 34 сутки, используя прямой иммуноферментный анализ (ИФА). Для математической обработки кривых титрования использовали компьютерную программу. Высокий титр антиЛОС антител определяется в широком диапазоне доз 5-25 мкг (фиг.2).
Четкое нарастание средних значений оптической плотности в ИФА – тесте при детекции антиЛОС антител (разведение сыворотки 1:1000; длина волны 492 нм) также свидетельствуют об индукции препаратом ЛОС выраженного иммунного ответа по IgG – типу (табл. 3).
Определение существенных количеств специфических антител на 34 сутки иммунного ответа служит доказательством активации иммунологической памяти и запуска долгоживущего иммунного ответа.
Пример 5 Иммуногенность при пероральном введении.
Мышей (СВА х C57/BL/6)F1 (самки весом 18-20 г) иммунизировали перорально препаратом ЛОС в дозах 1, 5, 25, 50, 125, 250 мкг. Специфические антиЛОС антитела определяли в периферической крови с помощью ИФА.
У мышей, иммунизированных дозой 25 мкг перорально, отмечается статистически достоверное повышение титра антител на 15 сутки первичного ответа (табл. 4). Эффект индукции системного IgG-антиЛОС ответа отмечен также при пероральной иммунизации ЛОС в дозах 50, 125, 250 мкг.
Представленное изобретение позволит расширить арсенал средств, обладающих противоменингококковой активностью. Улучшенный профиль безопасности препарата ЛОС не влияет на его высокую иммуногенность и позволяет использовать его для индукции системного гуморального иммунного ответа как при парентеральном, так и пероральном введении в расширенном диапазоне доз. g. Ни одно из иммунизированных животных не погибло при иммунизации ЛОС в диапазоне доз 25-250 мкг, то есть в зоне пирогенности ЛОС.
Титр ЛОС- специфических IgG антител определяли на 34 сутки, используя прямой иммуноферментный анализ (ИФА). Для математической обработки кривых титрования использовали компьютерную программу. Высокий титр антиЛОС антител определяется в широком диапазоне доз 5-25 мкг (фиг.2).
Четкое нарастание средних значений оптической плотности в ИФА – тесте при детекции антиЛОС антител (разведение сыворотки 1:1000; длина волны 492 нм) также свидетельствуют об индукции препаратом ЛОС выраженного иммунного ответа по IgG – типу (табл. 3).
Определение существенных количеств специфических антител на 34 сутки иммунного ответа служит доказательством активации иммунологической памяти и запуска долгоживущего иммунного ответа.
Пример 5 Иммуногенность при пероральном введении.
Мышей (СВА х C57/BL/6)F1 (самки весом 18-20 г) иммунизировали перорально препаратом ЛОС в дозах 1, 5, 25, 50, 125, 250 мкг. Специфические антиЛОС антитела определяли в периферической крови с помощью ИФА.
У мышей, иммунизированных дозой 25 мкг перорально, отмечается статистически достоверное повышение титра антител на 15 сутки первичного ответа (табл. 4). Эффект индукции системного IgG-антиЛОС ответа отмечен также при пероральной иммунизации ЛОС в дозах 50, 125, 250 мкг.
Представленное изобретение позволит расширить арсенал средств, обладающих противоменингококковой активностью. Улучшенный профиль безопасности препарата ЛОС не влияет на его высокую иммуногенность и позволяет использовать его для индукции системного гуморального иммунного ответа как при парентеральном, так и пероральном введении в расширенном диапазоне доз.
Формула изобретения
Белок – Менее 1 Нуклеиновые кислоты – Менее 2 Сиаловые кислоты – Не выявлены мол. м. продукта составляет 3,8 кД, продукт обладает низкой токсичностью (ЛД 50 = 200 мг/кг) и низкой пирогенностью (пороговая пирогенная доза = 0,0125 мкг/кг). РИСУНКИ
|
||||||||||||||||||||||||||
