Патент на изобретение №2161021
|
||||||||||||||||||||||||||
(54) ТРАНСПЛАНТАТ ДЛЯ СКЛЕРОПЛАСТИКИ
(57) Реферат: Предложенный трансплантат может быть использован в медицине, а именно в офтальмологии для совершенствования трансплантационных материалов, применяемых для склеропластических операций. Обрабатывают биологический высокомолекулярный полимерный материал требуемой формы в низкотемпературной плазме до образования в его приповерхностной области модифицированного слоя. Полученный трансплантационный биологический материал обладает улучшенной биосовместимостью и обеспечивает более выраженный склероукрепляющий эффект операции. 1 з.п.ф-лы. Изобретение относится к медицине, а именно к офтальмологии, и предназначено для совершенствования трансплантационных биологических материалов, применяемых для склеропластических операций. В то же время известно, что повышения биомеханической устойчивости комплекса склера-трансплантат можно достичь путем улучшения физико-механических и поверхностных адгезивных свойств биологического трансплантата путем его обработки в полимерной композиции (Е.П.Тарутта, Э.Ш.Шамхалова, Е.Н.Иомдина, Л. Д. Андреева, М. И.Винецкая. Способ лечения прогрессирующей близорукости. Авт. свид. N 1680161, опубл. Б.И. N 36, 1991). Склеральный трансплантат, погруженный непосредственно перед операцией в раствор “Вспенивающейся полимерной композиции для заполнения полостей в организме”, приобретал улучшенные упруго-прочностные свойства, более плотно фиксировался к склере реципиента, что в результате способствовало формированию более устойчивого к растяжению комплекса “склера-трансплантат”. Этот способ является ближайшим аналогом предлагаемого изобретения. Однако при использовании трансплантата, обработанного подобным образом, в раннем послеоперационном периоде отмечались тенониты в большем проценте случаев, чем при обычной склеропластике (Э. С. Аветисов и соавт. “Укрепление склеры у детей с повышенным риском прогрессирования близорукости”. Методические рекомендации. М., 1990, 11 с.). Известен, кроме того, способ модификации поверхности искусственных полимерных материалов, используемых для рефракционной кератопластики, путем их обработки в низкотемпературной газоразрядной плазме с целью улучшения биологической совместимости и снижения токсичности используемых синтетических трансплантатов. Обработка проводилась в газоразрядной плазме высокочастотного (f = 13,56 МГц) емкостного разряда в аргоне. В процессе обработки температура рабочего газа составляла 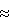 300K (комнатная температура), что позволяло обрабатывать материалы без разрушения их структуры. На поверхность материала воздействовали электроны со средней энергией 3-6 эВ, потоки ионов с энергией до 100 эВ, ультрафиолетовое излучение и метастабильные атомы аргона с энергией около 11,5 эВ. Процесс обработки проводился в течение времени (3-5 мин), достаточного для образования модифицированного слоя (Ю.А.Шустеров, И.Ш.Абдуллин, В.Е.Брагин, А.Н.Быканов, Е.В.Елисеева. Использование плазмы высокочастотного разряда для улучшения биосовместимости полимерных материалов в офтальмологии. Матер. Конф. Физика низкотемпературной плазмы. Петрозаводск, 1995, Часть 3, с. 398-399). В результате подобного воздействия на поверхности полимера создавался уплотненный модифицированный слой, обладающий свойствами повышенной гидрофильности. Этот слой уменьшал выход токсичных мономеров и олигомеров из полимера в окружающие ткани.
С целью сокращения сроков приживления трансплантата и повышения стабильности комплекса склера-трансплантат предлагается обработка биологического высокомолекулярного полимерного материала требуемой формы в низкотемпературной плазме до образования в его приповерхностной области модифицированного слоя.
Техническим результатом предлагаемого изобретения является получение трансплантационного биологического материала, обладающего улучшенной биосовместимостью и обеспечивающего более выраженный склероукрепляющий эффект операции. Технический результат достигается за счет использования трансплантата, обработанного таким образом, что на его поверхности образуется модифицированный слой.
Трансплантат для склеропластики изготавливают следующим образом. В стерильных условиях вырезают из предварительно обработанной в растворе антибиотиков биологической ткани (гомосклеры, твердой мозговой оболочки и др.) трансплантат требуемой формы; высушивают при комнатной температуре таким образом, что его масса уменьшается до 35-40% от исходной. Затем проводят обработку в плазме газового разряда следующим образом. Трансплантат располагают в области воздействия плазмы. Плазмохимический реактор вакуумируют и заполняют его рабочим газом (предпочтительно инертным, например, аргоном) до давления 0,1-3 тор, затем возбуждают разряд (например, высокочастотный разряд емкостного типа), подвергают трансплантат воздействию плазмы в течение времени, достаточного для образования поверхностного слоя модифицированных белковых молекул. Время воздействия плазмы для реализованных параметров разряда определили экспериментально, контролируя образование упомянутого модифицированного слоя методом микроскопии. В отличие от искусственных материалов, оптимальное время воздействия на склеральную ткань составило 2-3 мин.
С целью предотвращения деформации трансплантата при дегидратации и удобства его укладывания в процессе операции на поверхности глазного яблока перед обработкой его высушивают на сферической поверхности диаметром 24 мм.
После завершения плазменной обработки трансплантат помещают в раствор антибиотика или антисептика для хранения.
Наличие модифицированного слоя в гомосклеральпом трансплантате, прошедшем плазменную обработку, обнаруживается при микроскопическом (гистологическом и гистохимическом) исследовании. При оптимальном времени воздействия (2-3 мин) строение склеры в целом не отличается от нормального. Однако в наружных слоях отмечается разволокнение и рыхлое расположение коллагеновых волокон, которые с одной стороны как бы склеены, а с другой – диссоциированы на отдельные мелкие уплотненные коллагеновые структуры, лежащие на расстоянии друг от друга. При гистохимическом исследовании наблюдается более интенсивная окраска наружных уплотненных участков, что, по-видимому, связано с разрушением в них протеогликановых комплексов и высвобождением свободных гликозаминогликанов. Разрушение межмолекулярных и межфибриллярных связей, вызванное плазмохимической обработкой, приводит к частичной диссоциации коллагена поверхностного слоя склеры на продукты полураспада полипептиды и пептиды. Последние после пересадки трансплантата способны вызывать стимуляцию биосинтеза коллагена в фибробластах. Таким образом, обработанный трансплантат лучше адаптирован для целей склеропластики, чем интактный, что обуславливает его более активное приживление и перестройку при формировании комплекса склера-трансплантат.
Комплексное морфологическое изучение приживления склеральных трансплантатов в эксперименте на животных подтверждает лучшую биологическую совместимость трансплантатов, подвергшихся обработке, по сравнению с интактными. После склеропластической операции в обоих случаях развивается небольшая воспалительная реакция на чужеродную ткань. Однако процессы приживления и организации обработанных трансплантатов завершаются значительно раньше. Так, после склеропластики с применением обработанных трансплантатов уже к 7,5 месяцам происходит полное замещение их коллагенового каркаса и фибробластов, в то время как при использовании интактного материала эти процессы завершаются лишь через 12 месяцев после операции. Через 7,5 месяцев обработанный трансплантат стабилизирован и плотно сращен со склерой, сформирован единый комплекс, укрепляющий склеральную оболочку глаза. Сохраняются новообразованные сосуды, которые играют определенную роль в улучшении питания и повышении метаболической активности комплекса.
Трансплантаты гомосклеры, изготовленные предложенным способом, были использованы в клинической практике в ходе склеропластических операций при прогрессирующей близорукости, а также при травматических стафиломах склеральной оболочки глаза.
Пример 1. Больной Б., 1984 г. рожд., история болезни N 3780. Находился на стационарном лечении с диагнозом: миопия высокой степени OU, прогрессирующая. Объективно: VIS OD = 0,2 с корр – 7,0 D = 0,6; VIS OS = O,2 с корр – 6,5 D = 0,8; R OD = M 7,0 D; R OS = M 6,0 D. OU спокойны. Оптические среды прозрачны. ДЗН: границы стушеваны с височной стороны, бледно-розового цвета. Артерии сужены, вены полнокровны, ход извитой. Лечение: операция склеропластики OU по методу Атамередовой – Нурмамедова с помощью предложенного трансплантата (модифицированной донорской склерой). При выписке жалоб нет. Объективно: OU конъюнктива несколько инъецирована, шов состоятелен. Трансплантаты лежат хорошо. Оптические среды прозрачны. На глазном дне: OU значительно уменьшилась стушеванность границ ДЗН, сосуды стали полнокровнее. VIS OD = 0,2 с корр – 6,5 D = 0,6. VIS OS = 0,2 с корр – 6,5 D = 0,8; при повторном осмотре через 3 месяца жалоб нет. Объективно: VIS OD = 0,2 с корр – 5,5 D = 0,6; VIS OS = 0,2 с корр – 5,5 D = 0,8. OU спокойны. Трансплантаты лежат хорошо. Оптические среды прозрачны. ДЗН границы слегка завуалированы, бледно-розового цвета. Артерии несколько сужены, вены полнокровны, ход извитой. R OD = М 5,5 – 6,0 D. R OS = M 5,5 – 6,0 D, т.е. отмечается стабилизация миопического процесса на oбоих оперированных глазах.
Пример 2. Больная Ш., 1930 г. рожд., история болезни N 8602. Находилась на стационарном лечении с диагнозом: OU исход контузии тяжелой степени с разрывом склеры, стафилома склеры, подвывих хрусталика, осложненная катаракта. При поступлении жалобы на резкое снижение зрения OU. Снижение зрения заметила после удара в область переносицы несколько месяцев назад, но к врачу не обращалась. Объективно: VIS OD = счет пальцев на расстоянии 10 см; VIS OS = 0,01 не корр; OU спокойны. Имеется субконъюнктивальный разрыв склеры у лимба от 10 час. до 14 час., в месте разрыва под конъюнктивой проминирует сосудистая оболочка. Ширина разрыва до 4-5 мм, роговица рубцово изменена у лимба с 10 до 14 часов. Передняя камера неравномерной глубины, влага прозрачная. Полная колобома радужки на 12 часах. Хрусталик частично помутнен, подвывих в переднюю камеру. Глубжележащие отделы осмотру не доступны. Лечение: операция OD – склеропластика стафиломы склеры с помощью предложенного трансплантата (модифицированной гомосклерой). Послеоперационный период без особенностей. При выписке: шов на коньюнктиве снят, рубец состоятелен. Трансплантат лежит хорошо. Другие отделы глаза без динамики.
Таким образом, предложенный плазменно-модифицированный склеральный трансплантат может быть успешно использован для хирургического укрепления склеры при прогрессирующей близорукости, а также для склеропластических операций при посттравматических и других состояниях глаз. 300K (комнатная температура), что позволяло обрабатывать материалы без разрушения их структуры. На поверхность материала воздействовали электроны со средней энергией 3-6 эВ, потоки ионов с энергией до 100 эВ, ультрафиолетовое излучение и метастабильные атомы аргона с энергией около 11,5 эВ. Процесс обработки проводился в течение времени (3-5 мин), достаточного для образования модифицированного слоя (Ю.А.Шустеров, И.Ш.Абдуллин, В.Е.Брагин, А.Н.Быканов, Е.В.Елисеева. Использование плазмы высокочастотного разряда для улучшения биосовместимости полимерных материалов в офтальмологии. Матер. Конф. Физика низкотемпературной плазмы. Петрозаводск, 1995, Часть 3, с. 398-399). В результате подобного воздействия на поверхности полимера создавался уплотненный модифицированный слой, обладающий свойствами повышенной гидрофильности. Этот слой уменьшал выход токсичных мономеров и олигомеров из полимера в окружающие ткани.
С целью сокращения сроков приживления трансплантата и повышения стабильности комплекса склера-трансплантат предлагается обработка биологического высокомолекулярного полимерного материала требуемой формы в низкотемпературной плазме до образования в его приповерхностной области модифицированного слоя.
Техническим результатом предлагаемого изобретения является получение трансплантационного биологического материала, обладающего улучшенной биосовместимостью и обеспечивающего более выраженный склероукрепляющий эффект операции. Технический результат достигается за счет использования трансплантата, обработанного таким образом, что на его поверхности образуется модифицированный слой.
Трансплантат для склеропластики изготавливают следующим образом. В стерильных условиях вырезают из предварительно обработанной в растворе антибиотиков биологической ткани (гомосклеры, твердой мозговой оболочки и др.) трансплантат требуемой формы; высушивают при комнатной температуре таким образом, что его масса уменьшается до 35-40% от исходной. Затем проводят обработку в плазме газового разряда следующим образом. Трансплантат располагают в области воздействия плазмы. Плазмохимический реактор вакуумируют и заполняют его рабочим газом (предпочтительно инертным, например, аргоном) до давления 0,1-3 тор, затем возбуждают разряд (например, высокочастотный разряд емкостного типа), подвергают трансплантат воздействию плазмы в течение времени, достаточного для образования поверхностного слоя модифицированных белковых молекул. Время воздействия плазмы для реализованных параметров разряда определили экспериментально, контролируя образование упомянутого модифицированного слоя методом микроскопии. В отличие от искусственных материалов, оптимальное время воздействия на склеральную ткань составило 2-3 мин.
С целью предотвращения деформации трансплантата при дегидратации и удобства его укладывания в процессе операции на поверхности глазного яблока перед обработкой его высушивают на сферической поверхности диаметром 24 мм.
После завершения плазменной обработки трансплантат помещают в раствор антибиотика или антисептика для хранения.
Наличие модифицированного слоя в гомосклеральпом трансплантате, прошедшем плазменную обработку, обнаруживается при микроскопическом (гистологическом и гистохимическом) исследовании. При оптимальном времени воздействия (2-3 мин) строение склеры в целом не отличается от нормального. Однако в наружных слоях отмечается разволокнение и рыхлое расположение коллагеновых волокон, которые с одной стороны как бы склеены, а с другой – диссоциированы на отдельные мелкие уплотненные коллагеновые структуры, лежащие на расстоянии друг от друга. При гистохимическом исследовании наблюдается более интенсивная окраска наружных уплотненных участков, что, по-видимому, связано с разрушением в них протеогликановых комплексов и высвобождением свободных гликозаминогликанов. Разрушение межмолекулярных и межфибриллярных связей, вызванное плазмохимической обработкой, приводит к частичной диссоциации коллагена поверхностного слоя склеры на продукты полураспада полипептиды и пептиды. Последние после пересадки трансплантата способны вызывать стимуляцию биосинтеза коллагена в фибробластах. Таким образом, обработанный трансплантат лучше адаптирован для целей склеропластики, чем интактный, что обуславливает его более активное приживление и перестройку при формировании комплекса склера-трансплантат.
Комплексное морфологическое изучение приживления склеральных трансплантатов в эксперименте на животных подтверждает лучшую биологическую совместимость трансплантатов, подвергшихся обработке, по сравнению с интактными. После склеропластической операции в обоих случаях развивается небольшая воспалительная реакция на чужеродную ткань. Однако процессы приживления и организации обработанных трансплантатов завершаются значительно раньше. Так, после склеропластики с применением обработанных трансплантатов уже к 7,5 месяцам происходит полное замещение их коллагенового каркаса и фибробластов, в то время как при использовании интактного материала эти процессы завершаются лишь через 12 месяцев после операции. Через 7,5 месяцев обработанный трансплантат стабилизирован и плотно сращен со склерой, сформирован единый комплекс, укрепляющий склеральную оболочку глаза. Сохраняются новообразованные сосуды, которые играют определенную роль в улучшении питания и повышении метаболической активности комплекса.
Трансплантаты гомосклеры, изготовленные предложенным способом, были использованы в клинической практике в ходе склеропластических операций при прогрессирующей близорукости, а также при травматических стафиломах склеральной оболочки глаза.
Пример 1. Больной Б., 1984 г. рожд., история болезни N 3780. Находился на стационарном лечении с диагнозом: миопия высокой степени OU, прогрессирующая. Объективно: VIS OD = 0,2 с корр – 7,0 D = 0,6; VIS OS = O,2 с корр – 6,5 D = 0,8; R OD = M 7,0 D; R OS = M 6,0 D. OU спокойны. Оптические среды прозрачны. ДЗН: границы стушеваны с височной стороны, бледно-розового цвета. Артерии сужены, вены полнокровны, ход извитой. Лечение: операция склеропластики OU по методу Атамередовой – Нурмамедова с помощью предложенного трансплантата (модифицированной донорской склерой). При выписке жалоб нет. Объективно: OU конъюнктива несколько инъецирована, шов состоятелен. Трансплантаты лежат хорошо. Оптические среды прозрачны. На глазном дне: OU значительно уменьшилась стушеванность границ ДЗН, сосуды стали полнокровнее. VIS OD = 0,2 с корр – 6,5 D = 0,6. VIS OS = 0,2 с корр – 6,5 D = 0,8; при повторном осмотре через 3 месяца жалоб нет. Объективно: VIS OD = 0,2 с корр – 5,5 D = 0,6; VIS OS = 0,2 с корр – 5,5 D = 0,8. OU спокойны. Трансплантаты лежат хорошо. Оптические среды прозрачны. ДЗН границы слегка завуалированы, бледно-розового цвета. Артерии несколько сужены, вены полнокровны, ход извитой. R OD = М 5,5 – 6,0 D. R OS = M 5,5 – 6,0 D, т.е. отмечается стабилизация миопического процесса на oбоих оперированных глазах.
Пример 2. Больная Ш., 1930 г. рожд., история болезни N 8602. Находилась на стационарном лечении с диагнозом: OU исход контузии тяжелой степени с разрывом склеры, стафилома склеры, подвывих хрусталика, осложненная катаракта. При поступлении жалобы на резкое снижение зрения OU. Снижение зрения заметила после удара в область переносицы несколько месяцев назад, но к врачу не обращалась. Объективно: VIS OD = счет пальцев на расстоянии 10 см; VIS OS = 0,01 не корр; OU спокойны. Имеется субконъюнктивальный разрыв склеры у лимба от 10 час. до 14 час., в месте разрыва под конъюнктивой проминирует сосудистая оболочка. Ширина разрыва до 4-5 мм, роговица рубцово изменена у лимба с 10 до 14 часов. Передняя камера неравномерной глубины, влага прозрачная. Полная колобома радужки на 12 часах. Хрусталик частично помутнен, подвывих в переднюю камеру. Глубжележащие отделы осмотру не доступны. Лечение: операция OD – склеропластика стафиломы склеры с помощью предложенного трансплантата (модифицированной гомосклерой). Послеоперационный период без особенностей. При выписке: шов на коньюнктиве снят, рубец состоятелен. Трансплантат лежит хорошо. Другие отделы глаза без динамики.
Таким образом, предложенный плазменно-модифицированный склеральный трансплантат может быть успешно использован для хирургического укрепления склеры при прогрессирующей близорукости, а также для склеропластических операций при посттравматических и других состояниях глаз.
Формула изобретения
MM4A Досрочное прекращение действия патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 29.01.2001
Номер и год публикации бюллетеня: 34-2002
Извещение опубликовано: 10.12.2002
|
||||||||||||||||||||||||||
