Патент на изобретение №2329271
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) ДИАЛКИЛ(АРИЛ)-ЦИС-2-(2-ГИДРОКСИАРИЛ)-2-АЛКИЛ(АРИЛ)ЭТЕНИЛФОСФИНОКСИДЫ И СПОСОБ ИХ ПОЛУЧЕНИЯ
(57) Реферат:
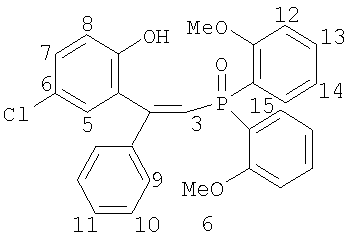
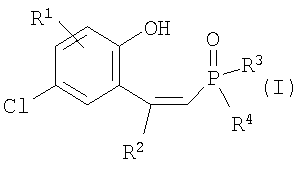
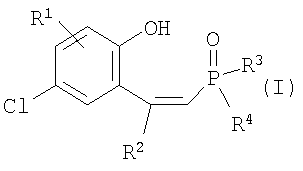
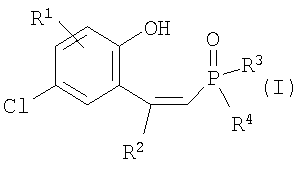
Изобретение может быть использовано для выделения редкоземельных и цветных металлов и относится к новым фосфорсодержащим комплексообразователям – фосфиноксидам общей формулы (I)
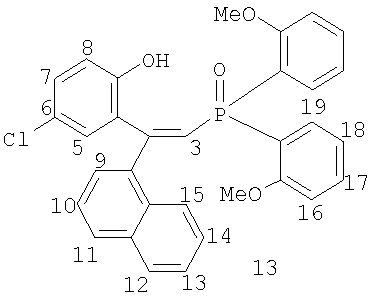
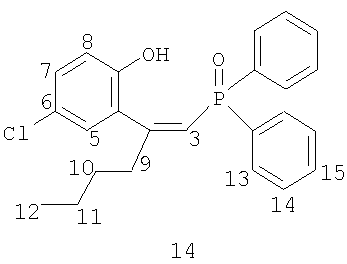
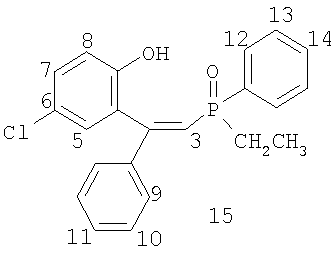
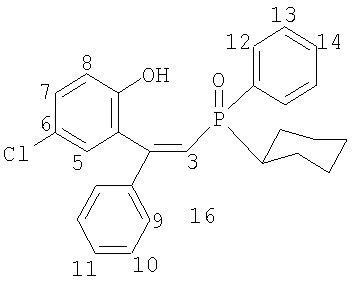
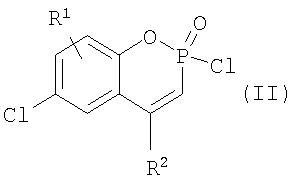
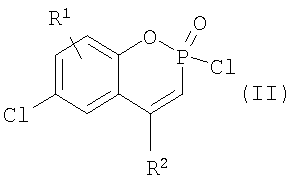
где R1=Н, R2=Ph, R3=R4=Ph, Me, Et, Pr, CH2Ph, 2-MeO-C6H4, C8H17; R1=4-Me, R2=Ph, R3=R4=Ph, CH2Ph, 2-МеО-С6Н4; R1=H, R2=1-нафтил, R3=R4=Ph, CH2Ph, 2-MeO-C6H4; R1=H, R2=Bu, R3=R4=Ph; R1=H, R2=Ph, R3=цикло-С6Н11, R4=Et, Ph, и способам их получения. Способ получения фосфиноксидов (I) включает взаимодействие в среде органического растворителя хлорфосфорининоксидов формулы (II)
с соответствующими реагентами Гриньяра, гидролиз реакционной массы и выделение целевых соединений. Технический результат – получение новых фосфорсодержащих комплексообразователей формулы (I). 2 н. и 1 з.п. ф-лы, 1 табл.
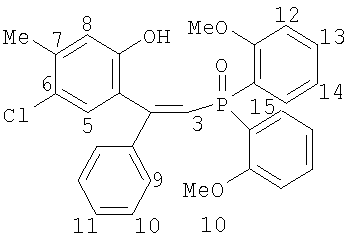
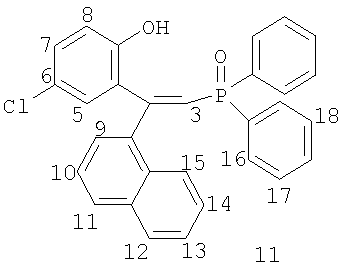
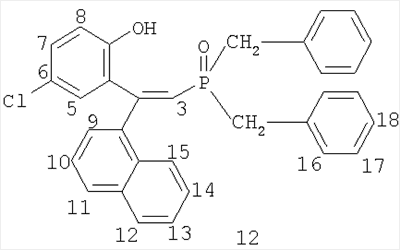
Изобретение относится к химии фосфорорганических соединений, а именно к новым фосфиноксидам общей формулы (I)
где R1=Н, R2=Ph, R3=R4=Ph, Me, Et, Pr, CH2Ph, 2-MeO-C6H4, C8H17 (1-7); R1=4-Me, R2=Ph, R3=R4=Ph, CH2Ph, 2-МеО-С6Н4 (8-10); R1=H, R2=1-нафтил, R3=R4=Ph, CH2Ph, 2-MeO-C6H4 (11-13); R1=H, R2=Bu, R3=R4=Ph (14); R1=H, R2=Ph, R3=цикло-С6Н11, R4=Et, Ph (15-16), и способу их получения. Известно, что фосфиноксиды обладают высокими экстракционными (комплексообразующими) свойствами по отношению к ионам редких, редкоземельных и цветных металлов и часто являются исходными соединениями для получения фосфинов, которые в свою очередь применяются как лиганды в металлокомплексном катализе ([1] Phosphine Oxides, Sulphides, Selenides and Tellurides, Vol.2, The Chemistry of Organophosphorus Compounds. Ed. by Frank R.Hartley. John Wiley & Sons – 1992, 664 p; [2] M.G. de Bolster. Phosphoryl Coordination Chemistry: The Period 1975-1981. In: Topics in Phosphorus Chemistry. Ed. By M.Grayson, E.J.Griffith. J.Wiley & Sons – 1983. N.-Y., Chichester, Brisbane, Toronto, Singapore. Vol.11. P.69-295). Соединения формулы (I) могут найти применение как исходные соединения в химии для получения фосфинов с гидроксильной группой в четвертом положении одного из радикалов в качестве лигандов хелатирующего типа для металлокомплексного катализа, а также как нейтральные хелатирующие лиганды для экстракции редких, редкоземельных и цветных металлов. Известны обычные триалкил(арил)фосфиноксиды формулы R3Р=О, способ получения которых заключается во взаимодействии реагентов Гриньяра с хлорокисью фосфора в диэтиловом эфире или тетрагидрофуране ([3] патент США №3338701, опубл. 29.08.1967 г), однако этот способ применим лишь для простых симметричных фосфиноксидов. Известен также способ получения простых симметричных фосфиноксидов из хлорокиси фосфора и реагентов Гриньяра в смеси углеводород – эфир или тетрагидрофуран ([4] патент Великобритании №1376028, опубл. 04.12.1974 г). Известны несимметричные фосфиноксиды формул R Известно также, что несимметричные фосфиноксиды могут быть получены по реакции O,O-диалкилалкил(арил)фосфонатов и O-алкилдиалкил(диарил)фосфинатов с реагентами Гриньяра ([6] H.R.Hays, D.J.Peterson. in Organic Phosphorus Compounds. Ed. by G.M.Kosolapoff, L.Maier. Wiley-Intersci., N.-Y., L., Sydney, Toronto. 1972. Vol.III. P.341-500). Структурными аналогами соединений (I) являются фосфоновые кислоты следующего строения:
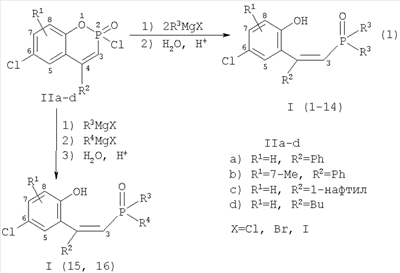
которые получают гидролизом производных 4-арил-2,5,6,7,8-пентахлорбензо[е]-1,2-оксафосфоринин-2-оксида ([7] В.Ф.Миронов, А.Т.Губайдуллин, А.А.Штырлина, И.А.Литвинов, Р.Р.Петров, А.И.Коновалов, А.Б.Добрынин, Т.А.Зябликова, Р.З.Мусин, В.И.Морозов. ЖОХ. 2002, Т.72, Вып.11, С.1868-1888; [8] В.Ф.Миронов, Т.А.Баронова, А.И.Коновалов, Н.М.Азанчеев, Ф.Ф.Алексеев, Т.А.Зябликова, Р.З.Мусин. ЖОрХ, 2002, Т.38, Вып.8, С.1235-1239). Комплексообразующие свойства этих кислот не исследовались (не выявлены). Целевые фосфиноксиды (I) не могут быть получены перечисленными методами, так как реагенты Гриньяра, содержащие в качестве дополнительного функционального заместителя гидроксильную группу, в литературе не известны. Авторами не найдено веществ, подобных синтезированным соединениям (I), в научной и патентной литературе. Задачей предлагаемого изобретения являются новые фосфиноксиды, расширяющие арсенал известных экстрагентов (комплексообразующих средств), и разработка метода их синтеза. Техническим результатом являются новые диалкил(арил)-цис-2-(2-гидроксиарил)-2-алкил(арил)этенилфосфиноксиды формулы (I) и способ их получения, позволяющий получать эти соединения с выходом не менее 80%. Технический результат достигается заявляемым способом получения диалкил(арил)-цис-2-(2-гидроксиарил)-2-алкил(арил)этенилфосфиноксидов формулы (I), обладающих комплексообразующими свойствами, путем взаимодействия шестичленных гетероциклических производных фосфора – замещенных в бензофрагменте 4-арил(алкил)-2-хлорбензо[е]-1,2-оксафосфоринин-2-оксидов (II) (далее «хлорфосфорининоксидов») с магнийорганическими соединениями (реагентами Гриньяра) (схема 1). R1=H, R2=Ph, R3=R4=Ph (1), Me (2), Et (3), Pr (4), Ch2Ph, (5) 2MeO-C6H4 (6), C8H17 (7); R1=4-ME, R2=Ph, R3=R4=Ph (8), CH2Ph (9), 2MeO-C6H4 (10); R1=H, R2=1-нафтил, R3=R4=Ph (11), CH2Ph (12), 2MeO-C6H4 (13); R1=H, R2=Bu, R3=R4=Ph (14); R1=H, R2=Ph, R3=цикло-C6H11, R4=Et (15), Ph (16). Схема 1. Способ включает обработку хлорфосфорининоксидов (II) реагентом Гриньяра R3MgX (X=Cl, Br, I) (R4=R3=перечисленные выше первичный алкил, бензил или арил) в мольном соотношении 1÷(2.0-2.6) или первоначальную обработку циклогексилмагнийбромидом (R3=цикло-С6Н11) в мольном соотношении 1÷(1.2-1.4) и последующую обработку другим реагентом Гриньяра R4MgBr (R4=Ph, Et) в мольном соотношении 1:(1.2-1.4). Целевые соединения (I) далее выделяют после обработки реакционной массы водой или водой, подкисленной соляной кислотой (рН 3-6) известными приемами: разделением водной и органической фаз, отгонкой органического растворителя (смесь бензола с эфиром, или с ТГФ, или с изооктаном) или фильтрацией выпадающего осадка. Затем полученные соединения (выход 80-95%, содержание основного вещества не ниже 95%) высушивают на воздухе или в вакууме (0.1-12 мм рт.ст.). Исходные хлорфосфорининоксиды (II) являются доступными соединениями, легко получаемыми из пентахлорида фосфора, соответствующего пирокатехина и арил- или алкилацетилена (методы их синтеза описаны в работах: [9] В.Ф.Миронов, А.И.Коновалов, И.А.Литвинов, А.Т.Губайдуллин, Р.Р.Петров, А.А.Штырлина, Т.А.Зябликова, Р.З.Мусин, Н.М.Азанчеев, А.В.Ильясов. ЖОХ. 1998, Т.68, Вып.9, С.1482-1509; [10] В.Ф.Миронов, А.А.Штырлина, Е.Н.Вараксина, А.Т.Губайдуллин, Н.М.Азанчеев, А.Б.Добрынин, И.А.Литвинов, Р.З.Мусин, А.И.Коновалов. ЖОХ. 2004, Т.74, Вып.12, С.1953-1972; [11] В.Ф.Миронов, Е.Н.Вараксина, А.А.Штырлина, А.Т.Губайдуллин, Н.М.Азанчеев, Р.З.Мусин, И.А.Литвинов, А.И.Коновалов. ЖОХ. 2006, Т.76, Вып.3, С.411-432). Заявляемый способ получения фосфиноксидов (I) исключает образование смеси соединений, получающихся при использовании способов, описанных в патенте [5] и в работах [6, 7]. Способ иллюстрируется следующими примерами. Пример 1. Раствор 30 г (0.0965 моля) хлорфосфорининоксида (IIa) в 20 мл бензола добавляли по каплям при перемешивании в токе аргона к фенилмагнийбромиду, приготовленному из 5.1 г (0.2125 моля) Mg и 22.4 мл (33.4 г, 0.2125 моля) бромбензола в 150 мл диэтилового эфира по стандартной методике ([12] Препаративная органическая химия. Перевод под ред. Н.С.Вульфсона. Изд. «Химия», Москва-Ленинград, 1964. 907 с). Полученную реакционную массу нагревали при кипении эфира 30 мин, затем охлаждали и нейтрализовали раствором 18 мл концентрированной соляной кислоты в 100 мл дистиллированной воды при интенсивном перемешивании и кипении эфира. Раствор перемешивали 30 мин до достижения комнатной температуры. При этом происходило образование осадка, который отфильтровывали и промывали 20-30 мл эфира и высушивали на воздухе или в вакууме 12 мм рт.ст. Получено 36 г (87%) 2-(2-гидрокси-5-хлорфенил)-2-фенилэтенилдифенилфосфиноксида (1) (с учетом дополнительного количества осадка, выпавшего из фильтратов после отгонки эфира и бензола), т.пл. 185-186°С. Найдено, %: С 72.65, Н 4.91, Р 7.29. С26Н20ClO2Р. Вычислено, %: С 72.47, Н 4.64, Р 7.20. Спектр ЯМР 31P-{1Н} (36.46 МГц, CDCl3):
Пример 2. К реагенту Гриньяра, полученному по стандартной методике из 2.2 г (0.0924 моля) магния и 5.75 мл (13.1 г, 0.0924 моля) йодметана в 100 мл диэтилового эфира, добавляли по каплям раствор 13.8 г (0.0444 моля) хлорфосфорининоксида (IIa) в 25 мл бензола. После окончания добавления раствора реакционную массу нагревали при интенсивном перемешивании 30 мин (при этом происходило расслоение). После охлаждения до комнатной температуры реакционную массу нейтрализовали при интенсивном перемешивании и кипении эфира 30 мл воды и затем 8 мл соляной кислоты. Органический слой отделяли, добавляли 2-4 мл ацетона и полученный однородный органический слой осаждали разбавлением водой. Выделено 13.0 г (96%) 2-(2-гидрокси-5-хлорфенил)-2-фенилэтенилдиметилфосфиноксида (2) в виде светло-коричневого порошка, т.пл. 172-175°С. Найдено, %: С 62.37, Н 5.49, Р 10.55. C16H16ClO2P. Вычислено, %: С 62.64, Н 5.22, Р 10.11. Спектр ЯМР 31P-{1Н} (36.46 МГц, CDCl3): Пример 3. К реагенту Гриньяра, полученному по стандартной методике из 0.43 г (0.0179 моля) магния, 1.44 мл (2.8 г, 0.0179 моля) йодэтана в 20 мл диэтилового эфира, добавляли по каплям раствор 2.5 г (0.0080 моля) хлорфосфорининоксида (IIa) в 10 мл бензола и нагревали при кипении 0.5 ч. Раствор охлаждали и гидролизовали 30 мл воды и 2.3 мл соляной кислоты. Органический и водный слои отфильтровывали и отделяли. Затем растворители отгоняли, затвердевший остаток зеленоватого цвета снова промывали раствором соляной кислоты (15 мл 10% раствора), отделяли от промывного раствора декантацией и затем высушивали в вакууме. Получено 2.52 г (94%) 2-(2-гидрокси-5-хлорфенил)-2-фенилэтенилдиэтилфосфиноксида (3) в виде коричневого порошка, т.пл. 75-77°С. Найдено, %: С 64.29, Н 6.12, Р 9.41. C18H20ClO2P. Вычислено, %: С 64.57, Н 5.98, Р 9.27. Спектр ЯМР 31P-{1Н} (36.46 МГц, CDCLQ: Пример 4. К реагенту Гриньяра, полученному по стандартной методике из 0.8 г (0.0333 моля) магния, 3.25 мл (5.67 г, 0.0333 моля) 1-йодпропана в 20 мл диэтилового эфира, добавляли по каплям раствор 5.2 г (0.0167 моля) хлорфосфорининоксида (IIa) в 15 мл бензола и нагревали при кипении 0.5 ч. При этом реакционная масса приобретала темно-коричневую окраску. Раствор охлаждали и гидролизовали 40 мл воды и 2 мл HCl, образующиеся слои разделяли. В органическом слое выпадет желтый осадок, который отфильтровывали, промывали ацетоном и высушивали в вакууме 12 мм рт.ст. Получено 4.7 г (81%) 2-(2-гидрокси-5-хлорфенил)-2-фенилэтенилдипропилфосфиноксида (4), т.пл. 143-145°С. Найдено, %: С 66.20, Н 6.15, Р 8.81, Cl 9.87. C20H24ClO2P. Вычислено, %: С 66.21, Н 6.62, Р 8.55, Cl 9.79. Масс-спектр (здесь и далее указаны наиболее распространенные изотопы), m/z: 364, 362 [М]+·, 347, 345 [М-ОН], 329, 327, 321, 319, 305, 304, 302, 294, 284, 275, 265, 262, 261, 259, 230, 228, 194, 166, 165, 139, 135, 134, 119, 106, 92, 78, 64, 41, 27. Спектр ЯМР 31P-{1Н} (162.0 МГц, ДМСО-D6): Пример 5. К реагенту Гриньяра, полученному по стандартной методике из 0.81 г (0.0338 моля) магния, 3.9 мл (4.28 г, 0.0338 моля) бензилхлорида в 40 мл диэтилового эфира, добавляли по каплям раствор 4.5 г (0.0145 моля) хлорфосфорининоксида (IIa) в 20 мл бензола. При этом происходило образование белого осадка. Реакционную смесь нагревали 30 мин, затем охладили и обработали при перемешивании раствором соляной кислоты (10 мл) в 30 мл воды. Выпавший из органического слоя осадок отфильтровывали, промывали небольшим количеством ацетона и высушивали в вакууме (65°С, 12 мм рт.ст.). Получено 6 г (90.5%) 2-(2-гидрокси-5-хлор-фенил)-2-фенилэтенилдибензилфосфиноксида (5), т.пл. 210-211°С. Найдено, %: С 72.91, Н 5.38, Р 6.92, Cl 7.78. С28Н24ClO2Р. Вычислено, %: С 73.28, Н 5.23, Р 6.76, Cl 7.74. Масс-спектр соединения, m/z: 460, 459, 458 [М]+ Пример 6. К реагенту Гриньяра, полученному по стандартной методике из 0.92 г (0.0383 моля) магния, 4.74 мл (7.16 г, 0.0383 моля) орто-броманизола в 20 мл тетрагидрофурана, добавляли по каплям раствор 5 г (0.0161 моля) хлорфосфорининоксида (IIa) в 10 мл бензола. После добавления реакционную массу нагревали при кипении 0.5 ч. Через сутки происходило частичное образование осадка. Осадок отфильтровывали, промывали водой, подкисленной соляной кислотой, и затем чистой водой. Фильтрат отдельно также обрабатывали водой (рН 3.0-4.0), образовывавшийся при этом осадок отделяли. Осадки объединяли и высушивали на воздухе, а затем в вакууме (65°С, 18 мм рт.ст.). Получено 6 г (76%) 2-(2-гидрокси-5-хлорфенил)-2-фенилэтенил-бис(2-метоксифенил)фосфиноксида (6), т.пл. 218-221°С. Найдено, %: С 68.77, Н 5.14, Cl 7.44, Р 6.12. C28H24ClO4P. Вычислено, %: С 68.50, Н 4.89, Cl 7.24, Р 6.32. Спектр ЯМР 31P-{1Н} (162.0 МГц, ДМСО-D6):
Пример 7. К 3.5 г (0.1458 моля) магниевых стружек, предварительно активизированных кристаллическим йодом, в 60 мл изооктана при перемешивании в атмосфере аргона добавляли по каплям 26.43 мл (35.02 г, 0.1458 моля) 1-йодоктана. К полученному после кипячения (30 минут) раствору прикапывали раствор 18 г (0.0579 моля) хлорфосфорининоксида (IIa) в 20 мл бензола. Наблюдали образование белой эмульсии, которую нагревали при кипении 40 мин, затем охладили и обработали раствором соляной кислоты (10 мл) в 30 мл воды. Изоктаново-бензольный слой отделили, растворители удалили перегонкой в вакууме 12 мм рт.ст. Остаток высушивали в вакууме (100°С, 0.1 мм рт.ст.). Получено 27.9 г (96%) 2-(2-гидрокси-5-хлорфенил)-2-фенилэтенилдиоктилфосфиноксида (7) в виде зеленоватого масла. Найдено, %: С 71.22, Н 9.07, Р 6.27. C30H44ClO2P. Вычислено, %: С 71.64, Н 8.76, Р 6.17. Масс-спектр, m/z: 502 [M]+ Пример 8. К раствору фенилмагнийбромида, полученного из 1.49 г (0.0621 моля) магния и 6.53 мл (9.75 г, 0.0621 моля) бромбензола в 90 мл эфира, добавили при перемешивании по каплям раствор 8 г (0.0246 моля) хлорфосфорининоксида (IIb) в 20 мл бензола, так чтобы смесь равномерно кипела. Полученную реакционную массу нагревали при кипении еще 0.5 ч, затем охладили и при перемешивании добавили 20 мл воды, затем раствор 10 мл концентрированной соляной кислоты в 20 мл воды. При этом происходило образование белого осадка. Реакционную смесь перемешивали до достижения комнатной температуры и затем отфильтровывали. Осадок высушивали сначала на воздухе, затем в вакууме 0.1 мм рт.ст.(80°С). Выделено 9.13 г (83.7%) 2-(2-гидрокси-4-метил-5-хлорфенил)-2-фенилэтенилдифенилфосфиноксида (8), т.пл. 194-197°С. Найдено, %: С 73.02, Н 5.13, Р 6.73. С27Н22ClO2Р. Вычислено, %: С 72.89, Н 4.95, Р 6.97. Спектр ЯМР 31P-{1Н} (162.0 МГц, ДМСО-D6): Пример 9. К реагенту Гриньяра, полученному по стандартной методике из 1.3 г (0.0542 моля) магния, 6.24 мл (6.86 г, 0.0542 моля) бензилхлорида в 90 мл диэтилового эфира, через капельную воронку с компенсатором добавляли по каплям раствор 6.7 г (0.0206 моля) хлорфосфорининоксида (IIb) в 20 мл бензола. Реакционную массу нагревали при кипении еще 0.5 часа, затем охлаждали до комнатной температуры и обрабатывали дистиллированной водой, затем раствором 10 мл конц. соляной кислоты в 20 мл воды. Выпадавший при этом белый осадок отфильтровывали и высушивали в вакууме (12 мм рт.ст., 100°С). Выделено 9.36 г (92%) дибензил-2-(2-гидрокси-4-метил-5-хлорфенил)-2-фенилэтенилфосфиноксида (9) с т.пл. 169-172°С. Найдено, %: С 73.44, Н 5.77, Р 6.24. С29Н26ClO2Р. Вычислено, %: С 73.65, Н 5.50, Р 6.56. Масс-спектр соединения, m/z: 472 [M]+·., 381 [М-CH2Ph], 290 [М-2CH2Ph], 243 [М-PO(СН2Ph)2], 230 [М-PO(CH2Ph)2-СН], 202, 183, 91 [CH2Ph]. Спектр ЯМР 31P-{1Н} (162.0 МГц, ДМСО-D6): Пример 10. К реагенту Гриньяра, полученному по стандартной методике из 1.45 г (0.0604 моля) магния, 7.48 мл (11.30 г, 0.0604 моля) орто-броманизола в 100 мл диэтилового эфира, добавляли по каплям раствор 7.8 г (0.0240 моля) хлорфосфорининоксида (IIb) в 50 мл бензола. Реакционную массу нагревали при кипении еще 0.5 часа, затем охлаждали до комнатной температуры и обрабатывали дистиллированной водой, затем раствором 10 мл конц. соляной кислоты в 20 мл воды. При этом был получен вязкий белый маслоподобный продукт, который отделяли от кислого водного раствора, промывали дистиллированной водой и высушивали в вакууме (12 мм рт.ст., 100°С). Выделено 10.77 г (89%) 2-(2-гидрокси-4-метил-5-хлорфенил)-2-фенил-бис(2-метоксифенил)фосфиноксида (10) с т.пл. 207-210°С. Найдено, %: С 69.17, Н 5.33, Р 6.24. С29Н26ClO4Р. Вычислено, %: С 68.98, Н 5.15, Р 6.14. Спектр ЯМР 31P-{1Н} (162.0 МГц, ДМСО-D6):
Пример 11. К реактиву Гриньяра, полученному из 0.8 г (0.0333 моля) магния и 3.50 мл (5.23 г, 0.0333 моля) бромбензола в 50 мл диэтилового эфира, при перемешивании в токе аргона добавляли по каплям раствор 5 г (0.0138 моля) хлорфосфорининоксида (IIc) в 10 мл бензола. Реакционную массу нагревали при кипении 0.5 ч, охлаждали до комнатной температуры и обрабатывали дистиллированной водой, раствором 5 мл концентрированной соляной кислоты в 20 мл воды, затем снова водой. Образовавшийся при этом желтый осадок отфильтровывали и высушивали в вакууме 12 мм рт.ст. (100°С). Выделено 6.45 г (97%) 2-(2-гидрокси-5-хлорфенил)-2-нафт-1-илэтенилдифенилфосфиноксида (11), т.пл. 173-175°С. Найдено, %: С 75.11, Н 4.77, Р 6.23. C30H22ClO2P. Вычислено, %: С 74.92, Н 4.58, Р 6.45. Спектр ЯМР 31P-{1Н} (162.0 МГц, ДМСО-D6):
Пример 12. К реактиву Гриньяра, полученному из 0.8 г (0.0333 моля) магниия и 3.86 мл (4.22 г, 0.0333 моля) бензилхлорида в 20 мл диэтилового эфира при перемешивании в токе аргона добавляли по каплям раствор 5 г (0.0138 моля) хлорфосфорининоксида (IIc) в 10 мл бензола. Далее полученную реакционную массу обрабатывали, как в примере 11. Выделено 6.62 г (94%) 2-(2-гидрокси-5-хлорфенил)-2-(нафт-1-ил)этенилдибензил-фосфиноксида (12), т.пл. 178-181°С. Найдено, %: С 75.34, Н 5.47, Р 6.29. C32H26ClO2P. Вычислено, %: С 75.52, Н 5.11, Р 6.10. Спектр ЯМР 31P-{1Н} (162.0 МГц, ДМСО-D6): Пример 13. К реактиву Гриньяра, полученному из 0.8 г (0.0333 моля) магния и 4.12 мл (6.23 г, 0.0333 моля) орто-броманизола в 50 мл диэтилового эфира при перемешивании в токе аргона добавляли по каплям раствор 5 г (0.0138 моля) хлорфосфорининоксида (IIc) в 10 мл бензола. Далее реакционную массу обрабатывали, как описано в примере 11. Выделено 6.59 г (88%) 2-(2-гидрокси-5-хлорфенил)-2-нафт-1-илэтенил-бис(2-меток-сифенил)фосфиноксида (13), т.пл. 145-148°С. Найдено, %: С 71.12, Н 5.19, Р 6.07. C32H26ClO4P. Вычислено, %: С 71.04, Н 4.81, Р 5.73. Спектр ЯМР 31P-{1Н} (162.0 МГц, ДМСО-D6):
Пример 14. К реактиву Гриньяра, полученному из 1.8 г (0.0750 моля) магния и 7.9 мл (11.9 г, 0.0750 моля) бромбензола в 100 мл диэтилового эфира, при перемешивании в токе аргона добавляли по каплям раствор 10 г (0.0344 моля) хлорфосфорининоксида (IId) в 10 мл бензола. Реакционную смесь нагревали при кипении 0.5 ч, затем охлаждали до комнатной температуры и обрабатывали водой, как это описано в примере 11. Из органического слоя перегонкой удаляли растворители, оставшееся стеклообразное вещество, 2-бутил-2-(2-гидрокси-5-хлорфенил)этенилдифенилфосфиноксид (14), высушивали в вакууме 12 мм рт.ст. (100°С), выход 12 г (85%). Найдено, %: С 70.24, Н 6.13, Р 7.73. С24Н24ClO2Р. Вычислено, %: С 70.16, Н 5.85, Р 7.55. Масс-спектр, m/z: 410 [M]+
Пример 15. Раствор 1.83 г (0.0057 моля) хлорфосфорининоксида (IIa) в 15 мл бензола добавляли по каплям через капельную воронку при перемешивании в токе аргона к циклогексилмагнийбромиду, приготовленному из 0.17 г Mg (0.0069 моля) и 0.84 мл (1.12 г, 0.0069 моля) циклогексилбромида в 30 мл диэтилового эфира по стандартной методике. Реакционную смесь нагревали при кипении 1 ч, затем охлаждали до комнатной температуры. К полученной реакционной массе (спектр ЯМР 31P-{1Н}, 36.46 МГц, CDCl3,
Пример 16. Раствор 3.0 г (0.01 моля) хлорфосфорининоксида (IIa) в 10 мл бензола добавляли по каплям при перемешивании в токе аргона к циклогексилмагнийбромиду, приготовленному из 0.33 г Mg (0.014 моля) и 1.43 мл (1.91 г, 0.014 моля) циклогексилбромида в 30 мл диэтилового эфира по стандартной методике. Реакционную смесь нагревали при кипении 1 ч, затем охлаждали до комнатной температуры. К полученной реакционной массе (спектр ЯМР 31P-{1Н}, 36.46 МГц,
Проблема экстракции редких, редкоземельных и цветных металлов крайне важна вследствие их большого значения в технике и других областях. При этом арсенал фосфорсодержащих комплексообразующих средств (экстрагентов), которые до сих пор используются для разделения лантанидов, невелик (в основном это триалкил(арил)фосфиноксиды, триалкилфосфаты и диалкилалкилфосфонаты). Отличительной особенностью строения предлагаемых фосфиноксидов (I) является наличие в качестве одного из радикалов этенильного фрагмента, содержащего 2-гидрокси-арильный заместитель, расположенный в цис-конфигурации относительно фосфорной части, который придает этим соединениям хелатирующий характер, т.е. способность к комплексообразованию. Ниже представлены примеры жидкостной экстракции гадолиния в системе вода – хлороформ некоторыми представителями фосфиноксидов (I) (соединениями 1, 2, 5, 10), подтверждающие их высокие экстрактивные свойства. Общая методика проведения экстракции. К 5 мл водного раствора Gd(NO3)3(С=1·10-3 моль/л) и пикриновой кислоты (HPic, С=6·10-4 моль/л) приливали 5 мл хлороформного раствора фосфиноксида (1, 2, 5, 10) (С=6.5·10-4÷9.2·10-3 моль/л). Двухфазную систему перемешивали в закрытой колбе на магнитной мешалке в течение 1.5 ч, затем оставляли на 24 ч в темном месте. После экстракции концентрацию Gd(Pic)3 в водной фазе определяли спектрофотометрическим методом по интенсивности пика электронного поглощения пикрат-иона при 353.40 нм ([13] К.Е.Koenig, G.M.Lein, P.Stuckler, T.Kaneda, D.J.Cram, J. Am. Chem. Soc., 1979, 101, №13, 3553, [14] R.C.Helgeson, G.R.Weisman, J.L.Toner, T.L.Tarnowski, Y.Chao, J.M.Mayer, D.J.Cram, J. Am. Chem. Soc., 1979, 101, №17, 4928). Электронные спектры поглощения записывали на приборе «Perkin Lambda 35» с использованием кювет толщиной l=10 мм. Степень экстракции (EPic) рассчитывалась по формуле: EPic=100%·(1-А/А0), где А0 и А – оптические плотности до и после экстракции соответственно. Данные о степени экстракции Gd(Pic)3 из воды в хлороформ в зависимости от концентрации фосфиноксидов (1, 2, 5, 10) в качестве экстрагентов представлены в таблице.
Установлено, что при концентрации экстрагента (фосфиноксида) >9.2·10-3 в двухфазной экстракционной системе выпадает осадок, представляющий собой комплекс иона гадолиния с фосфиноксидом. Выделение комплекса Gd(III) экстрагентом (1). К 100 мл водного раствора Gd(NO3)3(С=1·10-3 моль/л) и пикриновой кислоты (HPic, С=6·10-4 моль/л) приливали 100 мл хлороформного раствора фосфиноксида (1) (С=6.4·10-2 моль/л). Двухфазную систему перемешивали в закрытой колбе на магнитной мешалке в течение 1.5 ч, затем оставляли на 24 ч в темном месте. Водный раствор центрифугировали, выпавший осадок отделяли и сушили. На основании элементного анализа выпавшего осадка комплекса Gd(III) с экстрагентом (1) был определен его состав – Gd(Pic)3(Н2O)3(1)3. Найдено, %: С 50.62; Н 4.31; N 5.76; Р 4.67; Gd 6.92. Вычислено, %: С 52.69; Н 3.32; N 5.76; Р 4.25; Gd 7.19. Экспериментальные данные показывают, что полученные фосфиноксиды проявляют хорошие экстракционные свойства за счет комплексообразования при жидкостной экстракции иона Gd(III) в системе вода-хлороформ. Они образуют с ионом гадолиния комплексы в мольном соотношении Gd(III): лиганд =1:3, которые растворимы в хлороформе в области концентраций лиганда от 6.5·10-4 до 9.2·10-3 моль/л. При концентрациях лиганда (фосфиноксида) выше 9.2·10-3 моль/л в двухфазной системе в условиях экстракции наблюдается выпадение осадка, что облегчает выделение комплексов из раствора. Таким образом, предложен эффективный способ получения новых соединений – диалкил(арил)-цис-(2-гидроксиарил)-2-алкил(арил)этенилфосфиноксидов, обладающих хорошими комплексообразующими свойствами, алкилированием хлорфосфорининоксидов реагентами Гриньяра.
Формула изобретения
1. Диалкил(арил)-цис-2-(2-гидроксиарил)-2-алкил(арил)этенилфосфиноксиды общей формулы (I)
где R1=Н, R2=Ph, R3=R4=Ph, Me, Et, Pr, CH2Ph, 2-MeO-C6H4, C8H17; R1=4-Me, R2=Ph, R3=R4=Ph, CH2Ph, 2-МеО-С6Н4; R1=H, R2=1-нафтил, R3=R4=Ph; CH2Ph; R1=H, R2=Bu, R3=R4=Ph; R1=H, R2=Ph, R3=цикло-С6Н11, R4=Et, Ph. 2. Способ получения диалкил(арил)-цис-2-(2-гидроксиарил)-2-алкил-(арил)этенилфосфиноксидов (I) по п.1, включающий: взаимодействие в среде органического растворителя при нагревании хлорфосфорининоксидов формулы (II)
с реагентом Гриньяра R3MgX (X=Cl, Br, I) в мольном соотношении 1-(1,2-1,4), последующую обработку другим реагентом Гриньяра R3MgX (Х=Cl, Br, I) в том же мольном соотношении, а при R3=R4 обработку соединений (II) производят реагентом Гриньяра в мольном соотношении 1-(2,0-2,6), гидролиз реакционной массы водой или водным раствором соляной кислоты и выделение целевых соединений известными приемами. 3. Способ по п.2, характеризующийся тем, что в качестве органического растворителя используют смесь бензола с эфиром, или с ТГФ, или с изооктаном.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

 R2P=O и (R
R2P=O и (R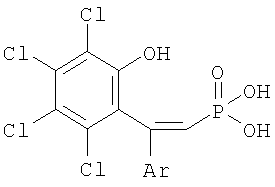
 P 22.6 м.д. ИК спектр, см-1: 431, 455, 511, 525, 543, 592, 630, 639, 665, 693, 720, 728, 739, 767, 812, 836, 893, 922, 933, 945, 977, 999, 1030, 1069, 1114, 1172, 1216, 1262, 1289, 1313, 1330, 1376, 1418, 1436, 1446, 1465, 1496, 1558, 1586, 1655, 1686, 1812, 1864, 1890, 1910, 1958, 2588, 2730, 2783, 2856, 2926, 3062, 3631, 3651, 3677. Спектр ЯМР 1Н (600 МГц, ДМСО-D6, 45°С,
P 22.6 м.д. ИК спектр, см-1: 431, 455, 511, 525, 543, 592, 630, 639, 665, 693, 720, 728, 739, 767, 812, 836, 893, 922, 933, 945, 977, 999, 1030, 1069, 1114, 1172, 1216, 1262, 1289, 1313, 1330, 1376, 1418, 1436, 1446, 1465, 1496, 1558, 1586, 1655, 1686, 1812, 1864, 1890, 1910, 1958, 2588, 2730, 2783, 2856, 2926, 3062, 3631, 3651, 3677. Спектр ЯМР 1Н (600 МГц, ДМСО-D6, 45°С, 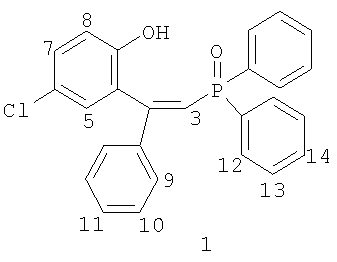
 , 443, 442, 441 [М-HCl], 433, 423, 422, 401, 377, 370, 369, 368, 367, 366, 349, 321, 320, 319, 304, 303, 301, 289, 285, 277, 275, 230, 229, 228, 166, 165, 139, 121, 91 [PhCH2], 65. Спектр ЯМР 31P-{1Н} (162.0 МГц, ДМСО-D6):
, 443, 442, 441 [М-HCl], 433, 423, 422, 401, 377, 370, 369, 368, 367, 366, 349, 321, 320, 319, 304, 303, 301, 289, 285, 277, 275, 230, 229, 228, 166, 165, 139, 121, 91 [PhCH2], 65. Спектр ЯМР 31P-{1Н} (162.0 МГц, ДМСО-D6):