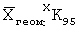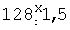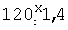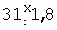Патент на изобретение №2326655
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ИНКАПСУЛИРОВАНИЯ БЕЛОКСОДЕРЖАЩИХ ВЕЩЕСТВ В МИКРОСФЕРЫ ИЗ СОПОЛИМЕРА ПОЛИЛАКТИД-ПОЛИГЛИКОЛИД
(57) Реферат:
Изобретение относится к биотехнологии и может быть использовано для получения микроинкапсулированных форм лекарственных препаратов. Микросферы представляют собой сополимер полилактид-полигликолид – полиэфир полимолочной и полигликолевой кислот. Он разрушается в организме до естественных метаболитов – молочной и гликолевой кислот, нетоксичен, не вызывает воспалительных реакций в месте введения, стабилен при хранении. Способ инкапсулирования белоксодержащих веществ в микросферы из сополимера полилактид-полигликолид включает: приготовление первичной эмульсии путем эмульгирования водного раствора действующего вещества в органической фазе; получение вторичной эмульсии посредством соединения первичной эмульсии и гидрофильной фазы, состоящей из водного раствора стабилизатора эмульсии; испарение органического растворителя. В качестве стабилизатора вторичной эмульсии использовался полиглюкин, разрешенный к применению в составе парентерально вводимых лекарственных средств. 2 табл.
Изобретение относится к биотехнологии и может быть использовано для получения микроинкапсулированных форм лекарственных препаратов. Лечение и профилактика эндокринных, онкологических, иммунных, инфекционных, наследственных и ряда других заболеваний зачастую требуют длительного поддержания необходимой концентрации соответствующих лекарственных средств в организме пациента, что обуславливает необходимость разработки лекарственных форм, обеспечивающих пролонгированное действие действующего начала препарата. Преимуществами депонированных лекарственных форм над недепонированными являются непрерывность терапевтического или профилактического воздействия, стабильная предсказуемая концентрация препаратов в плазме крови, возможность применения более низких терапевтических доз, снижение риска побочных эффектов, отсутствие необходимости многократного введения. В составе многих разрабатываемых депо-препаратов действующее вещество находится в растворяющихся полимерных микрокапсулах. Продолжительность действия таких препаратов зависит в том числе от размера и материала использованных микрокапсул. Существуют различные способы микроинкапсулирования действующего вещества с использованием ПЛ-ПГ, однако одним из наиболее распространенных из них является метод выпаривания растворителя. Общими существенными признаками описанного метода с заявляемым способом являются: 1. Включение действующего вещества в микросферы из биодеградируемого носителя; 2. Испарение органического растворителя из органической фазы, в результате которого эмульсия превращается в суспензию. К причинам, препятствующим достижению указанного ниже технического результата, относится то, что при использовании способа приготовления микросфер выпариванием органического растворителя из двойной (трехфазной) эмульсии, принятого за прототип, происходит неполная загрузка действующего вещества в микросферы в результате частичного его перехода в дисперсионную среду в процессе затвердевания микросфер. Потеря может достигать 80% и более использованного для загрузки действующего вещества. Кроме того, при использовании данного способа сохраняется необходимость отмывать готовые микросферы от дисперсионной среды, что делает технологию приготовления микросфер сложной, громоздкой и дорогой. Общими существенными признаками указанного метода с заявляемым способом являются: 1. Включение действующего вещества в микросферы из биодеградируемого носителя; 2. Использование эмульсии, состоящей из трех фаз: водная, органическая, водная; 3. Испарение органического растворителя из органической фазы, в результате которого эмульсия превращается в суспензию. Задачей изобретения является усовершенствование способа микроинкапсулирования белоксодержащих веществ. Технический результат изобретения – увеличение количества действующего вещества в составе конечного препарата и упрощение процедуры подготовки жидкого полуфабриката вакцинного препарата к стадии лиофильного высушивания. Указанный технический результат при осуществлении изобретения достигается тем, что в предлагаемом способе в качестве стабилизатора эмульсии вместо ПВС предложено использовать полиглюкин. Полиглюкин – это декстрановый препарат, 6%-ный водный раствор которого применяется в медицинской практике в качестве плазмозаменителя для улучшения реологических свойств крови. Он представляет собой частично гидролизованный полимер глюкозы с молекулярной массой около 60000 Д. Поскольку полиглюкин – препарат, официально допущенный к парентеральному применению, нет необходимости исключать его из состава лекарственной формы, как это имеет место при использовании ПВС. Помимо этого полиглюкин, как известно, с успехом используется в качестве криопротектора при лиофильном высушивании препаратов. Таким образом, заявляемый способ представляет собой следующую последовательность манипуляций: 1. Приготовление первичной (двухфазной) эмульсии: водный раствор белоксодержащего вещества эмульгируют в органической фазе, состоящей из органического растворителя и растворенного в нем полимера. 2. Приготовление вторичной (трехфазной) эмульсии: первичную эмульсию эмульгируют в гидрофильной фазе, состоящей из воды и растворенного в ней полиглюкина. 3. Выпаривание органического растворителя из органической фазы, в результате чего эмульсия превращается в суспензию. 4. Лиофильное высушивание готового препарата. Между совокупностью существенных признаков заявляемого способа и достигаемым техническим результатом существует причинно-следственная связь, а именно: использование полиглюкина в качестве стабилизатора эмульсии позволило оптимизировать схему микроинкапсулирования белоксодержащих веществ путем исключения стадии отмывки микросфер и упрощения стадии подготовки к лиофильному высушиванию. При этом действующее вещество, вышедшее в дисперсионную среду из микросфер в процессе испарения растворителя, остается в составе конечного препарата в свободном виде и не теряется, как это имеет место в методе-прототипе. Возможность осуществления заявляемого изобретения показана следующими примерами. Все нижеприведенные исследования проведены с использованием бычьего сывороточного альбумина (БСА) в качестве модели инкапсулируемого действующего вещества. Пример 1. Схема приготовления микросфер выпариванием растворителя из двойной эмульсии с использованием в качестве стабилизатора полиглюкина Для приготовления препарата 0,2 мл 1%-ного водного раствора БСА добавляли в органическую фазу, состоящую из 0,4 г ПЛ-ПГ, растворенного в 1,8 мл дихлорметана, и энергично эмульгировали на магнитной мешалке в течение 1 минуты. После этого полученную первичную эмульсию добавляли в 12 мл водного раствора полиглюкина. Вторичную (трехфазную) эмульсию перемешивали на магнитной мешалке 1 минуту на максимальной скорости, после чего скорость перемешивания понижали до минимальной (100 об/мин) и выдерживали такие условия в течение примерно 2 часов – до полного испарения дихлорметана. Готовую суспензию микросфер помещали в пенициллиновые флаконы в объеме 2,5 мл и подвергали лиофильному высушиванию. Пример 2. Физико-химические свойства микроинкапсулированного препарата БСА Для оценки влияния концентрации полиглюкина в дисперсионной среде на размер микросфер, на степень их загрузки и на характеристики лиофильно высушенного препарата предлагаемым способом (см. пример 1) был приготовлен ряд препаратов микросфер, загруженных БСА. При этом в качестве дисперсионной среды использовался водный раствор, содержащий различное количество полиглюкина. В лиофилизированных препаратах оценивалась потеря в массе при высушивании. При регидратации высушенных препаратов визуальным методом оценивались скорость ресуспендирования и наличие агрегатов. В регидратированных препаратах определяли средний диаметр микросфер микроскопическим методом посредством измерения 200 микросфер. Степень загрузки микросфер определялась спектрофотометрическим методом при длине волны 280 нм, оптическая плотность экстракта из микросфер сравнивалась с оптической плотностью референс-препарата, содержащего такое же количество БСА, которое использовалось для приготовления опытного образца. Результаты исследований представлены в таблице 1. Как видно из данных, представленных в таблице 1, с увеличением концентрации полиглюкина в дисперсионной среде средний размер микросфер уменьшается, при этом уменьшается и степень их загрузки БСА. Оптимальная концентрация полиглюкина в дисперсионной среде, при которой обеспечивается получение микросфер удовлетворительных характеристик, и, в то же время, после лиофильного высушивания удается получить хорошо ресуспендируемый препарат с низкой агрегацией микросфер, составляет 40%. Пример 3. Иммунохимические свойства микроинкапсулированного препарата БСА Лабораторные животные (морские свинки) иммунизировались препаратами БСА, приготовленными с использованием различных адъювантов. Препарат №1 представлял собой БСА, инкапсулированный в микросферы из ПЛ-ПГ (50:50) методом выпаривания растворителя из двойной эмульсии при использовании 40%-ного водного раствора полиглюкина в качестве сурфактанта. Препараты сравнения (№№2, 3) содержали идентичные количества БСА в комплексе с соответственно масляным (полный адъювант Фрейнда, ПАФ) и минеральным (гель гидроокиси алюминия, ГГА) адъювантами. Иммунизация морских свинок (по 20 животных в группе) проводилась подкожно во внутреннюю поверхность бедра в объеме 0,2 мл в дозе 20 мкг БСА. Через 3 месяца после иммунизации в сыворотке крови животных оценивался титр антител к БСА в РНГА с эритроцитарным антигенным диагностикумом лабораторного приготовления. В таблице 2 представлены результаты определения иммунохимических свойств сравниваемых препаратов. Данные таблицы 2 показывают, что через 3 месяца после иммунизации наибольший титр антител к БСА выявлялся в сыворотке крови животных, иммунизированных препаратом БСА, микроинкапсулированного в ПЛ-ПГ, либо эмульгированного в ПАФ. Среднегеометрический титр антител к БСА у животных, иммунизированных БСА, сорбированном на ГТА, был приблизительно в 4 раза ниже (различие достоверно для р=0,95).
Формула изобретения
Способ инкапсулирования белоксодержащих веществ в микросферы из сополимера полилактид-полигликолид методом выпаривания растворителя, включающий приготовление первичной эмульсии путем эмульгирования водного раствора действующего вещества в органической фазе, получение вторичной эмульсии посредством соединения первичной эмульсии и гидрофильной фазы, состоящей из стабилизатора эмульсии и воды, испарение растворителя, отличающийся тем, что в качестве стабилизатора вторичной эмульсии используется полиглюкин.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

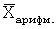 , мкм
, мкм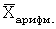 , мин
, мин