Патент на изобретение №2326114
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ 1-ЗАМЕЩЕННЫХ 3,3,4,4-ТЕТРАМЕТИЛ-3,4-ДИГИДРОИЗОХИНОЛИНОВ
(57) Реферат:
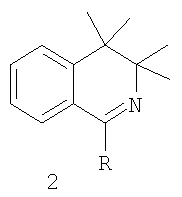
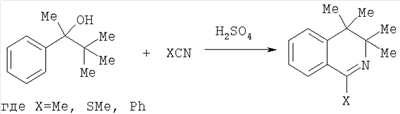
Изобретение относится к области химии гетероциклических соединений, а именно к способам получения 1-замещенных производных 3,3-диалкил-3,4-дигидроизохинолина. Описывается способ получения 1-замещенных 3,3,4,4-тетраметил-3,4-дигидроизохинолинов общей формулы 2
где R=Me, SMe, Ph, CH2CONH2, CH2COOEt взаимодействием смеси эквимолярных количеств 3,3-диметил-2-фенилбутанола-2 и нитрилов в среде концентрированной серной кислоты, с последующим выделением целевых продуктов известными приемами. Технический результат – расширение сырьевой базы для получения производных 3,4-дигидроизохинолина.
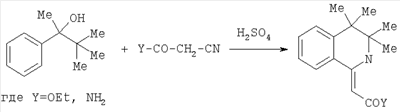
Изобретение относится к области химии гетероциклических соединений, а именно к способам получения 1-замещенных производных 3,3-диалкил-3,4-дигидроизохинолина, многие из которых проявляют биологическую активность, служат лигандами для комплексообразования, ингибиторами коррозии черных металлов, отвердителями в синтезе полиуретанов и прочее [1-3]. Известен способ получения 1-замещенных 3,4-дигидроизохинолинов по реакции Бишлера-Напиральского, заключающийся в нагревании Известен способ получения 3,3-диметил-6,7-(или 5,8-) диметокси-3,4-дигидроизохинолинов взаимодействием кислородсодержащего соединения, например, окиси изобутилена, орто- или пара-диметокси-бензола с нитрилом в среде концентрированной серной кислоты [5]. К недостаткам указанного способа относится использование окиси изобутилена – весьма дорогого и дефицитного реагента. Кроме того, данный способ позволяет получать 3,3-диалкил-3,4-дигидроизохинолины только при наличии в молекуле арена двух метоксигрупп. Известен способ получения 3,3-диметил-6,7-(или 5,8-) диметокси-3,4-дигидроизохинолинов взаимодействием смеси эквимолярных количеств дизамещенного арена, изомасляного альдегида и нитрила в среде концентрированной серной кислоты, с последующим выделением целевых продуктов известными приемами [6]. Наиболее близким к предлагаемому решению по совокупности признаков и достигаемому эффекту является способ получения целевых продуктов взаимодействием смеси эквимолярных количеств 2,3-диметил-3-фенилбутанола-2 и нитрила общей формулы 1 в среде концентрированной серной кислоты, с последующим выделением целевых продуктов известными приемами [7]. К недостаткам указанного способа относится необходимость получения 2,3-диметил-3-фенилбутанола-2, что представляет серьезную синтетическую задачу, и, кроме того, невозможность получения производных с другими типами нитрилов. Задачей предлагаемого изобретения является расширение сырьевой базы для получения производных 1-замещенных 3,3,4,4-тетраметил-3,4-дигидроизохинолинов, в частности, для получения ранее неизвестных производных 1-замещенных 3,3,4,4-тетраметил-3,4-дигидроизохинолинов. Для решения указанной задачи предлагается способ получения 1-замещенных 3,3,4,4-тетраметил-3,4-дигидроизохинолинов общей формулы 2
где R=Me, SMe, Ph, CH2CONH2, CH2COOEt взаимодействием смеси эквимолярных количеств 3,3-диметил-2-фенилбутанола-2 и нитрилов в среде концентрированной серной кислоты, с последующим выделением целевых продуктов известными приемами. Применение легко доступного 3,3-диметил-2-фенилбутанола-2 вместо 2,3-диметил-3-фенилбутанола-2 позволяет получать не описанные в литературе 1-замещенные 3,3,4,4-тетраметил-3,4-дигидроизохинолины, а также амиды изохинолилиден-1-уксусной кислоты, что позволяет расширить сырьевую базу для получения производных 3,4-дигидроизохинолина. Возможность применения предлагаемого решения подтверждается следующими примерами. Пример 1. Амид 3,3,4,4-тетраметил-1,2,3,4-тетрагидроизохинолилиден-1-уксусной кислоты 0.84 г (0.01 моля) цианацетамида растворяют при перемешивании в 2 мл холодной концентрированной серной кислоты и одной порцией добавляют 1.8 г (0.01 моль) 3,3-диметил-2-фенилбутанола-2. Реакционную массу перемешивают при комнатной температуре 40 мин, разбавляют 50 мл воды и подщелачивают до рН 8-9. Экстрагируют 10 мл диэтилового эфира, эфир отгоняют и остаток кристаллизуют из этилацетата. Получают 0.73 г (30%) амида 3,3,4,4-тетраметил-1,2,3,4-тетрагидроизохинолилиден-1-уксусной кислоты, бесцветные кристаллы, т.пл.148-152°С. Спектр ЯМР 1Н, Пример 2. Этиловый эфир 3,3.4,4-тетраметил-1,2,3,4-тетрагидроизохинолилиден-1-уксусной кислоты Смесь 1.8 г (0.01 моль) 3,3-диметил-2-фенилбутанола-2 и 1.13 г (0.01 моль) циануксусного эфира в 1 мл бензола прибавляют по каплям при перемешивании и температуре 5-10°С к 2 мл концентрированной серной кислоты. Реакционную массу перемешивают при комнатной температуре 40 мин, разбавляют 100 мл воды и подщелачивают до рН 8-9. Отгоняют с паром 50 мл воды, охлаждают, экстрагируют 30 мл диэтилового эфира, сушат сульфатом натрия. Эфир удаляют и получают 0.8 г (29%) этилового эфира 3,3,4,4-тетраметил-1,2,3,4-тетрагидроизохинолилиден-1-уксусной кислоты в виде вязкого светло-зеленого масла. Спектр ЯМР 1Н, Пример 3. 1,3,3,4,4-пентаметил-3,4-дигидроизохинолин Смесь 1.8 г (0.01 моль) 3,3-диметил-2-фенилбутанола-2 и 0.41 г (0.01 моль) ацетонитрила обрабатывают, как указано в примере 2. Получают 0.5 г (25%) 1,3,3,4,4-пентаметил-3,4-дигидроизохинолина. Спектр ЯМР 1Н, Пример 4. 1-Фенил-3,3,4,4-тетраметил-3,4-дигидроизохинолин Смесь 1.8 г (0.01 моль) 3,3-диметил-2-фенилбутанола-2 и 1.03 г (0.01 моль) бензонитрила обрабатывают, как указано в примере 2. Получают 0.9 г (34%) 1-фенил-3,3,4,4-тетраметил-3,4-дигидроизохинолина в виде светло-зеленого масла. Спектр ЯМР 1Н, Пример 5. 1-Метилтио-3,3,4,4-тетраметил-3,4-дигидроизохинолин 1.8 г (0.01 моль) 3,3-диметил-2-фенилбутанола-2 растворяют в 2 мл концентрированной серной кислоты, перемешивают 10 мин, прибавляют одной порцией при температуре 5-10°С 0.73 г (0.01 моль) метилтиоцианата и реакционную массу перемешивают 40 мин. После обработки, как в примере 2, получают 0.61 г (26%) 1-метилтио-3,3,4,4-тетраметил-3,4-дигидроизохинолина, масло. Спектр ЯМР 1Н, Таким образом, применение предлагаемого способа позволяет получать не описанные в литературе 1-замещенные 3,3,4,4-тетраметил-3,4-дигидроизохинолины, а также амиды изохинолилиден-1-уксусной кислоты, что позволяет расширить сырьевую базу для получения указанных продуктов. Источники информации 3. Патент SU №1620448, 5 МПК С08G 18/32. Способ получения полиуретановых эластомеров, 15.01.1991. 4. Вацуро К.В., Мищенко Г.Л. Именные реакции в органической химии. – М.: Химия, 1976. – С.59-60. 6. Патент RU №2213735, 7 МПК C07D 217/02. Способ получения 3,3-диметил-3,4-дигидроизохинолинов, 10.10.2003. 7. Патент US №6956033, 7 МПК C07D 401/02. 3,4-Dihydroisoquinoline derivative compound and a pharmaceutical agent comprising it active ingredient, 18.10.2005.
Формула изобретения
Способ получения 1-замещенных 3,3,4,4-тетраметил-3,4-дигидроизохинолинов общей формулы 2
где R – Me, SMe, Ph, CH2CONH2, CH2COOEt, взаимодействием смеси эквимолярных количеств 3,3-диметил-2-фенилбутанола-2 и нитрилов в среде концентрированной серной кислоты с последующим выделением целевых продуктов известными приемами.
|
||||||||||||||||||||||||||

 -фенэтиламидов с дегидратирующими агентами [4]. К недостаткам данного способа следует отнести крайне низкие (2-3%) выходы целевых продуктов при использовании в реакции амидов, полученных из пространственно затрудненных аминов при третичном атоме углерода.
-фенэтиламидов с дегидратирующими агентами [4]. К недостаткам данного способа следует отнести крайне низкие (2-3%) выходы целевых продуктов при использовании в реакции амидов, полученных из пространственно затрудненных аминов при третичном атоме углерода.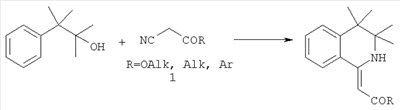
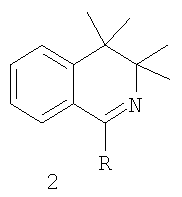
 , м.д. (ДМСО-d6, Mercury plus300, 300 MHz): 1.12 (с, 6Н, 2СН3); 1.18 (с, 6Н, 2СН3); 4.88 (уш.с, 2Н, NH2); 4.96 (с, 1Н, =СН); 7.18-7-41 (м, 3Н, Наром.); 7.57 (д, 1Н, 8-Наром.). ИК спектр (вазелиновое масло),
, м.д. (ДМСО-d6, Mercury plus300, 300 MHz): 1.12 (с, 6Н, 2СН3); 1.18 (с, 6Н, 2СН3); 4.88 (уш.с, 2Н, NH2); 4.96 (с, 1Н, =СН); 7.18-7-41 (м, 3Н, Наром.); 7.57 (д, 1Н, 8-Наром.). ИК спектр (вазелиновое масло),  , см-1: 3360(NH); 3220(NH); 1630(С=O). Найдено, %: С 73.9; Н 8.40; N 11.5. C15H20N2O. Вычислено, %: С 73.74; Н 8.25; N 11.46.
, см-1: 3360(NH); 3220(NH); 1630(С=O). Найдено, %: С 73.9; Н 8.40; N 11.5. C15H20N2O. Вычислено, %: С 73.74; Н 8.25; N 11.46.