|
(21), (22) Заявка: 2006129019/15, 10.08.2006
(24) Дата начала отсчета срока действия патента:
10.08.2006
(46) Опубликовано: 27.05.2008
(15) Информация о коррекции:
Версия коррекции № 1 (0,5×(ОПк К+1+ОП К- ср.). Значения ОП К- после добавления нейтрализующего и контрольного реагентов должны быть ниже значения ОП критического (ОП крит.), т.е. ОПн К- и ОПк К-<ОП крит. ОП крит. рассчитывают по формуле:
ОП крит. = ОП К- ср. + 0,06, где 0,06 – коэффициент, определяемый методом статистической обработки результатов постановки ИФА на предприятии-изготовителе.
Реакцию считают положительной, если значение ОП в лунке с образцом равно или превышает ОП крит.
Слабоположительный контрольный образец, содержащий HBsAg в концентрации 0,04±0,02 МЕ/мл, должен давать положительную реакцию.
Интерпретация результатов
Образец считают содержащим HBsAg, если
а) ОПк 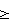 ОП крит., ОП крит.,
б) ОПн  0,5×(ОПк+ОП К- ср.), 0,5×(ОПк+ОП К- ср.),
где ОПк – ОП образца с контрольным реагентом, а ОПн – ОП образца с нейтрализующим реагентом. В этом случае присутствие в образце HBsAg следует считать доказанным и дальнейшая проверка не требуется.
Определение аналитической чувствительности тест-системы «ДС-ИФА-HBsAg-0,01» проводилось с использованием Отраслевого Стандартного Образца HBsAg вируса гепатита В ОСО 42-28-311-03П (ООО НПО «Диагностические системы»), откалиброванного по Международному Стандарту – Second International Standard for HBsAg, subtype adw2, genotype A, NIBSC code number: 00/588, в сравнении с тест-системой «ДС-ИФА-HBsAg» и «Hepanostika HBsAg ULTRA» (Biomerieux). Были приготовлены 10 последовательных разведений ОСО от 1 МЕ/мл до 0,01 МЕ/мл, с нормальной донорской плазмой, не содержащей антител к HBsAg. Полученные данные представлены в таблице 1.
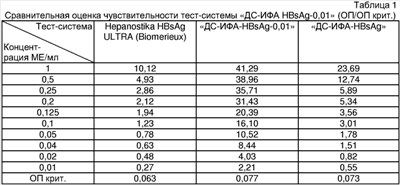
Аналитическая чувствительность тест-системы «ДС-ИФА-HBsAg-0,01» составила 0,01 МЕ/мл.
Оценка клинической чувствительности тест-системы «ДС-ИФА-HBsAg-0,01» проводилась с использованием стандартных панелей сывороток, содержащих и не содержащих HBsAg.
В таблице 2 представлены результаты сравнительного тестирования стандартной панели сывороток, содержащих и не содержащих HBsAg (ЗАО «Вектор-Бест»), серия 001.
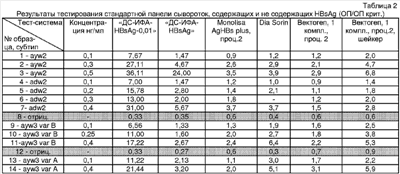
Была проведена сравнительная характеристика чувствительности и специфичности четырех тест-систем с использованием референс-панели сывороток крови человека, содержащих и не содержащих поверхностный антиген вируса гепатита В (HBsAg) субтипы ау и ad OCO 42-28-364-04П (Медицинский центр «Авиценна», Бостон Биомедика), серия №1. Полученные данные приведены в таблице 3.
| Таблица 3 |
| Результаты тестирования референс-панели сывороток крови человека, содержащих и не содержащих поверхностный антиген вируса гепатита В (HBsAg) субтипы ay и ad (ОП/ОП крит.) |
| № |
Субтип HBsAg |
Концентрация HBsAg нг/мл |
«ДС-ИФА-HBsAg-0,01» |
Abbott Auszyme EIA |
ИФА-HBsAg/м (ООО НПО «Диагностические системы», Россия) |
BIO-RAD Genetic systems HBsAg EIA |
| 01 |
– |
– |
0,68 |
0,1 |
0,26 |
Отр |
| 02 |
– |
– |
0,53 |
0,1 |
0,33 |
Отр |
| 03 |
– |
– |
0,49 |
0,1 |
0,13 |
Отр |
| 04 |
– |
– |
0,38 |
0,1 |
0,29 |
Отр |
| 05 |
ad |
1 |
40,11 |
3,4 |
21,50 |
Поз |
| 06 |
ad |
0,6 |
39,73 |
2,2 |
12,50 |
Поз |
| 07 |
ad |
0,2 |
17,22 |
1,0 |
3,22 |
Поз |
| 08 |
ay |
0,9 |
39,62 |
3,5 |
12,70 |
Поз |
| 09 |
ay |
0,8 |
39,94 |
3,1 |
13,10 |
Поз |
| 10 |
ay |
0,6 |
38,31 |
2,1 |
12,20 |
Поз |
| 11 |
ay |
0,4 |
30,35 |
1,4 |
4,37 |
Поз |
| 12 |
ay |
0,2 |
17,76 |
0,7 |
3,51 |
Поз |
| 13 |
ay |
0,1 |
7,31 |
0,4 |
1,21 |
Поз |
| 14 |
Неразв. образец |
2-3 |
42,26 |
8,2 |
23,98 |
Поз |
| 15 |
Неразв. образец |
2-3 |
40,85 |
10,1 |
22,17 |
Поз |
| 16 |
Неразв. образец |
1-1,5 |
42,51 |
4,0 |
28,23 |
Поз |
| 17 |
Неразв. образец |
0,5-0,7 |
40,87 |
2,0 |
19,52 |
Поз |
| 18 |
Неразв.
образец |
0,5-0,7 |
40,03 |
2,5 |
15,10 |
Поз |
| 19 |
Неразв. образец |
0,1-0,25 |
25,27 |
1,2 |
5,33 |
Поз |
| 20 |
Неразв. образец |
0,1-0,25 |
19,54 |
0,6 |
3,62 |
Поз |
В таблице 4 представлены результаты сравнительного исследования клинической чувствительности тест-системы «ДС-ИФА-HBsAg-0,01» с использованием панелей производства BBI Diagnostics (Boston Biomedica Inc. (BBI), West Bridgewater, Mass., USA) и Zeptometrix Corporation.
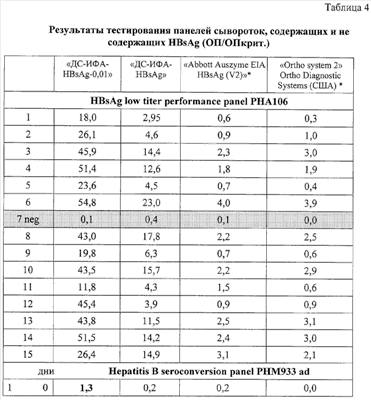
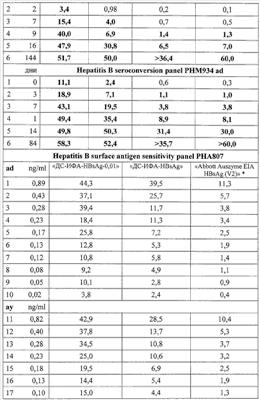
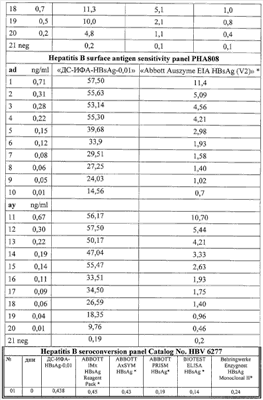
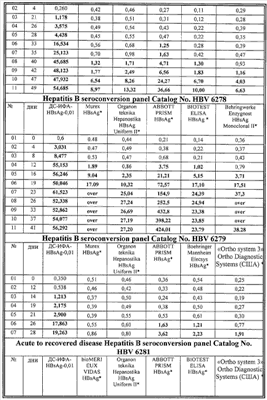
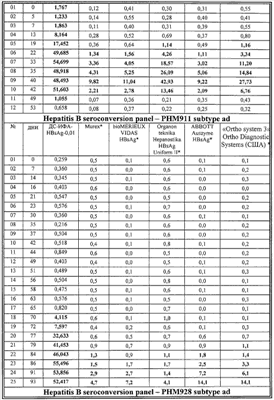
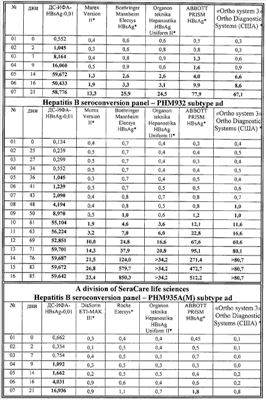
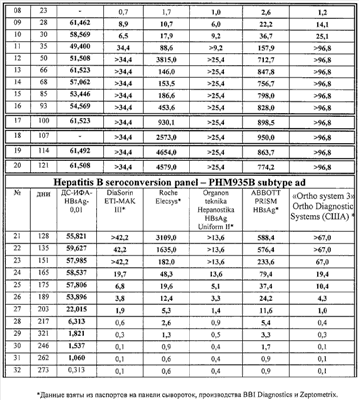
Новый тест с идентичной чувствительностью выявляет HBsAg субтипов ad и ay со значительным преимуществом относительно теста сравнения – системы Abbott Auszyme EIA HBsAg (V2). Из данных таблиц видно, что тест-система «ДС-ИФА-HBsAg-0,01» с идентичной чувствительностью определяет HBsAg субтипов ay и ad во всех позитивных образцах, представленных в панелях. Коэффициенты позитивности многих HBsAg-положительных образцов в тест-системе «ДС-ИФА-HBsAg-0,01» существенно превышают коэффициенты позитивности этих же образцов, протестированных на альтернативных тестах. В образцах низкотитражной панели (от 0,05 до 0,6 IU/ml) новая тест-система позволяет также детектировать HBsAg с более высокими коэффициентами позитивности в сравнении с альтернативными тестами.
Анализ сероконверсионных панелей показал, что тест-система «ДС-ИФА-HBsAg-0,01» позволяет детектировать HBsAg в положительных образцах на более раннем сроке его появления, по сравнению с зарубежными тест-системами, данные по которым приведены в паспортах к панелям. По результатам анализа двух панелей образцов, полученных от одного донора в динамике в период сероконверсии (от момента появления до момента исчезновения HBsAg) (РНМ935А (М) и РНМ935 В), следует, что новая система в сравнении с альтернативными тестами импортного производства начинает выявлять HBsAg на более раннем сроке его появления и продолжает определять на более позднем сроке по мере его исчезновения, в результате чего позитивный по HBsAg период увеличивается на 28 дней в сравнении с системой Abbott Prism HBsAg*.
Было установлено, что использование тест-системы «ДС-ИФА-HBsAg-0,01» для анализа образцов сероконверсионных панелей позволяет выявлять HBsAg одновременно с вирусной ДНК (BBI-PHM933, BBI-PHM934, BBI-РНМ935А (М), ZeptoMetrix Corporation Cat. No. HBV6281), а в двух случаях (ZeptoMetrix Corporation Cat. No. HBV6277 и Cat. No. HBV6279) опережает время 1-ой детекции ДНК.
Известно, что существует проблема выявления HBsAg при коинфицировании. Было проанализировано 473 образца сыворотки крови анти-ВИЧ-позитивных лиц. Среди них в 66 был выявлен HBsAg в тесте «ДС-ИФА-HBsAg». Дополнительно выявлено 16 образцов, содержащих HBsAg в концентрации ниже 0,1 МЕ/мл. Причем 7 из них содержали антитела к HBcore-антигену, а 9 образцов не имели никаких других маркеров, кроме HBsAg, детектируемого только в системе с высокой чувствительностью (таблица 5). Следовательно, повышение чувствительности тестов для выявления HBsAg позволит снизить количество случаев скрытого гепатита В как с наличием дополнительного маркера анти-НВс, так и при отсутствии любых маркеров.
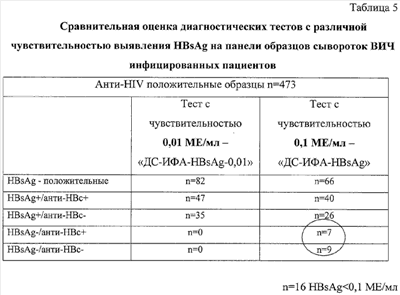
При тестировании 3348 образцов сыворотки крови доноров и 381 образца сыворотки крови беременных женщин в тест-системе «ДС-ИФА-HBsAg-0,01» было выявлено 6 и 1 образец, соответственно, содержащих HBsAg в концентрации ниже 0,1 МЕ/мл.
За счет повышенной чувствительности нового теста мутантные варианты HBsAg показывают более высокую реактивность в сравнении с другими системами (таблица 6).
| Таблица 6 |
| Сравнительное определение мутантных форм рекомбинатного HBsAg (ОПm/ОП крит.) |
| adw2 |
ДС-ИФА-HBsAg |
ДС-ИФА-HBsAg-0,01 |
“Hepanostika” (Biomerieux) |
«Рекоматгеп-В-стрип» (Эколаб) |
«Вектогеп-HBsAg-стрип» компл. №4 |
| K141Е |
1,6 |
10,4 |
8,6 |
1,3 |
2,2 |
| Q129H |
1,2 |
13,0 |
16,6 |
1,4 |
2,3 |
| Q129L |
1,5 |
14,1 |
11,0 |
1,7 |
1,2 |
| M133L |
2,8 |
16,9 |
13,6 |
1,6 |
2,2 |
| T126N |
2,9 |
17,7 |
8,1 |
1,6 |
1,4 |
| G145RI |
1,4 |
9,1 |
5,8 |
1,2 |
1,7 |
| G145RII |
1,6 |
15,7 |
18,8 |
1,2 |
0,8 |
| K142S |
2,0 |
5,6 |
44,1 |
1,5 |
1,3 |
| P142S |
1,5 |
11,8 |
54,8 |
1,5 |
1,4 |
| Т143К |
1,5 |
11,7 |
2,9 |
1,2 |
0,6 |
| K141BI |
3,6 |
2,5 |
54,6 |
0,9 |
0,9 |
| ayw1 G145R |
2,5 |
27,4 |
45,1 |
2,1 |
3,3 |
Для оценки специфичности тест-системы «ДС-ИФА-HBsAg-0,01» были использованы образцы сыворотки крови доноров; образцы сыворотки крови больных с различными инфекционными заболеваниями, не связанными с HBV-пневмонией, ангиной, бронхитом, вирусным гепатитом С; образцы сыворотки крови больных с различными неинфекционными заболеваниями – с патологией сердечно-сосудистой системы, желудочно-кишечного тракта, онкозаболеваниями и др.; образцы сыворотки крови беременных женщин; образцы сыворотки крови ВИЧ-инфицированных лиц. Всего протестировано 4710 образцов. Данные по числу ложноположительных результатов в тест-системе «ДС-ИФА-HBsAg-0,01» в группе здоровых и различных группах больных представлены в таблице 7.
| Таблица 7 |
| Оценка специфичности тест-системы «ДС-ИФА-HBsAg-0,01» на разных категориях населения |
| Обследуемая группа |
Количество исследуемых образцов |
Количество ложноположительных результатов |
% специфичности в данной группе |
| Здоровые доноры |
3348 |
7 |
99,8 |
| Больные с различными инфекционными заболеваниями, не связанными с вирусным гепатитом В |
392 |
5 |
98,7 |
| Больные с различными неинфекционными заболеваниями |
95 |
1 |
98,9 |
| Беременные женщины |
381 |
3 |
99,2 |
| ВИЧ-инфицированные |
494 |
4 |
99,2 |
| Всего |
4710 |
20 |
99,6 |
Таким образом, проведенные исследования показали, что специфичность тест-системы «ДС-ИФА-HBsAg-0,01» составляет 99,6% при исследовании образцов сыворотки крови нормальных доноров и больных с различными инфекционными и соматическими заболеваниями.
Была изучена возможность использования нового теста для детекции HBsAg в препаратах крови. В ходе исследований анализировался широкий спектр препаратов крови разных фирм-производителей: альбумин, фибринолизин, лейкоцитарный интерферон, иммуноглобулин нормальный для внутривенного введения и внутримышечного введения, иммуноглобулин противоаллергический и иммуноглобулин антистафилококковый. Жидкие препараты крови используют неразведенными; лиофильно высушенные препараты крови перед исследованием в тест-системе разводят в соответствии с инструкцией по применению данного препарата. Специфичность тест-системы по отношению к препаратам крови (были взяты пять разных серий препаратов) была исследована на трех экспериментально-производственных сериях тест-системы (таблица 8).
| Таблица 8 |
| Специфичность тест-системы «ДС-ИФА-HBsAg-0,01», установленная при исследовании препаратов крови |
| Наименование препарата |
ОП препаратов (о.е.) средняя (n=5) для каждой серии тест-системы |
| С.1 |
С.2 |
С.3 |
| Альбумин |
0,017 |
0,025 |
0,032 |
| Фибринолизин |
0,007 |
0,009 |
0,005 |
| Иммуноглобулин внутривенный |
0,009 |
0,011 |
0,015 |
| Иммуноглобулин внутримышечный |
0,014 |
0,008 |
0,010 |
| Интерферон |
0,005 |
0,007 |
0,008 |
| ОП крит.(о. е.) |
0,072 о.е. |
0,069 о.е. |
0,075 о.е. |
Из данных таблицы видно, что значения ОП всех препаратов были ниже ОП крит. (о.е.), т.е. тест-система «ДС-ИФА-HBsAg-0,01» показала 100% специфичность при тестировании препаратов крови.
Преимущество предлагаемой тест-системы для выявления HBsAg «ДС-ИФА-HBsAg-0,01» заключается в возможности детекции HBsAg в сыворотке (плазме) и препаратах крови с чувствительностью 0,01 МЕ/мл при сохранении высокой специфичности.
Формула изобретения
1. Тест-система для определения поверхностного антигена вирусного гепатита В (HBsAg) методом иммуноферментного анализа в биологическом образце, характеризующаяся тем, что содержит твердую фазу, содержащую иммуносорбент, представляющий собой сорбированные на стрипах планшета моноклональные антитела мыши к HBsAg; конъюгат-1 – биотин с моноклональными антителами к HBsAg и конъюгат-2 – стрептавидин, меченный пероксидазой хрена, представленные в виде жидких концентратов; положительный контрольный образец; отрицательный контрольный образец; промывочный раствор; растворы для разведения конъюгатов; субстратный буферный раствор; тетраметилбензидин в качестве хромогена; серную кислоту в качестве стоп-реагента; нейтрализующий реагент, жидкий или лиофилизированный, представляющий собой иммуноглобулины козы, содержащие антитела к HBsAg; контрольный реагент, жидкий или лиофилизированный, представляющий собой иммуноглобулины козы, не содержащие антител к HBsAg; слабоположительный контрольный образец, представляющий собой сыворотку крови в лиофилизированном виде, содержащую HBsAg в концентрации 0,02-0,06 МЕ/мл.
2. Тест-система по п.1, отличающаяся тем, что биологический материал представляет собой сыворотку или плазму крови.
3. Тест-система по п.1, отличающаяся тем, что биологический материал представляет собой препарат крови, выбранный из группы альбумин, фибролизин, иммуноглобулин, лейкоцитарный интерферон.
4. Способ определения поверхностного антигена вирусного гепатита В (HBsAg) методом иммуноферментного анализа в биологическом образце с помощью тест-системы по п.1, включающий выдерживание контрольных и исследуемых биологических образцов, внесенных в лунки планшета с сорбированными моноклональными антителами мыши к HBsAg при температуре (42±0,5)°С с последующим добавлением окрашенного раствора конъюгата, который представляет собой моноклональные антитела к HBsAg, связанные с биотином, а затем без стадии отмывки инкубационную смесь тщательно смешивают и выдерживают с окрашенным раствором конъюгата, представляющего собой стрептавидин, меченный пероксидазой хрена, при температуре (42±0,5)°С, реакцию останавливают добавлением стоп-реагента и проводят учет результатов спектрофотометрическим методом.
TH4A – Переиздание описания изобретения к патенту Российской Федерации
Причина переиздания: Коррекция названия изобретения
Извещение опубликовано: 27.11.2008 БИ: 33/2008
TK4A – Поправки к публикациям сведений об изобретениях в бюллетенях “Изобретения (заявки и патенты)” и “Изобретения. Полезные модели”
Напечатано: (54) Иммуноферментная тест-система для определения поверхностного антигена вируса гепатита В и способ определения поверхностного антитела вирусного гепатита В
Следует читать: (54) Иммуноферментная тест-система для определения поверхностного антигена вируса гепатита В и способ определения поверхностного антигена вирусного гепатита В
Номер и год публикации бюллетеня: 15-2008
Код раздела: FG4A
Извещение опубликовано: 27.11.2008 БИ: 33/2008
|
|