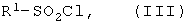Патент на изобретение №2325390
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ 2-СУЛЬФОНИЛАМИНО-1,2,4,-ТРИАЗОЛО[1,5-a] ПИРИМИДИНОВ
(57) Реферат:
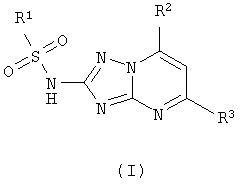
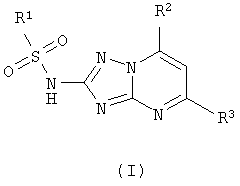
Изобретение относится к области получения органических веществ и может быть использовано в производстве гербицидов и других биологически активных соединений. Способ получения 2-сульфониламино-1,2,4-триазоло[1,5-а]пиримидинов общей формулы (I), где R1 представляет собой метильную, фенильную, 4-метилфенильную, 4-хлорфенильную группу, R2 представляет собой фенильную, 4-метилфенильную, 4-хлорфенильную, 4-метоксифенильную группу, R3 представляет собой метильную, фенильную, 4-метилфенильную, 4-хлорфенильную группу, осуществляется сульфонилированием 2-амино-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидинов (II) сульфохлоридами (III) в пиридине и окислением образовавшихся 2-сульфониламино-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидинов (IV) бромом в уксусной кислоте в присутствии ацетата натрия. Способ позволяет получать 2-сульфониламино-1,2,4-триазоло[1,5-а]пиримидины общей формулы (I) из дешевого и доступного сырья без применения сложных технологических операций.
Изобретение относится к области получения органических веществ и может быть использовано в производстве гербицидов и других биологически активных соединений. 3, а заместитель в положении 2 не является арилсульфониламиногруппой. Основным недостатком этого способа является низкая региоселективность реакции циклоконденсации и возможность образования смеси изомерных продуктов при использовании несимметричных 1,3-дикарбонильных соединений (R2
Задачей изобретения является разработка способа получения 2-сульфониламино-1,2,4-триазоло[1,5-а]пиримидинов общей формулы (I) из дешевых и доступных исходных веществ, позволяющего повысить выход целевых продуктов и сократить время синтеза. Поставленная задача достигается за счет сульфонилирования 2-амино-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидинов (II) сульфохлоридами (III) в пиридине и окисления полученных 2-сульфониламино-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидинов (IV) бромом (Br2) в уксусной кислоте в присутствии ацетата натрия (СН3COONa) В предлагаемом способе получения 2-сульфониламино-1,2,4-триазоло[1,5-а]пиримидинов общей формулы (I) к 2-амино-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидину общей формулы (II) прибавляют сульфохлорид (III) при мольном соотношении (II):(III)=1:1.1-1.3 и кипятят в пиридине. К раствору прибавляют воду, выпавший осадок 2-сульфониламино-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина общей формулы (IV) отфильтровывают, смешивают с ацетатом натрия и уксусной кислотой, к полученной смеси прибавляют бром при мольном соотношении (IV):(Br2):(CH3COONa)=1:1.00-1.05:2.1-2.2 при температуре 0-25°С и перемешивании. Затем к полученному раствору прибавляют воду, осадок 2-сульфониламино-1,2,4-триазоло[1,5-а]пиримидина общей формулы (I) отфильтровывают и перекристаллизовывают. Исследования показали, что изменение мольного соотношения (II):(III)=1:1.1-1.3 на стадии сульфонилирования приводит либо к неполному протеканию реакции и неудовлетворительной чистоте соединений (IV) (пример 6, 7), либо к перерасходу реагентов, что экономически неоправданно. Мольное соотношение (IV):(Br2):(СН3COONa)=1:1.00-1.05:2.1-2.2 на стадии окисления является оптимальным. Изменение соотношения приводит либо к неполному протеканию реакции, либо к образованию побочных продуктов, загрязняющих целевые соединения (пример 6). Проведение реакции при температуре ниже 0°С снижает скорость протекания процесса и приводит к увеличению продолжительности синтеза, что технически нецелесообразно. Повышение температуры выше 25°С уменьшает выход целевых продуктов вследствие протекания побочных реакций (пример 7). Пример 1 К смеси 1.0 г (4.4 ммоль) 2-амино-5-метил-7-фенил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина и 5 мл пиридина присыпают при перемешивании 1.0 г (5.3 ммоль) п-толуолсульфохлорида. Реакционную смесь кипятят с обратным холодильником 10-15 мин, охлаждают до 20°С и разбавляют 10 мл воды. Выпавший осадок отфильтровывают. Получают 1.4 г (87%) 2-[(4-метилфенил)сульфониламино]-5-метил-7-фенил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина. Тпл 226-228°С. Спектр ЯМР 1Н, Найдено (%): С 59.74; Н 5.04; N 18.39. C19H19N5O2S Вычислено (%): С 59.83; Н 5.02; N 18.36. К смеси 1.0 г (2.6 ммоль) 2-[(4-метилфенил)сульфониламино]-5-метил-7-фенил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина, 0.44 г (5.2 ммоль) ацетата натрия и 2 мл уксусной кислоты приливают 0.14 мл (2.6 ммоль) брома. Реакционную массу перемешивают при температуре 0-25°С в течение 20-30 мин, затем разбавляют 10 мл воды. Выпавший осадок отфильтровывают. Получают 0.9 г (90%) 2-[(4-метилфенил)сульфониламино]-5-метил-7-фенил-1,2,4-триазоло[1,5-а]пиримидина. Тпл 284-285°С (из смеси ДМФА/этанол 1:5). Спектр ЯМР 1Н, Найдено (%): С 60.19; Н 4.26; N 18.28. C19H17N5O2S Вычислено (%): С 60.14; Н 4.52; N 18.46. Пример 2 К смеси 1.0 г (3.5 ммоль) 2-амино-5,7-дифенил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина и 5 мл пиридина присыпают при перемешивании 0.8 г (3.8 ммоль) п-хлорбензолсульфохлорида. Реакционную смесь кипятят с обратным холодильником 15-20 мин, охлаждают до 20°С и разбавляют 10 мл воды. Выпавший осадок отфильтровывают. Получают 1.6 г (69%) 2-[(4-хлорфенил)сульфониламино]-5,7-дифенил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина. Тпл 274-276°С. Спектр ЯМР 1Н, Найдено (%): С 59.60; Н 4.01; N 15.29. C23H18N5ClO2S Вычислено (%): С 59.54; Н 3.91; N 15.10. К смеси 1.0 г (2.2 ммоль) 2-[(4-хлорфенил)сульфониламино]-5,7-дифенил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина, 0.38 г (4.6 ммоль) ацетата натрия и 2 мл уксусной кислоты приливают 0.12 мл (2.3 ммоль) брома. Реакционную массу перемешивают при температуре 0-25°С в течение 20-25 мин, затем разбавляют 10 мл воды. Выпавший осадок отфильтровывают. Получают 0.96 г (94%) 2-[(4-хлорфенил)сульфониламино]-5,7-дифенил-1,2,4-триазоло[1,5-а]пиримидина. Тпл 276-277°С (из смеси ДМФА/этанол 1:5). Спектр ЯМР 1Н, Найдено (%): С 60.02; Н 3.26; N 15.38. C23H16N5ClO2S Вычислено (%): С 59.80; Н 3.49; N 15.16. Пример 3 К смеси 1.0 г (3.3 ммоль) 2-амино-5-фенил-7-(4-метилфенил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина и 5 мл пиридина приливают при перемешивании 0.3 мл (4.3 ммоль) метансульфохлорида. Реакционную смесь кипятят с обратным холодильником 15-20 мин, охлаждают до 20°С и разбавляют 10 мл воды. Выпавший осадок отфильтровывают. Получают 0.75 г (60%) 2-метилсульфониламино-5-фенил-7-(4-метилфенил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина. Тпл 238-240°С. Спектр ЯМР 1Н, Найдено (%): С 59.70; Н 5.05; N 18.29. C19H19N5O2S Вычислено (%): С 59.83; Н 5.02; N 18.36. К смеси 1.0 г (2.6 ммоль) 2-метилсульфониламино-5-фенил-7-(4-метилфенил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина, 0.45 г (5.5 ммоль) ацетата натрия и 2 мл уксусной кислоты приливают 0.14 мл (2.7 ммоль) брома. Реакционную массу перемешивают при температуре 0-25°С в течение 25-30 мин, затем разбавляют 10 мл воды. Выпавший осадок отфильтровывают. Получают 0.89 г (90%) 2-метилсульфониламино-5-фенил-7-(4-метилфенил)-1,2,4-триазоло[1,5-а]пиримидина. Тпл 288-289°С (из смеси ДМФА/этанол 1:5). Спектр ЯМР 1Н, Найдено (%): С 60.01; Н 4.16; N 18.58. C19H17N5O2S Вычислено (%): С 60.14; Н 4.52; N 18.46. Пример 4 К смеси 1.0 г (3.3 ммоль) 2-амино-5-(4-метилфенил)-7-фенил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина и 5 мл пиридина приливают при перемешивании 0.5 мл (4.0 ммоль) бензолсульфохлорида. Реакционную смесь кипятят с обратным холодильником 10-15 мин, охлаждают до 20°С и разбавляют 10 мл воды. Выпавший осадок отфильтровывают. Получают 0.86 г (59%) 2-фенилсульфониламино-5-(4-метилфенил)-7-фенил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина. Тпл 250-252°С. Спектр ЯМР 1Н, Найдено (%): С 64.89; Н 5.06; N 15.28. C24H21N5O2S Вычислено (%): С 64.99; Н 4.77; N 15.79. К смеси 1.0 г (2.2 ммоль) 2-фенилсульфониламино-5-(4-метилфенил)-7-фенил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина, 0.39 г (4.6 ммоль) ацетата натрия и 2 мл уксусной кислоты приливают 0.12 мл (2.3 ммоль) брома. Реакционную массу перемешивают при температуре 0-25°С в течение 20-25 мин, затем разбавляют 10 мл воды. Выпавший осадок отфильтровывают. Получают 0.87 г (90%) 2-фенилсульфониламино-5-(4-метилфенил)-7-фенил-1,2,4-триазоло[1,5-а]пиримидина. Тпл>320°С (из смеси ДМФА/этанол 1:5). Спектр ЯМР 1Н, Найдено (%): С 65.01; Н 4.21; N 15.58. C24H19N5O2S Вычислено (%): С 65.29; Н 4.34; N 15.86. Пример 5 К смеси 1.0 г (3.1 ммоль) 2-амино-5-фенил-7-(4-метоксифенил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина и 5 мл пиридина присыпают при перемешивании 0.7 г (3.4 ммоль) п-хлорбензолсульфохлорида. Реакционную смесь кипятят с обратным холодильником 10-15 мин, охлаждают до 20°С и разбавляют 10 мл воды. Выпавший осадок отфильтровывают. Получают 1.1 г (71%) 2-[(4-хлорфенил)сульфониламино]-5-фенил-7-(4-метоксифенил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина. Тпл 256-257°С. Спектр ЯМР 1Н, Найдено (%): С 59.50; Н 3.98; N 14.22. С24Н20N5ClO3S Вычислено (%): С 59.36; Н 4.08; N 14.18. К смеси 1.0 г (2.0 ммоль) 2-[(4-хлорфенил)сульфониламино]-5-фенил-7-(4-метоксифенил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина, 0.34 г (4.2 ммоль) ацетата натрия и 2 мл уксусной кислоты приливают 0.11 мл (2.0 ммоль) брома. Реакционную массу перемешивают при температуре 0-25°С в течение 25-30 мин, разбавляют 10 мл воды. Выпавший осадок отфильтровывают. Получают 0.89 г (91%) 2-[(4-хлорфенил)сульфониламино]-5-фенил-7-(4-метоксифенил)-1,2,4-триазоло[1,5-а]пиримидина. Тпл 280-282°С (из смеси ДМФА/этанол 1:5). Спектр ЯМР 1Н, Найдено (%): С 58.73; Н 3.51; N 14.57. С24Н18N5ClO3S Вычислено (%): С 58.60; Н 3.69; N 14.24. Пример 6 К смеси 1.0 г (3.1 ммоль) 2-амино-5-фенил-7-(4-метоксифенил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина и 5 мл пиридина присыпают при перемешивании 0.7 г (3.1 ммоль) п-хлорбензолсульфохлорида. Реакционную смесь кипятят с обратным холодильником 15-20 мин, охлаждают до 20°С и разбавляют 10 мл воды. Выпавший осадок отфильтровывают. Получают 0.8 г (52%) 2-[(4-хлорфенил)сульфониламино]-5-фенил-7-(4-метоксифенил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина. Тпл 254-255°С. Спектр ЯМР 1Н, Найдено (%): С 59.50; Н 3.98; N 14.22. С24Н20N5ClO3S Вычислено (%): С 59.36; Н 4.08; N 14.18. К смеси 1.0 г (2.0 ммоль) 2-[(4-хлорфенил)сульфониламино]-5-фенил-7-(4-метоксифенил)-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина, 0.34 г (4.2 ммоль) ацетата натрия и 2 мл уксусной кислоты приливают 0.14 мл (2.5 ммоль) брома. Реакционную массу перемешивают при температуре 0-25°С в течение 25-30 мин, затем разбавляют 10 мл воды. Выпавший осадок отфильтровывают. Получают 0.68 г (70%) 2-[(4-хлорфенил)сульфониламино]-5-фенил-7-(4-метоксифенил)-1,2,4-триазоло[1,5-а]пиримидина. Тпл 280-282°С (из смеси ДМФА/этанол 1:5). Спектр ЯМР 1Н, Найдено (%): С 58.73; Н 3.51; N 14.57. C24H18N5ClO3S Вычислено (%): С 58.60; Н 3.69; N 14.24. Пример 7 К смеси 1.0 г (4.4 ммоль) 2-амино-5-метил-7-фенил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина и 5 мл пиридина присыпают при перемешивании 1.4 г (7.5 ммоль) п-толуолсульфохлорида. Реакционную смесь кипятят с обратным холодильником 10-15 мин, охлаждают до 20°С и разбавляют 10 мл воды. Выпавший аморфный осадок промывают 2 раза водой (10 мл) и отфильтровывают. Получают 1.2 г (75%) 2-[(4-метилфенил)сульфониламино]-5-метил-7-фенил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина. Тпл 224-228°С. Спектр ЯМР 1Н, Найдено (%): С 59.74; Н 5.04; N 18.39. C19H19N5O2S Вычислено (%): С 59.83; Н 5.02; N 18.36. К смеси 1.0 г (2.6 ммоль) 2-[(4-метилфенил)сульфониламино]-5-метил-7-фенил-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидина и 0.44 г (5.2 ммоль) ацетата натрия в 2 мл уксусной кислоты приливают 0.14 мл (2.6 ммоль) брома. Реакционную массу перемешивают при температуре 35-40°С в течение 25-30 мин, затем разбавляют 10 мл воды. Выпавший осадок отфильтровывают. Получают 0.6 г (61%) 2-[(4- метилфенил)сульфониламино]-5-метил-7-фенил-1,2,4-триазоло[1,5-а]пиримидина. Тпл 284-285°С (из смеси ДМФА/этанол 1:5). Спектр ЯМР 1Н, Найдено (%): С 60.19; Н 4.26; N 18.28. C19H17N5O2S Вычислено (%): С 60.14; Н 4.52; N 18.46.
Формула изобретения
Способ получения 2-сульфониламино-1,2,4-триазоло[1,5-а]пиримидинов общей формулы (I)
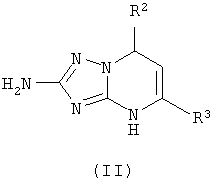
где R1 представляет собой метильную, фенильную, 4-метилфенильную, 4-хлорфенильную группу, R2 представляет собой фенильную, 4-метилфенильную, 4-хлорфенильную, 4-метоксифенильную группу, R3 представляет собой метильную, фенильную, 4-метилфенильную, 4-хлорфенильную группу, включающий сульфонилирование сульфохлоридами в присутствии пиридина, отличающийся тем, что к смеси 2-амино-4,7-дигидро-1,2,4-триазоло[1,5-а] пиримидина формулы (II)
где R2 и R3 имеют указанные значения, и пиридина прибавляют сульфохлорид общей формулы (III)
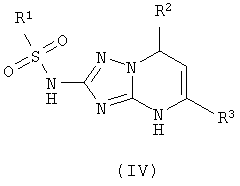
где R1 имеет указанные выше значения, при мольном соотношении (II):(III)=1:1.1-1.3, реакционную смесь кипятят с обратным холодильником, разбавляют водой, 2-сульфониламино-4,7-дигидро-1,2,4-триазоло[1,5-а]пиримидин общей формулы (IV)
где R1, R2 и R3 имеет указанные значения, отфильтровывают, смешивают с уксусной кислотой и ацетатом натрия, затем прибавляют бром при мольном соотношении (IV):(Br2):(СН3COONa)=1:1,00-1,05:2,1-2,2 и перемешивают при температуре 0-25°С.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 30.01.2009
Извещение опубликовано: 20.07.2010 БИ: 20/2010
|
||||||||||||||||||||||||||

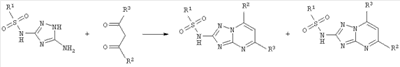
 R3), а также высокая стоимость исходных 3-арисульфониламино-5-амино-1,2,4-триазолов и 1,3-дикарбонильных соединений.
R3), а также высокая стоимость исходных 3-арисульфониламино-5-амино-1,2,4-триазолов и 1,3-дикарбонильных соединений. -дефицитного пиримидинового цикла, сопряженного с триазольным кольцом, а также высокая стоимость исходных 2-амино-1,2,4-триазоло[1,5-а]пиримидинов.
-дефицитного пиримидинового цикла, сопряженного с триазольным кольцом, а также высокая стоимость исходных 2-амино-1,2,4-триазоло[1,5-а]пиримидинов.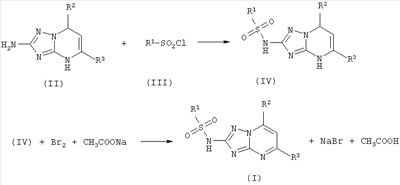
 , м.д. (J, Гц) (ДМСО-d6): 1.79 с (3Н, СН3), 2.34 с (3Н, СН3), 4.50 д (1Н, СН, J=3.7), 5.79 д (1Н, СН, J=3.7), 7.07 м (2Н, аром.), 7.24-7.30 м (5Н, аром.), 7.63 м (2Н, аром.), 9.56 с (1Н, NH), 10.71 с (1Н, NH).
, м.д. (J, Гц) (ДМСО-d6): 1.79 с (3Н, СН3), 2.34 с (3Н, СН3), 4.50 д (1Н, СН, J=3.7), 5.79 д (1Н, СН, J=3.7), 7.07 м (2Н, аром.), 7.24-7.30 м (5Н, аром.), 7.63 м (2Н, аром.), 9.56 с (1Н, NH), 10.71 с (1Н, NH).