|
|
(21), (22) Заявка: 2007116602/15, 02.05.2007
(24) Дата начала отсчета срока действия патента:
02.05.2007
(46) Опубликовано: 27.05.2008
(56) Список документов, цитированных в отчете о
поиске:
RU 2251546 C1, 10.05.2005. RU 2189817 С1, 27.09.2002. УШАКОВА Е.А. Проблемы применения гепатопротекторов, ФАРМАТЕКА, 2004, №4, с.45-55.
Адрес для переписки:
214019, г.Смоленск, ул. Крупской, 28, ГОУ ВПО Смоленская государственная медицинская академия федерального агентства по здравоохранению и социальному развитию
|
(72) Автор(ы):
Климкина Елена Ивановна (RU),
Смирнов Леонид Дмитриевич (RU)
(73) Патентообладатель(и):
ГОУ ВПО Смоленская государственная медицинская академия федерального агентства по здравоохранению и социальному развитию (RU)
|
(54) ГЕПАТОПРОТЕКТОР
(57) Реферат:
Изобретение относится к области медицины и касается применения 2,6-диметил-3-оксипиридина адамантилкарбоксилата в качестве гепатопротектора с высокой эффективностью. 3 ил., 3 табл.
Изобретение предназначено для использования в медицине и касается гепатопротекторных средств, относящихся к группе синтетических антигипоксантов и антиоксидантов.
Задачей изобретения является повышение эффективности терапии при поражениях печени токсической этиологии. Она решается применением в качестве гепатопротектора 2,6-диметил-3-оксипиридина адамантанкарбоксилата формулы
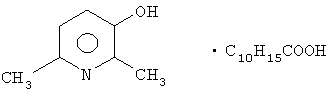
При экспериментальных исследованиях токсического гепатита было впервые выявлено его гепатопротекторное действие.
Пример. У крысы  массой 150 г вызывали токсическое повреждение печени ежедневным подкожным введением тетрахлорида углерода в виде 50% раствора в подсолнечном масле в дозе 0,6 мл 1 раз в день на протяжении 4-х первых дней опыта. Параллельно с тетрахлоридом углерода за один час до его введения вводили исследуемое соединение 1 раз в сутки первые 4 дня, затем еще три дня в дозе 10 мг/кг/сут внутрибрюшинно. На 8-е сутки от начала затравки животное было декапитировано с учетом требований этического комитета. В результате был произведен забор крови для получения сыворотки, в которой определяли активность печеночных трансаминаз (АлАТ, АсАТ), лактатдегидрогеназы (ЛДГ), а также активность перекисного окисления липидов (ПОЛ). Была забрана также ткань печени для гистологического исследования и для получения гомогената, в котором также определяли активность ПОЛ. массой 150 г вызывали токсическое повреждение печени ежедневным подкожным введением тетрахлорида углерода в виде 50% раствора в подсолнечном масле в дозе 0,6 мл 1 раз в день на протяжении 4-х первых дней опыта. Параллельно с тетрахлоридом углерода за один час до его введения вводили исследуемое соединение 1 раз в сутки первые 4 дня, затем еще три дня в дозе 10 мг/кг/сут внутрибрюшинно. На 8-е сутки от начала затравки животное было декапитировано с учетом требований этического комитета. В результате был произведен забор крови для получения сыворотки, в которой определяли активность печеночных трансаминаз (АлАТ, АсАТ), лактатдегидрогеназы (ЛДГ), а также активность перекисного окисления липидов (ПОЛ). Была забрана также ткань печени для гистологического исследования и для получения гомогената, в котором также определяли активность ПОЛ.
В результате биохимического исследования сыворотки крови было определено содержание АлАТ – 90 ед/л, что приближалось к показателям интактных животных (67,11 ед/л), тогда как у животных с CCLt-интоксикацией среднее значение АлАТ было 599,91 ед/л. Показатель АсАТ у этой крысы равнялся 240 ед/л, что тоже близко к среднему значению интактных животных, (195,44 ед/л), тогда как у крыс с CCl4-интоксикацией среднее значение АсАТ было 623,36 ед/л. Значение ЛДГ у данной крысы 952 ед/л, что даже ниже среднего показателя интактных животных (см. табл.1).
В результате исследования активности перекисного окисления липидов светосумма в гомогенате печени данной крысы 16603,7, что приближается к среднему значению интактных животных и значительно ниже среднего показателя животных с CCl4-интоксикацией (см. табл.2). Значение величины светосуммы в сыворотке крови у опытного животного определено на уровне 90806,5, что также значительно ниже средней величины животных с CCl4-интоксикацией и ближе к среднему значению интактных животных.
В результате гистологического исследования срезов ткани печени опытной крысы было выявлено значительное уменьшение выраженности жирового гепатоза по сравнению с животными с CCl4-гинтоксикацией (см. фигуры 2, 3).
В ходе экспериментального исследования было установлено, что соединение оказывает гепатопротекторное действие, эффективно снижая активность печеночных трансаминаз, уменьшая активность процессов перекисного окисления липидов, а также выраженность жирового гепатоза.
Эксперименты выполнены на 60 белых беспородных крысах-самцах массой 150-220 г в осенне-зимний период. Все животные были разделены на контрольную (интактные крысы) и 2 опытные группы (CCl4-интоксикация + вода очищенная; CCl4-интоксикация + лекарственное вещество).
Количество животных в каждой серии составляло не менее 10 особей. Все экспериментальные животные содержались в обычных условиях вивария в соответствии с нормами кормления и содержания лабораторных животных.
Соединение предварительно измельчали и готовили суспензию. В соответствии с объемами и кратностью введения активного вещества опытной группе в группе контроля внутрибрюшинно вводили воду очищенную в тех же объемах и с той же кратностью.
В качестве модели гепатита был выбран экспериментальный токсический гепатит, вызываемый введением раствора четыреххлористого углерода.
Опытным крысам ежедневно подкожно вводили тетрахлорида углерод в виде 50% раствора в подсолнечном масле в дозе 0,4 мл на каждые 100 г массы животного 1 раз в день на протяжении 4-х первых дней опыта. Эта схема и доза считаются достаточными для создания полноценной биохимической картины острого токсического поражения паренхимы печени крыс (Левшин Б.И. Экспериментальная фармакология препаратами селена и тиазолидина токсического поражения печени: Автореферат дис…. д-ра мед. наук. Харьков, 1973). На 8-е сутки от начала затравки животные подвергались одномоментной декапитации с учетом требований этического комитета.
Биохимическому исследованию подвергалась сыворотка, отделяемая путем центрифугирования в течение 15 минут при 3000 об/мин цельной крови, собираемой в момент декапитации животных. В ней определяли активность ферментов: аспарагиновой (АсАТ) и аланиновой аминотрансфераз (АлАТ), щелочной фосфатазы (ЩФ), лактатдегидрогеназы (ЛДГ).
Для определения активности аспарагиновой и аланиновой трансфераз использовался IFCC метод (по рекомендации международного комитета по клинической химии).
Так, 7-дневная интоксикация крыс тетрахлоридом углерода вызывала значительное повышение активности печеночных трансаминаз в сыворотке крови, являющихся, как известно, маркерами печеночного цитолиза. По результатам лабораторных исследований, соединение в условиях токсического поражения печени тетрахлорметаном вызывало снижение активности АлАТ на 77,4%, АсАТ – на 53,5%, ЛДГ – на 28,6%. Влияние соединения на биохимические показатели сыворотки крови при экспериментальном токсическом поражении печени отражено в таблице 1.
Оценку показателей свободнорадикального окисления (СРО) проводили методом хемилюминесценции в сыворотке крови и супернатанте гомогената ткани печени.
В качестве оценочного показателя использовалась величина светосуммы, отражающая интенсивность образования свободных радикалов и участие в процессе СРО антиоксидантных систем.
CCl4-интоксикация крыс приводила к выраженному повышению активности процессов перекисного окисления липидов как в печени, так и в сыворотке крови экспериментальных животных (см. табл.2, 3). Соединение эффективно снижает процессы ПОЛ в печени крыс на фоне интоксикации животных тетрахлоридом углерода. На фоне коррекции CCl4-индуцированного поражения печени соединением величина светосуммы превышала показатели интактных животных всего лишь на 8,3% (см. табл.2).
Применение соединения приводит также к снижению активности ПОЛ в сыворотке крови относительно животных с CCl4-индуцированным поражением печени без лечения (см. табл.3).
Преимущества от использования предлагаемого соединения.
1. Соединение снижает активность ферментов-маркеров печеночного цитолиза.
2. Соединение значительно уменьшает активность ПОЛ.
3. Соединение уменьшает выраженность жировой дистрофии печени.
Табл.1
| Группы животных |
АлТ (ед/л) |
АсТ (ед/л) |
ЛДГ(ед/л) |
| 1 |
2 |
3 |
4 |
| Интактные животные (контроль) |
67,11±7,95 |
195,44±13,63 |
1601,33±206,54 |
| CCl4-интоксикация (без лечения) |
599,91±153,14
р<0,01 |
623,36±40,25
р<0,01 |
2781,18±194,47
р<0,01 |
| CCl4-интоксикация + соединение |
135,8±17,85
р<0,01
p1<0,01 |
289,7±26,49
р<0,01
p1<0,01 |
1985,4±313,7
р>0,05
p1<0,05 |
Табл.2
| Группы животных |
Показатель светосуммы |
% к интакту |
| 1 |
2 |
3 |
| Интактные животные (контроль) |
12847,2±1028,7 |
100% |
| CCl4-интоксикация без лечения |
28558,6±1620,1
р<0,01 |
222,3% |
| CCl4-интоксикация + соединение |
13908,9±2850,2
р>0,05
p1<0,01 |
108,3% |
Табл.3
| Группы животных |
Показатель светосуммы |
% к интакту |
| 1 |
2 |
3 |
| Интактные животные (контроль) |
79086,1±2113,9 |
100% |
| CCl4-интоксикация без лечения |
154404,5±5419,1
р<0,01 |
195,2% |
| CCl4-интоксикация + соединение (1) |
95735,3±7865,9
р<0,05
p1<0,01 |
121% |
Формула изобретения
Применение 2,6-диметил-3-оксипиридина адамантанкарбоксилата формулы
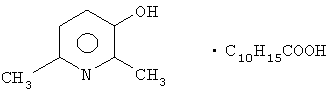
в качестве гепатопротектора.
РИСУНКИ
|
|