|
(21), (22) Заявка: 2006136954/13, 18.10.2006
(24) Дата начала отсчета срока действия патента:
18.10.2006
(46) Опубликовано: 20.05.2008
(56) Список документов, цитированных в отчете о
поиске:
KISHOR P. et al. PLANT PHISIOLOGY, 1995, v.108(4):1387-1394. HU C.A. et al. PROC NATL ACAD SCI USA, 1992, v.89(19):9354-8. US 2003/0233680 A1, 18.12.2003. US 2003/0211490 A1, 13.11.2003. JP 2001054385, 27.02.2001. WO 99/66785 A1, 29.12.1999. JP 10057069, 03.03.1998. US 5639950 A, 17.06.1997. US 5344923 A, 06.09.1997.
Адрес для переписки:
630090, г.Новосибирск, пр-кт Акад. Лаврентьева, 10, ИЦиГ СО РАН, Патентный отдел
|
(72) Автор(ы):
Титов Сергей Евгеньевич (RU),
Герасимова Софья Викторовна (RU),
Кочетов Алексей Владимирович (RU),
Колодяжная Янина Станиславовна (RU),
Комарова Марина Львовна (RU),
Романова Антонина Валерьевна (RU),
Шумный Владимир Константинович (RU)
(73) Патентообладатель(и):
Институт цитологии и генетики Сибирского отделения Российской академии наук (СО РАН) (RU)
|
(54) СПОСОБ ПОЛУЧЕНИЯ ТРАНСГЕННЫХ РАСТЕНИЙ ТАБАКА С ПОВЫШЕННЫМ СОДЕРЖАНИЕМ ПРОЛИНА
(57) Реферат:
Изобретение относится к генетической инженерии растений. Сущность изобретения: конструируют рекомбинантную плазмидную ДНК pBi-P5CS, размером 14681 п.н., обеспечивающую перенос целевой последовательности ДНК в геном растений и экспрессию гена P5CS люцерны, состоящую из следующих элементов:
– ДНК векторной плазмиды размером 13915 п.н.; – фрагмента ДНК, содержащего кДНК гена  1-пирролин-5-карбоксилатсинтетазы размером 2148 п.н.; – промотора 35S РНК из генома вируса мозаики цветной капусты; – 3’НТР области гена нопалинсинтазы. Сконструированную рекомбинантную плазмиду pBi-P5CS, несущую ген 1-пирролин-5-карбоксилатсинтетазы размером 2148 п.н.; – промотора 35S РНК из генома вируса мозаики цветной капусты; – 3’НТР области гена нопалинсинтазы. Сконструированную рекомбинантную плазмиду pBi-P5CS, несущую ген  1-пирролин-5-карбоксилатсинтетазы, переносят в штамм Agrobacterittm tumefaciens AGL0 с последующей прямой трансформацией листовых дисков Nicotiana tabacum SR1 сокультивацией с агробактерией. Отбор и генерацию производят непосредственно на средах, содержащих NaCl. Способ позволяет получать стрессоустойчивые растения табака с повышенным уровнем содержания пролина без использования антибиотиков. 3 ил., 1 табл. 1-пирролин-5-карбоксилатсинтетазы, переносят в штамм Agrobacterittm tumefaciens AGL0 с последующей прямой трансформацией листовых дисков Nicotiana tabacum SR1 сокультивацией с агробактерией. Отбор и генерацию производят непосредственно на средах, содержащих NaCl. Способ позволяет получать стрессоустойчивые растения табака с повышенным уровнем содержания пролина без использования антибиотиков. 3 ил., 1 табл.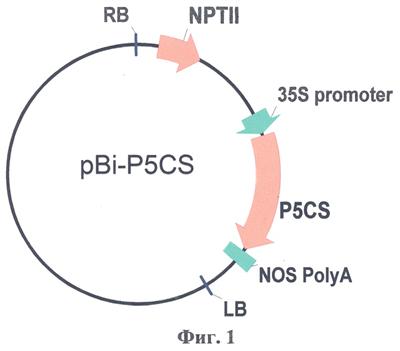
Изобретение относится к области биотехнологии, в частности к генетической инженерии высших растений, и касается способа получения трансгенных растений с повышенным содержанием пролина.
Известны два способа получения трансгенных растений с модифицированным метаболизмом пролина: с помощью повышения экспрессии гена 
Основными недостатками прототипа являются:
– необходимость введения в геном растений гена устойчивости к канамицину в составе Т-ДНК рекомбинантной плазмиды, который не играет никакой другой функциональной роли, кроме возможности отбора;
– использование для отбора трансгенных растений селективной среды с добавлением антибиотика канамицина, что не позволяет сразу отбирать растения с повышенным содержание пролина, а требует дополнительной стадии отбора растений на устойчивость к канамицину.
Технической задачей настоящего изобретения является повышение экологической безопасности способа.
Поставленная техническая задача достигается предлагаемым способом, заключающимся в следующем.
Плазмида состоит из следующих элементов:
– ДНК векторной плазмиды размером 13915 п.н.;
– фрагмента ДНК, содержащего кДНК гена  1-пирролин-5-карбоксилатсинтетазы размером 2148 п.н.; 1-пирролин-5-карбоксилатсинтетазы размером 2148 п.н.;
– Промотора 35S РНК из генома вируса мозаики цветной капусты;
– 3’НТР области гена нопалинсинтазы.
Сконструированную рекомбинантную плазмиду pBi-P5CS, несущую ген  1-пирролин-5-карбоксилатсинтетазы, переносят в штамм агробактерий (Agrobacterium tumefaciens) AGL0 с последующей прямой трансформацией листовых дисков табака (Nicotiana tabacum) SR1 кокультивацией с агробактерией с последующим отбором и генерацией непосредственно на средах, содержащих NaCl. 1-пирролин-5-карбоксилатсинтетазы, переносят в штамм агробактерий (Agrobacterium tumefaciens) AGL0 с последующей прямой трансформацией листовых дисков табака (Nicotiana tabacum) SR1 кокультивацией с агробактерией с последующим отбором и генерацией непосредственно на средах, содержащих NaCl.
Физическая карта плазмиды pBi-P5CS с указанием генетических маркеров приведена на фиг.1, где P5CS – нуклеотидная последовательность гена P5CS люцерны; 35S CaMV – промотор гена 35S РНК вируса мозаики цветной капусты; NOS PolyA – терминатор гена нопалинсинтазы из Ti-плазмиды агробактерий (Agrobacterium tumefaciens); NPTII-ген неомицинфосфотрансферазы II; LB, RB – левая и правая границы Т-ДНК области.
Определяющими отличительными признаками заявляемого способа, по сравнению с прототипом, являются:
– в качестве векторной плазмиды используют вектор pBi101, в котором ген  -глюкуронидазы был заменен на кДНК гена -глюкуронидазы был заменен на кДНК гена  1-пирролин-5-карбоксилатсинтетазы, что позволило получить конструкцию меньшего размера, более оптимальную для трансформации, в то время как в прототипе был использован вектор pBi121, где целевой ген с промотором и терминатором был встроен за геном 1-пирролин-5-карбоксилатсинтетазы, что позволило получить конструкцию меньшего размера, более оптимальную для трансформации, в то время как в прототипе был использован вектор pBi121, где целевой ген с промотором и терминатором был встроен за геном  -глюкуронидазы; -глюкуронидазы;
– отбор трансгенных растений осуществляют непосредственно на стрессовом фоне (на среде, содержащей 200 mM NaCl), что позволяет получать стрессоустойчивые формы растений и повысить экологическую безопасность способа за счет возможности исключения из сконструированной рекомбинантной плазмиды pBi-P5CS гена устойчивости к антибиотику канамицину.
Изобретение поясняется следующими примерами конкретного выполнения способа.
Пример 1.
Конструирование генетической конструкции pBi-P5CS.
Клонирование кДНК гена  1-пирролин-5-карбоксилатсинтетазы (P5CS) в составе вектора pBi101 осуществляли в один этап посредством тройного лигирования. В конструкцию собирали три фрагмента: промотор 35S РНК из плазмиды pRT104, кДНК P5CS и часть плазмиды pBi101, содержащую в Т-области ген NPTII и 3′-нетранслируемый участок гена нопалинсинтазы, включающий сигнал полиаденилирования. 1-пирролин-5-карбоксилатсинтетазы (P5CS) в составе вектора pBi101 осуществляли в один этап посредством тройного лигирования. В конструкцию собирали три фрагмента: промотор 35S РНК из плазмиды pRT104, кДНК P5CS и часть плазмиды pBi101, содержащую в Т-области ген NPTII и 3′-нетранслируемый участок гена нопалинсинтазы, включающий сигнал полиаденилирования.
Кодирующая последовательность гена P5CS была выделена с помощью обратной транскрипции суммарной РНК, выделенной из проростков люцерны (Medicago truncatula), и последующей ПЦР-реакции со специфическими праймерами. В качестве праймеров использовались олигонуклеотиды, гомологичные 5′- и 3′- районам кодирующей последовательности гена P5CS (праймеры: 5′-gttcatctcatagctgtactatcat-3′; 5′-caagtgaacttccttgcctgccgtc-3′). Полученная кДНК гена P5CS длиной 2252 п.н. с включенными сайтами SalI и Есl136II была обработана рестриктазами SalI и Есl136II. Плазмида pRT104 была обработана рестриктазами HindIII и Sfr274I (XhoI). Плазмида pBi101 была обработана рестриктазами HindIII и Есl136II. Продукты рестрикции разделяли в 1% агарозном геле, гель окрашивали раствором бромистого этидия в воде (1 мкг/мл) и методом сорбции ДНК на силикагеле выделяли фрагменты: ДНК P5CS длиной 2148 п.н., фрагмент pRT104 длиной 441 п.н., соответствующий 35S промотору, фрагмент pBi101 длиной 11996 п.н. Выделенные фрагменты были обработаны ДНК-лигазой, лигазной смесью трансформировали компетентные клетки E.coli штамма XL1 Blue. Трансформанты высевали на чашку с LB-агаром, содержащим 50 мкг/мл канамицина. Клоны, несущие рекомбинантные плазмиды со встроенным геном, отбирали методом ПЦР анализа ДНК отдельных колоний E.coli с праймерами на нуклеотидную последовательность P5CS люцерны.
Пример 2
Получение трансгенных растений, несущих конструкцию pBi-P5CS.
Полученная по примеру 1 конструкция pBi-P5CS, несущая кДНК гена 
А, Б – трансформация конструкциями pBi101 и pBi-P5CS, отбор на среде, содержащей 200 mM NaCl;
В – трансформация конструкцией pBi101, отбор на канамицине.
На фиг.2А видно, что каллусообразование на листовых дисках с конструкцией pBi-P5CS на среде с 200 mM NaCl происходило нормально, тогда как диски с контрольной конструкцией pBi101 (фиг.2Б) некротизировались. Листовые диски с контрольной конструкцией на среде с канамицином развивались нормально и давали побеги (фиг.2В).
На фиг.3 представлена электрофореграмма ПЦР-анализа геномной ДНК проростков трансгенных растений на наличие встройки кДНК гена  1-пирролин-5-карбоксилатсинтетазы. Нанесения по дорожкам: 1-2 – трансгенные табаки SR1, экспрессирующие ген 1-пирролин-5-карбоксилатсинтетазы. Нанесения по дорожкам: 1-2 – трансгенные табаки SR1, экспрессирующие ген  1-пирролин-5-карбоксилатсинтетазы; 3 – нетрансгенные табаки SR1 (отрицательный контроль): 4, 5 – трансгенные табаки SR1, экспрессирующие ген 1-пирролин-5-карбоксилатсинтетазы; 3 – нетрансгенные табаки SR1 (отрицательный контроль): 4, 5 – трансгенные табаки SR1, экспрессирующие ген  1-пирролин-5-карбоксилатсинтетазы. Из фиг.3 видно, что ПЦР-анализ с праймерами на нуклеотидную последовательность P5CS подтверждает наличие нуклеотидной последовательности P5CS люцерны в геномах отобранных растений. 1-пирролин-5-карбоксилатсинтетазы. Из фиг.3 видно, что ПЦР-анализ с праймерами на нуклеотидную последовательность P5CS подтверждает наличие нуклеотидной последовательности P5CS люцерны в геномах отобранных растений.
| Таблица |
| №№ |
Трансгенное растение |
мкг/гсм |
| Опыт |
контроль |
| 1 |
P5CS №2 |
|
767 |
| 2 |
P5CS №3 |
|
701 |
| 3 |
P5CS №4 |
|
711 |
| 4 |
P5CS №8 |
|
849 |
| 5 |
P5CS №9 |
|
675 |
| 6 |
P5CS №13 |
|
2067 |
| 7 |
P5CS №14 |
|
688 |
| 8 |
P5CS №17 |
|
1053 |
| 9 |
P5CS №18 |
|
1497 |
| 10 |
P5CS №20 |
|
1810 |
| 11 |
P5CS №23 |
|
2132 |
| 12 |
P5CS №24 |
|
1933 |
| 13 |
|
pBi №1 |
80 |
| 14 |
|
pBi №2 |
134 |
| 15 |
|
pBi №3 |
211 |
| 16 |
|
pBi №4 |
118 |
Из представленных в таблице данных видно, что полученные трансгенные растения табака, содержащие рекомбинантную плазмиду pBi-P5CS, имеют повышенный в несколько раз уровень содержания пролина, по сравнению с контрольными растениями.
Таким образом, предлагаемый способ отвечает требованиям экологической безопасности и позволяет получать трансгенные растения, несущие кДНК гена P5CS и эффективно повышать уровень содержания пролина в трансгенных растениях, что увеличивает их стрессоустойчивость.
Формула изобретения
Способ получения трансгенных растений табака с повышенным содержанием пролина, включающий конструирование рекомбинантной плазмидной ДНК, содержащей ген  1-пирролин-5-карбоксилатсинтетазы, передачу полученной плазмидной ДНК в штамм Agrobacterium tumefaciens, инфицирование последним растительного материала, отбор трансгенных растений на селективной питательной среде с последующим тестированием отобранных трансформантов на повышенное содержание пролина, отличающийся тем, что конструируют и передают в штамм указанной бактерии рекомбинантную плазмидную ДНК pBi-P5CS, состоящую из следующих элементов: 1-пирролин-5-карбоксилатсинтетазы, передачу полученной плазмидной ДНК в штамм Agrobacterium tumefaciens, инфицирование последним растительного материала, отбор трансгенных растений на селективной питательной среде с последующим тестированием отобранных трансформантов на повышенное содержание пролина, отличающийся тем, что конструируют и передают в штамм указанной бактерии рекомбинантную плазмидную ДНК pBi-P5CS, состоящую из следующих элементов:
ДНК векторной плазмиды pBI101, не содержащей ген бета-глюкуронидазы;
фрагмента ДНК, содержащего кДНК гена  1-пирролин-5-карбоксилатсинтетазы из Medicago truncatula размером 2148 п.н.; 1-пирролин-5-карбоксилатсинтетазы из Medicago truncatula размером 2148 п.н.;
промотора 35S РНК из генома вируса мозаики цветной капусты;
3’НТР области гена нопалинсинтазы, при этом отбор трансгенных растений осуществляют на питательной среде, содержащей 200 mM NaCl.
РИСУНКИ
|