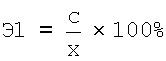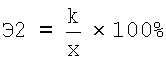Патент на изобретение №2324338
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ БИОМАССЫ IN VITRO
(57) Реферат:
Способ включает заготовку эксплантов, их стерилизацию, помещение эксплантов для каллусообразования и роста биомассы в стерильные пробирки с модифицированной питательной средой Мурасиге-Скуга с добавлением ростовых стимуляторов, термостатирование при 26±1°С. Стерилизацию эксплантов осуществляют в дистиллированной воде воздействием ультразвуковых колебаний с интенсивностью 1…2 Вт/кв.см на рабочей частоте 22…44 кГц в течение 3…6 мин. На этапах каллусообразования и роста биомассы пробирки с эксплантами погружают в водную среду и осуществляют через нее воздействие ультразвуковыми колебаниями с интенсивностью не менее 10…15 Вт/кв.см на частоте 22…44 кГц. Воздействие проводят со стороны дна пробирок с периодичностью не реже 1 раза в сутки в течение не менее 6 мин на каждом этапе. Прирост биомассы составляет 87,40-176,53%. Способ позволяет получить оздоровленный посадочный материал, увеличить эффективность стерилизации, увеличить способность неинфицированных эксплантов образовывать каллус. 5 табл.
Изобретение предназначено для использования в области сельского хозяйства и биотехнологии и может быть использовано для получения оздоровленного посадочного материала (микроразмножения при оздоровлении растений), выведении новых сортов и получения биомассы (каллуса) растительного сырья для фармацевтической и косметической промышленности. В настоящее время актуальным является получение биомассы (каллуса) растительного сырья для выведения новых сортов растений, придание им устойчивости к различным видам бактерий, грибов и вирусов, сорнякам, насекомым-вредителям и другим неблагоприятным факторам окружающей среды, а также для получения экстрактов биологически активных веществ из растительного сырья и сохранения видов исчезающих растений, занесенных в Красную книгу. Наиболее широко распространенными способами получения биомассы (каллуса) для указанных целей являются биотехнологические способы роста культур клеток и тканей in vitro [1, 2, 3, 4]. Все известные способы получения биомассы in vitro предполагают изоляцию зон роста в виде различных эксплантов из исходного растения, стерилизацию их и помещение в стерильных условиях на питательную среду Мурасиге-Скуга (МС) с заданным составом ростовых веществ. Для накопления биомассы (каллуса) обычно используются первичные экспланты в виде проростков семян, частей листьев и стеблей, пазушных и апикальных меристем и почек клубней или корнеплодов растений. Общим недостатком всех известных способов является их низкая производительность (эффективность), обусловленная: – низкой эффективностью стерилизации (менее 50%) исходного материала (эксплантов); – малой долей эксплантов, образующих каллус (эффективность каллусообразования не более 30…40% от общего количества неинфицированных эксплантов); – недостаточным приростом биомассы образовавшегося каллуса (не более 60% от исходной массы). Перечисленные недостатки ограничивают возможность применения известных способов для промышленного производства. В связи с этим возникает необходимость повышения эффективности способов получения биомассы in vitro на всех этапах осуществления процесса: стерилизация, каллусообразование и рост биомассы. Как правило, это осуществляют при помощи дополнительных воздействий на различных этапах реализации процесса (применение различных стерилизующих растворов, добавлением ростовых факторов каллусообразования, температурным воздействием и воздействием различных излучений). Наиболее близким по технической сущности к предлагаемому является способ получения биомассы in vitro по патенту РФ 2222933 [5], принятый за прототип. Способ получения биомассы in vitro, по [5], включает заготовку эксплантов из проростков, тканей или клеток, их стерилизацию, помещение эксплантов для каллусообразования и роста биомассы в стерильные пробирки с модифицированной питательной средой Мурасиге-Скуга с добавлением ростовых факторов каллусообразования, термостатирование при температуре 26±1 градус Цельсия и относительной влажности 70%. На этапе роста биомассы в известном способе осуществляется воздействие посредством индуктора последовательностью однонаправленных импульсов магнитной индукции с амплитудным значением 0,05 Тл, периодом 5, 12 с, скважностью от 100 до 4500, причем апикальную часть экспланта ориентируют противоположно направлению вектора магнитной индукции, а число импульсов устанавливают от 10 до 100. Способ позволяет увеличить количество образующейся биомассы in vitro. В этом случае рост биомассы происходит только на неинфицированных эксплантах, образовавших каллус. При этом основные потери исходного материала из-за инфицирования и отсутствия каллусообразования не были устранены. Таким образом, прототип не позволяет повысить производительность процесса и довести эффективность способа получения биомассы in vitro до промышленного применения. В предлагаемом способе получения биомассы in vitro решается задача увеличения производительности процесса получения биомассы за счет повышения эффективности всех основных стадий этого процесса: – стерилизации исходного материала (эксплантов) без применения химических дезинфицирующих растворов; – увеличения способности неинфицированных эксплантов образовывать каллус; – увеличения получаемой биомассы не только за счет увеличения прироста на каждом образовавшем каллус неинфицированном экспланте, но и за счет увеличения числа неинфицированных и образующих каллус первичных эксплантов. Предлагаемый способ получения биомассы in vitro включает заготовку эксплантов из различных частей растений (проростков, тканей или клеток), их стерилизацию, помещение эксплантов для каллусообразования и роста биомассы в стерильные пробирки с модифицированной питательной средой Мурасиге-Скуга с добавлением ростовых стимуляторов каллусообразования, термостатирование при температуре 26±1 градус Цельсия и относительной влажности 70%. Стерилизацию эксплантов осуществляют в дистиллированной воде воздействием на экспланты ультразвуковыми колебаниями с интенсивностью 1…2 Вт/кв.см на рабочей частоте 22…44 кГц в течение 3…6 минут. После помещения эксплантов на питательную среду, на этапах каллусообразования и роста биомассы пробирки с эксплантами погружают в водную среду и осуществляют через нее воздействие ультразвуковыми колебаниями с интенсивностью не менее 10…15 Вт/кв.см на частоте 22…44 кГц со стороны дна пробирок с периодичностью не реже 1 раза в сутки в течение не менее 6 минут на каждом этапе. Сущность предлагаемого способа заключается: – в рациональном (оптимальном по интенсивности и времени) воздействии на помещенные в стерильную воду экспланты ультразвуковыми колебаниями, обеспечивающими стерилизующий эффект за счет формирования и захлопывания в водной среде на поверхности эксплантов кавитационных пузырьков [6]. При этом происходит разрушение патогенных форм без применения каких-либо химических стерилизующих веществ; – в рациональном (оптимальном по интенсивности и времени) воздействии ультразвуковыми колебаниями на экспланты, находящиеся в стерильных пробирках на питательной среде. УЗ колебания, распространяясь в водной среде, проникают через стенки пробирок и питательную среду к поверхности эксплантов. При воздействии ультразвуковых колебаний на экспланты, находящиеся в питательной среде, интенсифицируются процессы массообмена и проникновения питательной среды внутри эксплантов и растущей биомассы. Ускорение процессов массообмена [6] обеспечивает интенсификацию подвода питательной среды к поверхности экспланта и растущей биомассы, а звукокапиллярный эффект [6] обеспечивает эффективное проникновение питательной среды по капиллярам эксплантов и через поры к растущей биомассе. Способ осуществляют следующим образом. Берется по 40 пробирок с питательной средой и эксплантами. Эксплантами являлись зародышевые листки проростков семян и пазушные почки растений гречихи, картофеля и сои. Эффективность стерилизации (Э1) определяют по количеству неинфицированных эксплантов после стерилизации (с) в процентах от исходного количества стерилизуемых эксплантов (х):
Эффективность каллусообразования (Э2) определяют по количеству стерильных эксплантов, образовавших каллус в пробирках с питательной средой (k) в процентах, от исходного количества вводимых в культуру эксплантов (х):
Прирост биомассы определяют в граммах и процентах. Прирост биомассы в граммах – это разница между конечным и начальным весом биомассы, образовавшейся за определенный промежуток времени. Прирост биомассы в процентах – это разница между конечным и начальным весом биомассы за определенный промежуток времени, отнесенный к начальному весу каллуса в культивационной пробирке. Результаты стерилизации эксплантов по способу, принятому за прототип (без ультразвука), и по предложенному способу представлены в таблице 1.
Эффективность каллусообразования по предложенному способу представлена результатами эксперимента, приведенными в таблице 2.
Результаты прироста биомассы представлены в таблицах 3, 4 и 5.
Таким образом, в результате реализации предлагаемого способа получения биомассы in vitro была решена проблема увеличения производительности процесса получения биомассы за счет повышения эффективности всех основных стадий этого процесса: – увеличения эффективности стерилизации с 60% до 90% без применения химических стерилизаторов; – увеличения в два раза способности неинфицированных эксплантов образовывать каллус; – увеличения, практически в два раза, получаемой биомассы за счет увеличения прироста на каждом образовавшем каллус неинфицированном экспланте; – многократное (не менее 10 раз) увеличение эффективности способа, то есть производительности получения конечного продукта – биомассы из заготовленного полевого исходного сырья (нестерилизованных эксплантов). Технический результат предлагаемого решения выражается в том, что полученные результаты позволяют использовать предложенный способ для промышленного применения, например, при получении биомассы лекарственных растений для последующего экстрагирования или сельскохозяйственных растений для дальнейшего получения оздоровленных растений – регенерантов. В настоящее время Бийским технологическим институтом Алтайского государственного технического университета ведется подготовка к серийному производству биомассы лекарственных и сельскохозяйственных растений на основе предложенного способа. Список литературы 1. Патент РФ №2286053. 2. Патент РФ №2279212. 3. Патент РФ №2180165. 4. Патент РФ №2282352. 5. Патент РФ №2222933 (прототип). 6. Хмелев В.Н. Многофункциональные ультразвуковые аппараты и их применение в условиях малых производств, сельском хозяйстве и домашнем хозяйстве / В.Н.Хмелев, О.В.Попова. – Барнаул: изд. АлтГТУ, 1997, – 160 с.
Формула изобретения
Способ получения биомассы in vitro, включающий заготовку эксплантов из проростков, тканей или клеток, их стерилизацию, помещение эксплантов для каллусообразования и роста биомассы в стерильные пробирки с модифицированной питательной средой Мурасиге-Скуга с добавлением ростовых стимуляторов каллусообразования, термостатирование при температуре 26±1°С и относительной влажности 70%, отличающийся тем, что стерилизацию эксплантов осуществляют в дистиллированной воде воздействием на экспланты ультразвуковыми колебаниями с интенсивностью 1…2 Вт/см2 на рабочей частоте 22…44 кГц в течение 3…6 мин, после помещения эксплантов на питательную среду на этапах каллусообразования и роста биомассы пробирки с эксплантами погружают в водную среду и осуществляют через нее воздействие ультразвуковыми колебаниями с интенсивностью не менее 10…15 Вт/см2 на частоте 22…44 кГц со стороны дна пробирок с периодичностью не реже 1 раза в сутки в течение не менее 6 мин на каждом этапе.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||