|
|
(21), (22) Заявка: 2006135873/15, 10.10.2006
(24) Дата начала отсчета срока действия патента:
10.10.2006
(46) Опубликовано: 20.04.2008
(56) Список документов, цитированных в отчете о
поиске:
ЗИМНУХОВ В.В. и др. Смертельные отравления дипиридамолом. Судебно-медицинская экспертиза. 1999, т.42, №3, с.34. ШВАЙКОВА М.Д. Токсикологическая химия. – М.: Медицина, 1975, С.119-123. МУРАВЬЕВА Г.М. и др. Судебно-химическое определение курантила и верапамила. Судебно-медицинская экспертиза. 01.03.1995, т.38, №1, с.21-23. STEYN J.M.
Адрес для переписки:
305041, г.Курск, ул. К. Маркса, 3, КГМУ, патентный отдел, З.Н. Куприяновой
|
(72) Автор(ы):
Шорманов Владимир Камбулатович (RU),
Квачахия Лексо Лорикович (RU),
Сипливая Любовь Евгеньевна (RU)
(73) Патентообладатель(и):
Шорманов Владимир Камбулатович (RU),
Квачахия Лексо Лорикович (RU),
Сипливая Любовь Евгеньевна (RU)
|
(54) СПОСОБ ОПРЕДЕЛЕНИЯ 2,6-БИС-[БИС-(БЕТА-ОКСИЭТИЛ)-АМИНО]-4,8-ДИ-N-ПИПЕРИДИНО-ПИРИМИДО(5,4-D)ПИРИМИДИНА В БИОЛОГИЧЕСКОМ МАТЕРИАЛЕ
(57) Реферат:
Изобретение относится к биологии и токсикологической химии, а именно к способам определения 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо (5,4-d)пиримидина в биологическом материале, и может быть использовано в практике химико-токсикологических и клинических лабораторий. Биологическую ткань измельчают, двукратно настаивают с ацетоном каждый раз в течение 30 минут, полученные извлечения объединяют, объединенное извлечение фильтруют, фильтрат испаряют до получения сухого остатка, остаток растворяют в хлороформе, экстрагируют 0,1 н. раствором хлороводородной кислоты, хлороформный слой отбрасывают, полученный кислотный экстракт промывают эфиром, эфирный слой отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до рН 8-10, насыщают хлоридом натрия, экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в смеси растворителей ацетонитрил – 1 н. раствор серной кислоты, взятых в соотношении 8:2 (по объему), хроматографируют в колонке с сорбентом «Силасорб С-18» с размером частиц 30 -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо (5,4-d)пиримидина в биологическом материале, и может быть использовано в практике химико-токсикологических и клинических лабораторий. Биологическую ткань измельчают, двукратно настаивают с ацетоном каждый раз в течение 30 минут, полученные извлечения объединяют, объединенное извлечение фильтруют, фильтрат испаряют до получения сухого остатка, остаток растворяют в хлороформе, экстрагируют 0,1 н. раствором хлороводородной кислоты, хлороформный слой отбрасывают, полученный кислотный экстракт промывают эфиром, эфирный слой отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до рН 8-10, насыщают хлоридом натрия, экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в смеси растворителей ацетонитрил – 1 н. раствор серной кислоты, взятых в соотношении 8:2 (по объему), хроматографируют в колонке с сорбентом «Силасорб С-18» с размером частиц 30  с использованием подвижной фазы ацетонитрил – 1 н. раствор серной кислоты (8:2), фракции элюата, содержащие анализируемое вещество, объединяют и измеряют оптическую плотность элюата при длине волны 286 нм. Способ обеспечивает снижение затрат времени на осуществление анализа, увеличение степени извлечения, точности и чувствительности определения. 3 табл. с использованием подвижной фазы ацетонитрил – 1 н. раствор серной кислоты (8:2), фракции элюата, содержащие анализируемое вещество, объединяют и измеряют оптическую плотность элюата при длине волны 286 нм. Способ обеспечивает снижение затрат времени на осуществление анализа, увеличение степени извлечения, точности и чувствительности определения. 3 табл.
(56) (продолжение):
CLASS=”b560m”Spectrofluorimetric determination of dipyridamole in serum-a comparison of two methods. J.Chromatogr. 01.12.1979, 164.(4), P. 487-494. WO 2006090428 A, 31.08.2006.
Изобретение относится к биологии и токсикологической химии, а именно к способам определения 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо (5,4-d)пиримидина в биологическом материале, и может быть использовано в практике химико-токсикологических и клинических лабораторий. Способ относится к числу массовых. -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо (5,4-d)пиримидина в биологическом материале, и может быть использовано в практике химико-токсикологических и клинических лабораторий. Способ относится к числу массовых.
Известен способ определения 2,6-бис-[бис-(
Способ характеризуется недостаточно высокой степенью извлечения 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина, относительно низкими точностью и чувствительностью определения. -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина, относительно низкими точностью и чувствительностью определения.
Известен способ определения органических веществ основного характера, к которым относится, в частности, 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидин, в биологическом материале, заключающийся в измельчении биологического объекта, неоднократном настаивании с этанолом (каждый раз в течение суток), объединении вытяжек, сгущении объединенного извлечения, осаждении в нем белков абсолютным этанолом, фильтровании, упаривании фильтрата до густоты сиропа и разбавлении его водой с последующей экстракцией анализируемых соединений из щелочного раствора (Швайкова М.Д. Токсикологическая химия. – М.: Медицина, 1975. – C.119-123). -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидин, в биологическом материале, заключающийся в измельчении биологического объекта, неоднократном настаивании с этанолом (каждый раз в течение суток), объединении вытяжек, сгущении объединенного извлечения, осаждении в нем белков абсолютным этанолом, фильтровании, упаривании фильтрата до густоты сиропа и разбавлении его водой с последующей экстракцией анализируемых соединений из щелочного раствора (Швайкова М.Д. Токсикологическая химия. – М.: Медицина, 1975. – C.119-123).
Способ характеризуется длительностью процесса определения, низкой степенью извлечения 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина, недостаточно высокими чувствительностью и точностью. -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина, недостаточно высокими чувствительностью и точностью.
Наиболее близким является способ определения 2,6-бис-[бис-(
Способ характеризуется значительными затратами времени на осуществление анализа, относительно низкой степенью извлечения анализируемого соединения, недостаточно высокой точностью и чувствительностью определения.
Задачей настоящего изобретения является снижение затрат времени на проведение анализа, повышение степени извлечения, а также точности и чувствительности определения.
Поставленная задача достигается с помощью предлагаемого способа, который заключается в том, что биологическую ткань двукратно настаивают с ацетоном каждый раз в течение 30 минут, полученные извлечения объединяют, объединенное извлечение фильтруют, фильтрат испаряют до получения сухого остатка, остаток растворяют в хлороформе, экстрагируют 0,1 н. раствором хлороводородной кислоты, хлороформный слой отбрасывают, полученный кислотный экстракт промывают эфиром, эфирный слой отбрасывают, водный слой подщелачивают 10%-ным раствором гидроксида натрия до рН 8-10, насыщают хлоридом натрия, экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в смеси растворителей ацетонитрил-1 н. раствор серной кислоты, взятых в соотношении 8:2 (по объему), хроматографируют в колонке с сорбентом «Силасорб С-18» с размером частиц 30  с использованием подвижной фазы ацетонитрил-1 н. раствор серной кислоты (8:2), фракции элюата, содержащие анализируемое вещество, объединяют и измеряют оптическую плотность элюата при длине волны 286 нм. с использованием подвижной фазы ацетонитрил-1 н. раствор серной кислоты (8:2), фракции элюата, содержащие анализируемое вещество, объединяют и измеряют оптическую плотность элюата при длине волны 286 нм.
Способ осуществляется следующим образом. Биологическую ткань, содержащую 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидин, двукратно настаивают с ацетоном каждый раз в течение 30 минут, полученные извлечения объединяют, объединенное извлечение фильтруют, фильтрат испаряют до получения сухого остатка, остаток растворяют в хлороформе, экстрагируют 0,1 н. раствором хлороводородной кислоты, хлороформный слой отбрасывают, полученный кислотный экстракт промывают эфиром, эфирный слой отбрасывают, водный слой подщелачивают 10%-ным раствором гидроксида натрия до рН 8-10, насыщают хлоридом натрия, экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в смеси растворителей ацетонитрил – 1 н. раствор серной кислоты, взятых в соотношении 8:2 (по объему), хроматографируют в колонке с сорбентом «Силасорб С-18» с размером частиц 30 -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидин, двукратно настаивают с ацетоном каждый раз в течение 30 минут, полученные извлечения объединяют, объединенное извлечение фильтруют, фильтрат испаряют до получения сухого остатка, остаток растворяют в хлороформе, экстрагируют 0,1 н. раствором хлороводородной кислоты, хлороформный слой отбрасывают, полученный кислотный экстракт промывают эфиром, эфирный слой отбрасывают, водный слой подщелачивают 10%-ным раствором гидроксида натрия до рН 8-10, насыщают хлоридом натрия, экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в смеси растворителей ацетонитрил – 1 н. раствор серной кислоты, взятых в соотношении 8:2 (по объему), хроматографируют в колонке с сорбентом «Силасорб С-18» с размером частиц 30  с использованием подвижной фазы ацетонитрил – 1 н. раствор серной кислоты (8:2), фракции элюата, содержащие анализируемое вещество, объединяют и измеряют оптическую плотность элюата при длине волны 286 нм. с использованием подвижной фазы ацетонитрил – 1 н. раствор серной кислоты (8:2), фракции элюата, содержащие анализируемое вещество, объединяют и измеряют оптическую плотность элюата при длине волны 286 нм.
Пример 1
Определение 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в ткани печени -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в ткани печени
К 25 г мелкоизмельченной ткани печени прибавляют 10 мг 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина, тщательно перемешивают биологическую ткань с веществом и оставляют на сутки при температуре 18-20°С. По истечении указанного времени биологический объект, содержащий анализируемое вещество, заливают 50 мл ацетона и выдерживают 30 минут при перемешивании. Извлечение отделяют, операцию настаивания повторяют еще раз в указанных условиях. Отдельные извлечения объединяют, фильтруют через стеклянный фильтр диаметром 3 см с 10 г безводного сульфата натрия. Через слой сульфата натрия дополнительно пропускают 25 мл ацетона. Отдельные фильтраты объединяют в фарфоровой чашке, растворитель испаряют в токе воздуха при комнатной температуре до получения сухого остатка. Остаток растворяют в 10 мл хлороформа, экстрагируют дважды порциями 0,1 н. раствора хлороводородной кислоты по 20 мл каждая, полученные извлечения отделяют, объединяют, встряхивают в делительной воронке в течение 3 минут с 40 мл эфира, эфирный слой отбрасывают, в водный слой вводят 3,6 г хлорида натрия, полученный раствор подщелачивают 10%-ным раствором гидроксида натрия до рН 8-10 и экстрагируют дважды порциями этилацетата по 40 мл каждая. Экстракты отделяют, объединяют в фарфоровой чашке и испаряют в токе воздуха при комнатной температуре до получения сухого остатка. Остаток растворяют в 2-3 мл смеси растворителей ацетонитрил – 1 н. раствор серной кислоты, взятых в соотношении 8:2 (по объему), и вводят полученный раствор в колонку размерами 490х11 мм, заполненную 7,5 г сорбента «Силасорб С-18» с размером частиц 30 -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина, тщательно перемешивают биологическую ткань с веществом и оставляют на сутки при температуре 18-20°С. По истечении указанного времени биологический объект, содержащий анализируемое вещество, заливают 50 мл ацетона и выдерживают 30 минут при перемешивании. Извлечение отделяют, операцию настаивания повторяют еще раз в указанных условиях. Отдельные извлечения объединяют, фильтруют через стеклянный фильтр диаметром 3 см с 10 г безводного сульфата натрия. Через слой сульфата натрия дополнительно пропускают 25 мл ацетона. Отдельные фильтраты объединяют в фарфоровой чашке, растворитель испаряют в токе воздуха при комнатной температуре до получения сухого остатка. Остаток растворяют в 10 мл хлороформа, экстрагируют дважды порциями 0,1 н. раствора хлороводородной кислоты по 20 мл каждая, полученные извлечения отделяют, объединяют, встряхивают в делительной воронке в течение 3 минут с 40 мл эфира, эфирный слой отбрасывают, в водный слой вводят 3,6 г хлорида натрия, полученный раствор подщелачивают 10%-ным раствором гидроксида натрия до рН 8-10 и экстрагируют дважды порциями этилацетата по 40 мл каждая. Экстракты отделяют, объединяют в фарфоровой чашке и испаряют в токе воздуха при комнатной температуре до получения сухого остатка. Остаток растворяют в 2-3 мл смеси растворителей ацетонитрил – 1 н. раствор серной кислоты, взятых в соотношении 8:2 (по объему), и вводят полученный раствор в колонку размерами 490х11 мм, заполненную 7,5 г сорбента «Силасорб С-18» с размером частиц 30  . После полного вхождения раствора в сорбент осуществляют хроматографирование, используя в качестве подвижной фазы систему растворителей ацетонитрил-1 н. раствор серной кислоты (8:2). Элюат собирают фракциями по 1 мл каждая. Фракции элюата №№5-7, содержащие 2,6-бис-[бис-( . После полного вхождения раствора в сорбент осуществляют хроматографирование, используя в качестве подвижной фазы систему растворителей ацетонитрил-1 н. раствор серной кислоты (8:2). Элюат собирают фракциями по 1 мл каждая. Фракции элюата №№5-7, содержащие 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидин, объединяют в мерной колбе вместимостью 10 мл, и доводят содержимое колбы до метки смесью растворителей ацетонитрил-1 н. раствор серной кислоты (8:2). Оптическую плотность полученного раствора измеряют на спектрофотометре СФ-46 при длине волны 286 нм в кюветах с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте. Количественное содержание 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидин, объединяют в мерной колбе вместимостью 10 мл, и доводят содержимое колбы до метки смесью растворителей ацетонитрил-1 н. раствор серной кислоты (8:2). Оптическую плотность полученного раствора измеряют на спектрофотометре СФ-46 при длине волны 286 нм в кюветах с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте. Количественное содержание 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидин определяют, используя уравнение калибровочного графика, и пересчитывают на навеску анализируемого вещества, внесенную в биологический материал. -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидин определяют, используя уравнение калибровочного графика, и пересчитывают на навеску анализируемого вещества, внесенную в биологический материал.
Построение калибровочного графика
В ряд мерных колб вместимостью 10 мл вносят 0,05, 0,1, 0,25, 0,5, 1,0, 2,0, 3,0, 4,0, 5,0 мл 0,004% раствора 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в смеси растворителей ацетонитрил-1 н. раствор серной кислоты (8:2) и доводят содержимое каждой колбы до метки смесью растворителей ацетонитрил-1 н. раствор серной кислоты (8:2). Полученные растворы фотометрируют при длине волны 286 нм на спектрофотометре СФ-46 в кювете с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте. По результатам измерений строят график зависимости оптической плотности раствора от концентрации определяемого вещества. Методом наименьших квадратов рассчитывают уравнение калибровочного графика, которое в данном случае имеет вид: -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в смеси растворителей ацетонитрил-1 н. раствор серной кислоты (8:2) и доводят содержимое каждой колбы до метки смесью растворителей ацетонитрил-1 н. раствор серной кислоты (8:2). Полученные растворы фотометрируют при длине волны 286 нм на спектрофотометре СФ-46 в кювете с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте. По результатам измерений строят график зависимости оптической плотности раствора от концентрации определяемого вещества. Методом наименьших квадратов рассчитывают уравнение калибровочного графика, которое в данном случае имеет вид:
D=0,06814·С+0.00089,
где D – оптическая плотность; С – концентрация определяемого вещества в фотометрируемом растворе, мкг/мл.
Результаты определения 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в ткани печени представлены в таблице 1. -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в ткани печени представлены в таблице 1.
Пример 2
Определение 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в крови -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в крови
К 25 мл крови прибавляют 10 мг 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина, тщательно перемешивают биологическую жидкость с веществом и оставляют на сутки при температуре 18-20°С. По истечении указанного времени биологический объект, содержащий анализируемое вещество, заливают 50 мл ацетона и выдерживают 30 минут при перемешивании. Извлечение отделяют, операцию настаивания повторяют еще раз в указанных условиях. Отдельные извлечения объединяют, фильтруют через стеклянный фильтр диаметром 3 см с 10 г безводного сульфата натрия. Через слой сульфата натрия дополнительно пропускают 25 мл ацетона. Отдельные фильтраты объединяют в фарфоровой чашке, растворитель испаряют в токе воздуха при комнатной температуре до получения сухого остатка. Остаток растворяют в 10 мл хлороформа, экстрагируют дважды порциями 0,1 н. раствора хлороводородной кислоты по 20 мл каждая, полученные извлечения отделяют, объединяют, встряхивают в делительной воронке в течение 3 минут с 40 мл эфира, эфирный слой отбрасывают, в водный слой вводят 3,6 г хлорида натрия, полученный раствор подщелачивают 10%-ным раствором гидроксида натрия до рН 8-10 и экстрагируют дважды порциями этилацетата по 40 мл каждая. Экстракты отделяют, объединяют в фарфоровой чашке и испаряют в токе воздуха при комнатной температуре до получения сухого остатка. Остаток растворяют в 2-3 мл смеси растворителей ацетонитрил-1 н. раствор серной кислоты, взятых в соотношении 8:2 (по объему), и вводят полученный раствор в колонку размерами 490×11 мм, заполненную 7,5 г сорбента «Силасорб С-18» с размером частиц 30 -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина, тщательно перемешивают биологическую жидкость с веществом и оставляют на сутки при температуре 18-20°С. По истечении указанного времени биологический объект, содержащий анализируемое вещество, заливают 50 мл ацетона и выдерживают 30 минут при перемешивании. Извлечение отделяют, операцию настаивания повторяют еще раз в указанных условиях. Отдельные извлечения объединяют, фильтруют через стеклянный фильтр диаметром 3 см с 10 г безводного сульфата натрия. Через слой сульфата натрия дополнительно пропускают 25 мл ацетона. Отдельные фильтраты объединяют в фарфоровой чашке, растворитель испаряют в токе воздуха при комнатной температуре до получения сухого остатка. Остаток растворяют в 10 мл хлороформа, экстрагируют дважды порциями 0,1 н. раствора хлороводородной кислоты по 20 мл каждая, полученные извлечения отделяют, объединяют, встряхивают в делительной воронке в течение 3 минут с 40 мл эфира, эфирный слой отбрасывают, в водный слой вводят 3,6 г хлорида натрия, полученный раствор подщелачивают 10%-ным раствором гидроксида натрия до рН 8-10 и экстрагируют дважды порциями этилацетата по 40 мл каждая. Экстракты отделяют, объединяют в фарфоровой чашке и испаряют в токе воздуха при комнатной температуре до получения сухого остатка. Остаток растворяют в 2-3 мл смеси растворителей ацетонитрил-1 н. раствор серной кислоты, взятых в соотношении 8:2 (по объему), и вводят полученный раствор в колонку размерами 490×11 мм, заполненную 7,5 г сорбента «Силасорб С-18» с размером частиц 30  . После полного вхождения раствора в сорбент осуществляют хроматографирование, используя в качестве подвижной фазы систему растворителей ацетонитрил-1 н. раствор серной кислоты (8:2). Элюат собирают фракциями по 1 мл каждая. Фракции элюата №№5-7, содержащие 2,6-бис-[бис-( . После полного вхождения раствора в сорбент осуществляют хроматографирование, используя в качестве подвижной фазы систему растворителей ацетонитрил-1 н. раствор серной кислоты (8:2). Элюат собирают фракциями по 1 мл каждая. Фракции элюата №№5-7, содержащие 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидин, объединяют в мерной колбе вместимостью 10 мл и доводят содержимое колбы до метки смесью растворителей ацетонитрил-1 н. раствор серной кислоты (8:2). Оптическую плотность полученного раствора измеряют на спектрофотометре СФ-46 при длине волны 286 нм в кюветах с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте. Количественное содержание 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидин, объединяют в мерной колбе вместимостью 10 мл и доводят содержимое колбы до метки смесью растворителей ацетонитрил-1 н. раствор серной кислоты (8:2). Оптическую плотность полученного раствора измеряют на спектрофотометре СФ-46 при длине волны 286 нм в кюветах с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте. Количественное содержание 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина определяют, используя уравнение калибровочного графика, и пересчитывают на навеску анализируемого вещества, внесенную в биологическую жидкость. -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина определяют, используя уравнение калибровочного графика, и пересчитывают на навеску анализируемого вещества, внесенную в биологическую жидкость.
Построение калибровочного графика
В ряд мерных колб вместимостью 10 мл вносят 0,05, 0,1, 0,25, 0,5, 1,0, 2,0, 3,0, 4,0, 5,0 мл 0,004% раствора 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в смеси растворителей ацетонитрил-1 н. раствор серной кислоты (8:2) и доводят содержимое каждой колбы до метки смесью растворителей ацетонитрил-1 н. раствор серной кислоты (8:2). Полученные растворы фотометрируют при длине волны 286 нм на спектрофотометре СФ-46 в кювете с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте. По результатам измерений строят график зависимости оптической плотности раствора от концентрации определяемого вещества. Методом наименьших квадратов рассчитывают уравнение калибровочного графика, которое в данном случае имеет вид: -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в смеси растворителей ацетонитрил-1 н. раствор серной кислоты (8:2) и доводят содержимое каждой колбы до метки смесью растворителей ацетонитрил-1 н. раствор серной кислоты (8:2). Полученные растворы фотометрируют при длине волны 286 нм на спектрофотометре СФ-46 в кювете с толщиной рабочего слоя 10 мм. Измерения проводят на фоне раствора, полученного в контрольном опыте. По результатам измерений строят график зависимости оптической плотности раствора от концентрации определяемого вещества. Методом наименьших квадратов рассчитывают уравнение калибровочного графика, которое в данном случае имеет вид:
D=0,06814·С+0,00089,
где D – оптическая плотность; С – концентрация определяемого вещества в фотометрируемом растворе, мкг/мл.
Результаты определения 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в крови представлены в таблице 2. -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в крови представлены в таблице 2.
Предлагаемый способ по сравнению с прототипом в 10 раз сокращает продолжительность одного определения (с 32 до 3-3,5 часов), в 1,3 раза увеличивает степень извлечения 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина из биологического материала (с 70,56% до 94,65%), в три раза повышает точность определения (относительная ошибка среднего результата уменьшается с ±10,71% до ±3,58%), характеризуется более высокой чувствительностью (открываемый минимум снижается с 4,0 до 0,8 мг в 100 г биологической ткани). -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина из биологического материала (с 70,56% до 94,65%), в три раза повышает точность определения (относительная ошибка среднего результата уменьшается с ±10,71% до ±3,58%), характеризуется более высокой чувствительностью (открываемый минимум снижается с 4,0 до 0,8 мг в 100 г биологической ткани).
Сравнительная характеристика предлагаемого и известного способов представлена в таблице 3.
| Таблица 1 |
Результаты определения 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в ткани печени (n=5; Р=0,95) -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в ткани печени (n=5; Р=0,95) |
| № |
Внесено 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина, мг в 25 г ткани печени -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина, мг в 25 г ткани печени |
Найдено |
Метрологические характеристики |
| мг |
% |
| 1. |
10,00 |
9,735 |
97,35 |
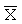 =94,65 =94,65 |
| 2. |
10,00 |
9,285 |
92,85 |
S=2,73 |
| 3. |
10,00 |
9,090 |
90,90 |
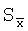 =1,22 =1,22 |
| 4. |
10,00 |
9,780 |
97,80 |
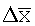 =3,39 =3,39 |
| 5. |
10,00 |
9,535 |
95,35 |
 =3,58 =3,58 |
| Таблица 2 |
Результаты определения 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-(1)пиримидина в крови (n=5; Р=0,95) -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-(1)пиримидина в крови (n=5; Р=0,95) |
| № |
Внесено 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-фпиримидина, мг в 25 г крови -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-фпиримидина, мг в 25 г крови |
Найдено |
Метрологические характеристики |
| мг |
% |
| 1. |
10,00 |
9,540 |
95,40 |
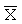 =97,94 =97,94 |
| 2. |
10,00 |
9,670 |
96,70 |
S=1,80 |
| 3. |
10,00 |
9,890 |
98,90 |
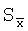 =0,80 =0,80 |
| 4. |
10,00 |
9,950 |
99,50 |
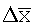 =2,22 =2,22 |
| 5. |
10,00 |
9,920 |
99,20 |
 =2,27 =2,27 |
| Таблица 3 |
| Сравнительная характеристика предлагаемого и известного способов (на примере исследования ткани печени) |
| Показатели |
Предлагаемый способ |
Известный способ |
| 1. Продолжительность одного определения |
3-3,5 часа |
Около 32 часов |
2. Степень извлечения 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина, в процентах от предварительно внесенного в биоматериал количества -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина, в процентах от предварительно внесенного в биоматериал количества |
94,65% |
70,56% |
| 3. Относительная ошибка среднего результата (n=5; Р=0,95) (при условии содержания 50 мг определяемого вещества в 100 г биоматериала) |
3,58% |
10,71% |
| 4. Чувствительность (открываемый минимум), мг в 100 г биоматериала |
0,8 |
4,0 |
Формула изобретения
Способ определения 2,6-бис-[бис-( -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в биологическом материале, заключающийся в том, что анализируемую пробу измельчают, неоднократно настаивают с органической жидкостью, полученные органические извлечения объединяют, анализируемое вещество переводят в раствор с сильно-кислой реакцией среды, раствор промывают эфиром, подщелачивают до щелочной реакции среды, экстрагируют гидрофобным органическим растворителем с последующим отделением экстракта, испарением экстрагента и определением анализируемого вещества в остатке, отличающийся тем, что настаивание проводят с ацетоном двукратно каждый раз в течение 30 мин, после объединения ацетоновых извлечений ацетон испаряют до сухого остатка, остаток растворяют в хлороформе, для переведения анализируемого вещества в раствор с сильно-кислой реакцией среды хлороформный раствор экстрагируют 0,1 н. раствором хлороводородной кислоты, после подщелачивания кислого раствора его насыщают хлоридом натрия, в качестве гидрофобного органического растворителя для экстракции применяют этилацетат, после испарения экстрагента остаток растворяют в смеси растворителей ацетонитрил-1 н. раствор серной кислоты, взятых в соотношении 8:2 (по объему), хроматографируют в колонке с сорбентом «Силасорб С-18» с размером частиц 30 мкм с использованием подвижной фазы ацетонитрил-1 н. раствор серной кислоты (8:2), фракции элюата, содержащие анализируемое вещество, объединяют и измеряют оптическую плотность элюата при длине волны 286 нм. -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо(5,4-d)пиримидина в биологическом материале, заключающийся в том, что анализируемую пробу измельчают, неоднократно настаивают с органической жидкостью, полученные органические извлечения объединяют, анализируемое вещество переводят в раствор с сильно-кислой реакцией среды, раствор промывают эфиром, подщелачивают до щелочной реакции среды, экстрагируют гидрофобным органическим растворителем с последующим отделением экстракта, испарением экстрагента и определением анализируемого вещества в остатке, отличающийся тем, что настаивание проводят с ацетоном двукратно каждый раз в течение 30 мин, после объединения ацетоновых извлечений ацетон испаряют до сухого остатка, остаток растворяют в хлороформе, для переведения анализируемого вещества в раствор с сильно-кислой реакцией среды хлороформный раствор экстрагируют 0,1 н. раствором хлороводородной кислоты, после подщелачивания кислого раствора его насыщают хлоридом натрия, в качестве гидрофобного органического растворителя для экстракции применяют этилацетат, после испарения экстрагента остаток растворяют в смеси растворителей ацетонитрил-1 н. раствор серной кислоты, взятых в соотношении 8:2 (по объему), хроматографируют в колонке с сорбентом «Силасорб С-18» с размером частиц 30 мкм с использованием подвижной фазы ацетонитрил-1 н. раствор серной кислоты (8:2), фракции элюата, содержащие анализируемое вещество, объединяют и измеряют оптическую плотность элюата при длине волны 286 нм.
|
|

 -оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо (5,4-d)пиримидина в биологическом материале, и может быть использовано в практике химико-токсикологических и клинических лабораторий. Биологическую ткань измельчают, двукратно настаивают с ацетоном каждый раз в течение 30 минут, полученные извлечения объединяют, объединенное извлечение фильтруют, фильтрат испаряют до получения сухого остатка, остаток растворяют в хлороформе, экстрагируют 0,1 н. раствором хлороводородной кислоты, хлороформный слой отбрасывают, полученный кислотный экстракт промывают эфиром, эфирный слой отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до рН 8-10, насыщают хлоридом натрия, экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в смеси растворителей ацетонитрил – 1 н. раствор серной кислоты, взятых в соотношении 8:2 (по объему), хроматографируют в колонке с сорбентом «Силасорб С-18» с размером частиц 30
-оксиэтил)-амино]-4,8-ди-N-пиперидино-пиримидо (5,4-d)пиримидина в биологическом материале, и может быть использовано в практике химико-токсикологических и клинических лабораторий. Биологическую ткань измельчают, двукратно настаивают с ацетоном каждый раз в течение 30 минут, полученные извлечения объединяют, объединенное извлечение фильтруют, фильтрат испаряют до получения сухого остатка, остаток растворяют в хлороформе, экстрагируют 0,1 н. раствором хлороводородной кислоты, хлороформный слой отбрасывают, полученный кислотный экстракт промывают эфиром, эфирный слой отбрасывают, водный слой подщелачивают 10% раствором гидроксида натрия до рН 8-10, насыщают хлоридом натрия, экстрагируют этилацетатом, полученный экстракт отделяют, обезвоживают, экстрагент испаряют, остаток растворяют в смеси растворителей ацетонитрил – 1 н. раствор серной кислоты, взятых в соотношении 8:2 (по объему), хроматографируют в колонке с сорбентом «Силасорб С-18» с размером частиц 30  с использованием подвижной фазы ацетонитрил – 1 н. раствор серной кислоты (8:2), фракции элюата, содержащие анализируемое вещество, объединяют и измеряют оптическую плотность элюата при длине волны 286 нм. Способ обеспечивает снижение затрат времени на осуществление анализа, увеличение степени извлечения, точности и чувствительности определения. 3 табл.
с использованием подвижной фазы ацетонитрил – 1 н. раствор серной кислоты (8:2), фракции элюата, содержащие анализируемое вещество, объединяют и измеряют оптическую плотность элюата при длине волны 286 нм. Способ обеспечивает снижение затрат времени на осуществление анализа, увеличение степени извлечения, точности и чувствительности определения. 3 табл.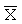 =94,65
=94,65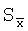 =1,22
=1,22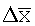 =3,39
=3,39 =3,58
=3,58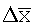 =2,22
=2,22