Патент на изобретение №2321592
|
||||||||||||||||||||||||||
(54) СПОСОБ ВВЕДЕНИЯ 1,2-ДВОЙНОЙ СВЯЗИ В 3-ОКСО-4-АЗАСТЕРОИДНЫЕ СОЕДИНЕНИЯ
(57) Реферат:
Описывается улучшенный способ получения 17
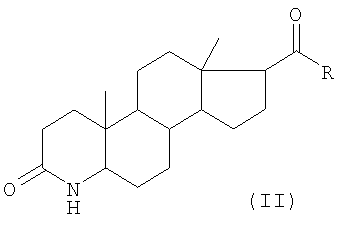
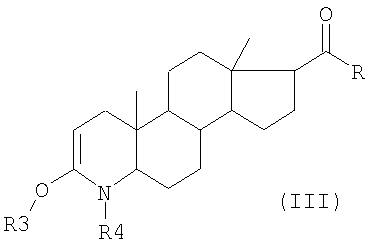
Настоящее изобретение относится к способу введения 1,2-двойной связи в 3-оксо-4-азастероиды путем дегидрирования 3-оксо-4-азастероидов, насыщенных в 1,2-положении, в частности, путем дегидрирования 17 Из патента EP 0 155 096 известно получение 17 Настоящее изобретение относится к такому альтернативному способу получения. Настоящее изобретение раскрывается в формуле изобретения. Настоящее изобретение относится к способу получения 17 в которой означают: R гидроксил, возможно замещенный, линейный или разветвленный (C1-C12)-алкил или (C1-C12)-алкенил; фенил или бензил; остаток -OR1, или остаток -NHR1, или остаток -NR1R2; R1 водород, возможно, замещенный, линейный или разветвленный (C1-C12)-алкил или (C1-C12)-алкенил, или фенил, возможно замещенный; R2 водород, метил, этил или пропил; или -NR1R2 5- или 6-членный гетероцикл, и для R = гидроксил также его фармацевтически приемлемая соль, отличающемуся тем, что (A) в 3-кето-4-аза-группу (лактамную группу) соединения общей формулы (II): вводят защитные группы, так что образуется соединение общей формулы (III): в котором означают: R3 триалкилсилил, или вместе с R4 остаток -C(О)-C(О)- или -C(О)-Y-C(О)-; R4 алкилоксикарбонил или фенилоксикарбонил, предпочтительно Boc (= трет-бутилоксикарбонил); или триалкилсилил, или вместе с R3 остаток -C(O)-C(O)- или -C(O)-Y-C(O)-; Y -[C(R5)(R6)]n-, или -CH(R5)=CH(R6)-, или ортофенилен; R5 и R6 – независимо друг от друга водород, линейный или разветвленный (C1-С8)-алкил или -алкенил, фенил, возможно замещенный, или бензил; и n целое число от 1 до 4; и в случае, если R означает гидроксил, оно, возможно, прореагировало с защитной группой; (B) полученное [согласно стадии (A)] соединение реагирует (i) в присутствии катализатора дегидрирования и (ii) в присутствии, возможно замещенного, бензохинона, аллилметилкарбоната, аллилэтилкарбоната и/или аллилпропилкарбоната, причем в 1/2-положение вводится (C) защитные группы R3 и R4 удаляют, и при R = гидроксил полученное соединение возможно преобразуют в соль. R предпочтительно означает линейный или разветвленный (C1-C6)-алкил, предпочтительно метил, этил, пропил или н-бутил, втор-бутил или трет-бутил, предпочтительно трет-бутил; или остаток -OR1, или остаток -NHR1, или остаток -NR1R2. Предпочтительно остаток означает -NHR1. Если R означает гидроксил (или остаток -C(О)R означает карбоксил), согласно изобретению может также быть получена фармацевтически приемлемая соль соединения формулы (I), предпочтительно соль щелочного металла, соль щелочно-земельного металла или аммонийная соль, предпочтительно соль натрия, калия или аммония, предпочтительно соль натрия или калия. R1 означает предпочтительно линейный или разветвленный (C1-C6)-алкил, или фенил, возможно замещенный. R1 как (C1-C6)-алкил означает предпочтительно метил, этил, пропил, н-бутил, втор-бутил или трет-бутил, предпочтительно трет-бутил. R1 как фенил, возможно замещенный, означает предпочтительно моно(трифторметил)фенил или бис(трифторметил)фенил, предпочтительно 2,5-бис(трифторметил)фенил. В остатке -NR1R2 R2 предпочтительно означает метил. Заместитель -NR1R2 как 5- или 6-членный гетероцикл означает предпочтительно остаток пиперидина или пирролидина. Предпочтительно заместитель является -NHR1, в котором R1 означает трет-бутил или 2,5-бис(трифторметил)фенил. R3 предпочтительно означает триметилсилил или вместе с R4 остаток -C(О)-C(О)- или -C(O)-Y-C(O)-. R4 предпочтительно означает BOC, триметилсилил или вместе с R3 остаток -C(О)-C(O)- или -C(О)-Y-C(О)-. Предпочтительно R4 означает Boc или вместе с R3 остаток -C(O)-C(О)- или -C(О)-Y-C(О)-. R4 как алкилоксикарбонил означает предпочтительно изобутилоксикарбонил, трет-бутилоксикарбонил, трет-амилоксикарбонил, циклобутилоксикарбонил, 1-метилциклобутилоксикарбонил, циклопентилоксикарбонил, циклогексилоксикарбонил, 1-метилциклогексил, предпочтительно трет-бутилоксикарбонил. R5 и R6 независимо друг от друга предпочтительно означают водород, линейный или разветвленный (C1-С4)-алкил, или фенил, предпочтительно водород, метил, этил или пропил или фенил. n означает предпочтительно 1 или 2, предпочтительно 1. Предпочтительно Y означает остаток -CH(R5)- или ортофенилен, предпочтительно метилен. Для введения защитной триалкилсилильной группы, т.е. для силилирования NH-группы и/или атома кислорода или OH-группы [согласно стадии (A)] предпочтительно применяют (алкил)3Si(галоген), например, (CH3)3SiCl, или бистриметилсилилтригалогенацетамид, бистриметилсилилацетамид, гексаметилдисилазан и/или бистриметилмочевину, предпочтительно бистриметилсилилтрифторацетамид, или триалкилсилилтрифторметансульфонат, предпочтительно триметилсилилтрифторметансульфонат. Условия реакции силилирования известны из патента EP 0473226. Для введения защитной группы, когда R3 вместе с R4 являются остатком -C(О)-C(О)- или -C(О)-Y-C(О)-, соединение общей формулы (II) или лактамную группу [согласно стадии (A)] подвергают взаимодействию с оксалилхлоридом (хлорангидрид щавелевой кислоты) или малонилхлоридом (хлорангидрид малоновой кислоты), причем оксалилхлорид предпочтителен. Условия реакции с оксалилхлоридом известны из патента EP 0428366, и с малонилхлоридом или аналогично реагирующими соединениями должны использоваться аналогичным образом. Для введения защитной группы, когда R4 означает алкилоксикарбонил, например, трет-бутилоксикарбонил (Boc), используют известный способ, в котором соединение общей формулы (II) приводят во взаимодействие, например, с Boc-ангидридом (Boc-О-Boc) {[(CH3)3C-О-C(О)]2-О} или с Boc-карбаматом [(CH3)3C-O-C(О)-N(C1-4-алкил)2]. При этом Boc может здесь означать и другие аналогично реагирующие соединения, то есть соединения, в которых трет-бутиловый остаток замещен другим аналогично реагирующим остатком, как, например, названные остатки трет-амил, циклобутил, циклопентил или циклогексил. Такие аналогичные реакции в большом количестве описаны в литературе. Если R3 означает триалкилсилил, а R4 означает Boc, то сначала вводят защитную Boc-группу, а затем силилируют. На стадии (B) соединение, полученное на стадии (A), превращают в присутствии (i) катализатора дегидрирования и в присутствии (ii) бензохинона, возможно замещенного, аллилметилкарбоната, аллилэтилкарбоната и/или аллилпропилкарбоната, при этом в 1-/2-положение вводится Для термической стабилизации палладиевого комплекса можно использовать дополнительный комплексообразователь, как 2,2′-дипиридил или 1,10-фенантролин, предпочтительно 2,2′-дипиридил. Для объяснения механизма катализа можно указать, что элемент Pd присоединяется к C-атому в 2-положение с отщеплением кислород-защищающей группы [например, группы -Si(CH3)3]. Последующее отщепление бета-водорода у C-атома в 1 положении приводит к образованию желаемой В качестве хинона можно применять также замещенный хинон, например, хинон, замещенный C1-4-алкилом, галогеном, циано или нитро. Такие хиноны известны. На стадии (C) полученное соединение превращают в соединение формулы (I) путем удаления введенных защитных групп. Это происходит предпочтительно обработкой подходящей кислотой, например, муравьиной кислотой, уксусной кислотой и/или трифторуксусной кислотой, предпочтительно муравьиной кислотой. Затем полученное соединение можно при необходимости известным путем перевести в фармацевтически приемлемую соль (для R = гидроксил). Предпочтительно полученное соединение перекристаллизовывают. Эту перекристаллизацию можно проводить в неполярных растворителях, таких как бензин, гептан, гексан и толуол, предпочтительно в толуоле. Под соединением формулы (I) имеется в виду, в частности, упоминавшееся выше соединение 17 Свойства 17 Для описанного способа со стадиями (A)-(C) в качестве растворителя могут применяться многочисленные органические безводные соединения, такие как, например, толуол, бензин, гексан, гептан, трет-бутиловый спирт, диэтиловый эфир, ацетон, бензол, диоксан, тетрагидрофуран, хлороформ, диметилформамид или пиридин. Следующие примеры поясняют изобретение. Пример 1 (Замещение дигидрофинастерида группой Boc по атому азота 3-кето-4-аза-группы) 10 г (26,7 ммоль) дигидрофинастерида помещают в тетрагидрофуран (ТГФ) и охлаждают до -78°C. К полученной суспензии прибавляют 15 мл (30 ммоль) раствора диизопропиламида лития (Li-ДА-раствор), и прозрачный раствор перемешивают около 30 минут. Затем прибавляют раствор 6,7 г (30 ммоль) Boc-ангидрида в ТГФ. Раствор оставляют нагреваться до комнатной температуры. После обычной обработки получают влажный желтый порошок, который в течение ночи выдерживают в сушильном шкафу и непосредственно используют в примере 2. Пример 2 (Силилирование соединения, полученного в примере 1) 1 г (2,1 ммоль) 4-Boc-дигидрофинастерида растворяют в ТГФ. К прозрачному желтому раствору добавляют при охлаждении смесью льда с метанолом 2,3 мл (4,6 ммоль) раствора Li-ДА. Суспензию перемешивают около 45 минут, после чего по каплям добавляют 0,46 г (4,2 ммоль) триметилхлорсилана (TMSCl) при 18-20°C. Прозрачный раствор концентрируют и остаток соединяют с гептаном. После фильтрации фильтрат концентрируют насколько возможно и полученное масло медово-коричневого цвета используют на следующих стадиях (пример 3 и пример 5). Пример 3 (Введение 0,145 г (0,65 ммоль) ацетата палладия растворяют с 0,07 г (0,65 ммоль) бензохинона в ацетонитриле и оставляют. 0,8 г (1,5 ммоль) силильного соединения, полученного согласно примеру 3, соединяют с ацетонитрилом и добавляют по каплям при внутренней температуре (ВТ) 20-25°C. Реакционную смесь перемешивают 8 часов и очищают силикагелем. Слабоокрашенный прозрачный раствор концентрируют при температуре окружающей среды 55-60°C. Полученное твердое вещество используют в примере 4. Пример 4 (Удаление защитных групп и кристаллизация) a) 0,5 г твердого вещества из примера 3 смешивают с 20 г (0,175 моль) трифторуксусной кислоты и нагревают с обратным холодильником около 15 часов. При этом трифторуксусную кислоту используют и как реагент, и как растворитель. После охлаждения реакционную смесь выливают на смесь 300 г насыщенного раствора бикарбоната натрия и 50 г льда и экстрагируют 20 г эфира уксусной кислоты; b) коричневый полупродукт, полученный на предыдущей стадии a), растворяют в толуоле при 90°C (массовое отношение толуол:сырье = 6:1), охлаждают до 20-25°C. Выпавшую в осадок серовато-белую массу отфильтровывают при 20-25°C и сушат. Получают финастерид полиморф I. Пример 5 (Введение 2,0 г (3,7 ммоль) соединения из примера 2 смешивают с 1,29 г (11,1 ммоль) аллилметилкарбоната в ацетонитриле. Смесь добавляют по каплям к нагретому до 60-70°C раствору 166 мг (0,74 ммоль) ацетата палладия-II в ацетонитриле. Через 1-2 часа нагрева с обратным холодильником обрабатывают, как описано в примере 3. Получено 3 г твердого вещества. Пример 6 (Введение A) 20 г (0,047 моль) оксалиленолового эфира дигидрофинастерида [соединение IIIa, с R = -NH-трет-бутил, R3 и R4 = -C(O)-C(О)-] нагревают вместе с 16,3 г (0,140 моль) аллилметилкарбоната и 76 г безводного ацетонитрила до температуры флегмообразования. Прибавляют поочередно 5 порций смеси, содержащей каждый раз по 18 г ксилола и по 0,049 г комплекса трис(дибензилиденацетон)дипалладий – хлороформ (полное мольное количество катализатора 0,284 ммоль). Каждый раз при добавлении наблюдается значительное газообразование. Через 12 ч нагрева с обратным холодильником реакцию возобновляют путем добавления второй порции горячей смеси, содержащей по 3 г ксилола и по 0,024 г катализатора дегидрирования (смесь медленно нагревают), при необходимости добавляют последующие порции. После фильтрации реакционную смесь по возможности концентрируют, после чего остается 24,5 г желтой, медообразной массы. B) Медообразную массу соединяют с 105 г метанола и охлаждают до 0-5°C. Медленно прибавляют 11,3 г (0,0403 моль) 25%-ного раствора метоксида калия и перемешивают около 1 часа при внутренней температуре 0-5°C. Затем добавляют 20 г воды и удаляют охлаждающую ванну, внутреннюю температуру повышают до 15-20°C. Смесь концентрируют до сухого состояния, к твердому остатку добавляют 50 г воды, 90 г толуола и 12 г метанола и 1 час нагревают при температуре флегмообразования. После остановки мешалки без проблем разделяют органическую и водную фазы; органическую фазу выделяют горячей. Охлаждение в пределах 2-4 часов до 25°C приводит финастерид в полиморфной форме I к кристаллизации. После сушки получают 8,1 г белого порошка. Пример 7 Осуществляют способ, аналогичный описанному в примерах с 1 по 6, когда вводят Пример 8 (Получение метилового эфира 3-оксо-4-аза-5 Стадия 1 (Получение соединения IIIb, т.е., соединения формулы (III), где R = -OMe, R3 и R4 = -C(O)-C(O)-) 2 г (0,005 моль, содержание >95%) метилового эфира 3-оксо-4-аза-5 1H-ЯМР (200 МГц, CDCl3, Стадия 2 (Введение 0,2 г (0,5 ммоль) полученного на стадии 1 соединения IIIb нагревают вместе с 8 г абсолютного ацетонитрила, 1,5 г хлороформа, 0,18 г (1,5 ммоль) аллилметилкарбоната и 0,05 г (0,05 ммоль) палладиевого катализатора при температуре флегмообразования (70-80°C). Уже при нагревании наблюдается образование газа. Через примерно 30 минут нагрева с обратным холодильником реакционную смесь концентрируют насколько возможно, остаток соединяют со смесью 15 г метанола и 5 г толуола и нагревают до образования прозрачного раствора. После охлаждения до 0-5°C медленно добавляют раствор, содержащий 0,18 г (1 ммоль) 30%-ного раствора метилата натрия в 2 г метанола, прозрачный раствор перемешивают 1 час. После удаления охлаждающей ванны добавляют к этому 3 г воды и мутную смесь перемешивают при комнатной температуре еще 1 час. Затем концентрируют насколько возможно и к остатку добавляют 10 г толуола, а также 3 г воды. Как только при нагревании смесь разделится на две прозрачные фазы, органическую фазу отделяют и охлаждают. Добавление 2-4 г гептана приводит к кристаллизации продукта. После фильтрации, повторной промывки примерно 5 г гептана и сушки отсасыванием остается 34 мг метилового эфира 3-оксо-4-аза-5 1H-ЯМР (200 МГц, CDCl3, Пример 9 (Получение дутастерида) Стадия 1 (получение 3-оксо-4-аза-5 Суспензию из 100 г (0,26 моль) дигидрофинастерида, 480 г 20%-ного раствора HCl (2,63 моль) и 120 г метанола нагревают до температуры флегмообразования и 8-12 часов интенсивно кипятят. Эдукт при нагревании переходит в раствор, через 8 часов получают суспензию, которую можно легко отфильтровать. Осадок трижды интенсивно промывают на нутч-фильтре, используя каждый раз по 100 г воды, примерно 15 минут сушат отсасыванием и затем сушат в течение ночи. Выход: 60 г. 1Н-ЯМР (200 МГц, DMSO, Стадия 2 (Получение соединения IIIc, т.е. соединения формулы (III), где R=Cl, R3 и R4 = -C(O)-C(O)- К суспензии 40 г (0,12 моль) соединения со стадии 1 в 633 г бензола при охлаждении по каплям в пределах 20-30 минут добавляют 159 г (1,2 моль) оксалилхлорида, суспензию перемешивают 12 часов (газообразования незаметно). При пониженном давлении и комнатной температуре дистилляцией отделяют бензол и избыточный оксалилхлорид до тех пор, пока объем первоначального раствора не сократится наполовину. При этом в осадок выпадает серовато-белое твердое вещество, которое после фильтрации трижды промывают гептаном, используя каждый раз по 150 г, и примерно 15 минут сушат отсасыванием. Выход: 37,1 г соединения IIIc. 1H-ЯМР (200 МГц, CDCl3, Стадия 3 (Получение соединения IIId (R= -NH-(2,5-(CF3)2-C6H3), R3 и R4 = -C(О)-C(O)- Суспензию из 1,48 г (6 ммоль) бис-2,5-трифторметиланилина, 2,35 г (5,3 ммоль) соединения IIIc со стадии 2 и 50 г толуола примерно 8 часов нагревают при температуре флегмообразования (100-110°C) и затем охлаждают. При пониженном давлении и комнатной температуре толуол и анилин отделяют дистилляцией до тех пор, пока объем первоначального раствора не уменьшится наполовину. К суспензии добавляют 30 г гептана и нагревают до 60-70°C. Через один час интенсивного перемешивания фильтруют на нутче, остаток на нутч-фильтре четыре раза интенсивно промывают, каждый раз по 10 г гептана, и примерно 30-45 минут сушат отсасыванием. Выход: 1,7 г соединения III. 1H-ЯМР (200 МГц, CDCl3, Стадия 4 (Получение дутастерида) 1 г (1,6 ммоль) соединения IIId со стадии 3 нагревают вместе с 8 г абсолютного ацетонитрила, 2 г хлороформа, 0,55 г (4,8 ммоль) аллилметилкарбоната и 0,17 г (0,16 ммоль) палладиевого катализатора до температуры флегмообразования (70-80°C). Уже при нагревании наблюдается образование газа. Через примерно 30 минут нагрева с обратным холодильником (образования газа больше не видно) реакционную смесь по возможности концентрируют и остаток соединяют с 5 г метанола. После охлаждения до 0-5°C медленно добавляют раствор, состоящий из 0,6 г (3,2 ммоль) 30%-ного раствора метилата натрия в 4 г метанола, и прозрачный раствор 1 час перемешивают также при внутренней температуре 0-5°C. После удаления охлаждающей ванны к этому прибавляют 3 г воды, снова перемешивают 1 час при комнатной температуре, мутную смесь концентрируют насколько возможно и к остатку добавляют 20 г толуола, а также 6 г воды. Смесь нагревают до температуры флегмообразования. Через 30 минут прозрачную органическую фазу отделяют горячей и охлаждают до комнатной температуры. Добавление 5-10 г гептана приводит к кристаллизации дутастерида. После фильтрования, трехкратного промывания гептаном, каждый раз по 4 г, и сушки отсасыванием выделяют 0,3 г дутастерида. 1H-ЯМР (200 МГц, CDCl3,
Формула изобретения
1. Способ получения 17
где R гидроксил, линейный или разветвленный (С1-С4)-алкил или (С1-C4)-алкенил; фенил или бензил; остаток -OR1, или остаток -NHR1, или остаток -NR1R2; R1 водород, линейный или разветвленный (С1-С4)-алкил или (C1-C4)-алкенил, или фенил, возможно замещенный; R2 водород, метил, этил или пропил; или -NR1R2 означает 5- или 6-членный гетероцикл, и в случае, когда R означает гидроксил, также их фармацевтически приемлемых солей, отличающийся тем, что (А) в 3-кето-4-аза-группу (лактамную группу) соединения общей формулы (II)
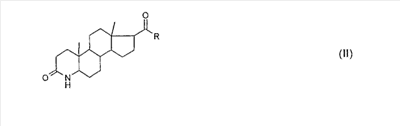
вводят защитные группы, так что образуется соединение общей формулы (III)
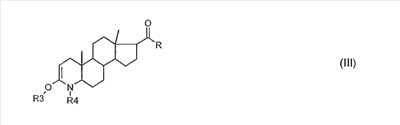
в которой R3 триалкилсилил, или вместе с R4 остаток -С(O)-С(O)- или -C(O)-Y-C(O)-; R4 алкилоксикарбонил или фенилоксикарбонил, предпочтительно Boc (=трет-бутилоксикарбонил); или триалкилсилил, или вместе с R3 остаток -С(O)-С(O)- или -C(O)-Y-C(O)-; Y-[С(R5)(R6)]n- или ортофенилен; R5 и R6 независимо друг от друга водород, метил или этил; и n целое число от 1 до 4; и в случае, если R означает гидроксил, возможно, реагирует с защитной группой; (В) полученное [согласно стадии (А)] соединение преобразовывают в присутствии (i) катализатора дегидрирования, выбранного из соединений металлов группы VIII периодической системы элементов, и в присутствии (ii) бензохинона, возможно замещенного, аллилметилкарбоната, аллилэтилкарбоната и/или аллилпропилкарбоната, при этом в 1-/2-положение вводится (С) защитные группы R3 и R4 удаляют, и при R=гидроксил полученное соединение при необходимости переводят в соль. 2. Способ по п.1, отличающийся тем, что R означает метил, этил, пропил или н-бутил, втор-бутил или трет-бутил, предпочтительно трет-бутил; или остаток -OR1, или остаток -NHR1, или остаток -NR1R2, предпочтительно остаток -NHR1, предпочтительно -NH-трет-бутил, или фенил, возможно замещенный. 3. Способ по п.1 или 2, отличающийся тем, что R1 означает метил, этил, пропил, н-бутил, втор-бутил или трет-бутил, предпочтительно трет-бутил. 4. Способ по п.1 или 2, отличающийся тем, что R означает остаток -NHR1, где R1 означает 2,5-бис(трифторметил)фенил. 5. Способ по п.1 или 2, отличающийся тем, что в остатке -NR1R2 заместитель R2 означает метил. 6. Способ по п.1 или 2, отличающийся тем, что заместитель -NR1R2 как 5- или 6-членный гетероцикл означает остаток пиперидина или пирролидина. 7. Способ по одному из пп.1-6, отличающийся тем, что R3 означает триметилсилил, или вместе с R4 остаток -С(O)-С(O)- или -C(O)-Y-C(O)-. 8. Способ по одному из пп.1-6, отличающийся тем, что R4 означает алкилоксикарбонил, предпочтительно изобутилоксикарбонил, трет-бутилоксикарбонил, трет-амилоксикарбонил, циклобутилоксикарбонил, 1-метилциклобутилоксикарбонил, циклопентилоксикарбонил, циклогексилоксикарбонил, 1-метилциклогексилоксикарбонил, предпочтительно трет-бутилоксикарбонил. 9. Способ по одному из пп.1-8, отличающийся тем, что R4 означает Boc, триметилсилил, или вместе с R3 остаток -С(O)-С(O)-или -C(O)-Y-C(O)-, предпочтительно Boc, или вместе с R3 означает остаток -С(O)-С(O)- или -C(O)-Y-C(O)-. 10. Способ по п.9, отличающийся тем, что R5 и R6 означают независимо друг от друга водород, метил, этил или пропил или орто-фенилен, предпочтительно остаток -CH(R5)- или орто-фенилен, предпочтительно метилен, и n равен 1 или 2, предпочтительно 1. 11. Способ по одному из пп.1-9, отличающийся тем, что для введения защитной группы Boc используют соединение общей формулы (II) Вос-ангидрид, или Вос-карбамат, или аналогичное соединение, в котором трет-бутиловый остаток заменен трет-амилом, циклобутилом, циклопентилом или циклогексилом. 12. Способ по одному из пп.1-11, отличающийся тем, что катализатор дегидрирования [на стадии (В)] выбран из соединений железа, рутения и осмия; кобальта, родия и иридия; никеля, палладия и платины; меди, серебра и золота; предпочтительно из соединений на основе родия, палладия и платины. 13. Способ по п.12, отличающийся тем, что катализатор дегидрирования [на стадии (В)] выбран из соединений Pd(0), и предпочтительно является комплексом трис(дибензилиденацетон) дипалладий – хлороформ. 14. Способ по п.12, отличающийся тем, что катализатор дегидрирования [на стадии (В)] выбран из соединений Pd(II), предпочтительно из PdCl2, Pd(dppe)2, dppe=бис-(1,2-дифенилфосфин)этан], Pd(dppe)Cl2, Pd(OAc)2, Pd(dppe)(OAc)2 и/или из комплексов 15. Способ по одному из пп.1-14, отличающийся тем, что для термической стабилизации катализатора дегидрирования, предпочтительно соли палладия или комплекса палладия, присутствует дополнительный комплексообразователь, предпочтительно 2,2 16. Способ по одному из пп.1-15, отличающийся тем, что в качестве хинона [на стадии (В)] используют замещенный хинон, предпочтительно хинон, замещенный C1-4-алкилом, галогеном, циано- или нитрогруппой. 17. Способ по одному из пп.1-16, отличающийся тем, что введенные [на стадии (С)] защитные группы удаляют путем обработки подходящей кислотой, предпочтительно обработкой муравьиной кислотой, уксусной кислотой и/или трифторуксусной кислотой, предпочтительно муравьиной кислотой. 18. Способ по одному из пп.1-17, отличающийся тем, что полученное [на стадии (С)] соединение, в котором R означает гидроксил, превращают в соль щелочного металла, соль щелочноземельного металла или аммонийную соль, предпочтительно в соль натрия, калия или аммония, предпочтительно в соль натрия или калия. 19. Способ по одному из пп.1-17, отличающийся тем, что полученное соединение формулы (I) кристаллизуют из неполярного растворителя, предпочтительно из бензина, гептана, гексана и/или толуола, предпочтительно из толуола. 20. Способ по п.19, отличающийся тем, что полученное соединение формулы (I), представляющее собой 17 21. Способ по п.19, отличающийся тем, что полученное соединение формулы (I), представляющее собой 17 Приоритеты по пунктам: 16.07.2002 по пп.1-21; 08.08.2002 по пп.1-21; 08.01.2003 по пп.1-21.
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 03.07.2009
Извещение опубликовано: 27.07.2010 БИ: 21/2010
|
||||||||||||||||||||||||||

 -замещенных 4-аза-андрост-1-ен-3-онов общей формулы (I), где R-OH, С1-4алкил, С1-4алкенил, фенил, бензил и др. или их фармацевтически приемлемых солей, заключающийся в том, что в 3-кето-4-аза (лактамную группу) соединения общей формулы II, где R имеет указанные значения, вводят защитные группы с образованием соединения общей формулы III, где R3 триалкилсилил, или вместе с R4 остаток -С(O)-С(O)- или -C(O)-Y-C(O)-, где R4 – предпочтительно трет-бутилоксикарбонил, Y – (CH2)n n=1÷4, или ортофенилен, после чего полученное соединение преобразовывают в присутствии катализатора дегидрирования и в присутствии бензохинона, аллилметилкарбоната, аллилэтилкарбоната и/или аллилпропилкарбоната, при этом в 1,2-положение вводится
-замещенных 4-аза-андрост-1-ен-3-онов общей формулы (I), где R-OH, С1-4алкил, С1-4алкенил, фенил, бензил и др. или их фармацевтически приемлемых солей, заключающийся в том, что в 3-кето-4-аза (лактамную группу) соединения общей формулы II, где R имеет указанные значения, вводят защитные группы с образованием соединения общей формулы III, где R3 триалкилсилил, или вместе с R4 остаток -С(O)-С(O)- или -C(O)-Y-C(O)-, где R4 – предпочтительно трет-бутилоксикарбонил, Y – (CH2)n n=1÷4, или ортофенилен, после чего полученное соединение преобразовывают в присутствии катализатора дегидрирования и в присутствии бензохинона, аллилметилкарбоната, аллилэтилкарбоната и/или аллилпропилкарбоната, при этом в 1,2-положение вводится  1-двойная связь, с последующим удалением защитных групп, и при необходимости (когда R-OH) переводом в соли. Способ дает высокий выход и степень чистоты продуктов. 20 з.п.ф-лы.
1-двойная связь, с последующим удалением защитных групп, и при необходимости (когда R-OH) переводом в соли. Способ дает высокий выход и степень чистоты продуктов. 20 з.п.ф-лы.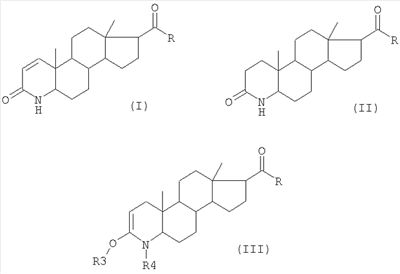
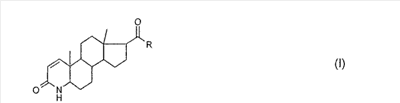
 -андрост-1-ен-17
-андрост-1-ен-17 ): 4,95 (1H, т); 3,68 (3H, с); 3,62-3,5 (1H, м); 3,22-3,06 (1H, м); 2,41-0,80 (17H, м); 0,97 (3H, с); 0,68 (3H, с)
): 4,95 (1H, т); 3,68 (3H, с); 3,62-3,5 (1H, м); 3,22-3,06 (1H, м); 2,41-0,80 (17H, м); 0,97 (3H, с); 0,68 (3H, с)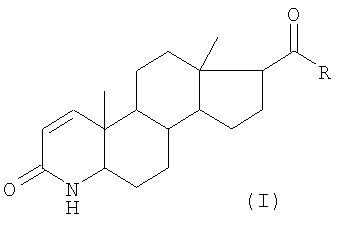
 -аллил-Pd, предпочтительно димера
-аллил-Pd, предпочтительно димера  -бипиридил или 1,10-фенантролин, предпочтительно 2,2
-бипиридил или 1,10-фенантролин, предпочтительно 2,2