Патент на изобретение №2321587
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ 2,4-ДИФЕНИЛТИОФЕНА
(57) Реферат:
Изобретение относится к области органического синтеза, в частности к способу получения 2,4-дифенилтиофена, который находит применение в качестве реагента в органическом синтезе, в синтезе лекарственных препаратов, инсектицидов, красителей. Сущность способа заключается во взаимодействии стирола и элементной серы под воздействием ультразвука с частотой 22 кГц и мощностью 1-3 Вт/см3. Процесс ведут при мольном соотношении стирол:сера, равном 1:1-3, при температуре от 20 до 160°С в течение 2 часов. Предложенный способ позволяет упростить технологический процесс и повысить выход целевого продукта до 57%.
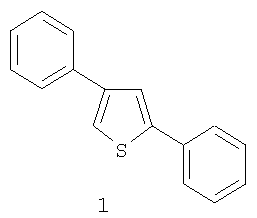
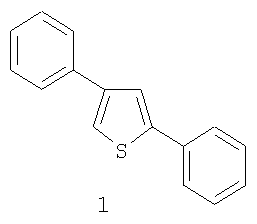
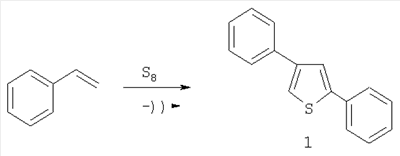
Предлагаемое изобретение относится к органической химии, в частности к способу получения 2,4-дифенилтиофена общей формулы (1):
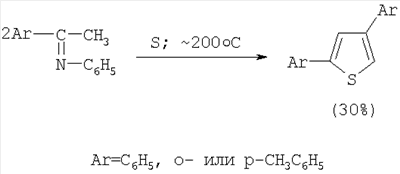
Соединения тиофенового ряда нашли применение как сополимеры для получения полимеров с фотофизическими свойствами (Wiley Periodicals, Inc J Polym Scientific, Part A: Polym Chem 2004; 42: 6061-6070) в качестве специальных реагентов для синтеза лекарственных препаратов (Fujita М, Hirayama Т, Ikeda N. Bioorg. Med. Chem. 2002; 10(10):3113-22), биологически активных препаратов с антибактериальными, антигрибковыми и антивирусными свойствами. Известен способ (Bogert М.Т., Herrera P.P., J. Am. Chem. Soc., 1923, 45, 238) синтеза 2,4-дифенилтиофена из анилидов и арилзамещенных метилкетонов и элементной серы при 200°С по схеме: Недостатками данного способа являются высокая температура и применение труднодоступных анилидов арилзамещенных метилкетонов.
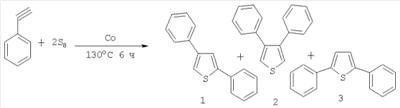
Недостатками данного способа являются высокая температура и применение галогенидов – бромстиролов. В данном способе недостатком является использование дорогостоящего катализатора – кобальта и труднодоступного фенилацетилена, выход 2,4-дифенилтиофена (1) составил 15%. Известен способ (Baumann E., Fromm Е., Ber., 1895, 28, 890) получения 2,5-дифенилтиофена, в частности взаимодействием двух молей стирола или коричной кислоты с элементной серой при нагревании, по схеме: Данный способ позволяет получать 2,4-дифенилтиофен как побочный продукт с небольшим выходом. Задачей данного изобретения является получение 2,4-дифенилтиофена с более высоким выходом и более простым способом. Предлагается новый способ синтеза 2,4-дифенилтиофена. Это достигается взаимодействием стирола с элементной серой под воздействием ультразвуковой кавитации. При ультразвуковой кавитации происходит образование, рост, пульсация и другие типы движения пузырьков, а также их взаимодействие с жидкостью, между собой и с твердыми поверхностями при условиях, когда в жидкости создается пониженное, а затем повышенное давление. При схлопывании пузырьков образуются ударные волны, вызывающие очень высокие локальные температуры и давления, инициирующие микроперемешивание. В этих условиях происходит образование активных частиц (радикалов, ионов, атомов, электронновозбужденных частиц), инициирующих различные реакции как в кавитационных полостях, так и в самой жидкости. Мольное соотношение реагентов стирол:сера равно 1:1-3. Изменение соотношения элементной серы менее 1 моль на 1 моль стирола приводит к понижению конверсии. Температура реакции регулируется мощностью ультразвука в пределах 1-3 Вт/см3. Целевой продукт реакции – 2,4-дифенилтиофен, выход которого достигает 57%. Существенные отличия предлагаемого способа. В предлагаемом способе в качестве инициатора химических превращений используется кавитация. В известном способе применяется нагревание исходных реагентов – стирола и элементной серы, с получением предпочтительно 2,5-дифенилтиофена (3), а 2,4-дифенилтиофен (1) является побочным продуктом с небольшим выходом. В других известных способах выход 2,4-дифенилтиофена не превышает 37%. Преимущества предлагаемого способа. Способ позволяет получать с высокой региоселективностью 2,4-дифенилтиофен (57%). Разработанный нами метод отличается простотой проведения эксперимента и не требует применения труднодоступных реагентов, нагревательных и перемешивающих устройств. Способ поясняется примерами. ПРИМЕР 1. В стеклянный реактор с обратным холодильником на половину глубины жидкости погружен волновод УЗНД-2Т с рабочей частью диаметром 15 мм и помещена термопара для определения температуры, подсоединенная к вольтметру. При комнатной температуре 20°С помещают 1 моль стирола, в состав которого входит ингибитор полимеризации (1%), и 3 моля элементной серы. В течение 10 мин происходит повышение температуры до 130°С. Дальнейшее повышение температуры имеет плавный характер: в течение часа температура поднимается до 140°С, в последующий час температура поддерживается в интервале 145-160°С. Затем реакционную массу охлаждали до 20°, при этом кристаллизуется сера, не вступившая в реакцию после центрифугирования и фильтрования, смесь продуктов разделяли вакуумной разгонкой из хлороформного экстракта. Получен 2,4-дифенилтиофен с выходом 57%, т.кип. 176°С при 6 мм ртутного столба. Спектральные характеристики (Спектры ЯМР 1Н зарегистрированы на спектрометре “Tesla BS-487” (100 МГц), ЯМР 13С на спектрометре “Jeol FX 90Q” (89.55 и 22.50 МГц), внутренний стандарт ТМС, растворитель CDCl3. Хромато-масс-спектральный анализ соединений проводили на приборе Finigan 4021.) 2,4-дифенилтиофена:
Спектр ЯМР 1Н ( Масс-спектр, m/z (Iотн, %): 236 (100) [M]+, 202 (28) [M-HSH]+, 191 (22) [M-SCH]+, 134 (13) [C8H6S]+, 102 (8) [С8Н6]+, 89 (76) [C7H5], 77 (10) [С6Н5]+. ПРИМЕР 2. Аналогичным способом при соотношение 1 моль стирола и 1 моль элементной серы получают 2,4-дифенилтиофен с выходом 22%.
Формула изобретения
Способ получения 2,4-дифенилтиофена
взаимодействием стирола и элементной серы при нагревании, отличающийся тем, что процесс осуществляется под воздействием ультразвука, инициирующего интенсивное перемешивание и нагрев реакционной массы от 20 до 160°С, в течение 2 ч при мольном соотношении стирол:сера, равном 1:1-3, в стирол вводят ингибитор полимеризации.
|
||||||||||||||||||||||||||

 – и
– и  -бромстиролов с сероводородом в жидкой фазе при 150-170°С с выходом (37%).
-бромстиролов с сероводородом в жидкой фазе при 150-170°С с выходом (37%).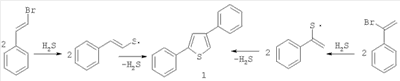
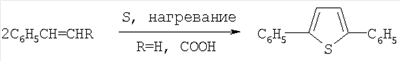
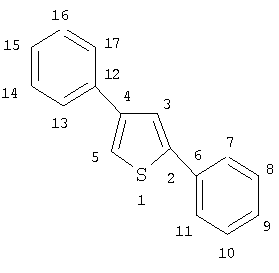
 , м.д.; (CDCL3) 7.28 уш.с (Н3), 7.18 уш.с (Н5), 7.97 уш.с ( Н7,11), 6.75-6.78 уш.с (Н8,10), 7.37 уш.с (Н9), 7.18 уш.с (Н13,17), 7.18, 7.22 уш.с (Н14), 7.44 уш.с (Н15), 7.22 уш.с (Н16). Спектр ЯМР 13С (
, м.д.; (CDCL3) 7.28 уш.с (Н3), 7.18 уш.с (Н5), 7.97 уш.с ( Н7,11), 6.75-6.78 уш.с (Н8,10), 7.37 уш.с (Н9), 7.18 уш.с (Н13,17), 7.18, 7.22 уш.с (Н14), 7.44 уш.с (Н15), 7.22 уш.с (Н16). Спектр ЯМР 13С (