|
(21), (22) Заявка: 2006130858/13, 28.08.2006
(24) Дата начала отсчета срока действия патента:
28.08.2006
(46) Опубликовано: 20.03.2008
(56) Список документов, цитированных в отчете о
поиске:
GIRLING A. et al. A core protein epitope of the polymorphic epithelial mucin detected by the monoclonal antibody SM-3 is selectively exposed in a range of primary carcinomas. Int. J. Cancer. 1989, v.43, n.6, p.1072-1076. CROCE M.V. et al. Tissue and serum MUC1 mucin detection in breast cancer patients. Breast Cancer Res. Treat. 2003, v.81, n.3,
Адрес для переписки:
117545, Москва, 1-й Дорожный пр-д, 1, ФГУП ГосНИИгенетика
|
(72) Автор(ы):
Аскерова Елена Валентиновна (RU),
Бобренева Римма Абрамовна (RU),
Гаврилова Наталья Андреевна (RU),
Рыкалина Наталья Владимировна (RU),
Юрин Виталий Львович (RU)
(73) Патентообладатель(и):
Федеральное государственное унитарное предприятие “Государственный научно-исследовательский институт генетики и селекции промышленных микроорганизмов” (ФГУП ГосНИИгенетика) (RU)
|
(54) ШТАММ ГИБРИДНЫХ КУЛЬТИВИРУЕМЫХ КЛЕТОК ЖИВОТНЫХ MUS MUSCULUS – ПРОДУЦЕНТ МОНОКЛОНАЛЬНЫХ АНТИТЕЛ К ГИПОГЛИКОЗИЛИРОВАННЫМ И ДЕГЛИКОЗИЛИРОВАННЫМ ИЗОФОРМАМ ОПУХОЛЬ-АССОЦИИРОВАННОГО АНТИГЕНА MUC I ЧЕЛОВЕКА
(57) Реферат:
Изобретение относится к биотехнологии и может быть использовано для получения моноклональных антител к опухоль ассоциированному антигену Muc I человека. С помощью гибридомных технологий получают штамм гибридных культивируемых клеток животных Mus musculus ВКПМ Н-98 – продуцент моноклональных антител, обладающих индивидуальной специфичностью к гипогликозилированным и дегликозилированным изоформам опухоль ассоциированного антигена Muc I человека. Оценку продуктивности штамма и специфичности продуцируемых антител проводят на основе иммуноферментного анализа с использованием нескольких маркеров специфичности: природного очищенного антигена Muc I, выделенного из молока человека; VNTR22-полипептида; синтетического мономерного полипептида (TR1); дегликозилированного антигена Muc I (de-Muc I), полученного в результате химического окисления природного Muc I; гипогликозилированного антигена Muc I (о-Muc I), полученного в результате периодатного окисления природного Muc I. Моноклональные антитела, продуцируемые заявляемым штаммом, распознают клинически значимые изоформы антигена Muc I и позволяют определить его концентрации в сыворотке крови человека при ранней диагностике опухолей. 2 ил.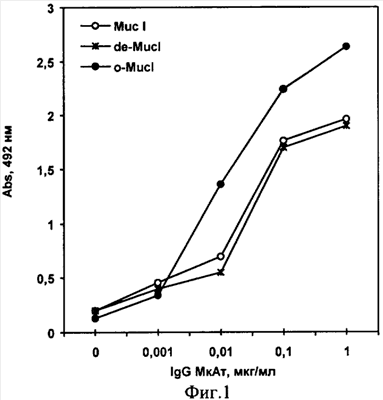
(56) (продолжение):
CLASS=”b560m”p.195-207. HANISCH F.G. Specificity clusters of MUC 1-reactive mouse monoclonal antibodies. Tumour Biol. 1998, v.19, Suppl. 1, p.111-117. RU 2119167 C1, 20.09.1998.
Штамм гибридных культивируемых клеток животных Mus musculus – продуцент моноклональных антител к гипогликозилированным и дегликозилированным изоформам опухоль ассоциированного антигена Muc I человека.
Изобретение относится к биотехнологии и иммунологии и касается получения моноклональных антител к опухоль ассоциированному Muc I антигену человека (онкомаркеру Muc I) с помощью гибридных культивируемых клеток (гибридом) животных. Наличие панели моноклональных антител к онкомаркеру Muc I перспективно для создания различных диагностикумов в клинической онкологии, в частности для применения в диагностическом двухсайтовом иммунометрическом способе определения концентрации Muc I в сыворотке крови человека (Br. Cancer Res. And Treat. 81:195-207, 2003).
Наибольший интерес с точки зрения ранней онкодиагностики представляют гипогликозилированные и дегликозилированные изоформы Muc I антигена человека, характерные для опухолей эпителиально-клеточного происхождения.
Известны некоторые продуценты моноклональных антител, обладающих специфичностью в отношении к различным эпитопам молекулы онкомаркера человека Muc I (Cancer Res.47:5476-5482, 1986). Ближайшими аналогами заявляемого изобретения по специфичности моноклональных антител являются штаммы гибридом SM3 ISOBM TD-4 N165 и ВС2 ISOBM TD-4 N138. Штаммы продуцируют моноклональные антитела, специфичные как к нативной молекуле онкомаркера, так и к пептидному каркасу молекулы Muc I (VNTR) (Inf. J.Cancer:43, 1072-1076, 1989; Br. Cancer Res. And Treat. 81:195-207, 2003). Известно, что моноклональные антитела SM3 и ВС2 распознают линейный пептидный участок молекулы антигена как в виде мономера (TR), так и в виде полимеров с разной степенью полимеризации (TR5-TR100), в то же время, степень гликозилирования антигена лишь в незначительной степени влияет на специфическую активность этих антител (Tumor.Biol.:19 (suppl 1), 111-117, 1998).
Спектр известных продуцентов клинически значимых моноклональных антител недостаточен для диагносцирования ранних стадий опухолей эпителиально-клеточного происхождения.
Задача заявляемого изобретения – расширить арсенал штаммов гибридом, продуцирующих моноклональных антитела к опухоль ассоциированному антигену Muc I человека.
Задача решена путем получения штамма М3В11 гибридных культивируемых клеток животных Mus musculus, продуцирующего моноклональные антитела, обладающие избирательной специфичностью и высоким сродством к гипогликозилированным и дегликозилированным изоформам онкомаркера человека Muc I.
Штамм депонирован во Всероссийской коллекции промышленных микроорганизмов и имеет номер ВКПМ Н-98.
Штамм получен путем гибридизации лимфоцитов иммунизированной мыши (Balb/c) с клетками миеломы (Sp2/0/Ag14) и применения подкожной схемы иммунизации с последующим выделением лимфоузельных В-лимфоцитов мыши. В качестве иммуногена применен дегликозилированный Muc I (deMuc) человека (Analitical Biochemistry: 82,289-309,1977).
– природного очищенного антигена Muc I, выделенного из молока человека (J.Immunol.:135, 3610-3616, 1985);
– VNTR22-полипетида (J.Biochem.: 263, 12820-12823, 1988);
– синтетического мономерного полипептида (TR1
– дегликозилированного антигена Muc I (de-Muc), полученного в результате химического окисления природного Muc I;
– гипогликозилированного Muc I (о-Muc I), полученного в результате периодатного окисления природного антигена (J.immunol. Methods: 78, 143-153, 1985).
Природный очищенный антиген Muc I, VNIR22-полипептид, гипогликозилированный и дегликозилированный антигены (о-Muc и de-Muc) представляют собой изоформы онкомаркера Muc I с различной степенью гликозилирования. Выделенный из молока антиген Muc I содержит комплекс гликопротеинов, состоящих из полипептидного скелета с вариабельным числом тандемных повторов из 20 аминокислот (VNTR) и олигосахаридных цепей. Этот антиген использован как контроль при оценке взаимодействия моноклональных антител с менее гликозилированными антигенами. Дегликозилированный антиген (de-Muc) содержит не более 1% углеводных цепей, а о-Muc I, полученный в результате более мягкого периодатного окисления характеризуется абберантным гликозилированием (гипогликозилированный антиген). Таким образом, указанные выше маркеры специфичности позволяют установить индивидуальную специфичность моноклональных антител в отношении клинически значимых гипогликозилированных и дегликозилированных изоформ Muc I онкомаркера человека.
Конечный продукт.
Моноклональные антитела класса IgG 1 (тест-система для изотипирования – ISO 2-1КТ, Sigma), обладающие высокой специфичностью к антигену Muc I в гипогликозилированной и дегликозилированной форме.
Культивирование штамма в питательной среде.
Для культивирования используют среду ДМЭМ (фирма Sigma), содержащую 10% фетальной сыворотки, 1% глутамина и пирувата, 50 ЕД/мл пенициллина и 25 мкг/мл стрептомицина. Клетки культивируют при 37°С в атмосфере, содержащей 5-7% CO2. Для культивирования используют пластиковые или стеклянные планшеты или флаконы объемом 50 мл (фирма Lux). Характер роста – стационарная суспензия. Частота пассирования 2-3 суток. Кратность рассева 1:3-1:4. Титр антител в культуральной жидкости 1:128.
Культивирование штамма в организме животного.
6 клеток в растворе Хенкса (производитель – Московский завод бактериальных препаратов). Рост асцитной опухоли отмечают на 7-10 день. Титр антител в культуральной жидкости составляет 1:128, а в асцитической – 1:10000.
Продуктивность.
Концентрация антител, продуцируемых штаммом, составляет в культуральной жидкости 15 мкг/мл, в асцитной жидкости – 8 мг/мл. Стабильность продуцирования антител сохраняется на протяжении 20 пассажей в культуре и 7 пассажей на животных, если гибридома перевивается.
Контаминация.
Бактерии и грибы в культурах не обнаружены при длительном наблюдении и посевах на стандартные питательные среды (МПА-для выявления бактерий и агар Сабуро – для грибов). Заражение микоплазмой не выявлено (тест-система Mycoplasma Stain Kit, фирмы Flow Lab.).
Консервация клеток.
Клетки замораживают после 2 и 3-го клонирования на 10 и 15 пассажах в культуре и после роста в виде асцитной опухоли в мышах. Клетки в криозащитной среде следующего состава (мас.%): ДМЭМ – 50, фетальной сыворотки – 40 и диметилсульфоксида – 10, помещают в холодильник при – 70°С, после чего переносят в жидкий азот. Выживаемость после размораживания составляет 70%.
Изобретение иллюстрируется следующими чертежами.
Фиг.1. Иммуноспецифичность моноклональных антител заявляемого штамма к гипогликозилированным и дегликозилированным изоформам опухоль ассоциированного антигена Muc I человека.
Фиг.2. Иммуноспецифичность моноклональных антител заявляемого штамма к мономерному пептиду TR1 и полипептиду – VNTR22 опухоль ассоциированного антигена Muc I человека.
Пример 1. Получение штамма ВКПМ Н-98.
Отбор растущих клонов клеток, секретирующих антитела заданной специфичности, проводят на 10-12 день на основе теста ИФА с использованием указанных ранее маркеров специфичности.
В результате получен штамм гибридных культивируемых клеток животных Mus musculus ВКПМ Н-98 – продуцент моноклональных антител к гипо- и дегликозилированным изоформам опухоль ассоциированного антигена Muc I человека.
Дважды проведенное клонирование полученных гибридом методом лимитирующих разведений путем рассева в лунки 96-луночного планшета из расчета 1 клетка на лунку в среде ДМЭМ и последующее тестирование на секрецию антител показало, что доля клонов, сохраняющих продукцию антител заданной специфичности, составляет 100%.
Пример 2. Получение, выделение и очистка моноклональных антител, продуцируемых штаммом ВКПМ Н-98.
Для получения моноклональных антител клетки штамма гибридомы выращивают в 24-луночных планшетах (фирма Nunc) на среде культивирования. При достижении концентрации клеток в лунке 106 собирают культуральную жидкость, содержащую клетки, центрифугируют 10 мин при 2000 g и удаляют надосадочную жидкость. Собранные клетки переводят в бессывороточную среду (ДМЭМ) и вводят мышам внутрибрюшинно из расчета 4·106 клеток/мышь. Через 7-10 дней наблюдают визуальный рост асцитной опухоли, мышей забивают и шприцем собирают асциты из брюшной полости. Асцитную жидкость центрифугируют 10 мин при 2000 g, чтобы освободиться от клеток, и надосадочную жидкость используют для выделения моноклональных антител.
С этой целью к асцитной жидкости мыши, содержащей моноклональные антитела, добавляют равный объем насыщенного (4 М) раствора сульфата аммония и центрифугируют при 5000 g 20 мин. Осадок растворяют, тщательно диализуют против 0,5 М фосфатного буфера рН 7,2 и очищают на колонке с DEAE целлюлозой (DE-52). (Иммунология: 4, 40-44, 1980). Из 1 мл асцитной жидкости получают 8 мг моноклональных антител. Чистота выделенных таким образом моноклональных антител подтверждена электорофоретически и составляет 90-95%.
Пример 3. Определение специфичности и концентрации моноклональных антител в культуральной и асцитной жидкостях методом ИФА.
В лунки 96-луночного планшета вносят по 100 мкл раствора антигена (Muc I, VNTR22-полипептид, мономерный полипептид TR1
Концентрация антител в культуральной жидкости составляет 15 мкг/мл, а в асцитной – 8 мг/мл.
На Фиг.1 и 2 представлены данные о гликопептидной специфичности полученных моноклональных антител. По оси Х отложены концентрации моноклональных антител, по оси Y – оптическая плотность при длине волны 492 нм. Активность взаимодействия моноклональных антител с антигеном увеличивается по мере возрастания концентрации антител от 1 нг до 1 мкг.
Как следует из представленных на Фиг.1 данных моноклональные антитела заявляемого штамма, взаимодействуют с дегликозилированным антигеном (de-Muc I) на том же уровне, что и с природным антигеном (Muc I). Эти данные свидетельствуют о высоком сродстве полученных антител к полипептидному участку молекулы антигена, что подтверждают результаты взаимодействия антител с VNTR как в мономерной, так и в полимерной форме (Фиг.2). При взаимодействии с гипогликозилированным антигеном, подвегшегося более мягкому разрушению углеводной структуры, полученные антитела резко повышают уровень связывания, что свидетельствует об избирательной гликопептидной специфичности полученных антител и высоком сродстве к гипогликозилированной форме Muc I антигена.
Таким образом, получен штамм гибридных культивируемых клеток животных Mus musculus ВКПМ Н-98 – продуцент клинически значимых моноклональных антител, обладающих индивидуальной специфичностью к гипо- и дегликозилированным изоформам Muc I онкомаркера человека.
Моноклональные антитела, продуцируемые заявляемым штаммом, распознают клинически значимые изоформы антигена Muc I и пригодны для определения его концентрации в сыворотке крови человека при ранней диагностике опухолей.
Формула изобретения
Штамм гибридных культивируемых клеток животных Mus musculus ВКПМ Н-98 – продуцент моноклональных антител к гипогликозилированным и дегликозилированным изоформам опухоль-ассоциированного антигена Muc I человека.
РИСУНКИ
|