Патент на изобретение №2318830
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ МОДИФИЦИРОВАННОГО ДЕРМАТАНСУЛЬФАТА
(57) Реферат:
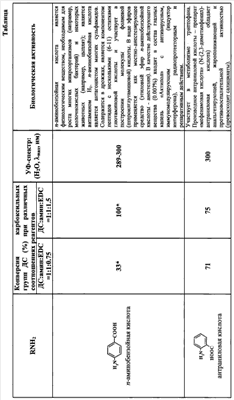
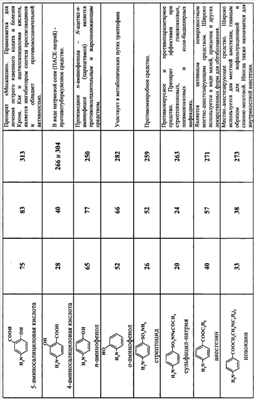
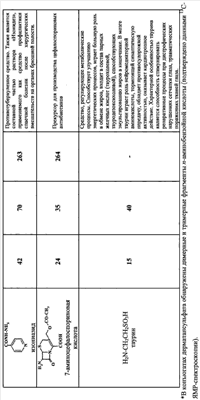
Изобретение относится к получению модифицированного дерматансульфата (ДС) путем его взаимодействия с аминосодержащими соединениями в водной среде при рН 4,7-4,8, в присутствии конденсирующего реагента 1-этил-3-[3-(диметиламино)пропил]карбодиимида (EDC). При этом в качестве аминосодержащих веществ используют соединения общей формулы RNH2, где R=C6H4OH (остатки n- или о-аминофенола), С6H4СООН (остатки n-аминобензойной или антраниловой кислот), С6Н3(ОН)СООН (остатки 4-или 5-аминосалициловых кислот), С6Н4СООС2Н5 (остаток этилового эфира n-аминобензойной кислоты), С6Н4СОО(СН2)2N(С2Н5)2 (остаток
Изобретение относится к области химии и биохимии, в частности к способу получения новых веществ, производных дерматансульфата, которые могут быть использованы в медицине, фармакологии. Дерматансульфат (хондроитинсульфат В) является полисахаридом линейного строения, относится к классу кислых гликозаминогликанов, содержится в коже, сухожилиях, связках млекопитающих и человека, состоит из остатков L-идуроновой кислоты и N-ацетил -D-галактозамин-4-сульфата, связанных между собой ( В последние годы проявляется большой интерес к получению и исследованию биологических свойств кислых гликозаминогликанов, модифицированных по карбоксильной функции. Модификация полисахаридов позволяет изменить их физико-химические и биологические свойства, конъюгаты полисахаридов с лекарственными субстанциями могут обладать большей растворимостью или продолжительностью действия по сравнению с самими лекарствами, могут использоваться как препараты комбинированного действия. Для ковалентного связывания аминосодержащих соединений с гликозаминогликанами (ГАГ-СООН) в качестве конденсирующих реагентов также применяются водорастворимые карбодиимиды, например EDC. При этом образуются соответствующие амиды.
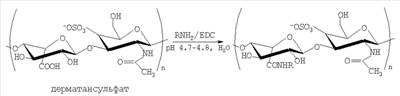
Авторами предлагается способ получения модифицированного дерматансульфата (из свиной кожи) путем его взаимодействия с соединениями, содержащими первичную аминогруппу (RNH2), в водной среде (рН 4.7-4.8) в присутствии EDC при различных соотношениях реагентов ДС:RNH2:EDC=1:1:0.75 и ДС:RNH2:EDC=1:1:1.5. Реакция протекает при комнатной температуре в течение 30 минут с образованием соответствующих конъюгатов с высокой конверсией карбоксильных групп дерматансульфата. В качестве аминосодержащих соединений были использованы фармакологически значимые n- и о-аминофенолы, 5- и 4-аминосалициловые, антраниловая и n-аминобензойная кислоты, этиловый эфир n-аминобензойной кислоты (анестезин), где R=C6H4OH (остатки n- или о-аминофенола), С6Н4СООН (остатки n-аминобензойной и антраниловой кислот), C6H3(OH)COOH (остатки 4- или 5-аминосалициловых кислот), С6Н4СООС2Н5 (остаток этилового эфира n-аминобензойной кислоты), С6Н4СОС(СН2)2N(С2Н5)2 (остаток бета-диэтиламиноэтилового эфира n-аминобензойной кислоты), C5H4NCONH (остаток гидразида изоникотиновой кислоты), C2HCH2SO3H (остаток 2-аминоэтансульфоновой кислоты), C9O5NSH10 (остаток 7-аминоиефалоспориновой кислоты), а также остатки сульфаниламидных препаратов, содержащих свободную аминогруппу, таких как C6H4SO2NH2 (остаток n-аминобензолсульфамида), C6H4SO2N(Na)COCH3, (остаток n-аминобензолсульфацетамид-натрия) и др. Пример 1. К смеси 74.5 мг (0.15 ммоль) дерматансульфата*(* Дерматансульфат выделяли из свиной кожи, очищали методом колоночной анионобменной хроматографии. Идентифицировали методом ЯМР-спектроскопии. Содержание серы 6.02%, белка (по Лоури) – 0.83%.) (ДС) и 0.15 ммоль соответствующего аминосодержащего соединения (RNH2) в 15 мл Н2О добавляют 0.1 н. NaOH (или, если требуется, 0.1 н. HCl) до рН 4.7-4.8, затем при интенсивном перемешивании и температуре 20-22°С вносят 21.5 мг (0.11 ммоль) EDC (соотношение реагентов ДС:RNH2:EDC=1:1:0.75), поддерживая рН 4.7-4.8 титрованием 0.1 н. HCl. Через 0.5 ч к охлажденной до 0°С реакционной смеси последовательно добавляют 0.1 н. NaOH (до рН 7-8), 2-3 мл насыщенного раствора NaCl и 45-60 мл охлажденного этанола. Выпавший осадок отделяют центрифугированием, растворяют в 10 мл 6% NaCl, добавляют 30-35 мл этанола. Вновь выпавший осадок центрифугируют, промывают этанолом (10×3 мл), затем эфиром (10×3 мл) и сушат при температуре Пример 2. Реакцию дерматансульфата с соответствующим амином проводят аналогично примеру 1, но при этом используют следующее соотношение реагентов: ДС:амин:EDC=1:1:1.5, т.е. к 74.5 мг (0.15 ммоль) дерматансульфата прибавляют 0.15 ммоль соответствующего амина и 43 мг (0.22 ммоль) карбодиимида. Конверсию карбоксильных групп дерматансульфата определяли из соотношения приведенных к одному протону суммарных интенсивностей сигналов протонов, отвечающих остаткам аминов, и сигналов метальных протонов ацетамидной группы N-ацетилгалактозамина в области 2.1 м.д. в 1Н-ЯМР-спектрах. Спектры 1Н-ЯМР регистрировали для растворов в D2O на спектрометре Bruker AMX-300 (рабочая частота для 1Н-ЯМР-300.13 МГц), в качестве внутреннего стандарта использовали натриевую соль 3-(триметилсилил)-1-пропансульфоновой кислоты. Контроль рН растворов проводили с помощью рН-метра «рН-340». Характеристика конъюгатов дерматансульфата приводится в таблице.
Формула изобретения
Способ получения модифицированного дерматансульфата (ДС) путем его взаимодействия с аминосодержащими соединениями в водной среде, рН 4,7-4,8, в присутствии конденсирующего реагента 1-этил-3-[3-(диметиламино)пропил]карбодиимида (EDC), отличающийся тем, что в качестве аминосодержащих веществ используют соединения общей формулы RNH2, где R=С6Н4ОН (остатки n- или о-аминофенола), С6Н4СООН (остатки n-аминобензойной или антраниловой кислот), С6Н3(ОН)СООН (остатки 4- или 5-аминосалициловых кислот), С6Н4СООС2Н5 (остаток этилового эфира n-аминобензойной кислоты), С6H4СОС(СН2)2N(C2Н5)2 (остаток
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 19.11.2007
Извещение опубликовано: 10.04.2009 БИ: 10/2009
|
||||||||||||||||||||||||||

 -диэтиламиноэтилового эфира n-аминобензойной кислоты), C5H4NCONH (остаток гидразида изоникотиновой кислоты), CH2CH2SO3H (остаток 2-аминоэтансульфоновой кислоты), C9O5NSH10 (остаток 7-аминоцефалоспориновой кислоты), а также остатки сульфаниламидных препаратов, содержащих свободную аминогруппу, таких как C6H4SO2NH2 (остаток n-аминобензолсульфамида), C6H4SO2N(Na)COCH3 (остаток n-аминобензолсульфацетамид-натрия) при мольном соотношении реагентов ДС:RNH2:EDC=1:1:(0,75-1,50), с последующей очисткой от низкомолекулярных реагентов. Полученные производные дерматансульфата могут быть использованы в медицине и фармакологии. 1 табл.
-диэтиламиноэтилового эфира n-аминобензойной кислоты), C5H4NCONH (остаток гидразида изоникотиновой кислоты), CH2CH2SO3H (остаток 2-аминоэтансульфоновой кислоты), C9O5NSH10 (остаток 7-аминоцефалоспориновой кислоты), а также остатки сульфаниламидных препаратов, содержащих свободную аминогруппу, таких как C6H4SO2NH2 (остаток n-аминобензолсульфамида), C6H4SO2N(Na)COCH3 (остаток n-аминобензолсульфацетамид-натрия) при мольном соотношении реагентов ДС:RNH2:EDC=1:1:(0,75-1,50), с последующей очисткой от низкомолекулярных реагентов. Полученные производные дерматансульфата могут быть использованы в медицине и фармакологии. 1 табл. 3) и (
3) и (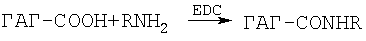
 60°С и пониженном давлении. Получают 65-80 мг соответствующих конъюгатов в виде белых порошков с розовым или желтым оттенком.
60°С и пониженном давлении. Получают 65-80 мг соответствующих конъюгатов в виде белых порошков с розовым или желтым оттенком.