Патент на изобретение №2318806
|
||||||||||||||||||||||||||
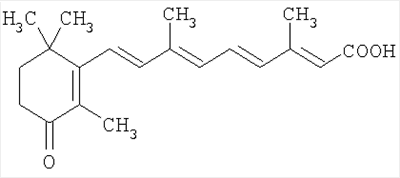
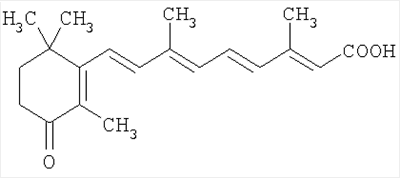
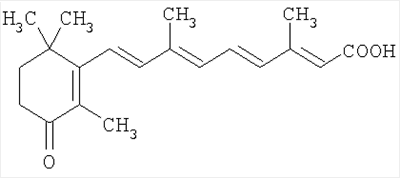
(54) РАВНОМЕРНОМЕЧЕННАЯ ТРИТИЕМ [3H]ТРАНС-3,7-ДИМЕТИЛ-9-(2,6,6-ТРИМЕТИЛ-3-ОКСО-1-ЦИКЛОГЕКСЕН-1-ИЛ)-2,4,6,8-НОНАТЕТРАЕНОВАЯ КИСЛОТА
(57) Реферат:
Изобретение относится к новой равномерномеченной тритием [3H]транс-3,7-диметил-9-(2,6,6-триметил-3-оксо-1-циклогексен-1-ил)-2,4,6,8-нонатетраеновой кислоте формулы: являющейся аналогом физиологически активного соединения, которая может найти применение в органической химии, в биологии и в медицине.
Изобретение относится к области органической химии и может найти применение в аналитической химии, биоорганической химии, биохимии и прикладной медицине. При изучении физиологически активных соединений бывают необходимы их меченые аналоги. Известно, что замена атомов водорода органического соединения на их изотопы не приводит к изменению каких-либо свойств исходного соединения (Evans E.A. – Tritium and its compounds. London, Butterworths, 1974, p.48) [1]. Известена транс-3,7-диметил-9-(2,6,6-триметил-3-оксо-1-циклогексен-1-ил)-2,4,6,8-нонатетраеновая кислота формулы: Однако ее меченный тритием аналог не описан. Техническим результатом, достигаемым настоящим изобретением, является расширение ассортимента меченых аналогов физиологически активных веществ. Достигается указанный технический результат получением нового меченого физиологически активного соединения – равномерномеченной тритием транс-3,7-диметил-9-(2,6,6-триметил-3-оксо-1-циклогексен-1-ил)-2,4,6,8-нонатетраеновой кислоты формулы: Ниже приведен пример реализации изобретения. Пример I. В первую камеру реакционной двухкамерной ампулы помещали катализатор – 25 мг окиси палладия и 25 мг 5% PdO/BaSO4, в другую – раствор 5 мг транс-3,7-диметил-9-(2,6,6-триметил-3-оксо-1-циклогексен-1-ил)-2,4,6,8-нонатетраеновой кислоты и 15 мкл триэтиламина в 150 мкл диоксана. Вторую камеру замораживали жидким азотом, ампулу вакуумировали до давления 0,1 Па и заполняли газообразным тритием до давления 333 гПа, затем первую камеру нагревали до 70°С. В результате реакции окись палладия восстанавливалась, тритиевая вода (10 Ки) перемораживалась во вторую камеру. Реакционную ампулу, не прекращая охлаждение второй камеры жидким азотом, вакуумировали до давления 0,1 Па и заполняли аргоном. Затем содержимое второй камеры переносили в первую камеру, которую затем запаивали. Таким образом, реакционная смесь состояла из паладиевого катализатора, тритиевой воды, триэтиламина и раствора транс-3,7-диметил-9-(2,6,6-триметил-3-оксо-1-циклогексен-1-ил)-2,4,6,8-нонатетраеновой кислоты в диоксане. Содержимое ампулы нагревали в течение 30 мин при 125°С. Затем ампулу вскрывали, реакционную смесь разбавляли 0,5 мл метанола, катализатор отделяли фильтрованием, промывали метанолом (5×1 мл). Тритиевую воду и триэтиламин отгоняли на роторе. Лабильный тритий удаляли, несколько раз растворяя вещество в метаноле (5×2 мл) и упаривая последний (общая радиоактивность остатка 180 мКи). Так как кроме продуктов деструкции в реакционной смеси содержались изомеры транс-3,7-диметил-9-(2,6,6-триметил-3-оксо-1-циклогексен-1-ил)-2,4,6,8-нонатетраеновой кислоты, очистку искомого препарата проводили в два этапа. Сначала отделяли продукты деструкции на колонке Kromasil 100C18, 8*150 мм, в системе 70% метанол-3 мМ Н3PO4, v – 2 мл/мин. Фракция, содержащая изомеры транс-3,7-диметил-9-(2,6,6-триметил-3-оксо-1-циклогексен-1-ил)-2,4,6,8-нонатетраеновой кислоты, имела радиоактивность 16,8 мКи, из которых 8 мКи приходилось на транс-3,7-диметил-9-(2,6,6-триметил-3-оксо-1-циклогексен-1-ил)-2,4,6,8-нонатетраеновую кислоту. Анализ проводили методом ВЭЖХ на колонке Kromasil C18, 4,0×150 мм, 7,0 мкм, скорость элюента – 1,0 мл/мин, в системе 70% метанол-3 мМ Н3PO4, время удерживания искомого меченого препарата – 9,77 мин. Изомеры разделяли методом препаративной ВЭЖХ на колонке Kromasil 100C18, 8,0×150 мм, 7,0 мкм, скорость элюента – 2,0 мл/мин, в системе А (60% метанол-3 мМ Н3PO4) и В (50% метанол), градиент от 0%В-до 50%В за 30 мин. Выход меченой транс-3,7-диметил-9-(2,6,6-триметил-3-оксо-1-циклогексен-1-ил)-2,4,6,8-нонатетраеновой кислоты после хроматографии составил 7 мКи (25%), молярная радиоактивность 1,8 Ки/ммоль. Таким образом, получено новое равномерномеченное тритием физиологически активное соединение.
Формула изобретения
Равномерномеченная тритием [3H]транс-3,7-диметил-9-(2,6,6-триметил-3-оксо-1-циклогексен-1-ил)-2,4,6,8-нонатетраеновая кислота формулы
|
||||||||||||||||||||||||||