Патент на изобретение №2318799
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ 3,4′-ДИАМИНО-4-R-БЕНЗОФЕНОНОВ
(57) Реферат:
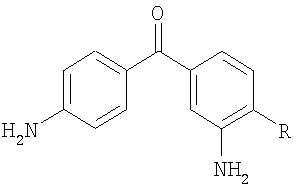
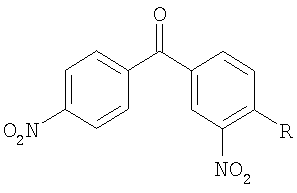
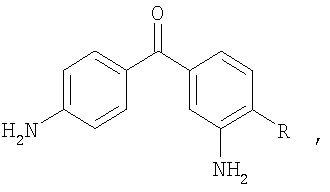
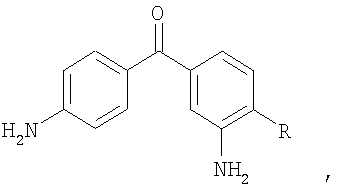
Изобретение относится к способу получения 3,4′-диамино-4-R-бензофенонов общей формулы
где R=Cl, Br, F, СН3, ОСН3,
которые используются в качестве полупродуктов в синтезе азокрасителей, пригодных для крашения белковых волокон и обладающих уникальными показателями термостабильности. Способ включает стадии нитрования замещенных бензофенонов нитратом калия в концентрированной H2SO4, нуклеофильного замещения галогена (для R=Cl), при взаимодействии с О- и N-нуклеофилами в ДМФА в присутствии K2СО3 и восстановления 3,4′-динитро-4-R-бензофенонов, причем нитрование полученных бензофенонов проводят при температуре 20°С в течение 5 ч и мольном соотношении 4′-нитро-4-R-бензофенон:KNO3=1.0:1.15, нуклеофильное замещение галогена проводят в течение 1-5 часов при температуре 40-60°С и мольном соотношении субстрат:нуклеофил=1.0:1.05, восстановление динитробензофенонов проводят SnCl·2H2O в 18-% HCl при мольном соотношении 3,4′-динитро-4-R-бензофенон:SnCl2·2H2O=1:6 при температуре 20°С в течение 0,15 ч. Целью изобретения является снижение стоимости синтеза, сокращение времени и температуры проведения процесса, повышение чистоты и выходов целевых продуктов. 4 табл.
Изобретение относится к способу синтеза ароматических диаминосоединений, в частности к получению 3,4′-диамино-4-R-бензофенонов общей формулы
где R=Cl, Br, F, СН3, ОСН3,
которые были использованы в качестве полупродуктов в синтезе азокрасителей. Известен способ получения 3,4′-диаминобензофенона, включающий следующие стадии: нитрование замещенного дифенилкетона 94% HNO3 (d=1.50) при температуре 70-75°С в течение 12 ч и каталитическое гидрирование динитропродукта, катализируемое 5% Pd/C, процесс проводят в течение 7 ч при температуре 45-47°С. (Process for preparation of 3,3′- or 3,4′-diaminobenzophenones. Y.Keizaburo, S.Kenichi, T.Yoshimitsu, K.Saburo, Y.Akihiro. Пат. 4618714 США. Заявл. 02.05.83, опубл. 21.10.1986. РЖХ 16Н89П, 1987). Недостатками известного способа синтеза диаминобензофенонов являются: применение агрессивных, вредных для здоровья реагентов (концентрированная HNO3), использование дорогостоящего катализатора (Pd/C), продолжительное время протекания каждой из стадий процесса, а также необходимость создания жестких условий проведения процессов, что неизбежно приводит к снижению степени чистоты и выходов получаемых соединений. Цель изобретения – снижение стоимости синтеза, оптимизация условий реакций – сокращение времени и температуры проведения процесса, повышение чистоты и выходов целевых продуктов. Поставленная цель достигается тем, что в качестве восстанавливающего агента используется SnCl2·2H2O, при этом пропадает потребность в использовании дорогостоящего катализатора. К тому же возможна электрохимическая регенерация данного реагента. Вместо концентрированной HNO3 применяется более удобный при осуществлении синтеза KNO3, выпускаемый промышленными методами. Нитрование замещенных субстратов осуществляют в течение 5 ч при температуре 20°С и мольном соотношении 4′-нитро-4-R-бензофенон:KNO3=1.0:1.15 (в прототипе 70-75°С, 12 ч), замещение галогена осуществляют в среде ДМФА в присутствии K2СО3 при температуре 40-60°С и мольном соотношении субстрат:нуклеофил=1.0:1.05, восстановление 3,4′-динитро-4-R-бензофенонов проводят раствором SnCl2·2H2O в 18%-ной соляной кислоте и мольном соотношении 3,4′-динитро-4-R-бензофенон:SnCl·H2O=1:6 при температуре 20°С в течение 0,15 ч, что позволяет снизить температуру с 45-47°С до 20°С и уменьшить время процесса с 7 ч до 0.15 ч. Строение и чистоту промежуточных соединений и целевых 3,4′-диамино-4-R-бензофенонов анализировали методом ПМР, определением температуры плавления и элементного состава. Изобретение иллюстрируется следующими примерами. Пример 1. 3,4′-динитро-4-хлорбензофенон К раствору 15 г (0,06 моль) 4′-нитро-4-хлорбензофенона в 150 мл концентрированной серной кислоты порциями вносили 6.9 г (0,069 моль) KNO3. Реакцию проводили в течение пяти часов при температуре 20°С. Затем реакционную массу выливали в воду, осадок отфильтровывали, высушивали и перекристаллизовывали из смеси пропанола-2 и N,N-диметилформамида (3:1). Получают 18 г (97.4% от теории) 3,4′-динитро-4-хлорбензофенона – желтый порошок, т.пл. 127-129°С. Найдено, %: С 50,7; Н 2,5; N 9,2. Вычислено, %: С 50,9; Н 2,5; N 9,3. 1Н ПМР (DMSO-d6) Аналогично получают 3,4′-динитро-4-R-бензофеноны, где R=Br, F, СН3, ОСН3. Физико-химические характеристики этих структур приведены в таблице 1.
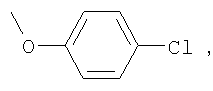
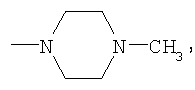
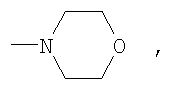
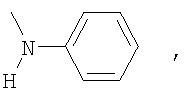
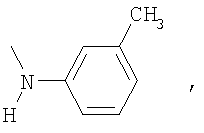
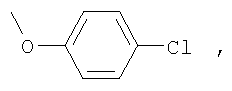
Пример 2. 3,4′-динитро-4-(4-хлорфенокси)бензофенон К 10.1 г (0.07 моль) карбоната калия и 6.9 г (0.05 моль) 4-хлорфенола в 50 мл N,N-ДМФА вносили 15 г (0,048 моль) 3,4′-динитро-4-хлорбензофенона. Реакцию проводили в течение 5 часов при температуре 40-60°С. Затем реакционную смесь выливали в воду, осадок отфильтровывали и перекристаллизовывали из смеси пропанола-2 и N,N-диметилформамида (3:1). Получают 19 г (97.1% от теории) 3,4′-динитро-4-(4-хлорфенокси)бензофенона – желтый порошок, т.пл. 142-144°С. Найдено, %: С 57,1; Н 2,89; N 7,1. Вычислено, %: С 57,2; Н 2,7; N 7,0. 1Н ПМР (DMSO-d6) Аналогично получают 3,4′-динитро-4-R-бензофеноны, где R=
Физико-химические характеристики этих структур приведены в таблице 2.
Пример 3. 3,4′-диамино-4-хлорбензофенон К раствору 5 г (0.016 моль) 3,4′-динитро-4-хлорбензофенона в 20 мл изопропилового спирта при температуре 40°С приливается раствор 43.39 г (0.192 моль) хлорида олова (SnCl2·2H2O) в 20 мл 18% HCl. Через 0.15 ч реакционная смесь подщелачивается 25% раствором аммиака до рН=8 и экстрагируется несколькими порциями хлороформа (S=400 мл). После отгонки хлороформа получают 3.6 г (95.1% от теории) 3,4′-диамино-4-хлорбензофенона – желтый порошок, т.пл. 159-160°С. Найдено, %: С 63,4; Н 4,2; N 11,1. Вычислено, %: С 63,2; Н 4,4; N 11.3. 1Н ПМР (DMSO-d6) Аналогично получают 3,4′-диамино-4-R-бензофеноны, где R=Br, F, СН3, ОСН3,
Физико-химические характеристики этих структур приведены в таблицах 3 и 4.
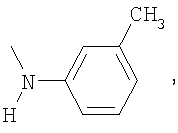
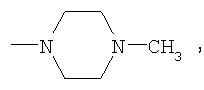
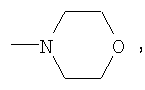
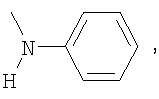
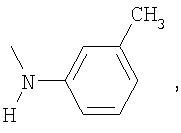
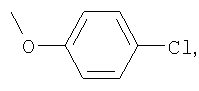
Пример 4. Получение азокрасителей на основе 3,4′-диамино-4-R-бензофенонов, где R=Br, F, СН3, ОСН3,
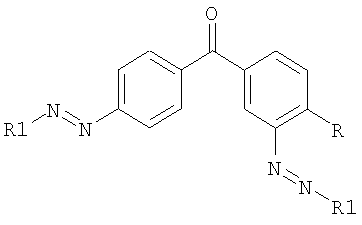
Указанные диамины диазотируются в стандартных условиях под действием нитрита натрия в среде соляной и серной кислот. Полученные диазосоединения проявили себя как активные диазосоставляющие в реакции азосочетания с ароматическими гидроксосоединениями бензольного, нафталинового и гетероциклического ряда. На их основе синтезированы бисазокрасители, обладающие повышенной устойчивостью к сухому и мокрому трению, стирке и поту, общей формулы:
где R1=
Формула изобретения
Способ получения 3,4′-диамино-4-R-бензофенонов общей формулы
где R=Cl, Br, F, СН3, ОСН3,
включающий нитрование замещенных 4′-нитро-4-R-бензофенонов нитратом калия в серной кислоте, нуклеофильное замещение галогена (для R=Cl) при взаимодействии с О- и N-нуклеофилами и восстановление 3,4′-динитро-4-R-бензофенонов общей формулы
где R=Cl, Br, F, СН3, ОСН3,
хлоридом олова (II) в кислом водно-этанольном растворе, отличающийся тем, что нитрование замещенных субстратов осуществляют в течение 5 ч при температуре 20°С и мольном соотношении 4′-нитро-4-R-бензофенон:KNO3=1,0:1,15, замещение галогена осуществляют в среде ДМФА в присутствии К2СО3 при температуре 40-60°С и мольном соотношении субстрат:нуклеофил=1,0:1,05, восстановление 3,4′-динитро-4-R-бензофенонов проводят раствором SnCl2·H2O в 18%-ной соляной кислоте и мольном соотношении 3,4′-динитро-4-R-бензофенон:SnCl2·2H2O=l:6 при температуре 20°С в течение 0,15 ч.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

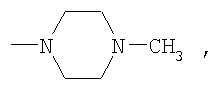
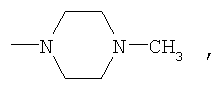
 , мд: 8.82 (d, 2-Н, Н3′, Н5′, J=9.5), 8.71 (d, 1-H, Н2, J=1.9), 8.18 (m, 3H, Н2′, Н6′, Н6), 7.87 (d, 1-H, Н5, J=8.9).
, мд: 8.82 (d, 2-Н, Н3′, Н5′, J=9.5), 8.71 (d, 1-H, Н2, J=1.9), 8.18 (m, 3H, Н2′, Н6′, Н6), 7.87 (d, 1-H, Н5, J=8.9).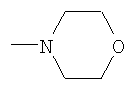 ,
, 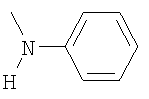 ,
, 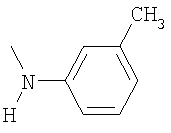 ,
, 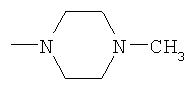 .
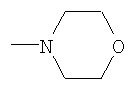
.
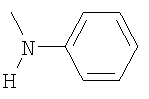
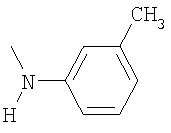
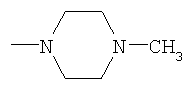
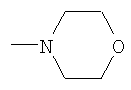 ,
, 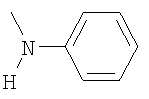 ,
, 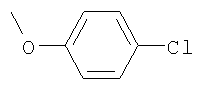 ,
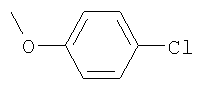
, 
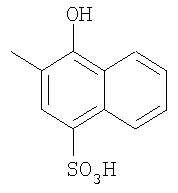 ,
, 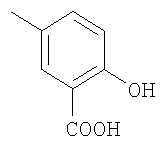 ,
,  ,
,