Патент на изобретение №2318496
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
(54) СОДЕРЖАЩАЯ СВЕХЧИСТУЮ ФЛУДАРУ ПЕРОРАЛЬНАЯ КОМПОЗИЦИЯ С БЫСТРЫМ ВЫСВОБОЖДЕНИЕМ ДЕЙСТВУЮЩЕГО ВЕЩЕСТВА
(57) Реферат:
Настоящее изобретение относится к области лекарственных средств, в частности к таблетированной композиции с быстрым высвобождением флудары со степенью чистоты >99,19% (сверхчистая флудара) с определенным составом остаточных примесей в количестве от 1 до 100 мг в сочетании с моногидратом лактозы, коллоидным диоксидом кремния, микрокристаллической целлюлозой (Avicel), натриевой солью кроскармеллозы (натрийкарбоксиметилцеллюлозой) и стеаратом магния. Кроме того, настоящее изобретение относится к применению указанной таблетированной композиции для получения лекарственного средства для лечения рака. 2 н. и 10 з.п. ф-лы, 1 табл.
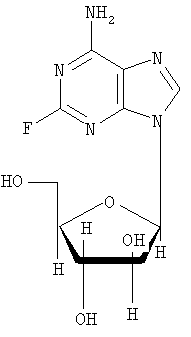
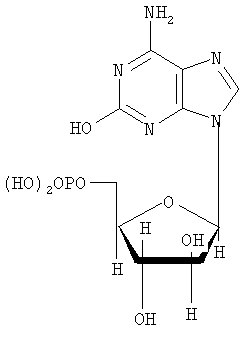
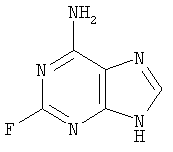
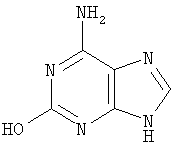
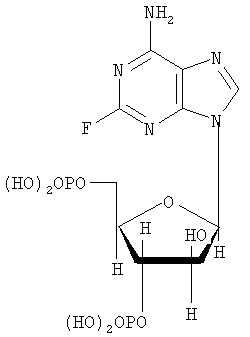
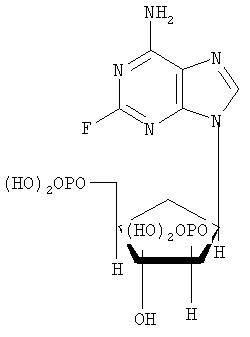
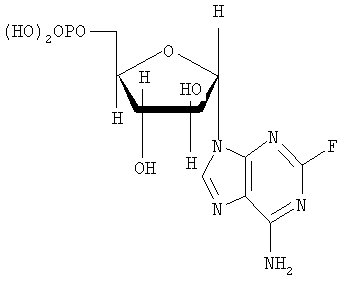
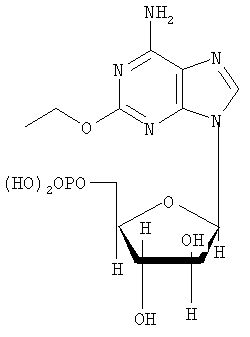
Настоящее изобретение относится к таблетированной композиции с быстрым высвобождением действующего вещества, в качестве которого она содержит флудару со степенью чистоты >99,19% (сверхчистую флудару)
с определенным составом остаточных примесей. Таблетированные композиции на основе флудары со степенью чистоты <98% уже известны из уровня техники. Композиции различного состава и рекомендуемые их дозировки описаны помимо прочего в следующих работах (7 Modern Pharmaceutics, главы 9 и 10, под ред. Banker и Rhodes, 1979; Liebennan и др., Pharmaceitical Dosage Forms: Tablets, 1981; Ansel, Introduction to Pharmaceutical Dosage Forms, 2-е изд., 1976). В патенте US 3903297 в качестве примера описана таблетированная композиция, которая помимо действующего вещества содержит лактозу, микрокристаллическую целлюлозу, коллоидный диоксид кремния и стеарат магния (пример 2). В этом же патенте в качестве примера описана также композиция, которая может содержать натриевую соль кроскармеллозы (пример 5). В заявке WO 00/71134 в общих чертах описаны таблетированные композиции, содержащие лактозу, микрокристаллическую целлюлозу, коллоидный диоксид кремния, натриевую соль кроскармеллозы и стеарат магния. В состав одной из подобных композиций может также входить химиотерапевтическое вещество. Из заявки WO 97/40846 известны материалы для нанесения на таблетки покрытий, содержащие гидроксипропилметилцеллюлозу, диоксид титана и красители, например железооксидные красители. Из заявки WO 00/50423 известны быстрорастворимые таблетированные композиции, содержащие лактозу, микрокристаллическую целлюлозу, натриевую соль кроскармеллозы и иные материалы. В US 6197785, ЕР 1065206, ЕР 819430, ЕР 1065204 и ЕР 985666 описаны таблетированные композиции для перорального применения, содержащие лактозу, микрокристаллическую целлюлозу, коллоидный диоксид кремния, стеарат магния, натриевую соль кроскармеллозы, тальк и иные материалы. В качестве действующего вещества такие композиции могут содержать, в частности, флудару. Композиции, которые в качестве действующего вещества содержат флудару со степенью чистоты >99,5% и в которых такое действующее вещество характеризуется определенным составом присутствующих в нем примесей, до настоящего времени не были известны. Действующее вещество флудара со степенью чистоты >99,19% известно из заявки WO 99/29710. Однако и в этой заявке не содержится никаких сведений о конкретном составе чистой, присутствующей в лекарственной композиции флудары. Исходя из вышеизложенного в основу настоящего изобретения была положена задача предложить стабильную таблетированную композицию, которая содержала бы флудару с высокой степенью чистоты и со строго определенной концентрацией в ней остаточных примесей и которая являлась бы быстрорастворимой и благодаря этому быстро высвобождала бы действующее вещество. При создании изобретения было установлено, что применение в составе таблетированной композиции в качестве действующего вещества флудары со степенью чистоты >99,19% в не микронизированной, а в просеянной форме со строго определенной концентрацией в ней остаточных примесей позволяет преодолеть недостатки известных таблеток. Содержание действующего вещества в предлагаемой в изобретении таблетированной композиции составляет от 5 до 100 мг, предпочтительно от 8 до 75 мг, более предпочтительно от 10 до 50 мг, наиболее предпочтительно от 10 до 20 мг. К числу предпочтительных веществ (адъювантов и добавок), включаемых в состав лекарственной композиции, относятся лактоза, коллоидный диоксид кремния, микрокристаллическая целлюлоза (Avicel), натриевая соль кроскармеллозы (натрийкарбоксиметилцеллюлоза) и стеарат магния. Вместе с тем в состав лекарственной композиции можно включать и иные известные специалистам вещества, используемые в технологии приготовления лекарственных средств. Общее содержание подобных используемых в технологии приготовления лекарственных средств веществ (адъювантов и добавок) в составе таблетки составляет от 100 до 250 мг, предпочтительно от 120 до 200 мг, наиболее предпочтительно от 130 до 180 мг. В соответствии с этим объектом настоящего изобретения является таблетированная композиция с быстрым высвобождением действующего вещества, которая содержит флудару в качестве действующего вещества со степенью чистоты >99,19% в количестве от 1 до 100 мг в сочетании с моногидратом лактозы, коллоидным диоксидом кремния, микрокристаллической целлюлозой (Avicel), натриевой солью кроскармеллозы (натрийкарбоксиметилцеллюлозой) и стеаратом магния и которая отличается тем, что процентное содержание примесей во флударе не превышает следующих значений: 0,02% 2-фтор-9-( 0,12% 6-амино-9-(5-O-фосфоно- 0,02% 2-фтор-9Н-пурин-6-амина, 0,02% 6-амино-9Н-пурин-2-ола, 0,05% 2-фтор-9-(5-O-фосфоно- 0,1% 9-(3,5-O-дифосфоно- 0,1% 9-(2,5-O-дифосфоно- 0,02% 2-фтор-9-(5-O-фосфоно- 0,06% 2-этокси-9-(5-O-фосфоно- 0,02% 2-(6-амино-9Н-пурин-2-ил)-9-(5-O-фосфоно- 0,1% 9-(2-хлор-2-дезокси-5-фосфоно- 0,1% 9-(2,5-ангидро- Предпочтительна таблетированная композиция с быстрым высвобождением действующего вещества, которая содержит в качестве действующего вещества флудару со степенью чистоты >99,19% в количестве от 1 до 70,00 мг совместно с моногидратом лактозы в количестве от 50 до 100 мг, коллоидным диоксидом кремния в количестве от 0,1 до 5 мг, микрокристаллической целлюлозой (Avicel) в количестве от 40 до 100 мг, натриевой солью кроскармеллозы (натрийкарбоксиметилцеллюлозой) в количестве от 1 до 10 мг и стеаратом магния в количестве от 0,5 до 10 мг. К особо предпочтительным относятся те таблетированные композиции с быстрым высвобождением действующего вещества, которые содержат в качестве действующего вещества флудару со степенью чистоты >99,19% в количестве от 1 до 50,00 мг совместно с моногидратом лактозы в количестве от 60 до 90 мг, коллоидным диоксидом кремния в количестве от 0,5 до 1 мг, микрокристаллической целлюлозой (Avicel) в количестве от 50 до 90 мг, натриевой солью кроскармеллозы (натрийкарбоксиметилцеллюлозой) в количестве от 1,5 до 5 мг и стеаратом магния в количестве от 1 до 3 мг. Наиболее предпочтительной является таблетированная композиция с быстрым высвобождением действующего вещества, которая содержит в качестве действующего вещества флудару со степенью чистоты >99,19% в количестве 10 мг совместно с моногидратом лактозы в количестве 74,75 мг, коллоидным диоксидом кремния в количестве 0,75 мг, микрокристаллической целлюлозой (Avicel) в количестве 60,00 мг, натриевой солью кроскармеллозы (натрийкарбоксиметилцеллюлозой) в количестве 3,00 мг и стеаратом магния в количестве от 1,5 до 2,00 мг. Предпочтительны также те композиции, которые содержат флудару в качестве действующего вещества со степенью чистоты >99,37%. Более предпочтительны те композиции, которые содержат флудару в качестве действующего вещества со степенью чистоты >99,57%. К особо предпочтительным относятся те композиции, которые содержат флудару в качестве действующего вещества со степенью чистоты >99,80%. Наиболее предпочтительны те композиции, которые содержат флудару в качестве действующего вещества со степенью чистоты >99,85%. Предлагаемые в изобретении композиции по общеизвестным методам перерабатывают в прессовочные массы, из которых затем прессуют сердцевины таблеток. На такие сердцевины таблеток в последующем можно наносить покрытия по общеизвестным методам. Для нанесения покрытий в принципе могут использоваться все известные специалистам по их применению в этих целях материалы. Одно из предпочтительных покрытий может содержать, например, следующие компоненты: гидроксипропилметилцеллюлозу в количестве от 1 до 5 мг, предпочтительно от 1 до 3 мг, наиболее предпочтительно 2,250 мг, тальк в количестве от 0,1 до 1 мг, предпочтительно от 0,1 до 0,8 мг, наиболее предпочтительно 0,450 мг, диоксид титана в количестве от 0,1 до 5 мг, предпочтительно 0,1 до 2 мг, наиболее предпочтительно 1,187 мг, желтый железооксидный краситель в количестве от 0,01 до 0,1 мг, предпочтительно от 0,01 до 0,05 мг, наиболее предпочтительно 0,036 мг, и красный железооксидный краситель в количестве от 0,01 до 0,1 мг, предпочтительно от 0,01 до 0,05 мг, наиболее предпочтительно 0,036 мг. Подобные покрытия также являются объектом настоящего изобретения. Предлагаемые в изобретении таблетированные композиции могут использоваться для получения медикамента, предназначенного для лечения рака. В соответствии с этим настоящее изобретение относится также к применению предлагаемых в нем композиций для получения медикамента, предназначенного для лечения рака. В последующих примерах описан способ получения предлагаемых в изобретении таблетированных композиций со сверхчистой флударой, а также дается сравнительный анализ флудары обычного состава со степенью чистоты <98% с флударой, степень чистоты которой составляет >99,19%. Пример 1 Получение таблетированной композиции Для получения предлагаемой в изобретении таблетированной композиции действующее вещество флудару (флударабина фосфат) сначала просеивают, после чего совместно с моногидратом лактозы, микрокристаллической целлюлозой (Avicel) и коллоидным диоксидом кремния перерабатывают в примерно 30%-ную сухую смесь. Эту смесь затем также просеивают. Качество, соответственно крупность частиц проверяют путем ситового анализа. После этого к сухой смеси на последующих стадиях смешения последовательно добавляют натриевую соль кроскармеллозы (натрийкарбоксиметилцеллюлозу) и стеарат магния. Полученную прессовочную массу спрессовывают в сердцевины таблеток. Полученная таким путем таблетированная композиция содержит, например, следующие отдельные компоненты, мг:
В завершение на сердцевины таблеток наносят лаковое пленочное покрытие из водной суспензии. Подобное пленочное покрытие содержит, например, следующие компоненты, мг:
Общая масса таблетки составляет 154 мг. Полученные таким путем таблетки с пленочным покрытием (филм-таблетки) можно направлять на дальнейшую переработку. Так, например, филм-таблетки можно упаковывать в алюминиевые блистерные упаковки, что обеспечивает стабильность состава композиции. Пример 2 В этом примере флудара традиционного состава со степенью чистоты <98% (97,67%) сравнивается с флударой, степень чистоты которой составляет >99,19%, соответственно >99,57%, и с очищенной ионитом флударой, степень чистоты которой составляет 99,19%. Полученные результаты приведены ниже в таблице.
Полученные в этом примере результаты свидетельствуют о том, что композиция с коммерчески доступной флударой (флударой с максимальной степенью чистоты 97,67%) или композиция с очищенной ионитом флударой (флударой с максимальной степенью чистоты 99,19%) содержит значительно большее количество побочных продуктов в качестве загрязняющих примесей по сравнению с предлагаемой в изобретении композицией со сверхчистой флударой (флударой со степенью чистоты от >99,37% до >99,57%). Традиционные методы очистки, такие, например, как исключительно эффективная ионообменная хроматография, позволяют получить продукт лишь со сравнительно умеренной степенью чистоты. Предлагаемые в изобретении композиции с флударой содержат полученную через образование натриевой соли сверхчистую флудару, как это уже описано в заявке WO 99/29710. Флудару с еще более высокой степенью чистоты можно получить через образование калиевой соли (степень чистоты 99,8%) или литиевой соли (степень чистоты 99,85%).
Формула изобретения
1. Таблетированная композиция с быстрым высвобождением действующего вещества, содержащая в качестве действующего вещества флудару в просеянной форме со степенью чистоты >99,19% в количестве от 1 до 100 мг в сочетании с моногидратом лактозы, коллоидным диоксидом кремния, микрокристаллической целлюлозой (Avicel), натриевой солью кроскармеллозы (натрийкарбоксиметилцеллюлозой) и стеаратом магния, отличающаяся тем, что процентное содержание примесей во флударе не превышает следующих значений: 0,02% 2-фтор-9-( 0,02% 2-фтор-9Н-пурин-6-амина, 0,02% 6-амино-9Н-пурин-2-ола, 0,05% 2-фтор-9-(5-O-фосфоно-( 0,1% 9-(3,5-O-дифосфоно- 0,1% 9-(2,5-O-дифосфоно- 0,02% 2-фтор-9-(5-O-фосфоно- 0,06% 2-этокси-9-(5-O-фосфоно- 0,02% 2-(6-амино-9Н-пурин-2-ил)-9-(5-O-фосфоно- 0,1% 9-(2-хлор-2-дезокси-5-фосфоно- 0,1% 9-(2,5-ангидро- 2. Таблетированная композиция с быстрым высвобождением действующего вещества по п.1, которая содержит в качестве действующего вещества флудару со степенью чистоты >99,19% в количестве от 1 до 70 мг совместно с моногидратом лактозы в количестве от 50 до 100 мг, коллоидным диоксидом кремния в количестве от 0,1 до 5 мг, микрокристаллической целлюлозой (Avicel) в количестве от 40 до 100 мг, натриевой солью кроскармеллозы (натрийкарбоксиметилцеллюлозу) в количестве от 1 до 10 мг и стеаратом магния в количестве от 0,5 до 10 мг. 3. Таблетированная композиция с быстрым высвобождением действующего вещества по п.1 и 2, которая содержит в качестве действующего вещества флудару со степенью чистоты >99,19% в количестве от 1 до 50 мг совместно с моногидратом лактозы в количестве от 60 до 90 мг, коллоидным диоксидом кремния в количестве от 0,5 до 1 мг, микрокристаллической целлюлозой (Avicel) в количестве от 50 до 90 мг, натриевой солью кроскармеллозы (натрийкарбоксиметилцеллюлозой) в количестве от 1,5 до 5 мг и стеаратом магния в количестве от 1 до 3 мг. 4. Таблетированная композиция с быстрым высвобождением действующего вещества по п.1 и 2, которая содержит в качестве действующего вещества флудару со степенью чистоты >99,19% в количестве 10 мг совместно с моногидратом лактозы в количестве 74,75 мг, коллоидным диоксидом кремния в количестве 0,75 мг, микрокристаллической целлюлозой (Avicel) в количестве 60,00 мг, натриевой солью кроскармеллозы (натрийкарбоксиметилцеллюлозой) в количестве 3,00 мг и стеаратом магния в количестве от 1,5 до 2,00 мг. 5. Таблетированная композиция с быстрым высвобождением действующего вещества по пп.1 и 2, которая содержит в качестве действующего вещества флудару со степенью чистоты >99,37%. 6. Таблетированная композиция с быстрым высвобождением действующего вещества по пп.1 и 2, которая содержит в качестве действующего вещества флудару со степенью чистоты >99,57%. 7. Таблетированная композиция с быстрым высвобождением действующего вещества по пп.1 и 2, которая содержит в качестве действующего вещества флудару со степенью чистоты >99,80%. 8. Таблетированная композиция с быстрым высвобождением действующего вещества по пп.1 и 2, которая содержит в качестве действующего вещества флудару со степенью чистоты >99,85%. 9. Таблетированная композиция с быстрым высвобождением действующего вещества по пп.1 и 2, отличающаяся тем, что на сердцевины таблеток нанесено покрытие, содержащее следующие компоненты: гидроксипропилметилцеллюлозу в количестве от 1 до 5 мг, тальк в количестве от 0,1 до 1 мг, диоксид титана в количестве от 0,1 до 5 мг, желтый железооксидный краситель в количестве от 0,01 до 0,1 мг и красный железооксидный краситель в количестве 0,01 до 0,1 мг. 10. Таблетированная композиция с быстрым высвобождением действующего вещества по пп.1 и 2, отличающаяся тем, что на сердцевины таблеток нанесено покрытие, содержащее следующие компоненты: гидроксипропилметилцеллюлозу в количестве от 1 до 3 мг, тальк в количестве от 0,1 до 0,8 мг, диоксид титана в количестве от 0,1 до 2 мг, желтый железооксидный краситель в количестве от 0,01 до 0,05 мг и красный железооксидный краситель в количестве от 0,01 до 0,05 мг. 11. Таблетированная композиция с быстрым высвобождением действующего вещества по пп.1 и 2, отличающаяся тем, что на сердцевины таблеток нанесено покрытие, содержащее следующие компоненты: гидроксипропилметилцеллюлозу в количестве 2,250 мг, тальк в количестве 0,450 мг, диоксид титана в количестве 1,187 мг, желтый железооксидный краситель в количестве 0,036 мг и красный железооксидный краситель в количестве 0,036 мг. 12. Применение таблетированной композиции по любому из пп.1-11 для получения лекарственного средства, предназначенного для лечения рака.
PD4A – Изменение наименования обладателя патента СССР или патента Российской Федерации на изобретение
(73) Новое наименование патентообладателя:
Адрес для переписки:
Извещение опубликовано: 27.12.2009 БИ: 36/2009
PC4A – Регистрация договора об уступке патента СССР или патента Российской Федерации на изобретение
Прежний патентообладатель:
(73) Патентообладатель:
Договор № РД0058858 зарегистрирован 28.12.2009
Извещение опубликовано: 10.02.2010 БИ: 04/2010
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

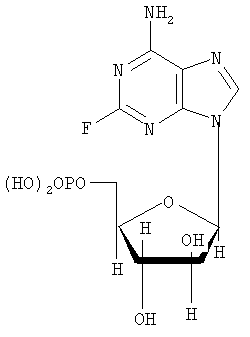
 -D-арабинофуранозил)-9Н-пурин-6-амина,
-D-арабинофуранозил)-9Н-пурин-6-амина, -D-арабинофураноз-5-ил]фосфата,
-D-арабинофураноз-5-ил]фосфата,