|
|
(21), (22) Заявка: 2006137879/14, 26.10.2006
(24) Дата начала отсчета срока действия патента:
26.10.2006
(46) Опубликовано: 20.02.2008
(56) Список документов, цитированных в отчете о
поиске:
Руководство по сердечно-сосудистой хирургии под ред. В.И.БУРАКОВСКОГО и Л.А.БОКЕРИЯ. – М.: Медицина, 1989, с.38-76. RU 2202276 С2, 20.04.2003. US 6325776, 04.12.2001. CN 2562775 Y, 30.07.2003. БАРОНИН А.А. Основные принципы хирургического лечения забрюшинных опухолей. Вестн. Рос. онколог. научн. центра им. Н.Н.Блохина. 2001, 3, с.48-52. YAGI S. et
Адрес для переписки:
350063, г.Краснодар, ул. Седина, 4, КГМУ, Зав. патентным отделом Т.А. Дорониной
|
(72) Автор(ы):
Оноприев Владимир Иванович (RU),
Восканян Сергей Эдуардович (RU),
Овсянникова Алла Васильевна (RU),
Артемьев Алексей Игоревич (RU)
(73) Патентообладатель(и):
Оноприев Владимир Иванович (RU),
Восканян Сергей Эдуардович (RU)
|
(54) СПОСОБ ВРЕМЕННОГО ШУНТИРОВАНИЯ МАГИСТРАЛЬНОГО КРОВООБРАЩЕНИЯ ПРИ ОПУХОЛЕВОМ ПОРАЖЕНИИ ЗАБРЮШИННОГО ПРОСТРАНСТВА И ВОВЛЕЧЕНИЕМ НИЖНЕЙ ПОЛОЙ ВЕНЫ
(57) Реферат:
Изобретение относится к медицине, а именно к хирургии. Правое предсердие канюлируют через интраперикардиальную часть нижней полой вены, а нижнюю полую вену непосредственно каудальнее ее поражения с оставлением площадки для формирования сосудистого анастомоза. Канюли соединяют между собой и системой для гепаринизации обхода. При этом временное шунтирование осуществляют в условиях сохраненной деятельности, нормотермии и без использования аппарата для принудительной подачи крови. При этом вены пересекают дистальнее зон их канюляции после включения системы временного сосудистого шунтирования, и функционирование его поддерживают весь период операции до этапа завершения сосудистой реконструкции, после чего канюли последовательно извлекают из просвета вен в условиях их бокового отжатия. Способ позволяет снизить гемодинамические и тромботические осложнения, исключить синдром реперфузии и проводить локальную гепаринизацию системы байпаса. 1 ил.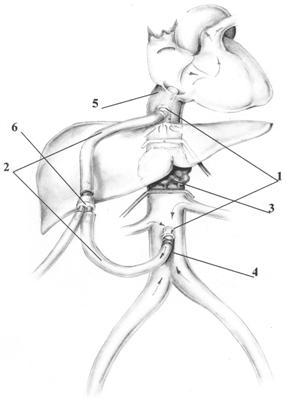
(56) (продолжение):
CLASS=”b560m”al. Optimal portal venous circulation for liver graft function after living-donor liver transplantation. Transplantation? 2006 Feb 15; 81(3):373-378.
Предлагаемое изобретение относится к медицине, а именно к хирургии, и может быть использовано при резекции нижней полой вены.
Основными показаниями к резекции нижней полой вены в сосудистой хирургии чаще всего является их окклюзионно-стенотическое поражение при опухолевых поражениях.
Необходимость обширной резекции нижней полой вены практически всегда связана с ее опухолевым поражением, и самая частая причина – это злокачественные новообразования органов забрюшинного пространства, которые в связи с высокой частотой местного распространения опухоли и поражением нижней полой вены характеризуются весьма низкой резектабельностью.
Радикальные операции при местнораспространенном раке органов забрюшинного пространства с инвазией нижней полой вены выполняются крайне редко и лишь в единичных клиниках. Ограничения в операции во многом обусловлены отсутствием эффективных технологий обеспечения непрерывности венозного кровотока по магистральным венам во время удаления опухоли. Эти обстоятельства в значительной мере обусловливают актуальность разработки технологий временного венозного сосудистого байпаса при резекции нижней полой вены при ее обширной опухолевой инвазии и мультиваскулярном характере поражения. Заявителями выявлен единственный источник, раскрывающий временное шунтирование магистрального кровообращения при опухолевом поражении забрюшинного пространства и вовлечении нижней полой вены, при этом в качестве ближайшего аналога взят способ использования временного сосудистого кардиопульмонального байпаса при резекции нижней полой вены при ее опухолевой инвазии (Kapasi A, Mullen JC, Bentley MJ, Moore RB, Todd GT Resection of renal cell carcinomas with inferior vena caval extension using deep hypothermic circulatory arrest. Can J Cardiol. 2001 Nov; 17(11):1183-8), который осуществляют следующим образом: выделяют пораженный участок нижней полой вены, налаживают работу аппарата искусственного кровообращения, именуемую кардиопульмональным байпасом.
Более подробно данный способ раскрыт в «Руководстве по сердечно-сосудистой хирургии» под редакцией В.И.Бураковского и Л.А.Бокерия, Москва «Медицина», 1989 г.
Методика подключения аппарата искусственного кровообращения (АИК) к магистралям носит стандартный характер. Сначала канюлируют аорту. Эту канюлю подключают к артериальной магистрали, эвакуируют воздух. Затем канюлируют верхнюю и нижнюю полые вены через ушко правого предсердия одно или двумя канюлями и подсоединяют венозную магистраль, также стараясь не допустить попадания в нее воздуха. Отдельный резервуар обычно используется для сбора крови из полости сердца и перикарда. Эта кровь фильтруется через фильтры с диаметром пор 15 мк. Фильтрация внутрисердечного возврата важна для исключения попадания материальных частиц в АИК. Оксигенатор располагается на 50 см ниже сердца оперируемого. Перфузия проводится под умеренной гипотермией (26-30 град. Цельсия) и гемодилюцией (гематокрит 25-30%, гемоглобин не ниже 80 г/л). Операция проводится в условиях кардиоплегии и остановки сердца, при этом гемодинамика контролируется работой системы кардиопульмонального байпаса.
Недостатки:
а) Технология использования способа предполагает остановку и последующее восстановление сердечной деятельности, что влечет за собой высокий риск фатальных осложнений кардиопульмонального байпаса: анемия, тяжелые нарушения сердечного ритма, острый инфаркт миокарда и летальный исход на этом этапе операции.
б) Предполагает проведение системной гепаринизации, что существенно увеличивает объем интраоперационной кровопотери, требует применения антидотов гепарина.
в) Технология за счет выраженной потери клеток тромбоцитарного звена на полихлорвиниловых элементах системы кардиопульмонального байпаса и АИКа приводит к значительному возрастанию риска развития неконтролируемого ДВС – синдрома, особенно при длительном функционировании системы, которая в ряде случаев послужит причиной летального исхода.
г) Использование способа сопряжено с разрушением значительной части эритроцитов элементами принудительной подачи крови байпаса, выраженность которого прямо коррелирует с продолжительностью осуществления кардиопульмонального байпаса, что в значительной части случаев приводит к острой почечной недостаточности в послеоперационном периоде.
д) Способ предполагает выполнение стернотомии, перикардиотомии, что значительно увеличивает травматичность операции и повышает частоту послеоперационных осложнений.
е) Технология способа в большинстве случаев предполагает применение гипотермии, которая значительно увеличивает риск вмешательства за счет выраженного патологического влияния на систему гемостаза больного.
ж) Способ предусматривает необходимость применения фармакологической и Холодовой кардиоплегии и использование многочисленных методов защиты миокарда, что повышает риск манифестации тяжелых нарушений сердечного ритма в послеоперационном периоде.
з) Технология осуществления данного сосудистого байпаса предусматривает использование дорогостоящей аппаратуры, большого числа одноразовых расходных материалов, что существенно увеличивает себестоимость операции.
Задачи: разработать способ временного сосудистого шунтирования, обеспечивающий адекватное временное протезирование магистрального кровообращения при резекции нижней полой вены и ее ветвей, различных вариантов мультиваскулярных поражений, исключающий необходимость избежать применение искусственного кровообращения и существенно уменьшить риск специфических осложнений.
Для решения поставленных задач:
способ временного шунтирования магистрального кровообращения при опухолевом поражении забрюшинного пространства и вовлечении нижней полой вены включает канюляцию правого предсердия и нижней полой вены и осуществление сосудистого байпаса. Правое предсердие канюлируют через интраперикардиальную часть нижней полой вены, а нижнюю полую вену непосредственно каудальнее ее поражения, канюли соединяют между собой и системой для гепаринизации обхода, при этом временное шунтирование осуществляют в условиях сохраненной сердечной деятельности, нормотермии, без использования аппарата для принудительной подачи крови.
По отношению к ближайшему аналогу заявляемый способ имеет следующий технический результат. Предлагаемый способ позволяет резецировать нижнюю полую вену (с ее последующей пластикой), особенно при ее обширном опухолевом поражении и мультиваскулярном его характере, без риска нарушения питания кровоснабжаемых ими органов и тканей и включает безопасную методику канюляции нижней полой вены, обладает высокой эффективностью и воспроизводимостью.
Способ поясняется чертежом, где п.1 – кисетный шов на передней стенке вены; п.2 – венозная канюля, п.3 – пораженная опухолью нижняя полая вена, п.4 – шунтированный дистальный конец нижней полой вены; п.5 – шунтированная интраперикардиальная часть нижней полой вены, п.6 – тройник.
Способ осуществляют следующим образом. После тотальной срединной лапаротомии выполняется мобилизация нижней полой вены вне зоны ее поражения, включая интраперикардиальную часть. При необходимости временного шунтирования нижней полой вены предварительно на переднюю стенку вены накладывают кисет (см. чертеж, п.1), в центре которого вену пунктируют канюлей (см. чертеж, п.2), фиксируют к стенке вены при помощи ранее наложенного кисетного шва (см. чертеж, п.1), после чего производят резекцию нижней полой вены. Правое предсердие канюлируют через интраперикардиальную часть нижней полой вены (см. чертеж, п.5), а нижнюю полую вену (см. чертеж, п.4) непосредственно каудальнеее ее поражения (см. чертеж, п.3), канюли (см. чертеж, п.2) соединяют между собой и системой для гепаринизации обхода посредством тройников (см. чертеж, п.6), при этом временное шунтирование осуществляют в условиях сохраненной сердечной деятельности, без использования аппарата для принудительной подачи крови. После удаления опухоли единым блоком с сосудами производится протезирование нижней полой вены синтетическими сосудистыми протезами из политетрофторэтилена или фторлонлавсана и последовательная деканюляция вен.
Заявляемый способ временного венозного сосудистого байпаса апробирован у 20 больных с местно-распространенным раком органов забрюшинного пространства с обширной опухолевой инвазией нижней полой вены. При этом всем больным выполнена расширенная резекция единым блоком с пораженной нижней полой веной. Госпитальной летальности не было. Осложненное течение раннего послеоперационного периода наблюдалось в 1% случаев, причем тромботических осложнений в данной группе больных не было.
Возможность практического использования заявляемого способа иллюстрируется примером его выполнения в клинической практике.
Пример 1. Больной З., 70 лет, поступил в клинику с диагнозом: местнораспространенный рак правого надпочечника с инвазией в правую почку, печень, нижнюю полую вену. По данным инструментального обследования данных за наличие отдаленных метастазов не получено. Выполнена операция: Расширенная нефроадреналэктомия, атипичная резекция печени единым блоком с сегментом нижней полой вены в условиях временного нижнекавально-правопредсердного обхода, протезирование нижней полой вены протезом из политетрофторэтилена, лимфаденэктомия, дренирование брюшной полости и полости перикарда. Выполнена мобилизация нижней полой вены вне зоны ее поражения, включая интраперикардиальную часть. Предварительно на переднюю стенку вены наложен кисет (см. чертеж, п.1), в центре которого вена пунктирована канюлей (см. чертеж, п.2), фиксированной к стенке вены при помощи ранее наложенного кисетного шва (см. чертеж, п.1), после чего проведена резекция нижней полой вены. Правое предсердие канюлировано через интраперикардиальную часть нижней полой вены (см. чертеж, п.5), а нижняя полая вена (см. чертеж, п.4) непосредственно каудальнеее ее поражения (см. чертеж, п.3), канюли (см. чертеж, п.2) соединили между собой и системой для гепаринизации обхода посредством тройников (см. чертеж, п.6), при этом временное шунтирование осуществляли в условиях сохраненной сердечной деятельности, нормотермии, без использования аппарата для принудительной подачи крови. После удаления опухоли единым блоком с сосудами выполнили протезирование нижней полой вены синтетическим сосудистым протезом из политетрофторэтилена и последовательно деканюлировали вены.
Послеоперационный период протекал без осложнений. Больной выписан из клиники в относительно удовлетворительном состоянии на 17-е сутки после операции. После операции больной неоднократно обследован. Через 3 года после операции состояние удовлетворительное, данных за рецидив заболевания не выявлено. Проходимость нижней полой вены удовлетворительная.
Таким образом, применение заявляемого способа позволяет выполнить радикальную операцию у больных с местнораспространенными опухолями органов забрюшинного пространства и брюшной полости с обширной опухолевой инвазией нижней полой вены.
Социально-экономическое значение. Разработанный способ позволяет выполнять радикальное хирургическое лечение опухолей с инвазией нижней полой вены, улучшить непосредственные и отдаленные его результаты, значительно повысить операбельность и отдаленную выживаемость больных местнораспространенным раком органов забрюшинного пространства и брюшной полости с поражением нижней полой вены.
Формула изобретения
Способ временного шунтирования магистрального кровообращения при опухолевом поражении забрюшинного пространства и вовлечением нижней полой вены, включающий канюляцию правого предсердия и нижней полой вены и осуществление сосудистого байпаса, отличающийся тем, что правое предсердие канюлируют через интраперикардиальную часть нижней полой вены, а нижнюю полую вену непосредственно каудальнее ее поражения, канюли соединяют между собой и системой для гепаринизации обхода, при этом временное шунтирование осуществляют в условиях сохраненной сердечной деятельности и нормотермии, без использования аппарата для принудительной подачи крови.
РИСУНКИ
|
|