|
|
(21), (22) Заявка: 2006116327/15, 15.05.2006
(24) Дата начала отсчета срока действия патента:
15.05.2006
(46) Опубликовано: 10.02.2008
(56) Список документов, цитированных в отчете о
поиске:
Daly J.W. el al. Frog secretions and hunting magic in the upper Amazon: Identification of a peptide that interacts with an adenosine receptor. Proc. Natl. Acad. Sci. U.S.A, 1992, Vol.89, P.10960-10963. RU 2183643 C1, 18.12.2000. RU 2083589 C1, 10.07.1997. RU 2172322 C1, 20.08.2001. RU 2002112327/13 A1, 20.11.2003. реф. Tetko IV, Bruneau P.
Адрес для переписки:
117997, Москва, ГСП-7, В-437, ул. Миклухо-Маклая, 16/10, ИБХ РАН, патентный отдел
|
(72) Автор(ы):
Полянский Антон Александрович (RU),
Волынский Павел Евгеньевич (RU),
Василевский Александр Александрович (RU),
Воронцова Ольга Валентиновна (RU),
Козлов Сергей Александрович (RU),
Феофанов Алексей Валерьевич (RU),
Арсеньев Александр Сергеевич (RU),
Гришин Евгений Васильевич (RU),
Ефремов Роман Гербертович (RU)
(73) Патентообладатель(и):
Институт биоорганической химии им. академиков М.М. Шемякина и Ю.А. Овчинникова Российской Академии Наук (RU)
|
(54) СПОСОБ ПОЛУЧЕНИЯ АНТИМИКРОБНЫХ ПЕПТИДОВ С ПОНИЖЕННОЙ ГЕМОЛИТИЧЕСКОЙ АКТИВНОСТЬЮ
(57) Реферат:
Изобретение относится к химико-фармацевтической промышленности, к биохимии, конкретно к биологически активным пептидам латарцинами, обладающим антимикробным действием, которые могут найти применение в биотехнологии и медицине. Способ получения антимикробных пептидов латарцинов с пониженной гемолитической активностью химическим или биотехнологическим синтезом включает предварительное моделирование пространственной структуры исходного пептида латарцина с высокой гемолитической активностью в  -спиральной конформации и замену гидрофобных аминокислотных остатков на гидрофильные в процессе синтеза, в ходе которого происходит замена гидрофобных аминокислот Ile7 и Phe10 на гидрофильные Gln7 и Lys10. При этом после моделирования пространственной структуры исходного пептида латарцина в -спиральной конформации и замену гидрофобных аминокислотных остатков на гидрофильные в процессе синтеза, в ходе которого происходит замена гидрофобных аминокислот Ile7 и Phe10 на гидрофильные Gln7 и Lys10. При этом после моделирования пространственной структуры исходного пептида латарцина в  -спиральной конформации дополнительно проводят расчет гидрофобных свойств пептида с учетом молекулярного гидрофобного потенциала в каждой точке поверхности пептида, выявление гидрофобных кластеров и аминокислотных остатков, локализованных в них, с последующим определением наиболее эффективных гидрофильных аминокислотных остатков для использования в процессе синтеза. Способ позволяет получать пептиды со значительно сниженными гемолитическими свойствами, а также понизить цитотоксичность пептидов латарцинов. 3 табл., 2 ил. -спиральной конформации дополнительно проводят расчет гидрофобных свойств пептида с учетом молекулярного гидрофобного потенциала в каждой точке поверхности пептида, выявление гидрофобных кластеров и аминокислотных остатков, локализованных в них, с последующим определением наиболее эффективных гидрофильных аминокислотных остатков для использования в процессе синтеза. Способ позволяет получать пептиды со значительно сниженными гемолитическими свойствами, а также понизить цитотоксичность пептидов латарцинов. 3 табл., 2 ил.
(56) (продолжение):
CLASS=”b560m”Application of ALOGPS to predict 1-octanol/water distribution coefficients, logP, and logD, of AstraZeneca in-house database”, J Pharm Sci. 2004; 93(12): 3103-10. PMID 15514985. реф. Poroikov V.V. Filimonov D.A. How to acquire new biological activities in old compounds by computer prediction, J Comput Aided Mol Des. 2002; 16(11): 819-24., PMID 12825794.
Изобретение относится к биохимии, конкретно к биологически активным пептидам, обладающим антимикробным действием, которые могут найти применение в биотехнологии и медицине.
 -спираль при контакте с мембранами, обсуждаются подходы к оптимизации их свойств с целью повышения терапевтического потенциала [Tossi A., Sandri L., Giangaspero A. Amphipathic, -спираль при контакте с мембранами, обсуждаются подходы к оптимизации их свойств с целью повышения терапевтического потенциала [Tossi A., Sandri L., Giangaspero A. Amphipathic, 
В числе свойств, которые необходимо контролировать у потенциальных антибиотиков, – цитотоксическое действие на клетки макроорганизма, чаще оцениваемое в стандартных тестах на гемолитическую активность. Наличие подобной активности у целого ряда антимикробных пептидов широкого спектра действия является серьезным недостатком и ограничивает возможность их применения в качестве лекарственных средств. Таким образом, важной задачей является оптимизация свойств пептидов, а именно снижение их гемолитической активности, токсичности в отношении нормальных клеток человека.

Наиболее близким к заявляемому является способ получения антимикробных пептидов с пониженной гемолитической активностью, включающий замену гидрофобных аминокислотных остатков, локализованных в кластерах гидрофобности [Chen Y. et al. Rational design of   -спирали. При таком способе детализации гидрофобных свойств пептида теряется информация о пространственном распределении гидрофобности в аминокислотных остатках, что приводит к невозможности корректной оценки вклада различных остатков пептида в формирование поверхностных гидрофобных паттернов. -спирали. При таком способе детализации гидрофобных свойств пептида теряется информация о пространственном распределении гидрофобности в аминокислотных остатках, что приводит к невозможности корректной оценки вклада различных остатков пептида в формирование поверхностных гидрофобных паттернов.
Изобретение решает задачу получения антимикробных пептидов с пониженной гемолитической активностью.
Поставленная задача решается за счет того, что в способе получения антимикробных пептидов с пониженной гемолитической активностью химическим или биотехнологическим синтезом, включающем моделирование пространственной структуры исходного пептида с высокой гемолитической активностью в  -спиральной конформации и замену гидрофобных аминокислотных остатков на гидрофильные в процессе синтеза, после моделирования пространственной структуры исходного пептида в -спиральной конформации и замену гидрофобных аминокислотных остатков на гидрофильные в процессе синтеза, после моделирования пространственной структуры исходного пептида в  -спиральной конформации дополнительно проводят расчет гидрофобных свойств пептида с учетом молекулярного гидрофобного потенциала в каждой точке поверхности пептида, выявление гидрофобных кластеров и аминокислотных остатков, локализованных в них, с последующим определением наиболее эффективных гидрофильных аминокислотных остатков для использования в процессе синтеза. -спиральной конформации дополнительно проводят расчет гидрофобных свойств пептида с учетом молекулярного гидрофобного потенциала в каждой точке поверхности пептида, выявление гидрофобных кластеров и аминокислотных остатков, локализованных в них, с последующим определением наиболее эффективных гидрофильных аминокислотных остатков для использования в процессе синтеза.
Способ осуществляют следующим образом:
1. моделируют пространственную структуру исходного пептида с высокой гемолитической активностью в  -спиральной конформации, -спиральной конформации,
2. рассчитывают молекулярный гидрофобный потенциал (МГП) для каждой точки поверхности пептида,
3. проецируют полученные значения МГП на поверхность цилиндра, аппроксимирующего  -спираль, и картируют эти значения на плоскости ( -спираль, и картируют эти значения на плоскости ( ; Z), где ; Z), где  – угол поворота, Z – смещение вдоль оси – угол поворота, Z – смещение вдоль оси  -спирали, -спирали,
4. выявляют гидрофобные паттерны (кластеры) на полученной плоскости и аминокислотные остатки, локализованные в них,
5. определяют наиболее эффективные гидрофильные аминокислотные остатки для замены идентифицированных гидрофобных аминокислотных остатков с целью сокращения гидрофобных кластеров,
6. проводят химический или биотехнологический синтез пептида с введением в его аминокислотную последовательность эффективных гидрофильных остатков.
В предлагаемом способе анализ пространственной организации гидрофобных свойств АМП основан на расчете МГП для каждой точки поверхности пептида в конформации идеальной 
Применение заявляемого способа позволяет значительно снизить гемолитическую активность пептидов (в десятки раз увеличить необходимую для лизиса эритроцитов концентрацию), а также цитотоксичность в отношении других клеток человека при сохранении высокой антимикробной активности.
Изобретение иллюстрируют примеры.
Пример 1.
Расчет карты гидрофобной поверхности линейного антимикробного пептида.
Для исходного гемолитически активного пептида (LtAMP-2a) проводят моделирование пространственной структуры в 
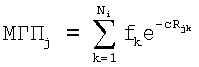
Здесь fk – атомная константа гидрофобности атома k, принадлежащего остатку i, Rjk – расстояние между атомом k и точкой j (в Å), Ni – число атомов в остатке i, с=1 Å-1. Значения атомных констант гидрофобности (fk , Z) ( , Z) ( – угол вращения относительно оси спирали, Z – смещение вдоль оси спирали) представляют с помощью контурных линий, соединяющих точки с одинаковым потенциалом. Для этого предварительно выполняют сплайн-интерполяцию данных ( – угол вращения относительно оси спирали, Z – смещение вдоль оси спирали) представляют с помощью контурных линий, соединяющих точки с одинаковым потенциалом. Для этого предварительно выполняют сплайн-интерполяцию данных ( i, Zi) для получения набора значений ( i, Zi) для получения набора значений ( ‘i,Z’i ‘i,Z’i
Пример 2.
Выбор аминокислотных замен для получения аналогов антимикробного пептида со сниженной гемолитической активностью.
На построенной двумерной карте гидрофобности (см. пример 1, фиг.1Б) исходного гемолитически активного пептида (LtAMP-2а) находят протяженные паттерны гидрофобности. Определяют ключевые остатки пептида, формирующие обширные гидрофобные области – Ile7, Phe10 (см. фиг.2). Предлагают замены соответствующих остатков на полярные или заряженные остатки, сходные по размеру и склонности к формированию  -спирали: Ile->Gln, Phe->Lys. Аминокислотные последовательности полученных аналогов (LtAMP-2a_I7Q, LtAMP-2a_F10K) приведены в таблице 1. -спирали: Ile->Gln, Phe->Lys. Аминокислотные последовательности полученных аналогов (LtAMP-2a_I7Q, LtAMP-2a_F10K) приведены в таблице 1.
Для пептидов LtAMP-2a_I7Q и LtAMP-2a_F10K проводят расчет двумерных карт гидрофобности согласно схеме, описанной в примере 1. Полученные карты используют для оценки влияния предложенных мутаций на структуру гидрофобных паттернов на поверхности пептидов. Из фиг.2 видно, что предложенная замена в случае пептида LtAMP-2a_I7Q приводит к уменьшению размера гидрофобной области, соответствующей остатку Gln7 по сравнению с исходным пептидом LtAMP-2а. Замена Phe->Lys приводит к разрыву исходного гидрофобного паттерна в области остатка Lys10.
Таблица 1
Аминокислотные последовательности исходного гемолитически активного пептида LtAMP-2a и предложенных аналогов. |
| Пептид |
Аминокислотная последовательность |
| LtAMP-2a (исходный) |
1GLFGKLIKKFGRKAISYAVKKARGKH26 |
| LtAMP-2a_F10K |
1GLFGKLIKKKGRKAISYAVKKARGKH26 |
| LtAMP-2a_I7Q |
1GLFGKLQKKFGRKAISYAVKKARGKH26 |
Пример 3.
Химический синтез пептидов.
Пептид LtAMP-2a синтезируют твердофазным методом путем наращивания цепи с С-концевого остатка на 2-хлор-тритил-хлоридной (с нагрузкой 0,8-1,44 ммоль/г) смоле (PepChem, Германия) для временной защиты  -NH2-групп используют флуоренилметоксикарбонильную группу (Fmoc) [Chan W.C., White P.D. Fmoc Solid Phase Peptide Synthesis. – 2000. – University Press, Oxford]. Защиту боковых групп аминокислотных остатков выбирают с расчетом на конечное деблокирование трифторуксусной кислотой: для защиты боковых групп остатков Ser и Tyr используют третбутильную группу, для Lys – третбутилоксикарбонильную группу, для His – тритильную группу, для Arg – 2,2,4,6,7-пентаметилдегидробензофуран-5-сульфонильную группу. -NH2-групп используют флуоренилметоксикарбонильную группу (Fmoc) [Chan W.C., White P.D. Fmoc Solid Phase Peptide Synthesis. – 2000. – University Press, Oxford]. Защиту боковых групп аминокислотных остатков выбирают с расчетом на конечное деблокирование трифторуксусной кислотой: для защиты боковых групп остатков Ser и Tyr используют третбутильную группу, для Lys – третбутилоксикарбонильную группу, для His – тритильную группу, для Arg – 2,2,4,6,7-пентаметилдегидробензофуран-5-сульфонильную группу.
Для присоединения первой (С-концевой) аминокислоты к смоле 1,5 экв (по отношению к количеству активных групп на смоле) Fmoc-защищенной аминокислоты растворяют в дихлорметане (из расчета 10 мл дихлорметана на 1 г смолы) с 1,5 экв диизопропилэтиламина.
К полученному раствору добавляют еще 1,5 экв диизопропилэтиламина и приливают к сухой смоле, мягко перемешивают в течение 45 мин. Непрореагировавшие активные группы на смоле блокируют метанолом (из расчета 1 мл метанола на 1 г смолы) в течение 20 мин, после чего смолу промывают тремя объемами дихлорметана, тремя объемами N,N-диметилформамида и тремя объемами этанола, высушивают под вакуумом. Аминокислотные остатки присоединяют к пептидил-полимеру с образованием гидроксибензотриазолового эфира в присутствии 1,3-диизопропилкарбодиимида, для активации 1 экв аминокислоты используют 1,2 экв N-гидроксибензотриазола и 1 экв 1,3-диизопропилкарбодиимида. Для наращивания полипептидной цепи в ходе каждого синтетического цикла проводят конденсацию пептидил-полимера с 5 экв активированной Fmoc-аминокислоты (1-12 часов при 37°С), содержание непрореагировавших аминогрупп контролируют визуально по окрашиванию рН-зависимого индикатора бромфенолового синего.
Отщепление продукта от 2-хлор-тритил-хлоридного полимера с одновременным деблокированием боковых групп проводят смесью трифторуксусной кислоты, воды и этандитиола (95:2,5:2,5, v/v/v) из расчета 1 мл смеси на 50 мг смолы. Суспензию перемешивают в течение 2 часов, затем раствор пептида в трифторуксусной кислоте отфильтровывают от полимера. Продукт высаживают 10-кратным избытком (по объему) охлажденного диэтилового эфира, отфильтровывают, дважды промывают эфиром, после чего высушивают лиофильно.
Синтезированный пептид подвергают очистке по методу ВЭЖХ на колонке с обращенной фазой Luna C18 (10×250 мм, размер пор 100 Å, диаметр частиц 10 мкм, Phenomenex, США). Фракционирование проводят в линейном градиенте концентрации ацетонитрила от 0 до 50% (v/v) в 0,1%-ной (v/v) трифторуксусной кислоте в течение 60 минут со скоростью элюции 2 мл/мин. Детекцию осуществляют по оптическому поглощению при 210 нм.
Содержание примесей в синтетическом препарате LtAMP-2a составляет 1%, что подтверждается разделением по методу ВЭЖХ на аналитической колонке Luna C18 (1×150 мм, размер пор 100 Å, диаметр частиц 3 мкм, Phenomenex, США) в линейном градиенте концентрации ацетонитрила от 20 до 50% (v/v) в 0,1%-ной (v/v) трифторуксусной кислоте в течение 40 минут со скоростью элюции 50 мкл/мин, детекцию осуществляют по оптическому поглощению при 210 нм.
Идентичность синтезированного LtAMP-2a природному доказывают при помощи масс-спектрометрического анализа, сравнением хроматографических подвижностей при разделении на аналитической колонке Luna C18 (1×150 мм, Phenomenex, США), а также сравнением биологических свойств.
Пептиды LtAMP-2a_F10K и LtAMP-2a_I7Q синтезируют аналогичным способом, внося необходимые аминокислоты. Для защиты боковой цепи Gln используют тритильную группу.
Пример 4.
Тестирование пептидов на антимикробную активность.
th ed. – Williams and Wilkins, Baltimore. – 1996. – P.52-111].
Бактерии культивируют в жидкой низкосолевой среде LB (1% бакто-триптон, 0,5% бакто-дрожжевой экстракт, 0,5% NaCl, pH 7) при 37°С и перемешивании со скоростью 220 об/мин в течение 18 ч. Полученные культуры разбавляют в 200 раз, используя среду LB, и выращивают в тех же условиях в течение 3-5 ч до достижения экспоненциальной фазы роста (оптическая плотность культуры при 620 нм OD6200,3-0,5), после чего снова разбавляют до концентрации клеток 105 колоний образующих единиц в 1 мл. Культуры помещают в стерильные 96-луночные планшеты, по 90 мкл в лунку, куда затем добавляют по 10 мкл растворов тестируемых веществ различных концентраций, получаемых серийными разведениями. Отрицательным контролем служит культура клеток с добавлением 10 мкл чистой воды, положительным – чистая среда для культивирования. Планшеты инкубируют в условиях, описанных выше, в течение 24 ч, после чего измеряют OD620, минимальные ингибирующие концентрации определяют как наименьшие концентрации веществ, полностью подавляющие рост микроорганизмов. Опыт проводят в трех независимых повторах.
Результаты определения минимальных ингибирующих концентраций для пептидов LtAMP-2a, LtAMP-2a_F10K, LtAMP-2a_I7Q представлены в таблице 2. Пептиды LtAMP-2a_F10K и LtAMP-2a_I7Q сохраняют высокую антимикробную активность.
Таблица 2
Антимикробные свойства исходного пептида LtAMP-2a и его аналогов |
| пептид |
минимальная ингибирующая концентрация, мкМ |
| Escherichia coli С600 |
Bacillus subtilis ВКМ В-501 |
| LtAMP-2a (исходный) |
3,0 |
0,7 |
| LtAMP-2a_F10K |
5,5 |
0,7 |
| LtAMP-2a_I7Q |
5,0 |
1,3 |
Пример 5.
Тестирование пептидов на гемолитическую активность.
Гемолитическую активность пептидов определяют с использованием крови здорового донора (группа В, Rh+). К 100 мкл свежей крови добавляют 900 мкл среды RPMI-1640, содержащей 2 мМ L-глутамин, 8% эмбриональной бычьей сыворотки (ЭБС) и гепарин (10 ед/мл). Определяют плотность клеток, после чего суспензию разводят средой RPMI-1640 до плотности 107 клеток/мл. К полученной суспензии добавляют тестируемый пептид нужной концентрации, в качестве отрицательного контроля используют клетки без добавления пептида. Инкубируют при 37°С и перемешивании со скоростью 120 об/мин в течение 3 ч, после чего клетки осаждают центрифугированием в течение 5 мин при 4000 g, 100 мкл супернатанта отбирают в стерильные 96-луночные планшеты, выход гемоглобина из эритроцитов оценивают по оптической плотности при 414 нм. Гемолитическая активность пептидов (см. табл. 3) выражается в % от максимально возможного гемолиза, максимально возможный лизис эритроцитов (положительный контроль) получают за счет ресуспендирования осажденных клеток в чистой воде до плотности 107 клеток/мл.
В результате получают, что предложенные аналоги LtAMP-2a_F10K и LtAMP-2a_I7Q для исходного гемолитически активного пептида подобной активности не проявляют (0% гемолиз) в концентрациях до 45 мкМ.
Пример 6.
Тестирование пептидов на цитотоксичность по отношению к лейкоцитам и клеткам эритролейкемии человека.
Оценку цитотоксических свойств латарцинов для лейкоцитов человека проводят на фракции крови здорового донора (группа В, Rh+), обогащенной лейкоцитами, которую получают отстаиванием гепаринизированной (10 ед/мл) крови в течение 2 ч при 15°С в темноте. Отбирают фракцию выше эритроцитарного столба, соотношение лейкоцитов и эритроцитов в которой 1:10, добавляют 1,5 объема среды RPMI-1640, содержащей 2 мМ L-глутамин и 8% ЭБС. Клетки осаждают центрифугированием в течение 5 мин при 200 g, супернатант удаляют, клетки ресуспендируют в равном объеме среды RPMI-1640. Операцию повторяют дважды, после чего клетки рассаживают в 96-луночные плоскодонные культуральные планшеты (106 клеток/мл, 150 мкл среды RPMI-1640, содержащей 2 мМ L-GIn и 8% ЭБС, на лунку).
Клетки эритролейкемии человека К562 культивируют в среде RPMI-1640 с добавлением 2 мМ L-глутамина и 8% ЭБС при 37°С, в атмосфере 100%-ной влажности с 5%-ным содержанием СО2. За день до эксперимента клетки рассаживают в 96-луночные планшеты (106 клеток/мл).
В лунки вносят исследуемые пептиды в нужной концентрации, в качестве отрицательного контроля в лунки добавляют чистую воду. Клетки (К562 и лейкоциты) инкубируют с различными концентрациями пептидов в течение 3 ч при 37°С, затем в лунки вносят флуоресцентные красители Hoechst33342 (20 мкМ, окрашивает ядра всех клеток) и пропидиум иодид (20 мкМ, окрашивает ядра мертвых клеток) и через 15 мин регистрируют флуоресцентные изображения клеток с помощью инвертированного флуоресцентного микроскопа Axiovert 200M (Zeiss, Германия) с цифровой камерой AxioCam MRc (Zeiss, Германия) в области флуоресценции Hoechst33342 (фильтры на возбуждение – ВР 365/12, на эмиссию – LP 397) и в области флуоресценции пропидиум иодида (фильтры на возбуждение – ВР 510-560, на эмиссию – LP 590). По этим изображениям для каждой концентрации пептида подсчитывают общее число клеток (1000 клеток на одно измерение) и число мертвых клеток среди них, а затем рассчитывают концентрацию пептида, вызывающую гибель 50% клеток, ИК50. Результаты (см. табл. 3) усредняют по трем независимым экспериментам.
В итоге получают, что предложенные аналоги LtAMP-2a_F10K и LtAMP-2a_I7Q для исходного цитотоксичного в отношении нормальных лейкоцитов пептида подобной активности не проявляют (0% лизис) в концентрациях до 45 мкМ. Однако пептиды сохраняют достаточно высокую цитотоксическую активность в отношении опухолевых клеток.
Таблица 3
Цитотоксические свойства исходного пептида LtAMP-2a и его аналогов |
| пептид |
эритроциты человека |
нормальные лейкоциты человека |
клетки эритролейкемии человека К562 |
ЭК50  , мкМ , мкМ |
ИК50  , мкМ , мкМ |
ИК50  , мкМ , мкМ |
| LtAMP-2a (исходный) |
9,2 |
17,9 |
3,3 |
| LtAMP-2a_F10K |
–  |
–  |
18,6 |
| LtAMP-2a_I7Q |
–  |
–  |
24,7 |
 – эффективная концентрация, вызывающая 50%-ный лизис – эффективная концентрация, вызывающая 50%-ный лизис
  – активность отсутствует (0% лизис) при концентрациях до 45 мкМ – активность отсутствует (0% лизис) при концентрациях до 45 мкМ |
Формула изобретения
Способ получения антимикробных пептидов с пониженной гемолитической активностью, включающий моделирование пространственной структуры исходного пептида с высокой гемолитической активностью в  -спиральной конформации и химический синтез с заменой гидрофобных аминокислотных остатков на гидрофильные в процессе синтеза, отличающийся тем, что после моделирования пространственной структуры исходного пептида в -спиральной конформации и химический синтез с заменой гидрофобных аминокислотных остатков на гидрофильные в процессе синтеза, отличающийся тем, что после моделирования пространственной структуры исходного пептида в  -спиральной конформации дополнительно проводят расчет гидрофобных свойств пептида с учетом молекулярного гидрофобного потенциала в каждой точке поверхности пептида, выявление гидрофобных кластеров и аминокислотных остатков, локализованных в них, с последующим определением наиболее эффективных гидрофильных аминокислотных остатков, являющихся полярными или заряженными, сходными по размеру и склонности к формированию -спиральной конформации дополнительно проводят расчет гидрофобных свойств пептида с учетом молекулярного гидрофобного потенциала в каждой точке поверхности пептида, выявление гидрофобных кластеров и аминокислотных остатков, локализованных в них, с последующим определением наиболее эффективных гидрофильных аминокислотных остатков, являющихся полярными или заряженными, сходными по размеру и склонности к формированию  -спирали, для использования в процессе синтеза, в ходе которого происходит замена гидрофобных аминокислот Ile7 и Phe10 на гидрофильные Gln7 и Lys10. -спирали, для использования в процессе синтеза, в ходе которого происходит замена гидрофобных аминокислот Ile7 и Phe10 на гидрофильные Gln7 и Lys10.
РИСУНКИ
|
|