Патент на изобретение №2315761
|
||||||||||||||||||||||||||
(54) СПОСОБ ПОЛУЧЕНИЯ ЭФИРОВ ДИОКСАНУКСУСНОЙ КИСЛОТЫ
(57) Реферат:
Данное изобретение относится к новому способу получения сложных эфиров диоксануксусной кислоты формулы (1), где R1 представляет собой уходящую группу, CN, ОН или группу COOR5, R3 и R4, каждый независимо, представляют собой C1-3алкильную группу, и R2 и R5, каждый независимо, представляют собой сложноэфирный остаток, при котором соответствующую соль формулы (2), где М представляет собой Н или щелочной (щелочно-земельный) металл, приводят в контакт с хлорангидрид-образующим агентом в инертном растворителе с образованием соответствующего хлорангидрида, и этот хлорангидрид приводят в контакт со спиртом формулы R2OH в присутствии N-метилморфолина. Предпочтительно М представляет собой щелочной металл, а R2 представляет собой алкильную группу, в частности трет-бутильную группу. Технический результат – повышение выхода целевого продукта. 10 з.п. ф-лы.
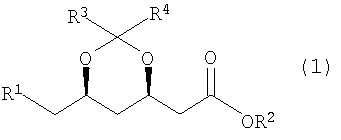
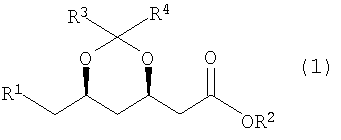
Изобретение относится к способу получения сложного эфира формулы (1)
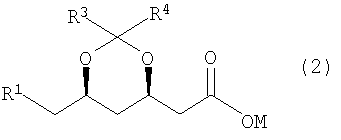
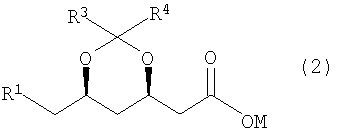
где R1 представляет собой уходящую группу, CN, ОН или группу COOR5, R3 и R4, каждый независимо, представляют собой C1-3алкильную группу, и R2 и R5, каждый независимо, представляют собой сложноэфирный остаток, при котором соответствующую соль формулы (2)
где М представляет собой Н или щелочной (щелочно-земельный) металл, приводят в контакт с хлорангидрид-образующим агентом в инертном растворителе с образованием соответствующего хлорангидрида и этот хлорангидрид приводят в контакт со спиртом формулы R2OH в присутствии N-метил-морфолина (N-MM). Из уровня техники известны многочисленные способы получения сложных эфиров, например получение сложных эфиров через образование хлорангидрида. Однако следовало ожидать, что такие способы не дадут высоких выходов из-за нестабильности настоящего соединения в кислых условиях. В задачу изобретения входило создание способа получения сложных эфиров со стабильно высоким выходом даже в крупномасштабном производстве и при относительно высоких концентрациях. Неожиданно было обнаружено, что даже пространственно затрудненные сложные эфиры, которые трудно получить посредством этерификации, такие как трет-бутиловые эфиры кислотонеустойчивых молекул формулы (1), могут быть получены с большим выходом легковоспроизводимым способом. Сложные эфиры формулы (1), которые являются нестабильными в кислых условиях, например при рН менее 4, могут быть получены с высоким выходом способом согласно изобретению. R1 представляет собой уходящую группу, CN, ОН или группу COOR5, в которой R5 представляет собой сложноэфирный остаток, например алкильную группу, например, из 1-6 атомов углерода, или арильную группу, например, из 6-12 атомов углерода. Уходящая группа по определению представляет собой группу, которая может быть легко заменена, такую как галоген, например Cl, Br или I; тозилатная группа; мезилатная группа; группа ацилокси из, например, 1-6 С-атомов, в частности группа ацетокси; группа фенацетилокси; группа алкокси из, например, 1-6 С-атомов, или группа (гетеро)арилокси из, например, 6-12 С-атомов. Предпочтительно R1 представляет собой Cl. R2 представляет собой сложноэфирный остаток, предпочтительно алкильную группу, например алкильную группу из 1-6 С-атомов, или арильную группу, например арильную группу из 6-12 С-атомов, в частности метильную, этильную, пропильную, изобутильную или трет-бутильную группу. Важной группой сложных эфиров, которые могут быть получены согласно способу по изобретению, являются трет-бутиловые сложные эфиры. R3 и R4, каждый независимо, представляют собой С1-С3 алкильную группу, например метильную или этильную группу. Предпочтительно R3 и R4 оба представляют собой метил. М в формуле (2) может быть выбран из группы, включающей водород, щелочные металлы, например литий, натрий, калий, и щелочно-земельные металлы, например магний или кальций. Предпочтительно М представляет собой натрий или калий. Хлорангидрид-образующий агент может быть выбран из группы реагентов, которые широко известны как таковые. Подходящими примерами хлорангидрид-образующих агентов являются оксалилхлорид, тионилхлорид, PCl3, PCl5 и POCl3. Предпочтительно хлорангидрид-образующий агент используют в избытке относительно количества соли формулы (2), например между 1 и 3 эквивалентами, более предпочтительно между 1,2 и 1,8 эквивалентами. При желании образование хлорангидрида может проходить в присутствии катализатора. Количество катализатора может, например, варьировать от 0 до 1, предпочтительно от 0 до 0,5 эквивалентов, в расчете на количество соли формулы (2). Возможны также большие количества катализатора, но, как правило, они не обеспечивают никакого дополнительного полезного эффекта. Предпочтительно количество катализатора, если таковой применяется, составляет от 0,05 до 0,2 эквивалентов в расчете на соль формулы (2). Подходящими катализаторами являются катализаторы, о которых известно, что они ускоряют образование хлорангидрида, например диметилформамид (ДМФ) и N-метилпирролидон (N-МП). Превращение хлорангидрида в сложный эфир формулы (1) осуществляют в присутствии спирта формулы R2OH. Количество спирта формулы R2OH не является особенно критичным и предпочтительно составляет от 1 до 15 эквивалентов в расчете на количество соли формулы (2), более предпочтительно от 2 до 13 эквивалентов, наиболее предпочтительно от 3 до 6 эквивалентов. Неожиданно было обнаружено, что даже трет-бутиловые сложные эфиры могут быть получены с высоким выходом при использовании относительно небольшого количества трет-бутилового спирта. Превращение хлорангидрида в сложный эфир формулы (1) осуществляют в присутствии N-MM. На практике используют небольшое количество N-MM, эффективно улавливающее остающуюся свободную HCl, например от 1,5 до 2,5, предпочтительно от 1,8 до 2,0 эквивалентов, в расчете на количество соли формулы (2). Когда используют большой избыток хлорангидрид-образующего агента, предпочтительно используют большие количества N-MM, а когда используют меньший избыток хлорангидрид-образующего агента, предпочтительно используют меньшие количества N-MM. Реакцию образования хлорангидрида предпочтительно осуществляют при температуре между -30 и 60°С, более предпочтительно между 20 и 50°С. Превращение хлорангидрида в сложный эфир формулы (1) предпочтительно осуществляют при температуре между 20 и 80°С, более предпочтительно между 20 и 50°С. Способ по настоящему изобретению может быть осуществлен в одну стадию. Предпочтительно сначала соль формулы (2) превращают в соответствующий хлорангидрид и затем этот хлорангидрид приводят в контакт со спиртом формулы R2OH и N-MM. В особенно предпочтительном воплощении образовавшийся хлорангидрид гасят N-MM и спиртом формулы R2OH. Продукт формулы 1, где R1 представляет собой уходящую группу, затем может быть превращен в соответствующее соединение, где R1 представляет собой группу ацилокси. Это может быть осуществлено известным способом, например, путем взаимодействия с ацилоксилирующим агентом, например карбоновой или сульфоновой кислотой, четвертичной солью аммония или фосфония, четвертичной солью аммония или фосфония и карбоновой или сульфоновой кислоты, или их комбинацией. В качестве ацилоксилирующего агента предпочтительно используют комбинацию четверичной соли фосфония и соли карбоновой или сульфоновой кислоты. Затем соединение формулы 1, где R1 представляет собой группу ацилокси, может быть превращено в соответствующее соединение, где R1 представляет собой гидрокси-группу, например, путем его сольволиза в присутствии основания. Подходящими основаниями являются, например, гидроксиды или карбонаты щелочных (щелочно-земельных) металлов или органические основания, например соли щелочно-земельных металлов и карбоновых кислот, например ацетаты, аммиак, пиридины, амины, например триэтиламин и другие. Изобретение разъясняется следующими примерами. Пример I (4R-цис)-(6-хлорметил)-2,2-диметил-1,3-диоксан-4-ил-уксусной кислоты трет-бутиловый эфир Смешивали 1864 г водного раствора натриевой соли (4R-цис)-(6-хлорметил)-2,2-диметил-1,3-диоксан-4-ил-уксусной кислоты (3,31 моль) и 4,8 л толуола, воду удаляли азеотропной перегонкой при пониженном давлении. Затем добавляли 870 г свежего толуола и удаляли его посредством перегонки. К полученной суспензии добавляли 33,4 г N-МП. Затем добавляли 588 г оксалилхлорида, при этом температуру поддерживали около 20°С. Полученную смесь перемешивали в течение 6 часов при 20-25°С и затем к этой смеси медленно добавляли 979 г трет-бутанола и 836 г N-метилморфолина. После перемешивания в течение 1 часа добавляли 3966 г 8%-ного (об./об.) водного раствора NaOH и полученную смесь перемешивали в течение 1,5 часов при 40°С. После промывки органической фазы водой в количестве 3300 г было получено 3064 г раствора искомого трет-бутилового эфира в толуоле, что соответствует 751 г (81%) продукта. Пример II (4R-цис)-(6-хлорметил)-2,2-диметил-1,3-диоксан-4-ил-уксусной кислоты трет-бутиловый эфир В HEL сосуде емкостью 100 мл, снабженном 4-лопастной мешалкой, в 41 г толуола и 0,3 г N-МП (3 ммоль) суспендировали 8,0 г натриевой соли (4R-цис)-(6-хлорметил)-2,2-диметил-1,3-диоксан-4-ил-уксусной кислоты (92,4%; 30 ммоль). 4,5 г (36 ммоль) оксалилхлорида дозировали в течение 1 часа при температуре 15-20°С. Реакционную смесь (50 г) перемешивали в течение 2,5 часов. Реакционную смесь делили на 2 части: часть А (23,83 г) и часть Б (24,25 г). Часть А реакционной смеси дозировали в течение 1 часа в смесь 22,2 г (20 экв.) трет-бутанола и 3,0 г (2 экв.) N-MM при 25°С. Реакционную смесь перемешивали в течение ночи и анализировали методом газовой хроматографии. Выход трет-бутилового эфира составлял 88%. Примеры III-V (4R-цис)-(6-хлорметил)-2,2-диметил-1,3-диоксан-4-ил-уксусной кислоты этиловый, изопропиловый и н-гексиловый эфиры Следуя методике, описанной в примере I, получали этиловые, изопропиловые и н-гексиловые эфиры соответственно, где вместо 4 экв. бутанола использовали 4 экв. этанола, 4 экв. изопропанола и 4 экв. н-гексанола соответственно. Выход искомых этиловых, изопропиловых и н-гексиловых эфиров составил 89 мол.%, 88 мол.% и 84 мол.% соответственно в расчете на натриевую соль исходного материала. Пример VI (4R-цис)-(6-трет-бутаноилоксиметил)-2,2-диметил-1,3-диоксан-4-ил-уксусной кислоты трет-бутиловый эфир Смесь 35,0 г трет-бутил-(4R-цис)-(6-хлорметил)-2,2-диметил-1,3-диоксан-4-ил-ацетата, 14,8 г тетрабутилфосфония бромида, 16,0 г ацетата калия и 5,9 г толуола нагревали до 105°С при пониженном давлении. Спустя 22 ч при этой температуре реакционную смесь охлаждали до температуры окружающей среды, после чего добавляли 400 г гептана и 350 г воды. Органическую фазу промывали водой в количестве 150 г и далее обрабатывали 3,0 г активированного угля. После того как уголь был отфильтрован, раствор концентрировали и далее охлаждали до -10°С, после чего кристаллический продукт выделяли посредством фильтрации. Выход составлял 24,9 г (76%) белого кристаллического вещества.
Формула изобретения
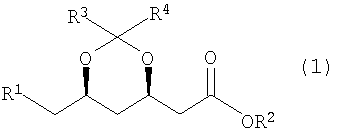
1. Способ получения сложного эфира формулы (1)
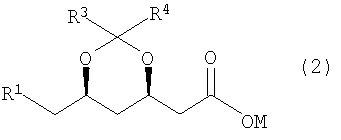
где R1 представляет собой уходящую группу, CN, ОН или группу COOR5, R3 и R4, каждый независимо, представляют собой С1-3алкильную группу, и R2 и R5, каждый независимо, представляют собой сложноэфирный остаток, при котором соответствующую соль формулы (2)
где М представляет собой водород или щелочной (щелочно-земельный) металл, в инертном растворителе приводят в контакт с хлорангидрид-образующим агентом с образованием соответствующего хлорангидрида, и этот хлорангидрид приводят в контакт со спиртом формулы R2ОН в присутствии N-метил-морфолина. 2. Способ по п.1, где М представляет собой щелочной металл. 3. Способ по п.1 или 2, где R2 представляет собой алкильную группу. 4. Способ по п.3, где R2 представляет собой трет.-бутильную группу. 5. Способ по п.1, где хлорангидрид-образующим агентом является оксалилхлорид. 6. Способ по п.1, при котором образование хлорангидрида осуществляют в присутствии катализатора. 7. Способ по п.1, при котором количество спирта формулы R2OH составляет от 3 до 6 эквивалентов в расчете на количество соли формулы (2). 8. Способ по п.1, при котором сначала соль формулы (2) превращают в соответствующий хлорангидрид, а затем этот хлорангидрид приводят в контакт со спиртом формулы R2ОН и N-метил-морфолином. 9. Способ по п.8, при котором хлорангидрид гасят спиртом формулы R2ОН и N-метил-морфолином. 10. Способ по п.1, где R1 представляет собой уходящую группу, при котором сложный эфир формулы 1, где R1 представляет сбой уходящую группу, затем превращают в соответствующий сложный эфир формулы 1, где R1 представляет собой группу ацилокси. 11. Способ по п.10, при котором сначала получают сложный эфир формулы 1, где R1 представляет собой группу ацилокси, а затем этот сложный эфир формулы 1 превращают в соответствующее соединение формулы 1, где R1 представляет собой ОН.
|
||||||||||||||||||||||||||