|
|
(21), (22) Заявка: 2006108385/04, 06.09.2004
(24) Дата начала отсчета срока действия патента:
06.09.2004
(30) Конвенционный приоритет:
17.09.2003 (пп.1-14) US 60/503,592
(43) Дата публикации заявки: 10.08.2006
(46) Опубликовано: 27.01.2008
(56) Список документов, цитированных в отчете о
поиске:
US 4681873 А, 21.06.1987. US 5969156 A , 19.10.1999. WO 0243667 A2, 06.06.2002. US 6583295 B1, 24.06.2003. RU 2158607 C1, 10.11.2000.
(85) Дата перевода заявки PCT на национальную фазу:
16.03.2006
(86) Заявка PCT:
IB 2004/002919 (06.09.2004)
(87) Публикация PCT:
WO 2005/026116 (24.03.2005)
Адрес для переписки:
129010, Москва, ул. Б.Спасская, 25, стр.3, ООО “Юридическая фирма Городисский и Партнеры”, пат.пов. Е.Е.Назиной, рег. № 517
|
(72) Автор(ы):
КЭМПЕТА Энтони Майкл (US),
КРЖИЗАНЯК Джозеф Фрэнсис (US),
ЛЕОНАРД Джейсон Альберт (US)
(73) Патентообладатель(и):
УОРНЕР-ЛАМБЕРТ КОМПАНИ ЛЛС (US)
|
(54) КРИСТАЛЛИЧЕСКИЕ ФОРМЫ [R-(R*,R*)]-2-(4-ФТОРФЕНИЛ)-БЕТА, ДЕЛЬТА-ДИГИДРОКСИ-5-(1-МЕТИЛЭТИЛ)-3-ФЕНИЛ-4-[(ФЕНИЛАМИНО)КАРБОНИЛ]-1Н-ПИРРОЛ-1-ГЕПТАНОВОЙ КИСЛОТЫ
(57) Реферат:
Данное изобретение относится к новым кристаллическим формам [R-(R*,R*)]-2-(4-фторфенил)- , , -дигидрокси-5-(1-метилэтил)-3-фенил-4-[(фениламино)карбонил]-1Н-пиррол-1-гептановой кислоты (свободной кислоты аторвастатина), обозначенным как формы А и В, которые охарактеризованы порошковой рентгенограммой и спектрами ЯМР твердых тел, а также к фармацевтическим композициям на их основе и способу лечения гиперлипидемии и гиперхолестеринемии, остеопороза, доброкачественной гиперплазии простаты и болезни Альцгеймера. 14 н.п. ф-лы, 6 табл., 4 ил. -дигидрокси-5-(1-метилэтил)-3-фенил-4-[(фениламино)карбонил]-1Н-пиррол-1-гептановой кислоты (свободной кислоты аторвастатина), обозначенным как формы А и В, которые охарактеризованы порошковой рентгенограммой и спектрами ЯМР твердых тел, а также к фармацевтическим композициям на их основе и способу лечения гиперлипидемии и гиперхолестеринемии, остеопороза, доброкачественной гиперплазии простаты и болезни Альцгеймера. 14 н.п. ф-лы, 6 табл., 4 ил.
Область техники, к которой относится изобретение
Настоящее изобретение относится к новым кристаллическим формам аторвастатина в форме свободной кислоты, которая известна под химическим названием [R-(R*,R*)]-2-(4-фторфенил)- , , -дигидрокси-5-(1-метилэтил)-3-фенил-4-[(фениламино)карбонил]-1H-пиррол-1-гептановая кислота, применяемой как промежуточный продукт при получении фармацевтически приемлемых солей аторвастатина, включая аторвастатин-кальций, и в качестве фармацевтических средств, кроме того, оно относится к способам их получения и выделения в виде фармацевтических композиций, которые включают эти соединения и фармацевтически приемлемый носитель, а также к способам использования таких композиций для лечения субъектов, включая людей, страдающих от гиперлипидемии, гиперхолестеринемии, доброкачественной гиперплазии простаты, остеопороза и болезни Альцгеймера. -дигидрокси-5-(1-метилэтил)-3-фенил-4-[(фениламино)карбонил]-1H-пиррол-1-гептановая кислота, применяемой как промежуточный продукт при получении фармацевтически приемлемых солей аторвастатина, включая аторвастатин-кальций, и в качестве фармацевтических средств, кроме того, оно относится к способам их получения и выделения в виде фармацевтических композиций, которые включают эти соединения и фармацевтически приемлемый носитель, а также к способам использования таких композиций для лечения субъектов, включая людей, страдающих от гиперлипидемии, гиперхолестеринемии, доброкачественной гиперплазии простаты, остеопороза и болезни Альцгеймера.
Предпосылки создания изобретения
Превращение 3-гидрокси-3-метилглутарил-коэнзима A (HMG-CoA) в мевалонат является начальной и определяющей скорость реакции стадией в ходе биосинтеза холестерина. Эту стадию катализирует фермент HMG-CoA-редуктаза. Статины ингибируют катализ этого превращения HMG-CoA редуктазой. Сами по себе статины являются сильнодействующими средствами, снижающими общий уровень липидов.
Аторвастатин-кальций обычно продают под товарным знаком Lipitor®, имеющий химическое наименование тригидрат кальциевой соли [R-(R*,R*)]-2-(4-фторфенил)- , , -дигидрокси-5-(1-метилэтил)-3-фенил-4-[(фениламино)карбонил]-1H-пиррол-1-гептановой кислоты (2:1) и формулу: -дигидрокси-5-(1-метилэтил)-3-фенил-4-[(фениламино)карбонил]-1H-пиррол-1-гептановой кислоты (2:1) и формулу:
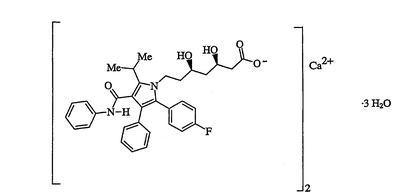
Незапатентованным наименованием, обозначенным в USAN (наименования, принятые в США, не подлежащие регистрации в качестве товарного знака), является аторвастатин-кальций, а обозначенным в INN (Международные Незапатентованные Наименования), является аторвастатин. По установленным руководящим принципам USAN соль включают в наименование, тогда как по руководящим документам INN описание соли не включают в наименование.
Аторвастатин и его фармацевтически приемлемые соли являются селективными, конкурентными ингибиторами HMG-CoA редуктазы. Сам по себе аторвастатин-кальций является сильнодействующим соединением, понижающим уровень содержания липидов, и, таким образом, является применимым в качестве гиполипидемического и/или гипохолестеринемического средства, а также применимым для лечения остеопороза, доброкачественной гиперплазии простаты и болезни Альцгеймера.
Ряд опубликованных патентов описывают препараты аторвастатин-кальция, а также способы получения аторвастатин-кальция и ключевые промежуточные соединения при его получении. Эти патенты включают нижеследующие патенты США: 4681893; 5273995; 5003080; 5097045; 5103024; 5124482; 5149837; 5155251; 5216174; 5245047; 5248793; 5280126; 5397792; 5342952; 5298627; 5,446054; 5470981; 5489690; 5489691; 5510488; 5686104; 5998633; 6087511; 6126971; 6433213; и 6476,35, которые введены в настоящее описание путем ссылки.
Аторвастатин-кальций может существовать в кристаллической, жидкокристаллической, некристаллической и аморфной формах.
Кристаллические формы аторвастатина кальция описаны в патентах США 5969156 и 6121461, которые введены в настоящий документ путем ссылки. Кроме того, кристаллические, жидкокристаллические, пластично-кристаллические, неупорядоченные формы и некристаллические формы, а также мезофазы описаны в совместно рассматриваемых заявках: в опубликованной международной заявке на патент WO 03/004470 и заявке на патент США серийный номер 60/414734, которые введены в настоящее описание путем ссылки.
Дополнительно в ряде опубликованных международных заявок на патент были описаны кристаллические формы аторвастатина кальция, а также способы получения аморфного аторвастатина кальция. Эти заявки включают: WO 00/71116; WO 01/28999; WO 01/36384; WO 01/42209; WO 02/41834; WO 02/43667; WO 02/43732; WO 02/051804; WO 02/057228; WO 02/057229; WO 02/057274; WO 02/059087; WO 02/072073; WO 02/083637; WO 02/083638; и WO 02/089788.
Аторвастатин получают в виде его кальциевой соли, то есть кальциевая соль [R-(R*,R*)]-2-(4-фторфенил)- , , -дигидрокси-5-(1-метилэтил)-3-фенил-4-[(фениламино)карбонил]-1H-пиррол-1-гептановой кислоты (2:1). Кальциевая соль является желательной, так как она дает возможность составить препарат аторвастатина, например, в виде таблеток, капсул, лепешек, порошков и тому подобного для орального введения. -дигидрокси-5-(1-метилэтил)-3-фенил-4-[(фениламино)карбонил]-1H-пиррол-1-гептановой кислоты (2:1). Кальциевая соль является желательной, так как она дает возможность составить препарат аторвастатина, например, в виде таблеток, капсул, лепешек, порошков и тому подобного для орального введения.
Аторвастатин в форме свободной кислоты, описанный в патенте США 5213995, может быть использован для получения кальциевой соли аторвастатина, а также других фармацевтически приемлемых основно-аддитивных солей аторвастатина. Дополнительно аторвастатин в форме свободной кислоты может быть использован в качестве фармацевтического средства. Однако до настоящего изобретения аторвастатин в форме свободной кислоты мог быть выделен только в виде масла. Поэтому существовала необходимость в получении аторвастатина в форме свободной кислоты в твердом состоянии, предпочтительно в кристаллической форме, для облегчения получения солей аторвастатина, а также фармацевтических композиций, содержащих аторвастатин в форме свободной кислоты.
К удивлению неожиданно были обнаружены новые кристаллические формы аторвастатина в форме свободной кислоты. Таким образом, настоящее изобретение обеспечивает аторвастатин в форме свободной кислоты в новых кристаллических формах, обозначаемых как формы A и B. В сравнении с некристаллической формой уровня техники новые кристаллические формы аторвастатина в форме свободной кислоты обладают большей стабильностью и чистотой и обладают лучшими характеристиками.
Сущность изобретения
Соответственно первый аспект настоящего изобретения относится к кристаллическим формам аторвастатина в форме свободной кислоты и ее гидратов.
Во втором аспекте изобретение относится к кристаллической форме A аторвастатина в форме свободной кислоты и ее гидратов, характеризуемых нижеследующей порошковой рентгенограммой, выраженной в значениях 2 , d-расстояниях и относительных интенсивностях, где относительные интенсивности, превышающие 20%, измерены на дифрактометре Bruker D5000 с использованием излучения CuK , d-расстояниях и относительных интенсивностях, где относительные интенсивности, превышающие 20%, измерены на дифрактометре Bruker D5000 с использованием излучения CuK . .
Градус 2 |
d
(Е) |
Относительная интенсивность (>20%) интенсивность (>20%) |
| 4,7 |
18,7 |
49,5 |
| 6,0 |
14,6 |
25,9 |
| 8,9 |
9,9 |
46,0 |
| 9,1 |
9,8 |
63,0 |
| 9,4 |
9,4 |
100,0 |
| 13,2 |
6,7 |
20,5 |
| 14,1 |
6,3 |
29,5 |
| 17,8 |
5,0 |
55,8 |
| 18,1 |
4,9 |
98,1 |
| 18,9 |
4,7 |
63,8 |
| 19,9 |
4,5 |
23,9 |
| 20,2 |
4,4 |
29,3 |
| 20,6 |
4,3 |
32,4 |
| 21,8 |
4,1 |
50,1 |
| 22,1 |
4,0 |
57,5 |
| 22,5 |
4,0 |
28,4 |
| 23,7 |
3,8 |
57,1 |
| 25,9 |
3,4 |
21,0 |
| 26,7 |
3,3 |
20,0 |
 Относительные интенсивности могут меняться в зависимости от размера и морфологии кристалла. Относительные интенсивности могут меняться в зависимости от размера и морфологии кристалла. |
Кроме того, в третьем аспекте настоящее изобретение относится к кристаллической форме A аторвастатина в форме свободной кислоты и ее гидратов, характеризуемых нижеследующим спектром 13C ядерного магнитного резонанса в твердом состоянии (SSNMR), где химический сдвиг выражают в миллионных долях (м.д.):
| Отнесение |
Химический сдвиг углерода (м.д.) |
| С39 |
180,6 |
| C39 |
174,3 |
| C8 |
167,1 |
| C8 |
166,3 |
| C27 |
163,6 |
| C27 |
161,5 |
| Следующие резонансные группы включают: С1, 2, 3, 4, 6, 7, 9, 10, 12, 13, 17, 18, 20, 21, 24, 25, 28, 29, 33, 34, 36 |
141,8 |
| |
140,7 |
| |
137,9 |
| |
135,2 |
| |
134,1 |
| |
132,9 |
| |
130,0 |
| |
128,8 (выступ) |
| |
128,0 |
| |
125,4 |
| |
123,3 |
| |
121,6 |
| |
119,3 |
| |
118,4 |
| |
116,4 |
| |
115,1 |
| |
113,7 |
| |
112,3 |
| Следующие резонансные группы включают: C26, 35 |
71,3 |
| |
70,0 |
| |
69,1 |
| |
68,6 |
| |
65,3 |
| Следующие резонансные группы включают: C11, 19, 30, 37 |
43,5 |
| |
42,9 |
| |
41,8 |
| |
40,6 |
| |
40,0 |
| |
38,9 |
| |
37,1 |
| Следующие резонансные группы включают: C14, 22, 23 |
26,8 |
| |
26,2 |
| |
25,5 |
| |
25,0 |
| |
21,2 |
| |
20,5 |
| |
18,8 |
| |
18,1 |
| Пик при 8,4 м.д. представляет собой побочный сигнал вращения |
|
 Величины выражены в м.д., при относительном сдвиге тетраметилсилана (ТМС), принимаемым за 0 м.д.; используя адамантан в качестве внешнего эталона сравнения с установлением высокопольного резонанса при 29,5 м.д. Величины выражены в м.д., при относительном сдвиге тетраметилсилана (ТМС), принимаемым за 0 м.д.; используя адамантан в качестве внешнего эталона сравнения с установлением высокопольного резонанса при 29,5 м.д. |
Дополнительно в четвертом аспекте настоящее изобретение относится к кристаллической форме A аторвастатина в форме свободной кислоты и ее гидратов, характеризуемых нижеследующим спектром 19F ядерного магнитного резонанса в твердом состоянии, где химический сдвиг выражен в миллионных долях:
| Отнесение |
Химический сдвиг фтора (м.д.) |
| F |
-105,6 |
| |
-110,6 |
| |
-112,6 |
| |
-114,1 |
 Величины выражены в м.д., при относительном сдвиге CCI3F, принимаемым за 0 м.д.; сравнение осуществляют, устанавливая сигнал 19F смеси трифторуксусная кислота (TFA)/H2O (1:1) при 76,54 м.д. Величины выражены в м.д., при относительном сдвиге CCI3F, принимаемым за 0 м.д.; сравнение осуществляют, устанавливая сигнал 19F смеси трифторуксусная кислота (TFA)/H2O (1:1) при 76,54 м.д. |
В пятом аспекте настоящее изобретение относится к кристаллической форме В аторвастатина в форме свободной кислоты и ее гидратов, характеризуемых нижеследующей порошковой рентгенограммой, выраженной в значениях 2 , d-расстояниях и относительных интенсивностях, где относительные интенсивности, превышающие 20%, измерены на дифрактометре Bruker D5000 с использованием излучения CuK , d-расстояниях и относительных интенсивностях, где относительные интенсивности, превышающие 20%, измерены на дифрактометре Bruker D5000 с использованием излучения CuK : :
Градус 2 |
d
(Е) |
Относительная интенсивность (>20%) интенсивность (>20%) |
| 4,6 |
19,0 |
48,3 |
| 5,9 |
15,0 |
32,4 |
| 8,6 |
10,2 |
46,6 |
| 9,3 |
9,5 |
100,0 |
| 13,3 |
6,6 |
33,7 |
| 14,1 |
6,3 |
33,4 |
| 17,4 |
5,1 |
46,7 |
| 17,7 |
5,0 |
43,1 |
| 18,0 |
4,9 |
77,0 |
| 18,8 |
4,7 |
66,4 |
| 19,3 |
4,6 |
21,5 |
| 19,8 |
4,5 |
23,5 |
| 20,2 |
4,4 |
21,5 |
| 21,1 |
4,2 |
36,7 |
| 21,5 |
4,1 |
38,3 |
| 21,9 |
4,1 |
31,6 |
| 23,6 |
3,8 |
44,8 |
 Относительные интенсивности могут меняться в зависимости от морфологии и размера кристалла. Относительные интенсивности могут меняться в зависимости от морфологии и размера кристалла. |
Как ингибиторы HMG-CoA редуктазы, новые кристаллические формы аторвастатина в форме свободной кислоты применимы в качестве гиполипидемических и гипохолестеринемических средств, a также средств для лечения остеопороза, доброкачественной гиперплазии простаты и болезни Альцгеймера.
Еще одним дополнительным вариантом осуществления настоящего изобретения является фармацевтическая композиция для введения эффективного количества кристаллических форм A или В аторвастатина в форме свободной кислоты в единичной дозированной форме при способах лечения, описанных выше. И, наконец, настоящее изобретение относится к способам получения форм A и В аторвастатина в форме свободной кислоты.
Краткое описание чертежей
Изобретение, кроме того, описывается с помощью нижеследующих примеров, не ограничивающих объем изобретения, которые относятся к сопроводительным фигурам 1-4, некоторые детали которых вкратце приведены ниже.
Фиг.1. Дифрактограмма формы A аторвастатина в форме свободной кислоты, полученная на дифрактометре Bruker D5000.
Фиг.2. Дифрактограмма формы В аторвастатина в форме свободной кислоты, полученная на дифрактометре Bruker D5000.
Фиг.3. Спектр 13C ядерного магнитного резонанса в твердом состоянии формы A аторвастатина в форме свободной кислоты.
Фиг.4. Спектр 19F ядерного магнитного резонанса в твердом состоянии формы A аторвастатина в форме свободной кислоты.
Подробное описание изобретения
Термин “кристаллический”, используемый в настоящем описании, относится к твердому веществу, образованному повторением трехмерной решетки из атомов, ионов или молекул, имеющей фиксированные расстояния между составляющими частями, и которое, кроме того, может быть идентифицировано специалистом в данной области при использовании таких методов, как, например, дифракция рентгеновских лучей, ЯМР твердых тел, спектроскопия комбинационного рассеяния, инфракрасная спектроскопия и тому подобное. Примеры кристаллических твердых веществ, описанных в настоящей заявке, включают кристаллическую форму A и кристаллическую форму В аторвастатина в форме свободной кислоты. Кристаллическая форма A и кристаллическая форма В аторвастатина в форме свободной кислоты могут быть охарактеризованы их порошковыми рентгенограммами и/или спектрами ядерного магнитного резонанса в твердом состоянии тел.
Порошковая дифракция рентгеновских лучей
Формы A и В аторвастатина в форме свободной кислоты характеризовали их порошковыми рентгенограммами. Таким образом, рентгенограммы форм A и В были получены на дифрактометре Bruker D5000 медного излучения (длина волны 1:1,54056). Напряжение в трубке и силу тока устанавливали на 40 кВ и 50 мА соответственно. Отклоняющую и рассевающую щели устанавливали на 1 мм, а принимающую щель устанавливали на 0,6 мм. Дифрагированное излучение обнаруживали с помощью детектора Kevex PSI. Использовали непрерывную развертку от тета до двух тета, при скорости 2,4°/мин, с шагом 1 сек/0,04°, меняя значения 2 от 3,0 до 40°. Для юстировки прибора осуществляли анализ оксида алюминия. Данные собирали и анализировали, используя версию 7.0 Bruker программы axis. Образцы готовили, помещая их в кварцевый держатель. Следует заметить, что фирма Bruker Instruments приобрела фирму Siemans; таким образом, прибор Bruker D5000, по существу, является тем же прибором, что и прибор Siemans D5000. от 3,0 до 40°. Для юстировки прибора осуществляли анализ оксида алюминия. Данные собирали и анализировали, используя версию 7.0 Bruker программы axis. Образцы готовили, помещая их в кварцевый держатель. Следует заметить, что фирма Bruker Instruments приобрела фирму Siemans; таким образом, прибор Bruker D5000, по существу, является тем же прибором, что и прибор Siemans D5000.
В таблице 1 перечисляются значения углов 2 и относительные интенсивности всех линий, имеющих относительную интенсивность, превышающую 20%, для образцов кристаллических форм A и В аторвастатина в форме свободной кислоты: и относительные интенсивности всех линий, имеющих относительную интенсивность, превышающую 20%, для образцов кристаллических форм A и В аторвастатина в форме свободной кислоты:
Таблица 1
ПОЛОЖЕНИЯ ПИКОВ И ИНТЕНСИВНОСТИ ДИФРАКЦИОННЫХ ЛИНИЙ для ФОРМ A и В АТОРВАСТАТИНА в ФОРМЕ СВОБОДНОЙ КИСЛОТЫ |
| Форма А |
Форма В |
Градус 2 |
Относительная интенсивность
(>20%) |
Градус 2 |
Относительная интенсивность
(>20%) |
| 4,7 |
49,5 |
4,6 |
48,3 |
| 6,0 |
25,9 |
5,9 |
32,4 |
| 8,9 |
46,0 |
8,6 |
46,6 |
| 9,1 |
63,0 |
9,3 |
100,0 |
| 9,4 |
100,0 |
13,3 |
33,7 |
| 13,2 |
20,5 |
14,1 |
33,4 |
| 14,1 |
29,5 |
17,4 |
46,7 |
| 17,8 |
55,8 |
17,7 |
43,1 |
| 18,1 |
98,1 |
18,0 |
77,0 |
| 18,9 |
63,8 |
18,8 |
66,4 |
| 19,9 |
23,9 |
19,3 |
21,5 |
| 20,2 |
29,3 |
19,8 |
23,5 |
| 20,6 |
32,4 |
20,2 |
21,5 |
| 21,8 |
50,1 |
21,1 |
36,7 |
| 22,1 |
57,5 |
21,5 |
38,3 |
| 22,5 |
28,4 |
21,9 |
31,6 |
| 23,7 |
57,1 |
23,6 |
44,8 |
| 25,9 |
21,0 |
|
|
| 26,7 |
20,0 |
|
|
Так как известны только две кристаллические формы аторвастатина в форме свободной кислоты, каждая форма может быть идентифицирована и отлична от другой кристаллической формы по отдельной линии или комбинации линий на порошковой рентгенограмме или по самой рентгенограмме, которая отличается от рентгенограммы другой кристаллической формы.
Например, в таблице 2 перечислены отдельные характеристические 2 пики для форм A и В аторвастатина в форме свободной кислоты, то есть набор дифракционных линий на порошковой рентгенограмме, который специфичен для каждой формы. пики для форм A и В аторвастатина в форме свободной кислоты, то есть набор дифракционных линий на порошковой рентгенограмме, который специфичен для каждой формы.
Таблица 2
АТОРВАСТАТИН В ФОРМЕ СВОБОДНОЙ КИСЛОТЫ, ФОРМЫ A и В; ХАРАКТЕРИСТИЧЕСКИЕ ПИКИ и КОМБИНАЦИИ 2 ПИКОВ ПИКОВ |
Форма А
Градус 2 |
Форма В
Градус 2 |
| 8,9 |
8,6 |
| 20,6 |
17,4 |
| 22,5 |
21,1 |
| 25,9 |
21,5 |
Ядерный магнитный резонанс в твердом состоянии
Форма A аторвастатина в форме свободной кислоты может также быть охарактеризована по спектрам ядерного магнитного резонанса в твердом состоянии. Таким образом, спектр ядерного магнитного резонанса в твердом состоянии для формы A получали на ЯМР спектрометре Bruker-Biospin Avance DSX с частотой 500 МГц.
19F SSNMR (ЯМР 19F твердом состоянии)
Для каждого анализируемого образца приблизительно 15 мг образца плотно упаковывали в 2,5 мм ZrO спиннере. Одномерные спектры 19F были получены при использовании кросс-поляризации при вращении под магическим углом (CPMAS), при 295 К и внешнем давлении, на ЯМР спектрометре Bruker-Biospin Avance DSX с частотой 500 МГц на датчике с зазором 2,5 мм. Образцы располагали под магическим углом и вращали с частотой 35,0 кГц, соответствующей максимальной скорости вращения, установленной для 2,5 мм спиннера. Большая скорость вращения минимизирует интенсивности побочных сигналов вращения и обеспечивает почти полное протонное разделение для сигналов 19F. Число сканирований регулируют для каждого образца индивидуально для получения допустимого соотношения сигнал/шум (S/N). Обычно необходимо 150 сканирований. До регистрации 19F измеряли времена релаксации 19F с помощью инверсионной восстановительной техники. Задержку регулировали для каждого образца, до пятикратного превышения наиболее длительного времени релаксации 19F в образце, что обеспечивало получение количественных спектров. При каждом чередующемся сканировании, после предварительного насыщения сигнала 19F вычитали фон базового сигнала. Трифторуксусную кислоту (разбавленную водой до 50% об./об) использовали в качестве внешнего эталона сравнения, устанавливая резонанс при 76,54 м.д.
13C SSNMR (ЯМР 13С твердых тел)
Для каждого анализируемого образца приблизительно 80 мг образца плотно упаковывали в 4 мм ZrO спиннере. Одномерные спектры ЯМР 13C были получены при внешнем давлении, используя 1H-13C CPMAS при 295 K, на ЯМР спектрометре Bruker-Biospin Avance DSX с частотой 500 МГц, на датчике с зазором 4 мм. Образцы вращали с частотой 15,0 кГц, соответствующей максимальной скорости вращения, установленной для 4 мм спиннера. Большая скорость вращения минимизировала интенсивности побочных сигналов вращения. Для оптимизации чувствительности сигнала время контакта при кросс-поляризации устанавливали на 1,5 мс, а энергию разделения для протонов устанавливали на 100 кГц. Для получения допустимого соотношения сигнал/шум (S/N) число сканирований регулировали для каждого образца индивидуально. Обычно требовалось 1900 сканирований с задержкой, составляющей 5 секунд. В качестве внешнего эталона сравнения использовали адамантан, устанавливая высокопольный резонанс 29,5 м.д.
Кристаллические формы A и В аторвастатина в форме свободной кислоты по настоящему изобретению могут находиться в виде безводных, гидратированных и сольватированных форм. Вообще говоря, гидратированные формы эквивалентны негидратированным формам и предназначаются для введения в объем настоящего изобретения. Кристаллическая форма A предпочтительно находится в виде гидрата. Предпочтительно форма A содержит 0,6 моль воды.
Кристаллические формы A и В аторвастатина в виде свободной кислоты по настоящему изобретению независимо от степени гидратации и/или сольватации, имеющие одинаковые порошковые рентгенограммы или спектры ЯМР в твердом состоянии, включены в объем настоящего изобретения.
Новые кристаллические формы аторвастатина в виде свободной кислоты, описанные в настоящем описании, обладают полезными свойствами. Например, формы A и В обладают хорошей химической стабильностью. Кроме того, растворимость форм A и В в растворителях, включающих воду и фосфатный буфер, сопоставима с формой I аторвастатин-кальция (описано в патенте США 5969156).
Настоящее изобретение предлагает способ получения кристаллических форм A и В аторвастатина в форме свободной кислоты, который включает кристаллизацию аторвастатина в форме свободной кислоты из раствора в растворителях, в которых получают кристаллические формы A и В аторвастатина в форме свободной кислоты и при условиях, в которых их получают.
Точные условия, при которых получают кристаллические формы A и В аторвастатина в виде свободной кислоты, могут быть определены эмпирически, и возможно только предложить ряд способов, которые оказались пригодными на практике.
Например, форма A может быть получена путем суспендирования аторвастатин-кальция в воде вместе с таким растворителем, как, например, ацетонитрил и тому подобное. Смесь фильтруют и фильтрат подкисляют такой кислотой, как, например, неорганическая кислота, такая как хлористоводородная кислота и тому подобное, с последующим удалением растворителя. Твердое вещество промывают водой и высушивают для получения формы A. Предпочтительно кристаллическую форму I аторвастатин-кальция суспендируют в смеси, состоящей из приблизительно 80 частей воды и 20 частей ацетонитрила; смесь фильтруют, фильтрат подкисляют 1 н. раствором HCl, растворитель удаляют, полученное твердое вещество промывают водой и высушивают при приблизительно комнатной температуре в течение приблизительно 24 часов для получения формы A.
Альтернативно форма A может быть получена экстракцией растворителя. Например, аторвастатин-кальций суспендируют в воде до смачивания, с последующим добавлением растворителя, такого как, например, трет-бутилметиловый эфир (MTBE), этилацетат и тому подобное. Суспензию подкисляют кислотой, как было описано выше, перемешивают до получения прозрачной двухфазной смеси, отделяют органическую фазу, удаляют растворитель, и полученное твердое вещество растворяют в таком растворителе, как вода и ацетонитрил для получения формы A. После растворения твердого вещества в смеси вода/ацетонитрил для ускорения образования формы A могут быть добавлены затравочные кристаллы формы A. Предпочтительно кристаллическую форму I аторвастатин-кальция суспендируют в смеси воды и MTBE; суспензию подкисляют 1 н. раствором HCl, две фазы разделяют, MTBE удаляют, полученное твердое вещество растворяют в смеси вода/ацетонитрил, добавляют затравочные кристаллы формы A и форму A отделяют фильтрованием.
Форму В получают нагреванием в вакууме формы A при приблизительно 45°C в течение приблизительно одного дня. Предпочтительно форму A нагревают в вакууме в печи при приблизительно 45°C в течение приблизительно одного дня. Альтернативно для получения формы B форму A выдерживают при низкой относительной влажности в течение приблизительно 72 дней. Предпочтительно для получения формы B форму A сохраняют в течение приблизительно 72 дней в камере с низкой относительной влажностью, которую поддерживают с помощью пятиокиси фосфора.
Соединения по настоящему изобретению могут быть получены и введены субъекту в виде множества оральных и парентеральных дозированных форм. Таким образом, соединения по настоящему изобретению могут быть введены посредством инъекций, то есть внутривенно, внутримышечно, интрадермально, подкожно, интрадуоденально или интраперитонеально. Кроме того, соединения по настоящему изобретению могут быть введены путем ингаляции, например интраназально. Кроме того, соединения по настоящему изобретению могут быть введены трансдермально.
Для получения фармацевтических композиций из соединений по настоящему изобретению могут быть использованы твердые или жидкие фармацевтически приемлемые носители. Препараты в виде твердой формы включают порошки, таблетки, пилюли, капсулы, крахмальные облатки, суппозитории и диспергируемые гранулы. Твердый носитель может представлять собой одно или несколько веществ, которые, кроме того, могут действовать как разбавители, флаворанты, солюбилизаторы, лубриканты, суспендирующие средства, связующие вещества, консерванты, средства, дезинтегрирующие таблетки или инкапсулирующие материалы.
В порошках носитель представляет собой тонкоизмельченное твердое вещество, которое находится в смеси с тонкоизмельченным активным компонентом.
В таблетках активный компонент смешивают в подходящем соотношении с носителем, обладающим необходимыми связующими свойствами, и уплотняют до требуемого размера и формы.
Порошки и таблетки предпочтительно содержат от двух или десяти до приблизительно семидесяти процентов активного соединения. Подходящими носителями являются карбонат магния, стеарат магния, тальк, сахар, лактоза, пектин, декстрин, крахмал, желатин, трагант, метилцеллюлоза, натрийкарбоксиметилцеллюлоза, воск, имеющий низкую температуру плавления, какао-масло и тому подобное. Термин “получение” включает объединение активного соединения вместе с инкапсулирующим веществом в качестве носителя с получением капсулы, в которой активный компонент, вместе с другими носителями или без них, окружен носителем, который, таким образом, оказывается с ним соединенным. Аналогично могут быть включены крахмальные облатки и лепешки. Таблетки, порошки, капсулы, пилюли, крахмальные облатки и лепешки могут быть использованы в виде твердых дозированных форм, пригодных для орального введения.
Для получения суппозиториев воск с низкой температурой плавления, такой как смесь глицеридов жирных кислот или какао-масло, сначала расплавляют, и в этой смеси гомогенно диспергируют активный компонент, как например, путем перемешивания. Расплавленную гомогенную смесь затем выливают в формы удобного размера и оставляют остывать для отверждения.
Препараты в жидкой форме включают растворы, суспензии, удерживающие клизмы и эмульсии, например воду или водные растворы пропиленгликоля. Для парентерального введения путем инъекции жидкие препараты могут быть сформированы в растворе, в водном растворе полиэтиленгликоля.
Водные растворы, пригодные для орального использования, могут быть получены при растворении активного компонента в воде, по необходимости добавляя подходящие красители, флаворанты, стабилизирующие средства и загустители.
Водные суспензии, пригодные для орального использования, могут быть получены при диспергировании тонкоизмельченного активного компонента в воде, содержащей вязкое вещество, такое как природные или синтетические камеди, смолы, метилцеллюлоза, натрийкарбоксиметилцеллюлоза и другие хорошо известные суспендирующие средства.
В изобретение также включены препараты в твердой форме, которые предназначены для превращения в жидкую форму для орального введения непосредственно перед употреблением.
Такие жидкие формы включают растворы, суспензии и эмульсии. Эти препараты могут содержать, в дополнение к активному компоненту, красители, флаворанты, стабилизаторы, буферы, искусственные и естественные подсластители, диспергаторы, загустители, солюбилизирующие средства и тому подобное.
Фармацевтический препарат предпочтительно находится в единичной дозированной форме. В такой форме препарат подразделен на единичные дозы, содержащие соответствующие количества активного компонента. Единичная дозированная форма может представлять собой препарат в упаковке, упаковка содержит дискретные количества препарата, такие как упакованные таблетки, капсулы и порошки, во флаконах или ампулах. Кроме того, единичная дозированная форма сама по себе может представлять собой капсулу, таблетку, крахмальную облатку или лепешку, или это может быть соответствующее количество любой из этих форм в упаковке.
Количество активного компонента в единичной дозе препарата может варьировать или быть откорректированным таким образом, чтобы содержать от 0,5 мг до 100 мг, предпочтительно от 2,5 мг до 80 мг, в соответствии с конкретным применением и эффективностью активного компонента. Композиция может, при необходимости, кроме того, содержать другие совместимые терапевтические средства.
При терапевтическом использовании в качестве гиполипидемических и/или гипохолестеринемических средств и средств для лечения остеопороза, доброкачественной гиперплазии простаты, болезни Альцгеймера, кристаллические формы A и В аторвастатина в форме свободной кислоты, используемые в фармацевтическом способе по данному изобретению, вводят в начальной дозе, от приблизительно 2,5 мг до приблизительно 80 мг ежедневно. Диапазон от приблизительно 2,5 мг до приблизительно 20 мг является предпочтительным для ежедневной дозы. Дозирование, однако, может варьироваться в зависимости от потребностей больного, тяжести состояния, подлежащего лечению, и соединения, которое используют. Определение соответствующей дозировки в конкретной ситуации находится в компетенции специалиста в данной области. Обычно лечение начинают с меньших доз, которые ниже оптимальной дозы для данного соединения. Затем дозировку увеличивают небольшими порциями, пока не достигают оптимального эффекта при данных обстоятельствах. Для удобства, при желании, общая ежедневная доза может быть разделена и введена частями в течение дня.
Нижеследующие примеры, не ограничивающие объем изобретения, иллюстрируют способы получения соединения по изобретению, которые авторы изобретения считают предпочтительными.
Пример 1
[R-(R*,R*)]-2-(4-Фторфенил)- , , -дигидрокси-5-(1-метилэтил)-3-фенил-4-[(фениламино)карбонил]-1H-пиррол-1-гептановая кислота -дигидрокси-5-(1-метилэтил)-3-фенил-4-[(фениламино)карбонил]-1H-пиррол-1-гептановая кислота
Форма A аторвастатина в форме свободной кислоты
Способ A
В 600 мл химическом стакане получали суспензию, загружая 100 мл ацетонитрила (ACN) и 400 мл деионизированной воды (20:80 ACN/вода) к 0,5 граммам кристаллической формы I аторвастатин-кальция (патент США 5969156). Суспензию перемешивали в условиях окружающей среды в течение 15 минут. Все нерастворенное вещество удаляли фильтрованием под вакуумом, используя нейлоновый (нейлон-66) мембранный фильтр с размером пор 0,45 мкм. Определяли pH фильтрата, который составлял от 6,5 до 7,0, и который затем устанавливали на 2,35, используя 1 н. HCl. Образовывался непрозрачный осадок, который представлял собой мелкие капельки масла, как было определено с помощью поляризующей световой микроскопии (PLM). Растворитель выпаривали, пропуская азот сверху над раствором при перемешивании, до образования тяжелого белого осадка (15 минут). Суспензию фильтровали под вакуумом через мембранный фильтр с фильтровальной перегородкой из нейлона-66 и размером пор 0,45 мкм. Твердое вещество затем промывали 100 мл деионизированной воды и сушили на воздухе в условиях окружающей среды в течение 24 часов для получения 0,3 грамм кристаллической формы A аторвастатина в форме свободной кислоты.
Способ В
Кристаллическую форму I аторвастатин-кальция (патент США 5969156) (10 грамм) помещали в колбу Эрленмейера (4 л). В колбу добавляли воду (1 л) и одновременно опускали стержень магнитной мешалки. Содержимое перемешивали, пока не смачивали все твердые вещества. Совместно с перемешиванием к реакционной смеси добавляли MTBE (трет-бутилметиловый эфир – 1 л) для образования белой суспензии. Затем к суспензии, перемешивая, добавляли хлористоводородную кислоту (20 мл – 1 н. раствора). Содержимое перемешивали до тех пор, пока не фиксировали наличие прозрачной (2-х фазной) смеси (около 5 мин). Затем смесь переносили в делительную воронку (4 л). Содержимое тщательно перемешивали, и слои разделяли. Водный слой (нижняя фаза) помещали обратно в делительную воронку и добавляли дополнительное количество MTBE (1 л). Содержимое тщательно перемешивали, и слои разделяли. Водный слой отбрасывали, а слой MTBE объединяли вместе со слоем MTBE первой экстракции. Объединенные слои MTBE помещали обратно в воронку и добавляли воду (0,5 л). Содержимое тщательно перемешивали, и слои разделяли. Водный слой отбрасывали, а слой MTBE помещали в круглодонную колбу (3 л). Затем MTBE удаляли в роторном испарителе, получая тонкую пленку или аморфное твердое вещество. Пленку/твердое вещество растворяли ацетонитрилом (0,2 л) для образования раствора. К раствору добавляли воду (0,8 л) при перемешивании, используя магнитную мешалку. Образовывалась белая суспензия, которая при исследовании с помощью PLM (поляризованной световой микроскопии), оказалась мелкими капельками масла. Добавляли затравочные кристаллы кристаллической формы A аторвастатина в форме свободной кислоты. Содержимое затем быстро перемешивали под током азота в течение, приблизительно, одного часа. Твердые вещества отделяли фильтрованием под вакуумом, используя воронку Бюхнера, с бумажным фильтром (№ 2). Твердые вещества промывали водой (0,5 л) и помещали в кристаллизатор. Кристаллизатор помещали в термостат при 25°C, поддерживая атмосферу азота до высушивания (около 1 дня). Эта процедура позволила получить кристаллическую форму A аторвастатина в форме свободной кислоты с выходом приблизительно 92%.
Форма В аторвастатина в форме свободной кислоты
Способ A
Кристаллическую форму A аторвастатина в форме свободной кислоты (пример 1) хранили в вакуумном термостате при температуре 45°C (продувка азотом, вакуумирование) в течение, приблизительно, одного дня для получения кристаллической формы В аторвастатина в форме свободной кислоты.
Способ В
Кристаллическую форму A аторвастатина в форме свободной кислоты (пример 1) хранили в камере с низкой относительной влажностью (получаемой при использовании пятиокиси фосфора) в течение, приблизительно, 72 дней для получения кристаллический формы В аторвастатина в форме свободной кислоты.
Формула изобретения
1. Кристаллическая форма А аторвастатина в форме свободной кислоты или ее гидрата, имеющая порошковую рентгенограмму, содержащую нижеследующие значения 2 , измеренные с использованием излучения CuK , измеренные с использованием излучения CuK : 8,9, 20,6, 22,5 или 25,9. : 8,9, 20,6, 22,5 или 25,9.
2. Кристаллическая форма А аторвастатина в форме свободной кислоты или ее гидрата, имеющая порошковую рентгенограмму, содержащую нижеследующие значения 2 , измеренные с использованием излучения CuK , измеренные с использованием излучения CuK : 4,7, 6,0, 8,9, 9,1, 9,4, 13,2, 14,1, 17,8, 18,1, 18,9, 19,9, 20,2, 20,6, 21,8, 22,1, 22,5, 23,7, 25,9 и 26,7. : 4,7, 6,0, 8,9, 9,1, 9,4, 13,2, 14,1, 17,8, 18,1, 18,9, 19,9, 20,2, 20,6, 21,8, 22,1, 22,5, 23,7, 25,9 и 26,7.
3. Кристаллическая форма А аторвастатина в форме свободной кислоты или ее гидрата, имеющая порошковую рентгенограмму, содержащую нижеследующие значения 2 , измеренные с использованием излучения CuK , измеренные с использованием излучения CuK : 8,9, 20,6, 22,5 или 25,9. : 8,9, 20,6, 22,5 или 25,9.
4. Кристаллическая форма А аторвастатина в форме свободной кислоты, имеющая порошковую рентгенограмму, содержащую нижеследующие значения 2 , измеренные с использованием излучения CuK , измеренные с использованием излучения CuK : 4,7, 6,0, 8,9, 9,1, 9,4, 13,2, 14,1, 17,8, 18,1, 18,9, 19,9, 20,2, 20,6, 21,8, 22,1, 22,5, 23,7, 25,9 и 26,7. : 4,7, 6,0, 8,9, 9,1, 9,4, 13,2, 14,1, 17,8, 18,1, 18,9, 19,9, 20,2, 20,6, 21,8, 22,1, 22,5, 23,7, 25,9 и 26,7.
5. Кристаллическая форма А аторвастатина в форме свободной кислоты или ее гидрата, характеризующаяся тем, что она имеет 13С ядерный магнитный резонанс в твердом состоянии с нижеследующими химическими сдвигами, выраженными в м.д.: 18,1, 18,8, 20,5 и 21,2.
6. Кристаллическая форма А аторвастатина в форме свободной кислоты или ее гидрата, характеризующаяся тем, что она имеет 13С ядерный магнитный резонанс в твердом состоянии с нижеследующими химическими сдвигами, выраженными в м.д.: 161,5, 163,6, 166,3, 167,1, 174,3 и 180,6.
7. Кристаллическая форма А аторвастатина в форме свободной кислоты или ее гидрата, характеризующаяся тем, что она имеет 13С ядерный магнитный резонанс в твердом состоянии с нижеследующими химическими сдвигами, выраженными в м.д.: 18,1, 18,8, 20,5, 21,2, 25,0, 25,5, 26,2, 26,8, 37,1, 38,9, 40,0, 40,6, 41,8, 42,9, 43,5, 65,3, 68,6, 69,1, 70,0, 71,3, 112,3, 113,7, 115,1, 116,4, 118,4, 119,3, 121,6, 123,3, 125,4, 128,0, 128,8 (выступ), 130,0, 132,9, 134,1, 135,2, 137,9, 140,7, 141,8, 161,5, 163,6, 166,3, 167,1, 174,3 и 180,6.
8. Кристаллическая форма А аторвастатина в форме свободной кислоты или ее гидрата, характеризующаяся тем, что она имеет 19F ядерный магнитный резонанс в твердом состоянии с нижеследующими химическими сдвигами, выраженными в м.д.: -114,1, -112,6, -110,6 или -105,6.
9. Кристаллическая форма А аторвастатина в форме свободной кислоты, характеризующаяся тем, что она имеет 19F ядерный магнитный резонанс в твердом состоянии с нижеследующими химическими сдвигами, выраженными в м.д.: -114,1, -112,6, -110,6 или -105,6.
10. Кристаллическая форма В аторвастатина в форме свободной кислоты или ее гидрата, имеющая порошковую рентгенограмму, содержащую нижеследующие значения 2 , измеренные с использованием излучения CuK , измеренные с использованием излучения CuK : 8,6, 17,4, 21,1 или 21,5. : 8,6, 17,4, 21,1 или 21,5.
11. Кристаллическая форма В аторвастатина в форме свободной кислоты или ее гидрата, имеющая порошковую рентгенограмму, содержащую нижеследующие значения 2 , измеренные с использованием излучения CuK , измеренные с использованием излучения CuK : 4,6, 5,9, 8,6, 9,3, 13,3, 14,1, 17,4, 17,7, 18,0, 18,8, 19,3, 19,8, 20,2, 21,1, 21,5, 21,9 и 23,6. : 4,6, 5,9, 8,6, 9,3, 13,3, 14,1, 17,4, 17,7, 18,0, 18,8, 19,3, 19,8, 20,2, 21,1, 21,5, 21,9 и 23,6.
12. Кристаллическая форма В аторвастатина в форме свободной кислоты, имеющая порошковую рентгенограмму, содержащую нижеследующие значения 2 , измеренные с использованием излучения CuK , измеренные с использованием излучения CuK : 4,6, 5,9, 8,6, 9,3, 13,3, 14,1, 17,4, 17,7, 18,0, 18,8, 19,3, 19,8, 20,2, 21,1, 21,5, 21,9 и 23,6. : 4,6, 5,9, 8,6, 9,3, 13,3, 14,1, 17,4, 17,7, 18,0, 18,8, 19,3, 19,8, 20,2, 21,1, 21,5, 21,9 и 23,6.
13. Фармацевтическая композиция, обладающая гиполипидемической и гипохолестеринемической активностью, содержащая кристаллический аторвастатин в форме свободной кислоты по пп.1-12 в смеси с, по крайней мере, одним фармацевтически приемлемым эксципиентом, разбавителем или носителем.
14. Способ лечения гиперлипидемии, гиперхолестеринемии, остеопороза, доброкачественной гиперплазии простаты и болезни Альцгеймера, включающий введение реципиенту, страдающему от этих заболеваний, терапевтически эффективного количества соединения по пп.1-12 в единичной дозированной форме.
РИСУНКИ
MM4A – Досрочное прекращение действия патента СССР или патента Российской Федерации на изобретение из-за неуплаты в установленный срок пошлины за поддержание патента в силе
Дата прекращения действия патента: 07.09.2009
Извещение опубликовано: 27.07.2010 БИ: 21/2010
|
|